德国2022版脊髓损伤/疾病神经源性肠道功能障碍管理指南解读(附一例临床病例应用报告)
2023-09-21刘根林周红俊郑樱郝春霞张缨卫波王一吉康海琼逯晓蕾袁媛蒙倩茹
刘根林,周红俊,郑樱,郝春霞,张缨,卫波,王一吉,康海琼,逯晓蕾,袁媛,蒙倩茹
脊髓损伤(spinal cord injury,SCI)是由于各种原因引起的脊髓结构、功能损害,造成损伤水平以下脊髓神经功能(运动、感觉、括约肌及自主神经功能)的障碍。脊髓损伤往往造成不同程度的四肢瘫或截瘫,是一种严重致残性创伤[1]。据统计,截至2018年,国内23个省的外伤性脊髓损伤年发病率为65/100万人口,最常见的致伤原因是车祸和高处坠落[2]。近年来国内儿童脊髓损伤发病有增多趋势,儿童舞蹈下腰动作是其重要原因[3]。2019年全球新发脊髓损伤病例估计为90万例,患病人数超过2 000万例。脊髓疾病(spinal cord disease,SCD)指非外伤性脊髓损伤,常见原因是炎症和血管损害[4]。
脊髓损伤/疾病(spinal cord injury/disease,SCI/D)对身体的伤害主要表现为肢体瘫痪和大小便障碍。下肢瘫痪导致的移动障碍,目前已经有很多康复方法,如使用手动轮椅或电动轮椅作为代步工具;大小便障碍的康复方法相对较少。在大多数情况下,排尿障碍可以采取间歇导尿或留置尿管的方法来解决,但对于排便障碍,目前临床上还缺少实用有效的处理方法[5]。
大多数SCI/D患者的排便障碍都由神经源性肠道功能障碍(neurogenic bowel dysfunction,NBD)引起。NBD如果不做治疗,将导致很严重的健康后果。由大便失禁导致的羞耻感和恐惧可以引起患者的社会孤立。因此,认识和分析SCI/D引起的NBD以及多种影响因素是非常重要的[6]。
本文通过介绍德国2022版《脊髓损伤/疾病神经源性肠道功能障碍管理指南》的主要内容,并报告1例临床病例的应用效果,希望有助于提高国内SCI/D NBD患者的康复疗效。
1 指南解读
《脊髓损伤/疾病神经源性肠道功能障碍管理指南》由德国医学科学协会2022年发布。该指南的发布获得2022年国际脊髓学会的独家授权。该指南的内容分为前言、方法、结果和建议、讨论和结论5个部分[6]。
1.1 前言 先简要说明现有NBD管理指南的循证证据水平较低,因此有必要在德语地区制定循证证据水平较高的指南[7],目的是汇总现有的关于NBD的定义和诊断以及肠道管理知识,为NBD患者的治疗提供实用指导;强调成功的肠道管理需要跨学科团队之间的多专业协作。
1.2 方法 介绍了该指南是在德国截瘫医学会的领导下制定的。来自截瘫学、直肠病学、内脏外科学、神经泌尿学、胃肠病学、卫生保健和护理领域的专家,以及护理科学和营养师/医学营养师组成多专业跨学科的“肠功能障碍指南编写小组”一起工作。文献检索范围包括PubMed、Science direct、Cochrane和CINAHL数据库。搜索词是神经源性肠道功能障碍、神经源性肠道和脊髓、神经源性肠道和多发性硬化、神经源性肠道和脊髓脊膜膨出/脊柱裂、肠道管理、便秘和脊髓、大便失禁和脊髓。对这些文献检索的分析作为本指南的编写基础。编写小组确定了相关的重点问题后,多次召开会议以制定指南的建议草案。每个建议所针对的临床问题都经过讨论,以促进建议的采纳。随后,召集专门会议对建议的最终稿进行投票。最后,指南草案提交给德国科学医学协会的指南相关专业协会的委托代表进行投票,作为第1次外部审查。在5轮指南委员会会议期间,以适当和可行方式,按规定步骤,采取结构性专门小组评议机制,确定共识内容。在第1次外部审查、形成专家共识之后,在提交给德国科学医学协会获得批准和发布之前,由德国截瘫医学会的所有成员对指南进行第2次外部审查。所有建议的证据水平是专家共识。1.3 结果和建议
1.3.1 临床表现 根据不同损伤水平、损伤程度和发病时间,肠道功能障碍临床上表现为:肌源性失禁、神经源性失禁、慢传输性便秘、出口梗阻。
脊髓完全性损伤后上、下运动神经元损伤的功能紊乱和症状表现,见表1。这些症状原则上会出现于不完全性瘫痪的情况,但在保留部分感觉和运动功能的患者中这些症状的表现有所不同。
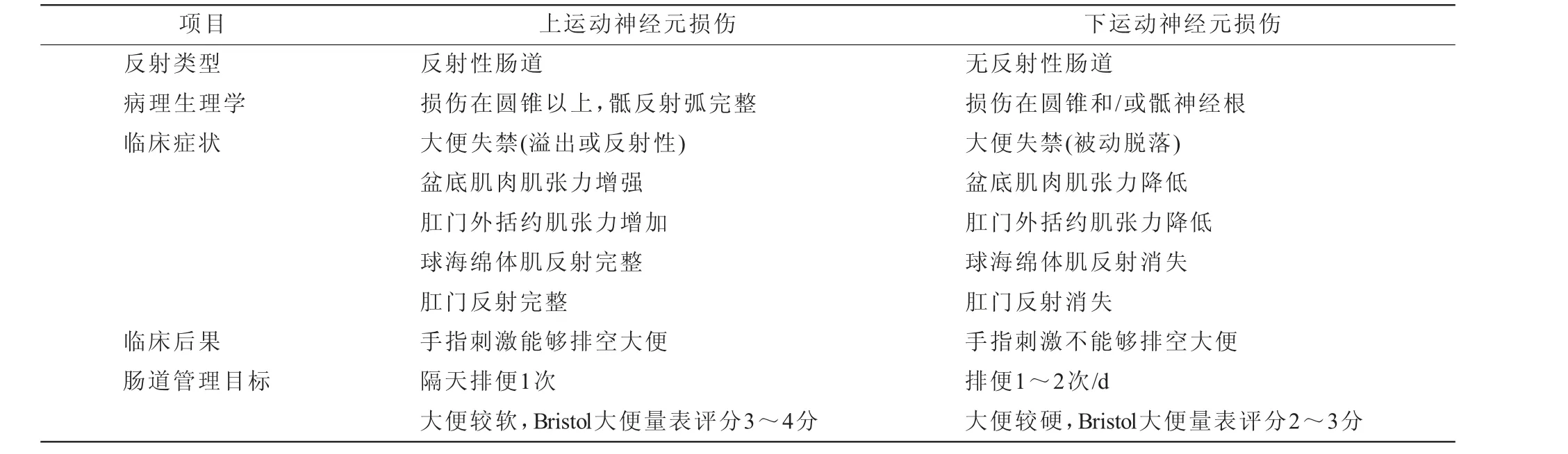
表1 上、下运动神经元完全性损伤的功能障碍和症状比较与肠道管理策略
肠道管理不当或对推荐的措施实施不当可能导致以下严重的并发症:腹痛/不适、肛门出血、肛裂、自主神经反射异常(T6以上的脊髓损伤)、压疮、呼吸功能受限、粪便嵌塞/反常性腹泻、痔疮、尿路感染、巨结肠/巨直肠、胃肠胀气、脱垂(直肠、肛门)、脊柱痉挛。
1.3.2 诊断 依据病史、大便观察(使用Bristol大便量表)、腹部检查、肛肠检查进行评估。
1.3.3 肠道管理 总体目标是基本实现自主控制排便,根据患者日程安排能够规律地定时、在限定时间内充分排空大便。肠道管理是一个循环过程,见表2。

表2 脊髓损伤/疾病神经源性肠道功能障碍管理建议
1.4 讨论 大多数SCI/D患者,即使是轻微不完全受伤,也会经历排便问题,如便秘、排便困难和大便失禁。NBD(以及神经源性膀胱功能障碍)的后果通常比移动受限对患者的生活质量有更大的影响。因此,为受NBD困扰的患者以及来自各行业为他们提供服务的照顾者提供最好的实用指导和建议非常重要。已发表的有关NBD管理建议的科学证据仍然很低。在制定本指南时,世界范围内尚无证据水平高于专家建议的指南。
专家组确定的SCI/D肠道管理目标如下:①实现自我管理,在方便社交的时间和地点,能够定期、可预测地排便。②使用最少的物理和药物干预在可接受的时间内完全排空。③预防肠道意外、便秘、自主神经反射异常(可能危及生命)和其他并发症。指南能够应用于日常生活当中才算真正的成功。指南所描述措施的选择和应用必须始终考虑到患者具体情况,正确的应用是成功的先决条件。
1.5 结论 患者具体的肠道管理必须以明确的诊断为基础,并考虑损伤类型的影响。由于神经损伤和肠道功能受多种因素的影响,简单的列表式管理是无效的。均衡、适当高纤维膳食和充足液体摄入是肠道管理的基础。NBD治疗需要应用多种多样的复杂的肠道管理模式。通常需要采取一种以上的措施来制定有效的肠道日常管理方案。NBD患者肠道管理的总体目标是减少肠道相关并发症和改善生活质量。
2 病例摘要(附1例临床病例应用报告)
2.1 一般情况 患者,男,1967年出生,6年前车祸导致四肢瘫。伤后4 d在某医院行颈椎后开门椎管扩大成形术,伤后22 d入住我院,曾在多个医院住院治疗。首次入院查体:双侧正常感觉平面位于颈4,颈5以下感觉消失;双侧屈肘肌肌力1级,伸腕肌、伸肘肌、指深屈肌和小指外展肌肌力0级,下肢肌力0级;肛门深压觉存在,肛门括约肌无自主收缩。颈椎MRI提示:颈4~5椎间盘水平脊髓长T2信号。诊断:颈4不完全脊髓损伤。康复治疗:PT、OT、理疗、针灸、按摩、中药等。
2.2 神经功能恢复 伤后1个月,全身轻触觉部分恢复。伤后6个月,双侧肱二头肌3级,伸腕肌左/右:1/0级,伸肘肌左/右:1/0级,双侧指深屈肌和小指外展肌肌力0级,左侧长伸2级,其余下肢肌力0级。伤后5年7个月,双侧最低正常感觉平面位于颈4。针刺觉:右侧颈5~胸1减退,胸2及其以下丧失;左侧颈5及其以下丧失。轻触觉:双侧颈5及其以下减退。屈肘肌左/右:4/3级;伸腕肌左/右:1/0级;伸肘肌左/右:1/0级;指深屈肌左/右:0/0级;小指外展肌左/右:0/0级;髂腰肌左/右:0/0级;股四头肌左/右:2/2;胫骨前肌左/右:0/0级;长伸肌左/右:3/0级;小腿三头肌左/右:1/1级。2.3 并发症
2.3.1 痉挛 伤后3个月腹部和下肢开始出现明显痉挛,肌张力Ashworth评分2~3级,长期联合应用巴氯芬(最大剂量30 mg,3次/d)、乙哌立松(最大剂量50 mg,3次/d)和替扎尼定(最大剂量6 mg,3次/d)抗痉挛治疗。
2.3.2 尿失禁 伤后2个半月开始频繁漏尿,联合使用琥珀酸索利那新(最大剂量10 mg,1次/d)和酒石酸托特罗定(最大剂量4 mg,2次/d)效果不佳,采取长期留置尿管。尿动力检查提示逼尿肌反射亢进。
2.3.3 神经病理性疼痛 伤后7个月开始下肢麻胀不适,开始长期口服氨酚羟考酮和普瑞巴林。此后因为腹痛的出现,需要加大每日剂量,氨酚羟考酮最大剂量5 mg,4次/d,普瑞巴林最大剂量16 mg,2次/d。
2.3.4 排便障碍 伤后1个月即开始使用开塞露辅助排便,早期每日使用20 mL,等待约数分钟后可排出成形软便。伤后半年,每日排便前需使用60 mL,排便等待时间延长。此后,每日排便前需使用的开塞露剂量不断增加,排便等待时间不断延长。伤后3年,每日排便前需使用110 mL以上,每次排便等待时间超过30 min。伤后4年,开始出现腹胀、腹痛;左半腹为主,每次持续数小时,程度不重,部位不固定,与进食、排便、体位等无明确相关性,无明确诱因和缓解因素;便常规无异常,腹部CT:乙状结肠冗长,结肠内明显积气;结肠镜检查结果:结肠壁黑化,直肠黏膜损伤。伤后6年,开始出现严重的腹胀、腹痛,患者每天晚上需要灌肠后腹胀、腹痛才能缓解,次日早上04:00—05:00又开始出现这些症状,早餐后会突然加重,每天需要服用氨酚羟考酮3~4片才能忍受腹部不适。
处理:患者曾使用乳果糖、培菲康、马来酸曲美布汀、二甲硅油片等药物口服对症治疗,也曾使用多种中成药治疗,效果不确定。使用肛管排气效果不佳。2022年9月开始使用手指牵张肛门排气,2次/d,有一定效果。建议逐步减少使用抗痉挛药物、抑制逼尿肌反射亢进药物和止疼药物,结合汤药治疗3个月,腹胀、腹痛症状基本缓解。
随访:末次出院半年后询问患者,排便1次/d,排便前用两个小开塞露(40 mL),等待约数分钟后可排出成形软便。口服巴氯芬2片(20 mg),2次/d,痉挛程度可接受。不再口服止疼药和治疗尿失禁药物。继续留置尿管。无腹胀、腹痛。腹部由原来鼓起变扁平。
3 讨论
慢性期脊髓损伤患者排便功能障碍,表现为腹胀、腹痛、痔疮、便血等情况,常常会逐步加重,可能有以下几个方面的原因。
3.1 脊髓损伤对排便的影响 脊髓损伤后肠蠕动障碍,表现为排便和排气障碍。由于每次排便后有部分粪便残留,这些残留粪便慢慢在肠道内集聚,然后被肠道内细菌分解发酵,产生大量气体,积聚在结肠和直肠内;对于骶髓以上损伤的患者,因肛门括约肌肌张力高(处于痉挛状态),使积聚在结肠和直肠内的气体无法通过肛门从身体内排出,肠道平滑肌被过度牵张,导致出现剧烈腹胀、腹痛。如果每次排便时间过长,排便后出现的直肠黏膜肿胀无法消退,则容易形成痔疮,严重时可出现脱肛。经常灌肠或反复使用开塞露可能损伤直肠黏膜导致便后出血[5]。
3.2 药物治疗的副作用 临床上用于治疗痉挛的药物,如巴氯芬、乙哌立松和替扎尼定通过抑制脊髓的运动神经元活性而降低肌张力[8],同时可抑制肠道平滑肌的蠕动;治疗尿失禁的药物,如琥珀酸索利那新和酒石酸托特罗定通过抑制膀胱逼尿肌中M受体活性而抑制膀胱逼尿肌反射亢进[9],同时可影响肠道平滑肌中M受体活性;治疗神经病理性疼痛的药物,如氨酚羟考酮[10]和普瑞巴林[11],如果长期服药均可能引起或加重便秘。
3.3 膳食纤维摄入不足 膳食纤维具有刺激肠道平滑肌蠕动的作用,如果膳食纤维数量过少,肠蠕动缓慢,可诱发或加重便秘[5]。
3.4 排便管理经验不足 主要体现在对上述药物治疗影响肠蠕动的副作用认识不足,对于膳食纤维摄入重视不够。
患者描述灌肠后腹胀、腹痛缓解,每次排出软便,量不多,但排气不少。说明灌肠的作用,不仅是排便,而且是排气。同时说明腹痛症状是胀气引起,不是神经病理性疼痛引起,为我们说服患者减少止痛药的使用提供了依据。理论上患者在肠胀气明显的情况下,使用肛管排气是正确的选择,但患者拒绝使用。原因在于,患者日常排出的是软便,采取肛管排气时容易堵塞肛管,在开始使用几次肛管排气效果不佳的情况下,患者不愿再使用。在学习新版神经源性肠道管理指南之后,我们采用指南推荐的第九条、第十七条建议,尝试使用手指牵张肛门排气,取得了比较好的效果。实施该操作后,患者的剧烈腹痛可在数分钟内彻底缓解,认为“这个办法真管用”。
使用手指牵张肛门排气对该患者虽有一定的缓解腹胀、腹痛效果,但并未解决肠蠕动减慢这一根本问题。为此,我们反复解释病情,说服患者减少各种有可能影响肠蠕动药物的使用,同时积极配合中医汤药“健脾”治疗,并保证每日膳食纤维摄入,最终取得了患者满意的治疗效果。总之,脊髓损伤患者排便功能障碍的管理,需要考虑多种因素的影响,采取综合措施和手段[12-15],值得我们给予更多关注。
