MgSO4-LiCl@MEG复合储热材料的制备与吸附储热性能
2023-09-20张雪龄谷军恒荀浩云程传晓金听祥张业强
张雪龄,叶 强,谷军恒,荀浩云,张 琦,程传晓,金听祥,张业强
(郑州轻工业大学能源与动力工程学院,河南 郑州 450002)
热储能是最具应用前景的规模储能技术之一,是未来规模储能的中坚力量[1]。热储能技术分为显热储热、潜热储热和热化学储热(TCHS)三大类。热化学储热是通过发生可逆的热化学反应来进行热量的存储和释放,具有高储热密度、工作温度范围广、可长期储热、热损失小的明显优势[2]。其中水合盐热化学吸附储热只涉及水蒸气和无机盐的化合与分解,储热温度低,绿色环保,可以应用于建筑供暖,是最具有前景的储热技术之一。
吸附储热材料一直是热化学吸附储热领域研究的热点,国内外学者针对水合盐热化学吸附储热材料制备和特性进行了大量研究。Nguyen等[3]针对MgSO4吸附能力差的问题,制备了MgSO4-珠状活性炭复合材料,吸附能力比珠状活性炭的0.138 g/g提高了2.32倍,在经过10次循环测试后表现出良好的稳定性。张叶龙等[4]采用等体积浸渍法制备的MgSO4-硅藻土复合材料的负载含盐量为51.6%,储热密度达557.1 kJ/kg,最高吸附量为0.336 g/g。Wang 等[5]采用浸渍法制备了MgSO4-硅藻土复合材料,最高吸附量为0.37 g/g,当MgSO4的质量分数达到60%,储热密度达到772.9 kJ/kg。Zhang等[6]制备了LiCl-活性氧化铝复合材料,最高含盐量为14.68%,吸附量达到0.41 g/g,导热系数为0.37 W/(m·K)。类似的,其他复合材料还有MgCl2-沸石[7]、LiCl-碳纳米管[8]等。由以上文献可知,以浸渍法为主要的制备方法,所得材料具有含盐量低、储热密度小的缺点,需要寻找更适合的制备方法;也需要寻找导热系数高、孔隙率高的多孔基质,从而改善传热性能和吸附性能及循环稳定性,提高综合储热性能。
为提高储热材料的吸附储热性能,学者们提出将不同的无机盐进行复配实现优劣互补,协同提高单一盐的吸附储热性能。Li等[9]将不同比例的LiOH与LiCl混合盐与膨胀石墨(EG)进行复配,导热系数提高到1.2 W/(m·K)左右,避免了漏液现象,储热密度为1120 kJ/kg,有效提高了吸附动力学。孙有改等[10]将LiCl 与CaCl2浸渍到活性氧化铝之中,材料的吸水率最高达到0.296 g/g。同样地,Li等[11]将MgSO4与SrCl2进行复合,最大吸水率为0.4872 g/g。不同的无机盐复配可以起到协同作用,但目前对多种盐的复配的研究较少。本工作选用低吸湿性的MgSO4和强吸湿性的LiCl 混合并调配其最佳比例,在其中添加亲水改性的膨胀石墨(MEG),采用混合球磨法制备了新型MgSO4-LiCl@MEG 复合储热材料,分析了不同MEG 含量的复合储热材料的吸附与储热性能。复合储热材料有效地改善了MgSO4的硬化结块和LiCl液解问题,实现了二元混合盐的相互促进,提高了吸水率、储热密度、动力学吸附常数、导热系数,降低了储热温度,相比其他水合盐储热材料具有良好的循环稳定性,展现出良好的应用潜能。
1 材料制备与方法
1.1 MgSO4-LiCl@MEG复合储热材料的制备
本工作选择的水合盐为上海麦克林生化科技有限公司的无水MgSO4和LiCl,纯度>99.9%。多孔介质为青岛腾盛达碳素石墨公司的膨胀石墨(EG),目数为325,并用上海麦克林生化科技有限公司的曲拉通X-100(纯度>99.9%)进行改性。
多孔碳材料EG 具有比表面积大、导热能力强、物质蓬松的优点,但与无机材料复配,存在相容性差,且材料疏水等问题[12],因此需将EG 进行亲水改性。将曲拉通X-100溶于足量的无水乙醇制成溶液,再加入EG(曲拉通X-100 与EG 质量比为1∶10),并利用超声波清洗机超声5 min,将混合均匀的样品在80 ℃的干燥箱内干燥10 h,得到亲水改性的膨胀石墨(MEG)。
为了考察曲拉通X-100 对EG 的改性效果,将改性前后干燥的膨胀石墨材料在相同的压力下进行压制,并平放在平整的实验台上,使用高速摄像机(POC.DIMAX HS4 PCO AG,德国)拍摄一滴去离子水滴落在压片表面后1 s后的形状,利用MATLAB中编写的图像分析代码对拍摄照片进行接触角测量,结果如图1 所示。改性前后EG 的接触角分别为117.8°、16.8°。改性后EG 具有较小的接触角,说明曲拉通X-100 对EG 的亲水性改性良好,亲水的表面有利于复合储热材料对水蒸气的吸附。

图1 EG改性前后的水接触角(a) 未改性EG;(b) 改性EGFig.1 Water contact angle before and after EG modification (a) unmodified EG; (b) modification EG
复合储热材料的制备如图2所示,首先添加不同比例的无水MgSO4与LiCl,然后加入去离子水配成溶液使其混合,后放入干燥箱内干燥。制备LiCl质量分数分别为10%、15%、20%、25%、30%的五种样品,分别命名为L10、L15、L20、L25、L30。对上述五种样品进行实验优选,随后将最佳比例混合无机盐与MEG 以不同的比例添加到去离子水中,充分均匀混合后,用干燥箱烘干,并进行混合球磨获得MgSO4-LiCl@MEG 复合储热材料,其中MEG 的混合比例(质量分数)分别为5%、10%、15%、20%。为了方便下面的描述,将这些复合储热材料的样品分别标记为MEG5、MEG10、MEG15和MEG20,数字表示MEG的质量分数。
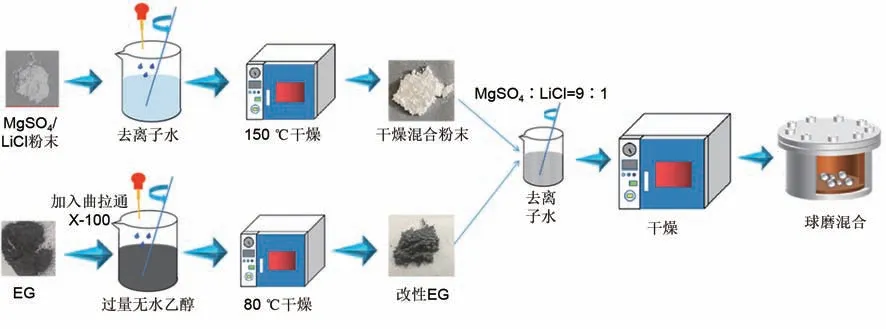
图2 复合储热材料的制备流程Fig.2 The preparation process of composite heat storage materials
1.2 实验测试与表征方法
(1) 吸/脱附特性测试
将干燥后的样品(10 g)平铺在玻璃皿中,置于恒温恒湿箱(JY-80)内(量程温度±0.5 ℃、湿度±2%RH),测试储热材料的吸附性能。每隔15 min将样品从恒温恒湿箱中取出,用天平测量一次样品的质量(天平的精度为±0.01 g),由于称重时间短(约30 秒),环境温度和湿度低(20 ℃—25%RH),称重过程中样品的质量变化可以忽略。公式(1)定义了吸附材料的单位质量吸水率W(g/g)。
式中,mt与m0分别为样品t时刻的质量与初始质量,g。
对于脱附过程,将吸附平衡后的样品置于电热恒温干燥箱中(101-3SB),测定了材料的脱水能力。测量步骤与吸附过程相同。
(2) 扫描电子显微镜测试
采用扫描电子显微镜(Sigma 300,德国)的高能电子束,扫描制备的储热材料,利用光与物质的相互作用成像,观测储热材料的微观结构与形貌特征。
(3) X射线衍射仪测试
采用X射线衍射仪(Rigaku Ultima Ⅳ,日本)对储热材料的元素成分进行检测,测量范围为20°~80°,扫描速度为2°/min。
(4) 比表面积/孔隙分析
使用比表面积/孔隙分析仪(ASAP 2460,美国)进行N2吸附测得储热材料的比表面积和孔结构数据。测试前需对样品进行预处理,在150 ℃的真空干燥箱内真空12 h,排除材料内的空气,然后在77 K 下进行N2等温吸附,从而测得储热材料的孔径信息及比表面积等数据。
(5) 差式扫描热分析
采用差示扫描量热仪(DSC Q2000,美国)测量材料的热流变化,将5~10 mg 的储热材料放入仪器的坩埚内,在25~300 ℃范围内,以2 ℃/min的升温速率扫描(温度分辨率为0.1 ℃)。N2为保护气,吹扫速度为40 mL/min。根据热流变化曲线,积分计算材料的储热密度。
(6) 导热系数分析
使用激光闪光分析仪(LFA-460,德国)测量。把复合储热材料压成直径12.7 mm、厚3 mm 的块状,放入样本模具,测储热材料的热扩散率。根据固定温度下的热扩散率、比热容和密度的乘积求得导热系数。
2 结果与讨论
2.1 MgSO4与LiCl复合比例探究
在化学吸附储热实验研究中,材料的理论吸水率是判断材料的吸附性能的重要指标。复合储热材料的理论吸水率的计算公式为
式中,a、b分别表示1 mol的MgSO4与LiCl的理论结合水量分别为7 mol 与1 mol;mx与my分别为复合储热材料中MgSO4与LiCl的质量,g;Mx与My为MgSO4与LiCl 的摩尔质量,Mh为水的摩尔质量,g/mol。
图3为不同比例混合盐在25 ℃—80%RH条件下吸附12 h 的实际吸水率与理论吸水率的对比图。单一MgSO4实际吸水率为0.691 g/g,远远小于MgSO4的理论吸水率1.05 g/g,说明其具有较差的吸附性能;单一的LiCl实际吸水率远高于理论吸水率,这是因为它为强吸湿性无机盐,在实际吸水过程中达到平衡吸水率后会继续吸水逐步形成溶液。LiCl 含盐量从10%增大到30%,即从L10 增大到L30,吸水率由1.046 g/g 增加到1.53 g/g,说明LiCl比例的增加提高了混合盐的吸附性能。效果。为了进一步改善其性能,需要后续添加适当的多孔材料。
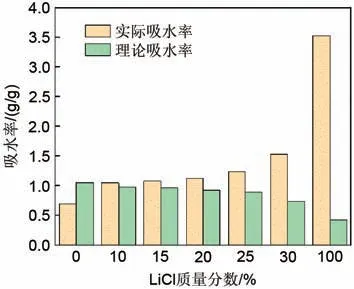
图3 不同比例混合盐吸附后理论吸水率与实际吸水率Fig.3 Theoretical and actual water absorption rates of mixed salts with different proportions after adsorption

图4 不同比例混合盐吸附后形貌图Fig.4 Morphology of mixed salt adsorption with different proportions
2.2 MEG复合储热材料的吸附和脱附性能分析
(1) 吸附性能分析
在优选出LiCl∶MgSO4的最佳质量比为1∶9的混合盐储热材料基础上,添加不同比例MEG 改善其吸附储热性能。在化学储热体系中,储热材料的水蒸气吸附速率和吸水率对其储热性能影响较大,吸附试验在25 ℃—80%RH条件下的恒温恒湿箱中进行。
图5 为不同比例MEG 复合储热材料的吸水率随时间的变化图。由图可知,4 种复合储热材料的吸水率初始阶段快速增加,在720 min左右基本稳定,达到了平衡吸水率。随着MEG 含量的增加平衡吸水率逐渐降低,MEG5、MEG10、MEG15、MEG20的平衡吸水率分别为0.985 g/g、0.925 g/g、0.891 g/g 和0.879 g/g,4 种样品通过式(2)计算的理论吸水率分别为0.903 g/g、0.882 g/g、0.833 g/g和0.784 g/g,对比可知,实际吸水率均高于该含盐量下复合储热材料的理论吸水率,这得益于MEG 提供了丰富的微观结构,从而促进了水蒸气的吸附并能“锁住”部分水分不产生泄漏。其中MEG5 具有最高的吸水率,但出现轻微液解现象。而MEG10 既有较高的吸水率(0.925 g/g),又未出现液解现象。所以应该控制MEG 的合适比例,既保障足够的含盐量提高吸水率,又能保障足够的多孔基质改善液解问题。
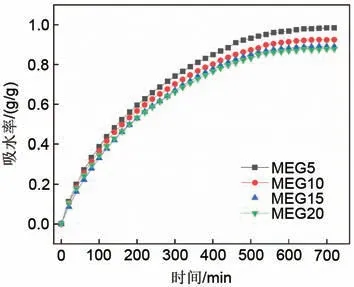
图5 不同比例MEG复合储热材料在25 ℃、RH=80%条件下的吸附特性曲线Fig.5 Adsorption characteristics of MEG composite heat storage materials with different proportions at 25 ℃ and RH=80%
在化学储热体系中,了解吸脱附反应过程中的机理是非常重要的,在以往的研究中可以用Clausius-Clapeyron方程来描述[14]:
式中,Δh、R、peq与T分别表示为反应焓(kJ/mol)、通用气体常数[J/(mol·K)]、平衡压力(Pa)和平衡温度(K)。由上述公式可知,材料在化学吸附过程中水蒸气的温度与分压是影响材料放热性能的重要参数,所以探究温度与压力对吸附过程的影响是非常有必要的。
图6(a)为相同水蒸气分压下不同温度下(pv=2.5 kPa,温度25 ℃,80%相对湿度的水蒸气分压)四种材料平衡吸水率的对比。由图可知,随着环境温度的升高,4 种复合储热材料的平衡吸水率逐渐降低,且4种样品的平衡吸水率的差别越来越小。由于吸附过程是一个放热的过程,所以随着温度的升高,材料的放热能力减弱,材料的吸水率也随之减小。

图6 不同比例MEG复合储热材料在 (a) pv=2.5 kPa时不同温度;(b) 25 ℃时不同湿度下的平衡吸水率Fig.6 The equilibrium water absorption of MEG composite heat storage materials with different proportions at(a) pv=2.5 kPa at different temperatures and (b) 25 ℃ at different humidity
图6(b)为相同温度(25 ℃)不同湿度下(水蒸气分压不同)4 种材料的平衡吸水率的对比。由图可知,随着环境相对湿度的增加,4 种复合储热材料的平衡吸水率逐渐提升。这说明较高的相对湿度有利于提升材料的吸附性能,这与公式(3)相吻合,即提高平衡水蒸气分压,可以增大反应焓,这是因为提高了吸水率,增大了放热量。这为材料的系统应用提供了思路,在保证环境温度的同时,尽可能地提高材料环境的相对湿度,以达到充分放热的目的。
(2) 吸附动力学分析
对于热化学吸附储热材料的吸附动力学,一般采用线性驱动力学模型(LDF)来描述[15]。该模型表示了吸附速率和平衡吸水率与当前吸水率的差值之间的关系,具有计算简单准确等优点[16]。其数学表达式如下所示。
式中,t为时间,min;x为复合储热材料在当前时间点的吸水率,g/g;ks为吸附速率常数,s-1;xeq为复合储热材料达到平衡状态的吸水率,g/g。
对上述公式进行积分变换可得
此式引入无量纲吸附量X,x0为吸附过程初始时刻的吸水率(g/g)。
将复合储热材料在25 ℃—80%RH条件下的动态吸附结果代入方程(5)进行无量纲处理,表1 为4 种MEG 复合储热材料拟合实验数据得到的吸附速率常数结果。由表可知,四种复合储热材料的拟合效果较好,其拟合系数R2均达到了0.99,说明了LDF模型能够描述复合储热材料的吸附过程。四种复合储热材料的吸附速率常数ks差异不大,均在0.005 s-1左右。其中MEG10 有着最高的吸附速率常数ks,其值为0.00504 s-1。MEG15的吸附动力学常数最小为0.00491 s-1,说明吸附速率最慢。对比MgSO4的吸附动力力学常数1.67×10-5s-1[17],MEG复合储热材料的吸附动力学特性得到了有效提高,使材料拥有较快的吸附反应速率。

表1 不同比例MEG复合储热材料在25 ℃、RH=80%的吸附速率常数Table 1 Adsorption rate constants of MEG composite heat storage materials with different proportions at 25 ℃ and RH=80%
为了更好地展现LDF模型的拟合效果,给出了最高吸附速率常数MEG10 的拟合图像,如图7 所示。ks是化学反应速率的关键参数。在本研究中,MEG10 复合储热材料的ks高达0.00504 s-1,比以往研究的几种复合储热材料高10倍以上,如表2所示。复合储热材料大的反应动力学常数可以加快放热反应速率,提高放热功率。

表2 吸附速率常数对比Table 2 Comparison of adsorption rate constants
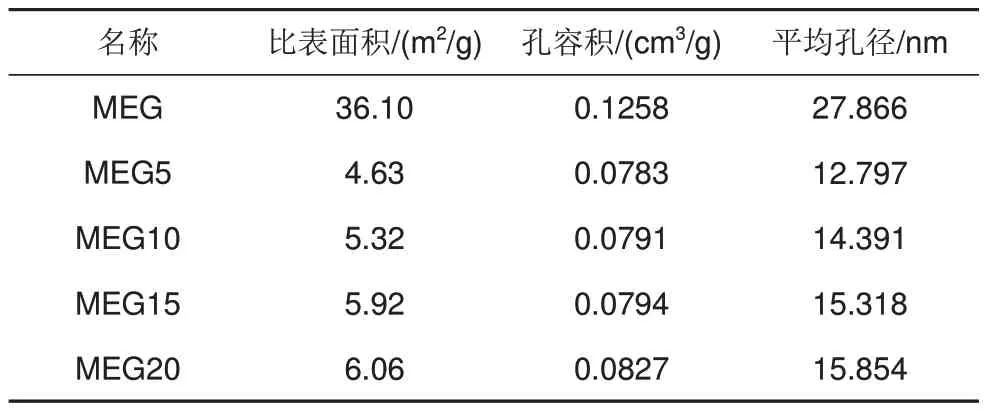
表3 材料的比表面积、孔容积和平均孔径的测试结果Table 3 Tests of specific surface, pore volume and average pore size of materials
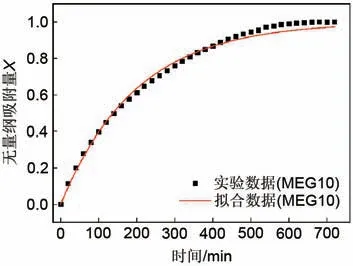
图7 在25 ℃、RH=80%条件下MEG10的吸附动力学曲线Fig.7 Adsorption kinetics curve of MEG10 at 25 ℃,RH=80%
(3) 脱附性能分析
图8显示在25 ℃—80%RH条件下,吸附平衡后的MEG5、MEG10、MEG15、MEG20四种复合储热材料在150 ℃条件下的脱附过程吸水率随时间的变化曲线。四种样品在前60 min,吸水率快速下降,60~120 min 吸水率缓慢下降,到120 min 后吸水率保持稳定不再变化,四种储热材料的吸水率由 初 始 的0.985 g/g、0.925 g/g、0.891 g/g 和0.879 g/g 降低为最终的0.149 g/g、0.133 g/g、0.136 g/g、0.121 g/g,脱水率均大于84%。且脱水过程中吸水率由下降达到平衡的先后顺序为MEG20,MEG15,MEG10,MEG5,说明随着MEG 含量的增加,解吸速度加快。达到脱附平衡时,随着MEG含量的增加,最终吸水率逐渐降低,但均不能降低到0,这是由于150 ℃的脱附温度不能使MgSO4与LiCl 的水合盐完全脱水。四种储热材料在120 min均可达到脱附平衡,这满足了系统快速储热的需求。
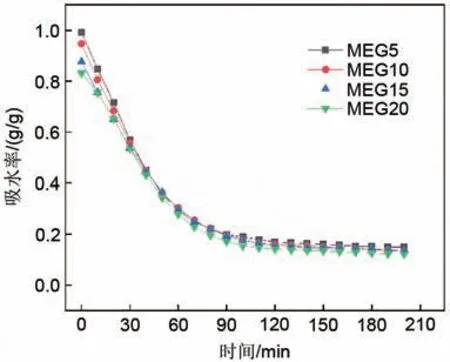
图8 不同比例MEG复合储热材料在25 ℃、RH=80%条件下吸附平衡后150 ℃的脱水特性曲线Fig.8 The dehydration characteristic curves of MEG composite heat storage materials with different proportions at 150 ℃ after adsorption equilibrium at 25 ℃ and RH=80%
2.3 MEG复合储热材料的形貌特征与XRD测试结果分析
图9为MgSO4、MEG和四种不同MEG比例复合储热材料的SEM 图,在环境状态下LiCl 快速吸水成液态无法制样观测其微观结构。观察图9(a)MgSO4为形状不规则的堆积结构。图9(b)可以看出MEG 有清晰的鳞片层状结构,其层状的孔隙结构增加了孔隙空间。图9(c)~(f)显示了四种MEG 复合储热材料的形貌结构,由图可以看出MEG 的层状孔隙有效地负载了无机盐,大量颗粒物均匀分散在MEG 的孔隙结构间,覆盖了层状结构;随着MEG含量的增加,暴露的MEG的层状结构逐渐增加,可以增加水蒸气的传质通道。

图9 不同材料的SEM测试(a) MgSO4;(b) MEG;(c) MEG5;(d) MEG10;(e) MEG15;(f) MEG20Fig.9 SEM test of different materials:(a) MgSO4; (b) MEG; (c) MEG5; (d) MEG10; (e) MEG15; (f) MEG20
图10 给出了MEG、MgSO4、LiCl 和四种复合储热材料的XRD 图谱。经标准卡片库对比可知改性膨胀石墨在26°和54°分别有一个较强的衍射峰和一个小衍射峰,这与先前研究的描述相对应[20]。MgSO4的衍射峰在18.1°、25.8°和34.8°处出现,LiCl 的衍射峰在29.6°、34.2°、49.5°和58.1°处。四种复合储热材料中均能观察到MEG、MgSO4和LiCl 的衍射峰。LiCl 的衍射峰较弱,在34.2°、49.5°、58.1°处可观察到,是由于LiCl 含量过低。四种复合储热材料都可以清晰地看到MgSO4在18.1°、25.8°和34.8°处的衍射峰。复合储热材料在26°和54°处为MEG 的衍射峰,且随着MEG 含量的增加其峰值增高。四种复合储热材料没有新的衍射峰出现,说明无机盐和MEG 的复合仅为物理过程,没有生成新物质。
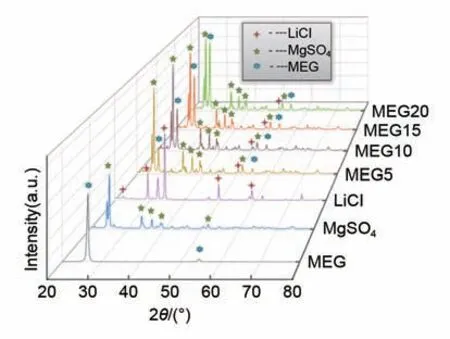
图10 MEG、MgSO4、LiCl和四种复合储热材料的XRD曲线Fig.10 XRD curves of MEG, MgSO4, LiCl and four kinds of composite heat storage materials
2.4 MEG复合储热材料的比表面积/孔隙测试结果分析
内被盐占据的孔隙减小,被填充的孔隙减小,从而平均孔径增大。
2.5 MEG 复合储热材料的导热系数测试与DSC测试
储热材料的导热系数决定了储热系统的传热性能。图11 给出4 种不同MEG 含量的复合储热材料的导热系数。如图所示,随着MEG 含量的增加,复合储热材料的导热系数显著增加,由MEG5 的0.97 W/(m·K)增加到MEG20 的3.58 W/(m·K),导热系数提升了72.9%。对比单一MgSO4导热系数[0.122 W/(m·K)],最低实现7.95 倍的提升。这是因为MEG的导热系数为6.1 W/(m·K),这远高于硅胶[0.174 W/(m·K)]、活性氧化铝[0.28 W/(m·K)]和沸石分子筛[0.07 W/(m·K)]等传统多孔介质,从而使以MEG为基体的复合储热材料导热系数得到明显提高。对比之前的文献研究,Zhang等[4]制备的LiCl-活性氧化铝最高导热系数为0.37 W/(m·K);LiOHLiCl@EG复合材料的导热系数为1.2 W/(m·K)[6];MgSO4-CaCl2@13X分子筛的导热系数为0.421 W/(m·K)[21],本工作所制备的复合储热材料的导热性能得到了有效提高,材料高的导热系数使TCES系统拥有更优异的传热性能。
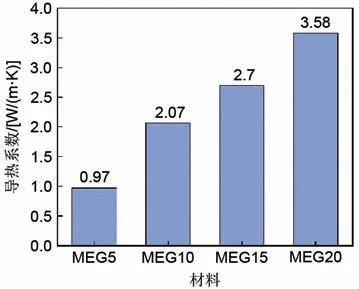
图11 MEG复合储热材料的导热系数Fig.11 Thermal conductivity of MEG composite heat storage material
图12(a)为MgSO4与LiCl水合物的DSC测试曲线,对热流曲线进行面积分获得储热密度(HSD)。由于MgSO4在100 ℃内即可完成大量脱水,所以主要脱水峰值为83 ℃,在150 ℃内的总的脱附热(储热密度)为824 kJ/kg,在实际吸附过程中由于MgSO4的硬化结块现象使其低于其理论储热密度,除此以外,MgSO4水合盐在155 ℃有一个小的脱水峰值。LiCl存在一个99 ℃峰值的强脱水峰,这与先前文章的测试结果相似[4],且在196 ℃处也存在一个脱水峰,其脱附HSD 为942 kJ/kg。由图12(b)可知,四种复合储热材料随着MEG 含量的增加,其峰值面积逐渐降低,MEG5、MEG10、MEG15、MEG20 的HSD 分 别 为1039 kJ/kg、957 kJ/kg、812 kJ/kg 和738 kJ/kg;且随着材料MEG 含量的升高,脱附峰值温度向左偏移,峰值温度分别为122.4 ℃、115.2 ℃、110.7 ℃、109.3 ℃,这一方面与MEG高的导热系数有关,随着MEG含量的增加,材料的导热系数逐渐增加,降低了温度传导的阻力,从而降低了材料的峰值温度[12,22];另一方面,由于MEG 的添加可以明显改善反应动力学,降低了反应阈值,从而降低了解吸温度和解吸焓,提高了解吸速率,这与图8的脱附过程相一致,这在文献中也有发现[23-24]。储热峰值温度的降低有利于降低储热材料的热源温度,有利于储存低品位的热源。

图12 (a) MgSO4、LiCl 和 (b) MEG复合储热材料的DSC曲线Fig.12 DSC curve of (a) MgSO4, LiCl and (b) MEG composite heat storage material
复合储热材料的吸附储热性能需要对储热密度、导热系数、吸水率、吸附动力学、储热温度等进行综合考虑,尤其是储热密度和导热系数的影响最为重要。本工作中针对4种不同MEG质量含量的复合储热材料,储热密度随着MEG 含量的增加逐渐减小,但MEG5 出现液解现象,MEG10 拥有最高的储热密度且未液解;导热系数随着MEG含量的增加而逐渐提高,且MEG10相对MEG5提升幅度最大,达到较高值2.07 W/(m·K),超过MEG10 后,随着MEG含量增加,导热系数的提升速度较慢。因此,综合考虑储热密度和导热系数两方面的影响,优选MEG10 为本研究制备的最佳复合储热材料。同时在不液解的情况下,MEG10拥有最高的吸水率,在25 ℃—80% RH 条件下吸水率为0.925 g/g,最高吸附动力学常数0.00504 s-1,较低的储热峰值温度115.2 ℃,有利于低品位热源的储存与利用。
将MEG10 复合储热材料与前人报道的储热材料进行了对比,如表4所示,可知本工作制备的复合储热材料具有高的吸附能力、质量储热密度和导热性能,可应用于中低温化学吸附储热系统。

表4 MEG10实验结果与文献对比Table 4 Comparison of MEG10 experimental results with literature
2.6 MEG10复合储热材料稳定性测试
对复合储热材料进行了40 次循环试验,试验的吸附过程在恒温恒湿箱内进行,条件为25 ℃—80%RH;脱附过程在电热恒温干燥箱内进行,条件为150 ℃。为了比较材料的吸附过程和脱附过程的吸水率将其归一化为Nad和Nde,表示为
式中,Wad,i和Wde,i(i=1,2…10)分别为复合储热材料在25 ℃—80%RH下的平衡吸水率(g/g)和在150 ℃下的脱水率(g/g)。
图13 显示了MEG10 经过40 次脱附与吸附的吸脱水率与HSD 的对比图。经过40 次循环后,MEG10 的HSD 由957 kJ/kg 下降到676.1 kJ/kg,下降约29.4%,无量纲的吸脱附过程的吸水率分别下降15.1%和19.6%。对比分析LiOH的HSD,10次循环后HSD 下降约31.4%[23],CaCl2-MgSO4@13X的HSD 循环10 次后降低了约15%[21],浸渍在金属有机框架复合储热材料中的SrBr2的Nad和Nde在5次循环后下降了9.5%[27],这充分说明了MEG10复合储热材料具有良好的循环稳定性。
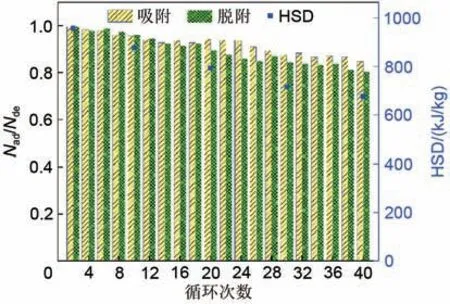
图13 MEG10复合材料的循环稳定性Fig.13 Cyclic stability of MEG10 composites
3 结 论
本工作采用混合球磨法制备了MgSO4-LiCl 混合无机盐与MEG 复配的新型复合储热材料,并对材料进行了吸脱附和储热性能测试,主要结论如下。
(1)MgSO4和LiCl的混合盐中,LiCl占比10%的样品为最佳配比,提高了吸水率,达到1.046 g/g,改善了MgSO4的结块硬化问题,但材料存在微弱液化问题。
(2)对优选的混合盐添加4种不同比例的MEG,复合材料的吸水率随着MEG含量的降低而升高,随湿度的增加和温度的降低而提高,均在120 min达到脱附平衡。但MEG5发生液解,MEG10表现出最优的吸附性能,吸水率达到0.925 g/g,吸附动力学常数最高,为0.00504 s-1,储热密度为957 kJ/kg,储热峰值温度为115.2 ℃,导热系数为2.07 W/(m·K),比MgSO4提高16.97倍。
(3)SEM 结果和XRD 元素分析表明,混合盐均匀物理分散在MEG 的片状孔隙结构内。复合储热材料的比表面积、孔容积和平均孔径随着MEG含量的增加而增加。
(4)对优选的MEG10进行40次循环测试,其吸脱附性能分别下降15.1%和19.6%,储热密度下降29.4%,储热材料表现出良好的循环稳定性。采用混合球磨法制备的改性膨胀石墨-复合水合盐吸附储热材料,可以大大提高含盐量、储热密度和导热系数,为高密度长周期储热技术提供较好的指导参考。
