重组人源化胶原蛋白促进创面修复研究及其医用敷料应用
2023-09-19何杜鹃马旭刘盛徐剑南毛小华
何杜鹃,马旭*,刘盛,徐剑南,毛小华
(1.长沙聚源医疗科技有限公司,湖南浏阳 410300;2.浙江诸暨聚源生物技术有限公司杭州分公司,浙江杭州 310051)
胶原蛋白由三条左旋多肽α-链缠绕而成,是细胞外基质的主要成分。近年来,随着胶原蛋白提取制备技术的发展,市场发展迅速,2022 年全球胶原蛋白市场规模为91 亿美元,预计从2023 年到2030 年将以10.2%的复合年增长率(CAGR)增长[1]。其中,天然胶原占比相对较大,是从动物组织、皮肤提取物获取,但其具有免疫原性、病毒传播等风险,加工性弱,限制开发[2-6]。重组胶原是由基因工程菌制备,无病毒隐患、生物相容性高、水溶性优良,被广泛用于组织工程、生物医学、药物释放等领域[7-9]。据统计,2021 年我国重组胶原市场规模已达到108 亿元,预计2027 年将扩增至千亿。近年来,国家市场监督管理总局陆续发布文件,鼓励重组胶原产业创新和高质量发展[10-12]。国内胶原企业已突破重组胶原生产技术瓶颈,可实现规模化生产[13-14]。本研究选用江苏江山聚源生物技术有限公司生产的重组人源化胶原蛋白开展细胞、动物功效研究和透皮研究,以贴敷料产品开展医用敷料性能和生物安全性研究,同时收集已有重组胶原蛋白医用敷料临床文献,评估该原料制备医用敷料的应用前景。
1 材料与方法
1.1 材料、试剂及仪器
重组人源化胶原蛋白(分子量为55 000 Da),江苏江山聚源生物技术有限公司;硫乙醇酸盐流体培养基、胰酪大豆胨液体培养基、L-929 小鼠成纤维细胞系,美国菌种保存中心(ATCC);新西兰兔、豚鼠(天竺鼠),无锡恒泰实验动物养殖有限公司;二月龄大白猪、磷酸盐缓冲液(PBS)、角质形成细胞,广东博溪生物科技有限公司;CLM-170B-8-NF CO2培养箱,新加坡ESCO 公司;SW-CJ-2FD 超净工作台,苏州安泰空气技术有限公司;PHS-3C pH 计,上海仪电科学仪器股份公司;KDN-19H 自动定氮仪,上海纤检仪器有限公司;Permergear 扩散池,世联博研(北京)科技有限公司。
1.2 重组人源化胶原蛋白促进创面修复研究试验
1.2.1 细胞试验
开展重组人源化胶原蛋白(RHC)对成纤维细胞和表皮细胞的促细胞增殖、迁移试验[15]。
1.2.1.1 促细胞增殖试验
取生长良好细胞制成单细胞悬浮液并统计数量,使细胞密度为104个/mL,接种于96 孔板,每孔加入200μL 细胞悬浮液,待细胞贴壁后,加入待测样品(浓度为0.01%、0.05%、0.10%),每个样品设置9 个复孔,放置在37 ℃和5% CO2培养箱中连续孵育48 h 后移除培养基,每孔用200 μL PBS 清洗。去除洗涤液后,向30 mL 培养基中添加15 mg 噻唑蓝(MTT)制备MTT-培养基溶液,向每个培养孔中加入200 μL MTT-培养基溶液,然后在37 ℃和5% CO2条件下培养3 h。快速翻转培养板,弃去上清液,向每孔加入150 μL 二甲基亚砜(DMSO),振荡10 min,使MTT蓝紫色结晶完全溶解。用酶联检测仪检测各孔在490 nm 处的吸光值(OD490值),同时设置无细胞孔作为对照组进行调零,取6 孔平均值。
1.2.1.2 细胞迁移试验
细胞铺板:先用记号笔在6 孔板背后用直尺均匀划横线,每隔0.5 ~1.0 cm 一道,横穿过孔。每孔至少穿过3 条线。在孔中加入约5×105个细胞,具体数量因细胞不同而异,基本为过夜能铺满。划痕实验:第2 天用枪头比着直尺,尽量垂直于背后的横线划痕,枪头要垂直,不能倾斜。用PBS 清洗细胞3 次,去除划下的细胞,以不加入药物的无血清培养基为对照组,加入待测样品为实验组,终浓度为0.01%、0.05%和0.10%,放入37 ℃、5% CO2培养箱培养。按0 h 和24 h 取样,拍照。用ImageJ-win 64 软件测量划痕面积并计算每组的细胞迁移速率。细胞迁移速率=固定划痕区移行细胞的总面积/初始划痕区面积×100%。
1.2.2 豚鼠湿疹模型试验
选用豚鼠模型,利用2,4-二硝基氯苯(DNCB)一次性大剂量致敏,多次小剂量激发的方法诱发豚鼠湿疹皮炎模型[16]。选用豚鼠70 只,随机分为5 组(每组14 只,考虑试验操作成功率,实际8 只),包括致敏模型组4 组和空白对照组(无致敏操作),其中3 组致敏模型当天涂抹给药,分别给予1%重组人源化胶原蛋白(RHC)100 μL、200 μL 以及400 μL,致敏模型空白组和空白对照组给予同等溶剂(0.9%氯化钠注射剂)。每日给药1 次,连续给药30 d,研究5 个实验组病理学变化。
评判标准:试验组、模型组和对照组末次给药后2 h 处死豚鼠,耳朵处打孔取材制作切片,进行常规病理学检测并观察其组织学改变,对表皮增厚、角化过度、血管扩张、内皮肿胀和间质水肿情况进行评分,根据严重情况评分(0 ~2 分),将这些指标评分相加(8只实验动物评分)后进行数据统计,使用SPSS 25.0 进行统计学分析。
1.3 重组人源化胶原蛋白医用敷料应用研究试验
1.3.1 重组人源化胶原蛋白修护贴敷料制备
取纯化水溶解搅拌卡波姆;加纯化水溶解羟苯甲脂、乙二胺四乙酸二钠和甘油(需加热);冷却后,合并上述两种溶液,再加入纯化水预溶的三乙醇胺和重组人源化胶原蛋白,搅拌均匀定容,灌装,灭菌。
1.3.2 完整和浅表创口透皮吸收试验
测试方法依据《化学品 皮肤吸收 体外试验方法》(GB/T 27818—2011)[17]。供试完整皮肤选用2 月龄大白猪腹部皮肤,去除脂肪和毛发组织,生理盐水浸泡后常温保存备用。上述完整皮肤用手术刀制造5 mm 长度的浅表创口作为浅表创口皮肤,用生理盐水浸泡,常温保存备用。
扩散池:15 mL;接收池:50 mL,液体均为pH 7.0 的PBS 缓冲溶液;实验组分别配制0.05%、0.10%、0.50%、1.00%的重组人源化胶原蛋白开展试验。
1.3.3 基本性能检测
取上述修护贴敷料,依据《重组胶原》(YY/T 1849—2022)[12]和《中华人民共和国药典(2020 版)》[18]检验方法开展外观(目视、手感、鼻嗅)、pH 值和总蛋白含量的检测。
1.3.4 生物学试验
按照GB/T 16886.1—2022[19]要求,根据贴敷料预期和人体表皮短期接触开展体外细胞毒性[20]。开展细胞毒性利用MEM 培养基于37 ℃条件下浸提样品24 h,取样品终浓度100%、75%、50%、25%开展试验,同时设置阴性(高密度聚乙烯处理)和阳性(二乙基二硫代氨基甲酸锌处理)对照组以及皮肤刺激[21]和皮肤致敏试验[21],验证修护贴敷料的生物相容性。
1.4 重组胶原蛋白敷料临床应用
通过检索数据库,如中国期刊全文数据库、万方数据库、维普数据库(1999—2023 年),收集相关重组胶原临床应用文献汇总统计相关数据。
2 结果与分析
2.1 重组人源化胶原蛋白促进创面修复研究
2.1.1 重组人源化胶原蛋白对细胞生长和迁移的促进作用
胶原蛋白及其衍生片段调控许多细胞功能,如细胞形状维持,细胞分化、迁移和许多蛋白质的合成[22],在创面愈合过程中刺激细胞活性,吸引细胞定向迁移到伤口部位促进新胶原基质的沉积等[23]。李滨等[15]研究发现,重组胶原蛋白(2 000 Da)能明显促进细胞(成纤维细胞和表皮细胞)生长和细胞迁移,起效浓度为0.002 5%。本次试验选用重组人源化胶原蛋白(55 000 Da),开展对表皮细胞和成纤维细胞的生长促进和划痕试验细胞迁移研究,见图1 和图2。可以看出,敷料常用浓度(0.01%~0.10%)均能促进细胞生长活性和细胞迁移,重组人源化胶原蛋白对表皮细胞生长活性和细胞迁移的促进作用明显,且具有一定的浓度依赖性。
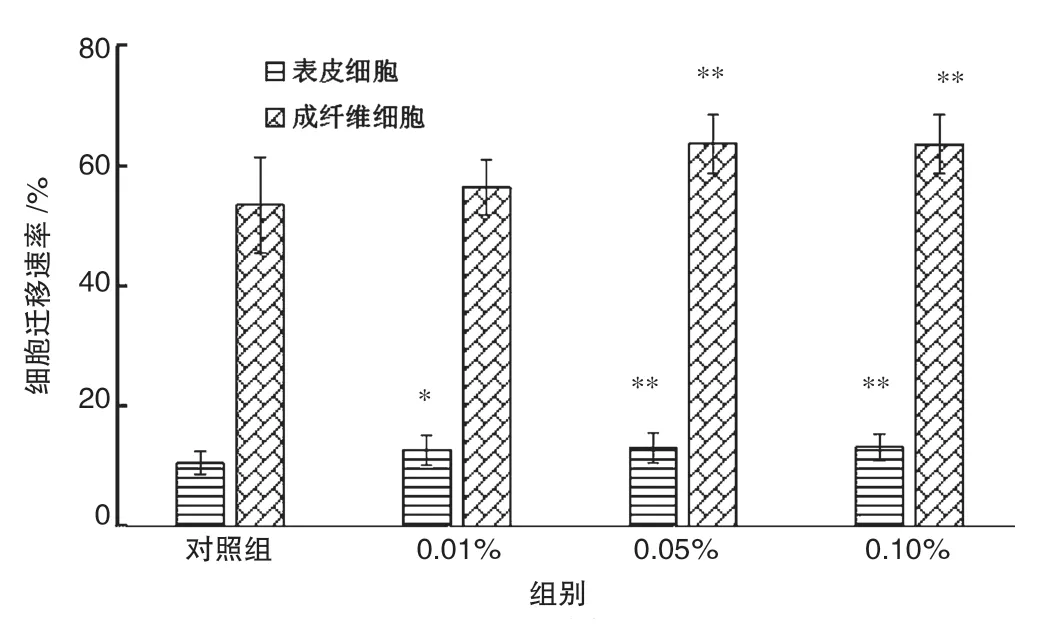
图2 细胞在不同重组人源化胶原蛋白浓度的迁移速率
2.1.2 重组人源化胶原蛋白对DNCB 所致豚鼠湿疹皮炎的修复作用
湿疹皮炎包含湿疹、脂溢性皮炎、接触性皮炎等,会严重影响患者工作生活。豚鼠试验组病理学切片评分统计结果见图3,可见皮炎模型组耳部评分(9.00 分)显著高于空白对照组(3.13 分)(P<0.01)。病理切片光学显微镜观察结果见图4,模型对照组皮肤组织病灶区表皮显著增生,皮肤附属器减少,分布欠均匀,乳头层血管增生伴炎症细胞浸润;重组人源化胶原蛋白3个剂量实验组耳部组织表皮完整伴轻度角化,局灶区表皮轻度增生,真皮层胶原纤维排列有序,皮肤附属器分布正常,乳头层血管轻度增生,未见明显炎症细胞浸润。重组人源化胶原蛋白400 μL 实验组病理学组织评分显著低于模型组,表明重组人源化胶原能有效改善湿疹皮炎损伤后耳部皮肤的病理学变化。
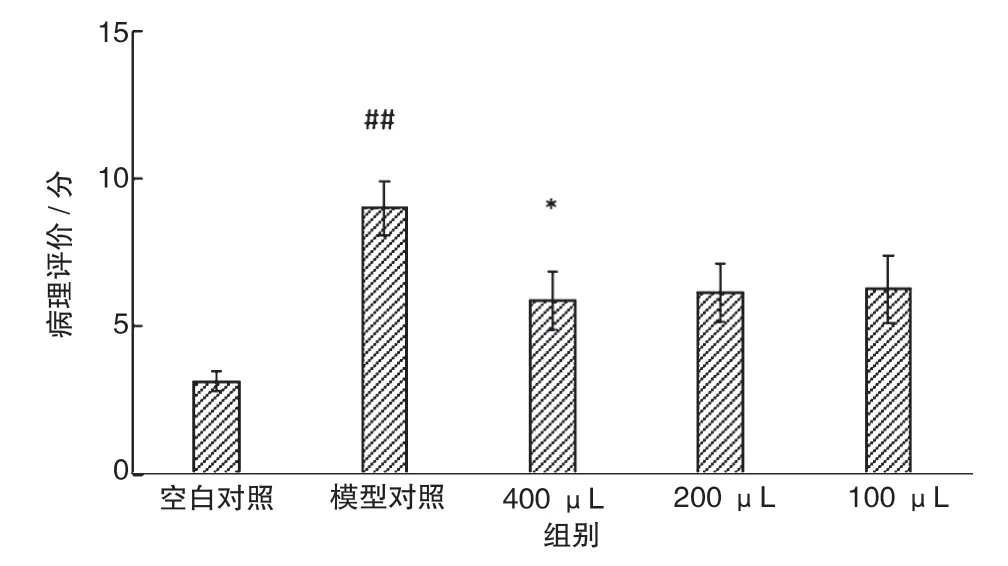
图3 重组人源化胶原蛋白对湿疹皮炎豚鼠耳朵皮肤影响的病理学评分
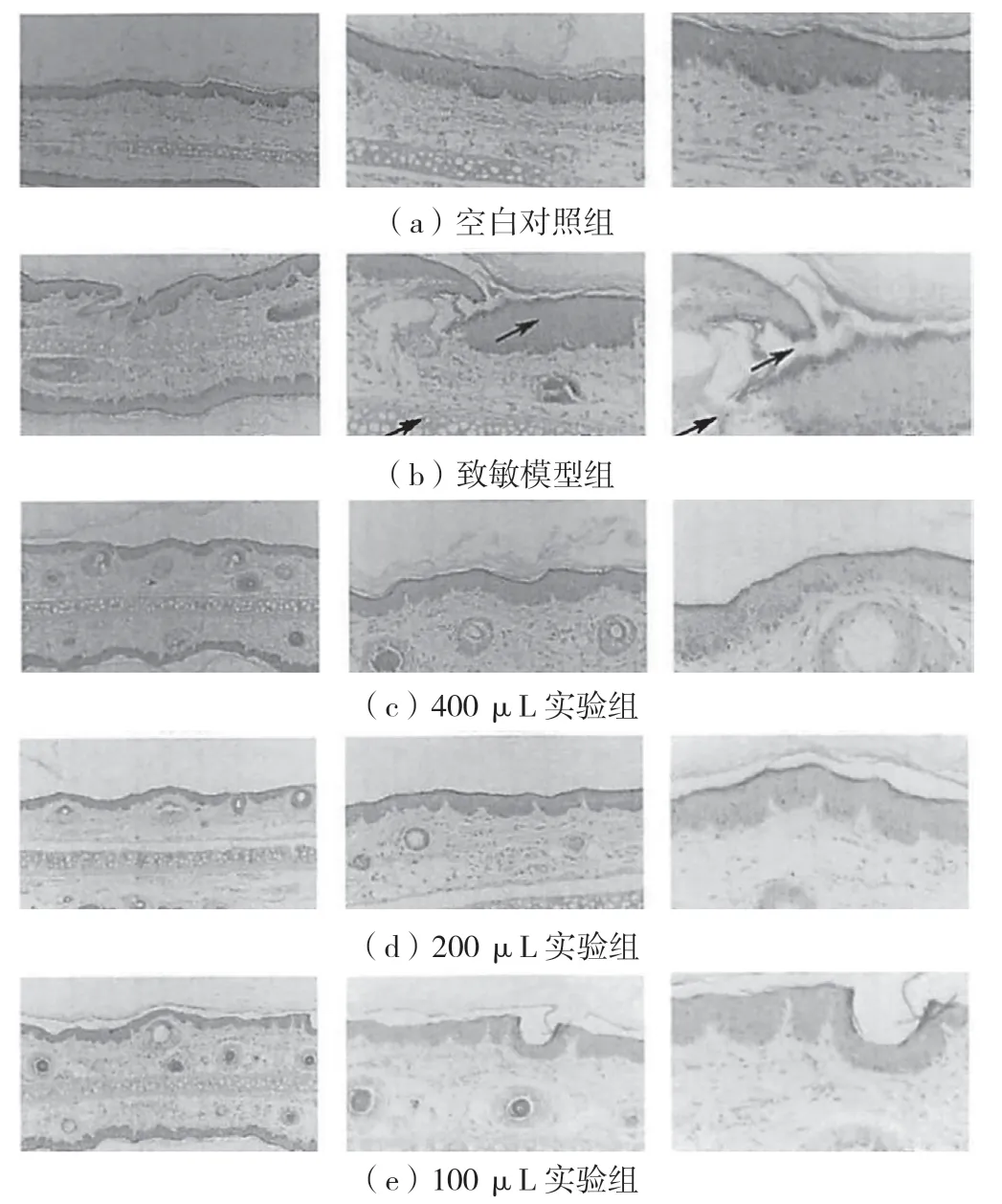
图4 不同组别的湿疹皮炎豚鼠耳朵皮肤病理学结果(HE 染色)
2.2 重组人源化胶原蛋白医用敷料应用研究
2.2.1 重组人源化胶原蛋白(RHC)透皮试验结果
收集相应时间点的接收液利用高效液相色谱检测重组人源化胶原蛋白,采用面积归一法计算。结果发现重组人源化胶原蛋白(0.05%、0.10%、0.50%以及1.00%实验组)在24 h 内未出现透皮吸收现象。浅表创面透皮试验发现,1.00%重组人源化胶原蛋白在24 h 内未出现创面透皮吸收现象(表1)。重组胶原蛋白在基因构建时,可通过控制氨基酸含量控制重组胶原蛋白的分子量。本研究所用重组胶原分子量为55 000 Da[24],表皮非慢性创面敷料应用时,不会被人体吸收,符合Ⅱ类医用敷料应用基本要求。
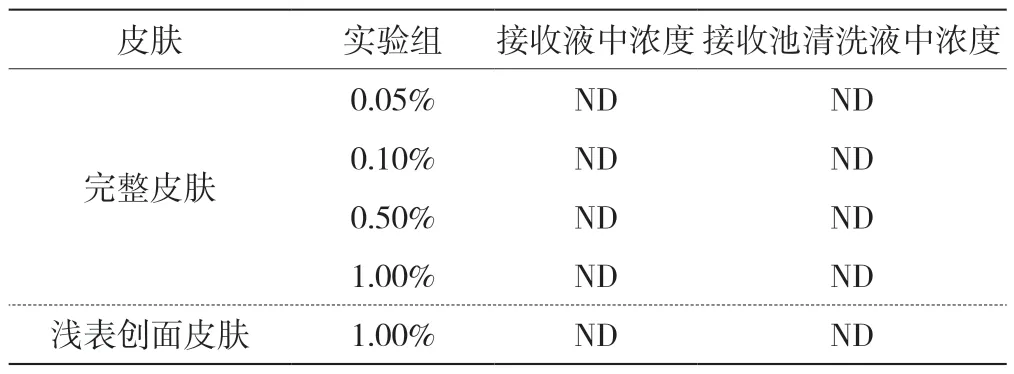
表1 重组人源化胶原蛋白24 h 皮肤透皮量(单位:mg/L)
2.2.2 重组人源化胶原蛋白修护贴敷料基本性能
对重组人源化胶原蛋白修护贴敷料开展外观、pH 值、总蛋白含量的基本性能检测,结果见表2。外观检测结果证明选用膜布和药物辅料原料,在洁净车间生产,终端灭菌后产品可达到外观要求;pH 值满足产品预期人体表皮使用要求(表皮pH 为4.0 ~7.5)[25];总蛋白含量根据原料对比研究氮转化蛋白系数,降低非蛋白氮误差,可确保对产品含量的把控。

表2 重组人源化胶原蛋白修护贴敷料基本性能检测结果
2.2.3 重组人源化胶原蛋白修护贴敷料生物学性能
观察重组人源化胶原蛋白修护贴敷料样品浸提液对L-929 细胞形态的影响,发现无负面影响,细胞培养良好;细胞毒性生物学定量检测结果如图5,实验组细胞活性数值和阳性对照组均存在显著差异(P<0.01),其中100%样品浸提液组在孵育细胞24 h 后细胞形态基本完好,细胞活力值为73.99%,证明无细胞毒性。皮肤刺激试验过程中动物未出现异常症状或死亡,样品对皮肤无刺激作用。皮肤致敏试验中,动物皮肤完好,未出现红斑和水肿反应,样品不会引起皮肤致敏反应。上述试验结果均证明重组人源化胶原蛋白修护贴敷料医用敷料应用能满足医疗器械生物相容性要求。
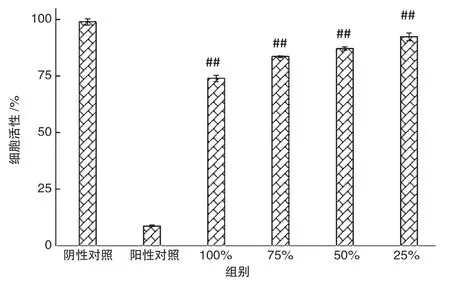
图5 重组人源化胶原蛋白修护贴敷料MTT 细胞毒性检测结果
2.3 重组胶原蛋白临床应用
根据《重组胶原生物材料命名指导原则》,重组胶原蛋白医用敷料产品名称中的核心词根据重组胶原蛋白制备基因片段的来源不同,主要分为“重组人胶原蛋白”“重组人源化胶原”和“重组类胶原蛋白”[11];根据对已上市产品收集,医用敷料名称特征词也包含“酵母重组胶原”“类人胶原蛋白”等。根据上述关键词组合筛选数据库获取到临床应用文献共计40 余篇,涵盖不同品类和用途,见图6。其中贴敷料产品临床应用最早,占比最多(56.25%);皮炎以及术后修复、皮肤屏障的应用最多。通过文献查阅信息收集发现重组胶原蛋白医用敷料临床应用均无不良反应反馈,重组胶原联合激光等术后应用均展现良好的相容性,能缓解术后疼痛,促进创面恢复,皮肤屏障功能修复效果良好[26-29]。重组人源化胶原蛋白满足行业标准《重组胶原》(YY/T 1849—2022)要求。
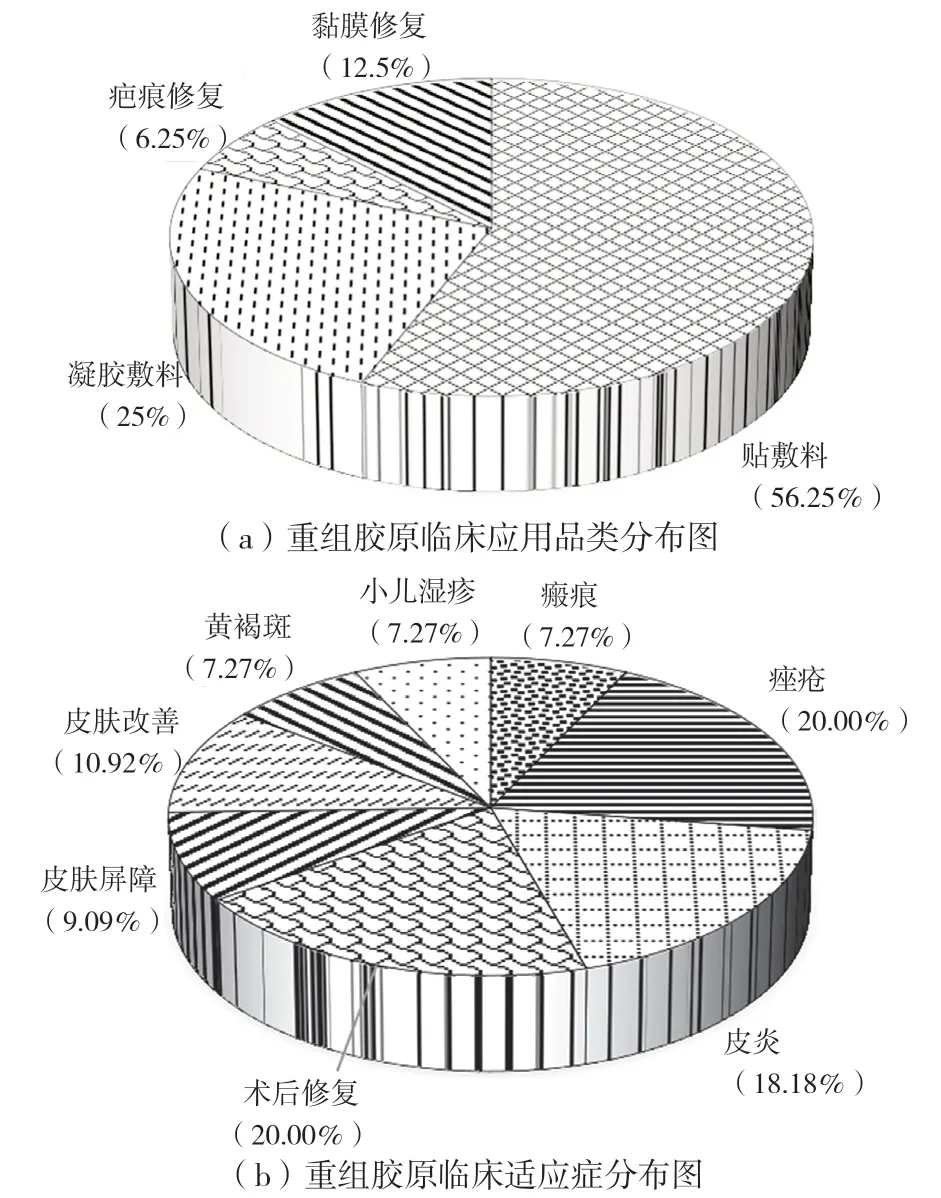
图6 重组胶原蛋白临床应用文献产品品类及应用分布情况
3 讨论与结论
皮肤具有致密的“砖墙结构”,是化学物质透皮吸收的主要屏障,一般只允许水、电解质等结构简单的小分子物质通过[30]。研究人员通过酶解胶原扩散池试验发现,胶原蛋白肽分子质量越大,透皮吸收能力越小[31-32];本研究选用猪腹皮肤[33]发现重组人源化胶原蛋白在皮肤表层短暂(<24 h)使用时,不会透皮吸收,进入血液,不参与人体内循环。表皮细胞和成纤维细胞的促生长和迁移试验结果证明重组人源化胶原在细胞层面发挥结构和功能作用;豚鼠动物模型试验切片能直观分析重组人源化胶原蛋白对病理变化的影响。修护贴敷料性能和生物学评价满足敷料产品基本使用要求。临床文献发现,重组人源化胶原含量≥0.1 mg/mL 可抑制和缓解皮炎、敏感性肌肤、痤疮、激光治疗后等各种原因引起的皮肤炎症反应,促进创面愈合与皮肤修复,缩短病程[34-35]。重组人源化胶原(55 000 Da)在医用Ⅱ类表皮接触敷料的应用可大力开发。
