CT模拟定位机在调强放疗位置验证中的应用
2023-09-19齐洪志杨玉刚郝洁许林尚革
齐洪志,杨玉刚,郝洁,许林,尚革
新疆医科大学第一附属医院 肿瘤中心,新疆 乌鲁木齐 830054
引言
影像技术和计算机能力的最新发展使人们能够获取大型三维影像数据集,用于放射治疗定位和复杂治疗计划的设计,得益于此,调强放射治疗逐渐取代了三维适形放射治疗,成为放射治疗的主要应用技术[1-2]。调强放射治疗技术的优点在于靶区剂量高度适形、靶区内不同剂量强度可以灵活调节以及靶区边缘剂量快速跌落,使照射区内靶区获得致死剂量,危及器官受照最小剂量成为可能,这对放射治疗摆位的精准度也提出了更高的要求。目前,在放射治疗前进行靶区位置验证已经成为放疗共识[3]。在加速器机载影像设备出现之前,主要使用常规模拟定位机进行位置验证。利用电子射野影像系统(Electronic Portal Imaging Device,EPID)和锥形束CT(Cone Beam Computed Tomography,CBCT)进行位置验证虽然具有一定的优势[4-5],但受制于加速器配置,并且在使用时间上也与放疗实施有一定的冲突。据调查,截至2022 年,全国仍有50%以上的放疗机构未配置CBCT,且各医疗机构CT 模拟定位机配置数量呈现快速增长的趋势[6]。如果使用CT 模拟定位机进行放疗前的位置验证,既可以解决位置验证患者与放疗患者使用机器时间冲突的问题,又可为尚未配置EPID 和CBCT的医疗机构确保实施精准放射治疗提供选择依据。
1 资料与方法
1.1 仪器设备
飞利浦BrillianceTMBig Bore CT 模拟定位机,可提供85 cm 物理孔径,治疗床位移精度0.5 mm,满足放射治疗定位中各种扫描体位需求。Lap 可移动激光灯,位移精度0.1 mm。采用瓦里安CX 医用电子直线加速器EPID 和医科达CBCT XVI 系统。
1.2 一般资料
选取2021 年6 月至2021 年12 月在我院实施调强放疗的60 例患者,其中头颈部、胸腹部和盆腔部各20 例。体位固定方式使用定位膜加塑型垫固定,并在患者身上用记号笔勾画出水解热塑膜的边界,固定患者的碳纤维底座与CT 模拟定位机床板通过适配器固定。塑型垫使用前置于80℃的恒温烤箱中加热,然后取出置于患者体下,根据患者照射体位进行塑形,待温度冷却后定型,优势在于无须抽放气且形状保持较好,不易变形。放射治疗前使用CT 模拟定位机进行位置验证,记录验证结果,将患者随机分配到瓦里安EPID 系统和医科达CBCT XVI系统重新进行放疗前的位置验证并记录结果。
1.3 位置验证方法
在放疗计划系统中选取患者照射等中心横断面,显示照射等中心位置,并通过测量工具测量等中心至固定解剖结构(如颅骨边缘、椎体、骨盆边缘等相对稳定的解剖结构)之间的距离,测量患者左右(Lateral,Lat)和前后(Vertical,Vrt)两个方向的距离(图1)。在CT模拟定位机上,按照计划系统给出的移床坐标将可移动激光灯从定位参考位置移动到照射等中心位置,并在该位置设置金属标记点,扫描条件层厚2 mm,1 mm 重建,扫描范围以金属标记点为中心扫描48 mm(该CT 模拟定位机最小扫描范围),以减少患者不必要接受的辐射剂量。在CT 扫描图像中找到3 个金属标记点的层面,与计划系统中等中心层面比较,确定照射等中心后,调节可移动激光灯,在体膜等中心处粘贴胶布,画好标记线,医生、物理师、技师签字确认,位置验证工作即结束。

图1 等中心在治疗计划系统(a)和CT模拟定位机(b)中测量结果
1.4 加速器离线配准和模拟加速器复位过程
将患者移至加速器上,按照等中心标记线进行摆位,并进行EPID 拍片或者CBCT 采集照射部位图像。瓦里安CX 加速器采用EPID 进行位置验证,医科达Synergy采用CBCT 进行位置验证。
1.5 CT图像与CBCT图像的差异
由于影像采集方式和图像重建算法等因素的差异,CT 模拟定位机提供的三维影像从对比度、分辨率和伪影等方面,均明显优于CBCT 提供的三维影像(图2),尤其是在局部有气腔存在的情况,CBCT 影像有明显的条状伪影,造成周围器官影像对比度变差,无法辨识清楚器官与器官之间以及正常器官与肿瘤之间的关系,这给位置验证带来了一定的困扰。
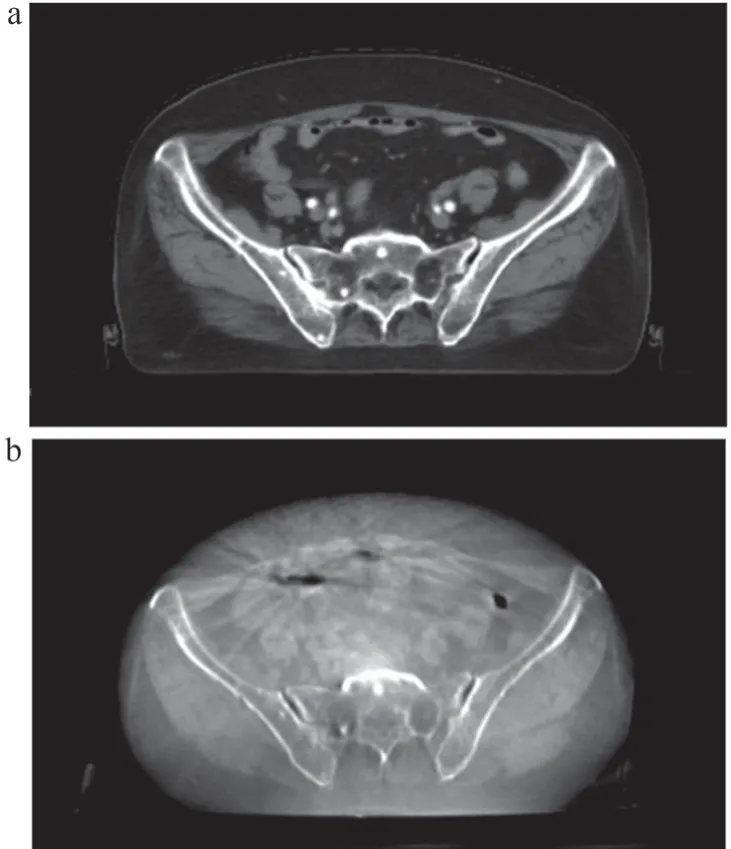
图2 同一横断面CT图像(a)与CBCT图像(b)对照图
1.6 位置验证前后计划比较
将CT 模拟定位机获取的位置验证影像回传至放疗计划系统,与原计划影像进行图像融合,融合后将原放疗计划移至位置验证影像上,重新计算剂量分布,得到验证影像的放疗计划。在原放疗计划CT 图像中选取与位置验证影像相同层面的影像,重建1 组与验证影像相同层数和层厚的影像结构,并将原放疗计划移至该影像上,计划等中心不变,重新计算剂量分布,得到定位CT 影像的放疗计划(图3)。将两组放疗计划与放疗剂量输出,导入Arc-CHECK 软件,进行分析。同时将放疗计划移至CT 模拟机位置验证影像上进行剂量计算,并与相同层厚与层数的原定位CT 影像上生成的计划进行比较,判断通过不同分析标准得到的γ 通过率是否符合临床要求,从剂量学角度证明应用的准确性。
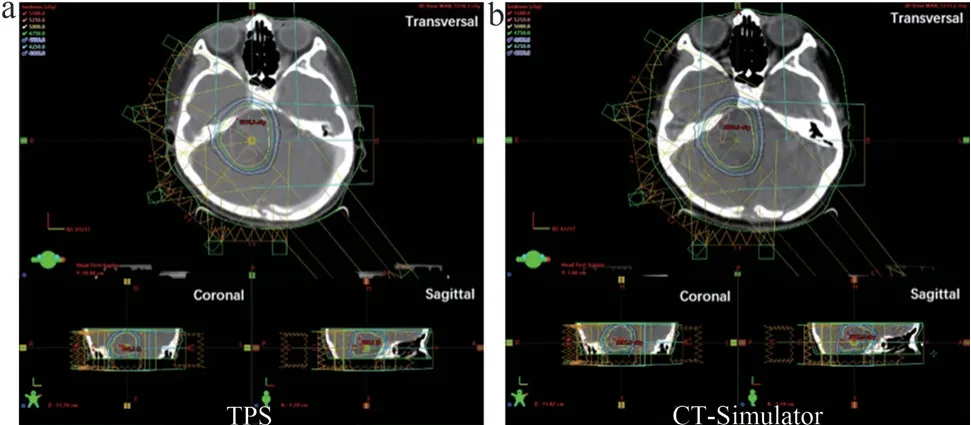
图3 位置验证前后治疗计划系统(a)和CT模拟定位机(b)剂量分布对照图
1.7 统计学分析
采用SPSS 25.0 统计软件将上述不同位置验证方式的结果进行平均值比较和配对样本t检验,数据采用±s表示,以P<0.05 为差异有统计学意义。
2 结果
2.1 位置验证位移偏差结果
CT 模拟定位机位置验证人数共60 例,其中,CBCT 和EPID 位置验证各30 例。3 种方式位置验证在Lat、Vrt、Lng 方向的平均位移结果如表1 所示。其中,在Lat、Vrt 方向,3 种位置验证方式的平均位移差异无统计学意义(Lat 方向:CTvs.CBCTt=1.045、P=0.305,CTvs.EPIDt=0.474、P= 0.639;Vrt 方向:CTvs.CBCTt=0.282、P=0.780,CTvs.EPIDt=-0.460、P=0.649),在Lng 方向,CT 模拟机验证方式平均位移显著低于CBCT和EPID(CTvs.CBCTt=-3.630、P=0.001,CTvs.EPIDt=-5.297、P<0.001)。
表1 3种方式位置验证结果(±s,mm)
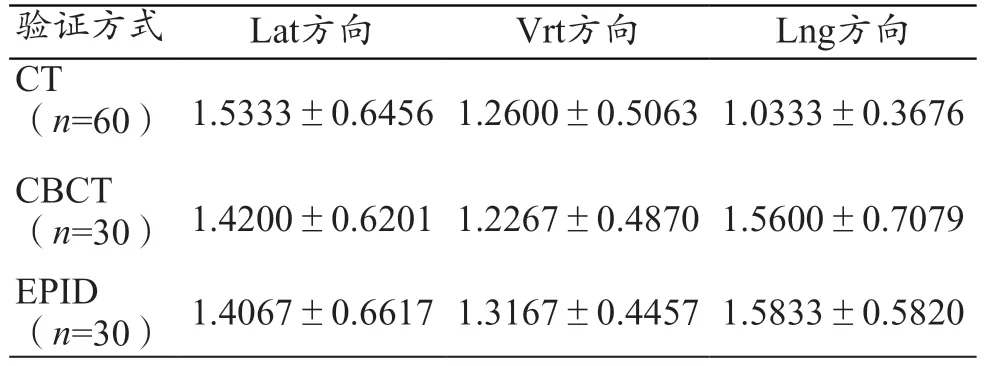
表1 3种方式位置验证结果(±s,mm)
注:Lat:左右;Vrt:前后;Lng:头脚。
验证方式Lat方向Vrt方向Lng方向CT(n=60) 1.5333±0.6456 1.2600±0.5063 1.0333±0.3676 CBCT(n=30) 1.4200±0.6201 1.2267±0.4870 1.5600±0.7079 EPID(n=30) 1.4067±0.6617 1.3167±0.4457 1.5833±0.5820
2.2 3种验证方法结果比较
60 例患者随机分配到瓦里安和医科达加速器,每台加速器30 例患者,对验证结果进行分析,见表2、图4,使用CT 模拟定位机进行位置验证在Lng 方向摆位误差的范围显著小于CBCT 和EPID(P<0.05)。
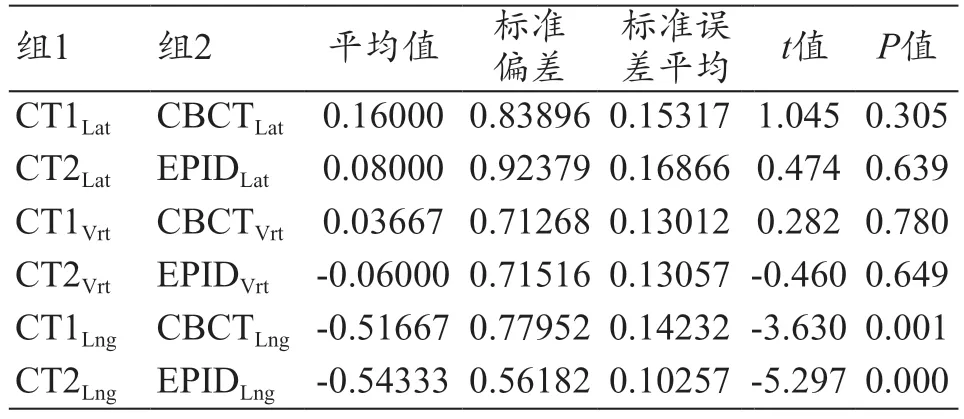
表2 3种验证方法结果比较(mm)
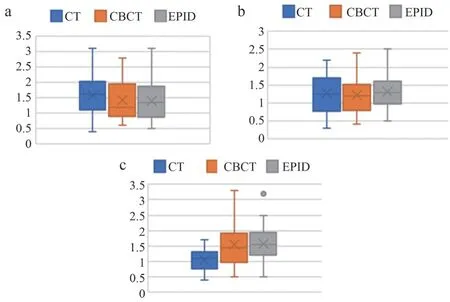
图4 3种位置验证方式摆位误差分布图
2.3 两组放疗计划剂量分布比较
位置验证前后两组CT 影像有略微变化,导致同一组计划在两组影像上的剂量分布也发生了轻微改变,将两组计划的剂量文件导入到ArcCHECK 软件中,并设置3 组不同的分析标准(1 mm/3%、2 mm/3%和3 mm/3%),将两组计划进行比较,3 个轴面的剂量分布如图5 所示,通过软件分析得到1 mm/3%、2 mm/3%和3 mm/3%的γ 通过率通过率分别为95.48%±0.7543%、98.60%±0.7920%、99.80%±0.2847%,可以看出同一计划在位置验证前后两组影像的剂量分布的γ 通过率均大于95%,满足临床要求。
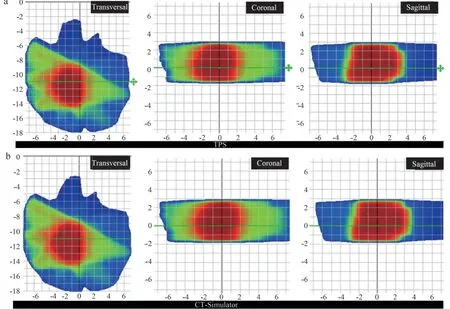
图5 等中心在治疗计划系统(a)和CT模拟定位机(b)在3个轴面的剂量分布
3 讨论
随着放射治疗技术的发展,放疗位置验证的形式也在不断更新,从二维影像到三维影像引导放射治疗[7-9],以及光学体表监测和运动管理策略的运用[10-11],均表明了位置验证对于精准放疗的重要性。以往对于放疗位置验证多围绕与EPID 和CBCT 的应用[12-15],或不同CBCT 配准技术之间对位置验证的研究[16-17],以及不同影像引导方式的影像剂量差异[18]。张爱华等[19]利用研发的CT 模拟验证软件系统,使用CT 模拟定位机对腹部肿瘤进行放疗位置验证。而临床上,大部分的医院仍然使用常规模拟定位机进行放疗前的位置验证,CT 模拟定位机更多是用于放疗定位使用。
本研究通过使用CT 模拟定位机进行放疗前位置验证,一方面增加了CT 模拟定位机的使用率,为那些没有配备CBCT 或者EPID 的医疗机构以及放疗患者人数较多,无法满足所有患者在加速器上进行位置验证的医疗机构提供了一个新途径;另一方面,相对于常规模拟定位机、EPID 和CBCT 进行位置验证,CT 模拟定位机的扫描图像质量更有优势,诊断级的影像更有利于观察等中心附近危及器官的相对位置,尤其是软组织的分辨率明显优于上述3 种验证方式。位置验证后将扫描图像回传至计划系统与CT 定位影像进行融合配准,可以进一步分析位置验证结果。
本研究中,Lng 方向的位移是通过回传位置验证影像与CT 定位影像融合配准得到的,在位置验证时只能测量Lat 方向和Vrt 方向的位移。从结果上看,使用CT模拟定位机验证时,Lng 方向的平均位移要小于EPID和CBCT 验证方式的结果,原因是测量时首先要确定照射等中心的层面,即3 个金属标记点所在的层面。如果发现该层面与CT 定位时的等中心层面不相符,就需要做相应的调整,通过医生和物理师相互确认找到最相符的层面,将金属标记点重新标记后再次扫描得到与CT定位时最相符的等中心层面,再将十字标记线移至3 个金属标记的中心,得到等中心点,从等中心点测量Lat方向和Vrt 方向的位移。在3 个轴向旋转角度方面,使用二维影像进行位置验证是无法获取摆位角度偏差的,CT 模拟定位机可以通过将位置验证影像回传到计划系统中,通过图像融合获取角度摆位误差,属于离线位置验证,使用CBCT 在位置验证的过程中就能获得角度摆位误差,属于在线位置验证。本研究并未在结果中体现角度偏差的数据,是因为本机构的加速器没有配置六维床,在实际使用过程中角度摆位偏差只用于评估,并不能直接按照位置配准给出的角度误差进行校正。从CBCT 和EPID 位置验证的结果看,在Lat 方向和Vrt 方向的平均位移与CT 模拟定位机相比无统计学差异,说明CT 模拟定位机位置验证总体上是符合位置验证要求的,将放疗计划移至CT 模拟机位置验证影像上进行剂量计算,通过不同分析标准得到的γ 通过率均符合临床要求,从剂量学角度证明了其应用的准确性[20-21]。
此外,需注意,无论采取何种方式进行放疗前位置验证,均必须对所采用的验证设备进行严格的质量保证措施,尤其是对于CBCT 的使用,务必要定期对影像中心和加速器等中心进行校准,确保二者一致时才能保证影像引导的正确性。另外实施放射治疗的一个重要限制因素是治疗期间和分次治疗间的运动不确定性导致的目标位置偏差。在放射治疗的路径中,运动管理策略已从治疗前定位、治疗计划、成像和验证过程中得到越来越多的开发和临床实施[22-23]。所以,了解在放疗中使用运动管理的科学基础和临床原理,以及在此类情况下准确应对处理系统和随机误差至关重要。
4 结论
CT 模拟定位机能够满足临床上调强放疗位置验证的需求,以及获取软组织分辨率更好的位置验证影像,方便医生观察靶区和危及器官的相对关系,可在最大程度地利用该设备的同时,解决部分医院未配置CBCT 进行调强放疗位置验证的难题。