意外胆囊癌二次术后早期复发的危险因素及辅助化疗疗效分析
2023-09-11李起刘恒超李孟柯高琦陈晨张东耿智敏
李起,刘恒超,李孟柯,高琦,陈晨,张东,耿智敏
(西安交通大学第一附属医院 肝胆外科,陕西 西安 710061)
方法:回顾性收集2011年1月—2021年12月于西安交通大学第一附属医院肝胆外科因IGBC行意向性根治术的170例患者的临床病理资料,分析患者术后早期复发的影响因素(早期复发定义为二次意向根治术后12个月内),以及患者术后无复发生存(RFS)与总体生存(OS)的影响因素。
结果:170例行IGBC意向性根治术后患者,随访期间复发者73例(42.94%)、早期复发者41例(24.12%)。IGBC术后早期复发患者中位OS时间明显短于非早期复发患者(χ2=192.910,P<0.001)。病理分化程度(OR=20.758,95% CI=5.557~80.239)、CA19-9水平(OR=7.920,95% CI=1.557~39.771)及病灶残留(OR=8.050,95% CI=3.062~21.160)是IGBC术后早期复发的独立危险因素(均P<0.05)。病理分化程度(HR=6.160,95% CI=2.877~13.193)、CA19-9水平(HR=2.538,95% CI=1.297~4.965)、手术切除范围(HR=2.111,95% CI=1.154~3.860)、病灶残留(HR=2.571,95% CI=1.547~4.273)是IGBC术后RFS时间的独立危险因素(均P<0.05)。病理分化程度(HR=3.225,95% CI=1.461~7.121)、早期复发(HR=29.558,95% CI=14.250~61.311)、病灶残留(HR=2.416,95% CI=1.361~4.287)是IGBC术后OS时间的独立危险因素(均P<0.05),辅助化疗是术后OS时间的独立保护性因素(HR=0.260,95% CI=0.123~0.551,P<0.05)。按有无病灶残留及是否早期复发分层分析的结果显示,辅助化疗可延长病灶残留患者术后RFS时间及OS时间,亦可延长早期复发患者术后OS时间(均P<0.05)。
结论:病灶残留是IGBC二次术后早期复发及预后的独立危险因素,术后辅助化疗可以有效改善病灶残留及早期复发患者的预后。
意外胆囊癌(incidental gallbladder cancer,IGBC)是因胆囊结石、胆囊息肉等胆囊良性疾病行胆囊切除术,术中或术后病理检查偶然发现的胆囊癌[1-2]。近年来,随着腹腔镜胆囊切除术在各级医疗机构的广泛应用,IGBC病例数量呈逐年增长的趋势[3-4]。目前,二次根治性切除手术仍然是治愈IGBC,使患者获得长期生存的有效方式[5]。然而,胆囊癌患者即使行根治性切除术,术后发生局部或远处转移率可高达30%~50%。根治性切除患者一旦出现术后复发,即使接受辅助治疗或再次手术切除,5年总体生存(overall survival,OS)率仅为15%~20%[6-9]。
越来越多的证据表明,术后早期复发是胆囊癌[6-7]、肝内胆管癌[10]、肝门部胆管癌[11]、胰腺癌[12]等肝胆胰恶性患者预后的重要危险因素。研究发现,辅助化疗可使肝门部胆管癌[11]、胰腺癌[12-13]术后早期复发患者获益,可作为辅助化疗选择潜在的客观指标。因此,IGBC早期复发的危险因素识别及其是否可以获益于辅助化疗具有重要的临床价值有助于临床治疗方案的制定。基于此,本研究回顾性分析因IGBC行二次意向性根治术患者的临床病理资料,探讨术后早期复发的危险因素,以及辅助化疗对于早期复发患者的预后影响,以期为IGBC的综合治疗提供临床决策支持。
1 资料与方法
1.1 研究对象
回顾性分析2011年1月—2021年12月于西安交通大学第一附属医院肝胆外科因IGBC行意向性根治术的170例患者的临床病理资料,其中男性41例(24.1%),女性129例(75.9%);年龄30~83岁,平均(57.79±10.34)岁。纳入标准:⑴ 初次胆囊切除术后病理证实为胆囊癌者;⑵ 行二次意向性根治术者,病理切缘为R0/R1者;⑶ 术前未接受新辅助治疗或其他针对恶性肿瘤治疗者;⑷ 临床病理及随访资料完整者。排除标准:⑴ 合并消化系统其他恶性肿瘤者;⑵ 姑息性手术切除者;⑶ 存在远处转移(M1)者;⑷ 因为非胆囊癌转移复发者;⑸ 术后围术期30 d内死亡者。本研究通过西安交通大学第一附属医院伦理委员会审批(批号:XJTU1AF2022LSK-089)。所有患者及家属均签署知情同意书。
1.2 手术治疗及二次术后病理情况
本研究纳入170例患者中,其中3例(1.8%)患者为院内术后病理发现行二次根治手术;初次胆囊切除术后病理提示,胆囊肿瘤位置:颈部14例、体部29例、底部10例、体底部9例、弥漫6例、位置不详102例;肿瘤细胞病理类型:腺癌157例、黏液腺癌5例、腺鳞癌2例、神经内分泌癌1例、不详5例。二次手术中,152例患者行根治性切除术(肝楔形切除/IVb+V段切除+淋巴结清扫),18例患者行扩大根治术(肝楔形切除/IVb+V段切除+淋巴结清扫+胃部分切除/胆管切除/门静脉部分切除/结肠部分切除),二次术后病理切缘R0165例、R15例。根据第8版AJCC分期对170例患者重新分期,T1b 42例、T2期14例、T3期110例、T4期4例;N0期135例、N1期26例、N2期9例;TNM分期:I期38例、ⅡA期8例、ⅡB期3例、ⅢA期83例、ⅢB期25例、ⅣA期4例、ⅣB期9例。病灶残留指二次术后病理标本中任何组织经病理检查发现癌细胞,包括邻近脏器、脂肪组织、结缔组织及淋巴结[14]。本组病例中病灶残留68例(40.0%),其中I期3例、ⅡB期1例、ⅢA期26例、ⅢB期25例、ⅣA期4例、ⅣB期9例。
1.3 辅助化疗情况
辅助化疗方案的采用美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)制定的《肿瘤临床实践指南》[15]。26例患者接受GS方案(吉西他滨1 000 mg/m2,第1、8天;替吉奥40~60 mg,第1~14天,每3周为1个周期);5例患者接受GEMOX方案(吉西他滨1 000 mg/m2;第1、8天;奥沙利铂130 mg/m2,第1天,每3周为1个周期);3例患者接受GP方案(吉西他滨1 000 mg/m2+顺铂30 mg/m2,第1、8天,每3周为1个周期);3例患者接受AG方案(白蛋白紫杉醇 125 mg/m2+吉西他滨1 000 mg/m2,第1、8天,每3周为1个周期);2例患者接受SOX方案(替吉奥40~60 mg,第1~14天;奥沙利铂100 mg/m2,第1天,每3周为1个周期);联合使用贝伐珠单抗4例,多西他赛2例。术后辅助化疗中位周期为6(3~10)周期,化疗期间无因不良反应死亡患者,相关不良反应经对症治疗后缓解,能够维持原剂量化疗。
1.4 随访
所有患者术后均接受随访。术后以门诊和电话方式进行常规随访,术后1年内每3个月复查肝功能、肿瘤标志物:癌胚抗原(CEA)、糖类抗原19-9(CA19-9)、CA125、上腹部B超、CT或MRI检查。随后每3~6个月随访1次。观察术后无复发生存(recurrence free survival,RFS)时间及OS时间,RFS时间定义为从患者治疗开始到肿瘤进展、复发或远处转移的时间;OS时间定义从手术治疗开始到死亡或末次随访的时间;早期复发定义为肿瘤复发在二次手术切除术后12个月内[7,16]。观察终点即为手术日期到随访截止日期或因肿瘤复发及转移致死亡的日期。随访截至2023年4月7日。
1.5 统计学处理
应用SPSS 25.0统计软件进行分析。计数资料以频数(百分比)[n(%)]表示。正态分布计量资料以均数±标准差(±s)表示,非正态分布计量资料以中位数(范围)表示,早期复发单变量分析采用χ2检验或Mann-WhitneyU检验,多变量分析采用Logistic回归模型,生存单变量分析采用Kaplan-Meier法和Log-rank检验,采用单变量及多变量Cox比例风险回归模型进行预后分析。采用Graphpad Prism 8绘制生存曲线。P<0.05为差异有统计学意义。
2 结 果
2.1 随访及生存分析结果
170例行IGBC意向性根治术后患者,中位随访时间50个月,随访期间复发者73例(42.94%)、早期复发者41例(24.12%);存活106例(62.35%),死亡64例(37.65%),死亡原因均为肿瘤复发转移致多器官功能衰竭后死亡;术后RFS时间1~139个月、OS时间2~139个月;中位RFS时间及OS时间分别为73.0个月、85.0个月;1、3、5年RFS率分别为75.9%、59.2%、48.3%,1、3、5年OS率分别为84.7%、62.4%、51.7%。早期复发患者中位OS时间仅为10.0个月,明显差于非早期复发患者(χ2=192.910,P<0.001)(图1)。

图1 早期复发与非早期复发的IGBC患者术后Kaplan-Meier生存曲线Figure 1 Kaplan-Meier survival curves for IGBC patients with early recurrence and non-early recurrence after surgery
2.2 IGBC早期复发危险因素分析
单变量分析显示,初次术后T分期、病理分化程度、初次术后胆囊管切缘、CA19-9水平、CA125水平、手术切除范围、二次术后病理切缘、N分期、肝侵犯、病灶残留是影响IGBC术后复发的危险因素(均P<0.05)(表1)。多因素Logistic回归模型分析显示,病理分化程度、CA19-9水平及病灶残留是影响IGBC术后早期复发的独立危险因素(均P<0.05)(表2)。

表1 IGBC患者术后早期复发影响因素的单变量分析[n(%)]Table 1 Univariate analysis of influencing factors for early postoperative recurrence in IGBC patients [n (%)]

表2 IGBC患者术后早期复发影响因素的多变量分析Table 2 Multivariate analysis of influencing factors for early postoperative recurrence in IGBC patients
2.3 IGBC术后预后分析
多变量Cox回归模型分析显示,病理分化程度、早期复发、病灶残留是影响IGBC术后OS时间的独立危险因素(均P<0.05),辅助化疗是术后OS时间的独立保护性因素(P<0.05)。病理分化程度、CA19-9水平、手术切除范围、病灶残留是影响IGBC术后RFS时间的独立危险因素(均P<0.05)(表3)。
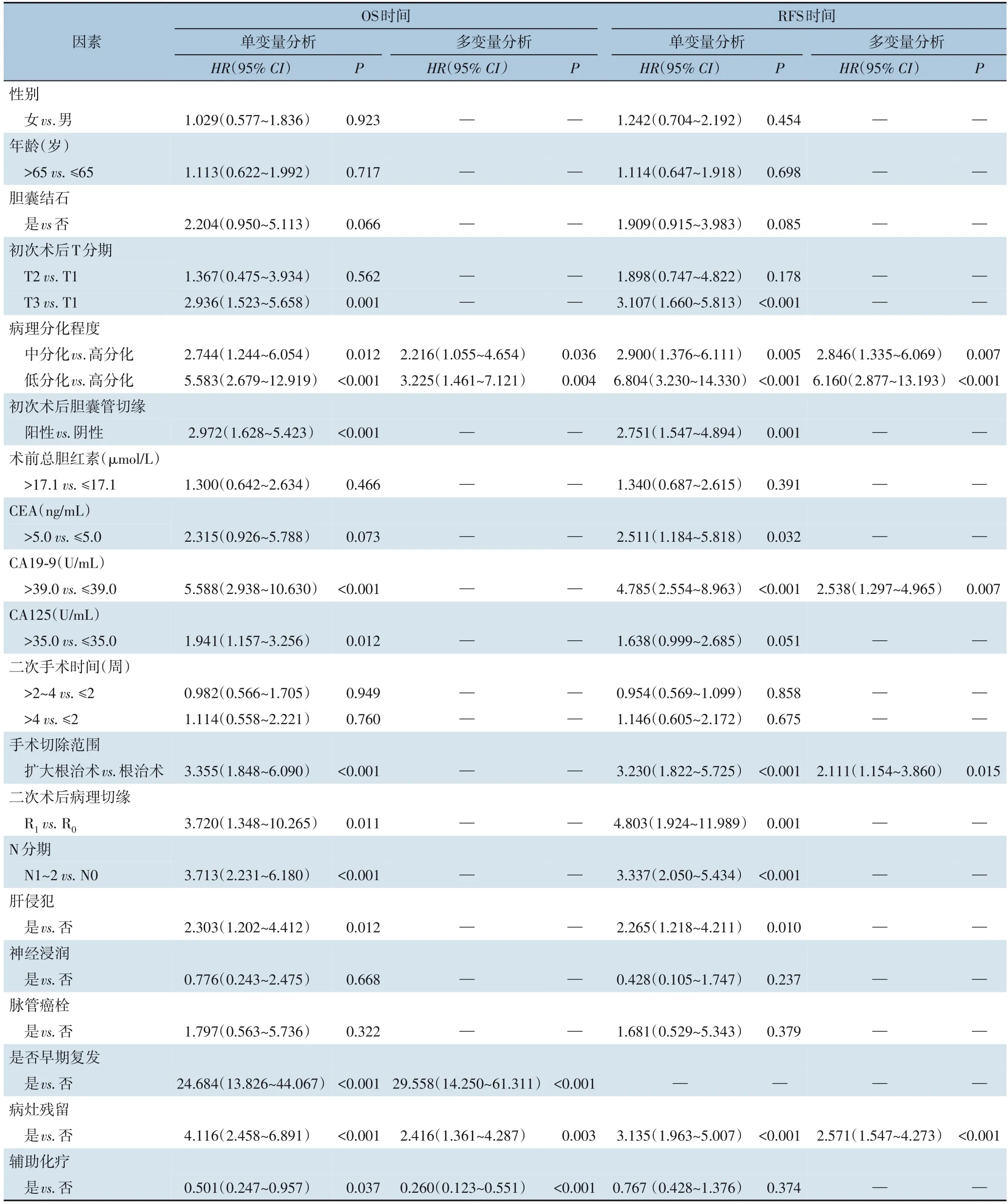
表3 IGBC预后影响因素的单变量与多变量Cox回归模型分析Table 3 Univariate and multivariate Cox regression model analysis of influencing factors for prognosis in IGBC patients
2.4 辅助化疗对病灶残留者预后的影响
分析辅助化疗对于有无病灶残留及是否早期复发的影响,结果显示,病灶残留患者中,未接受辅助化疗和接受辅助化疗者中位RFS时间分别为11.0、52.0个月(χ2=4.722,P<0.05),未接受辅助化疗者中位OS时间为17.0个月、辅助化疗者中位OS时间未获得(χ2=8.326,P<0.05)(图2);早期复发患者中,未接受辅助化疗和接受辅助化疗者中位OS时间分别为9.0、19.0个月(χ2=5.738,P<0.05)(图3)。

图2 辅助化疗对有无病灶残留的IGBC患者术后预后的影响 A:无病灶残留患者的RFS曲线;B:无病灶残留患者的OS曲线;C:病灶残留患者的RFS曲线;D:病灶残留患者的OS曲线Figure 2 The influence of adjuvant chemotherapy on postoperative prognosis of IGBC patients with and without residual lesions A: RFS curves for patients without residual lesions; B: OS curves for patients without residual lesions; C: RFS curves for patients with residual lesions; D: OS curves for patients with residual lesions

图3 辅助化疗对是否早期复发的IGBC患者术后预后的影响 A:非早期复发患者的RFS曲线;B:非早期复发患者的OS曲线;C:早期复发患者的RFS曲线;D:早期复发患者的OS曲线Figure 3 The influence of adjuvant chemotherapy on postoperative prognosis of IGBC patients with and without early recurrence A: RFS curves for non-early recurrence patients; B: OS curves for non-early recurrence patients; C: RFS curves for early recurrence patients; D: OS curves for early recurrence patients
3 讨 论
随着腹腔镜胆囊切除术的广泛开展,IGBC病例数量呈逐年增长的趋势。受医疗条件限制,部分患者即使术中发现为IGBC,也无法完成根治性手术,这对胆囊癌术前精准评估提出更高的要求[3]。近年来,尽管更多的证据[17-18]表明新辅助或辅助治疗可以使胆囊癌患者获益,但毋庸置疑,IGBC二次根治手术切除仍是治疗过程中的关键环节,能够有效改善患者预后[19]。本研究结果发现,IGBC患者二次术后中位RFS时间及OS时间分别为73.0个月与85.0个月,5年RFS率及OS率分别为48.3%、51.7%,预后明显优于Fuks等[20]报告的IGBC二次术后的5年OS率41%。近期,四川大学华西医院程南生教授团队[21]报道IGBC二次术后中位OS时间为74.52个月,5年OS率高达74.7%。因此,IGBC规范的二次手术治疗对于患者预后改善十分重要。
研究[6-7]表明,早期复发是进展期胆囊癌患者不良预后的重要原因,早期复发患者的OS时间明显差于非早期复发者。本研究发现,IGBC早期复发患者中位OS时间仅为10个月,明显差于非早期复发者,多变量分析发现,早期复发是患者预后不良的独立危险因素。因此,重视识别IGBC早期复发对制定患者综合诊疗策略具有重要参考价值。本研究还发现,初次术后T分期、病理分化程度、初次胆囊管切缘状态、肿瘤标志物、手术切除范围、N分期、肝侵犯、二次手术切缘及病灶残留等是影响IGBC术后早期复发及预后的影响因素,与既往研究[6-7,22-23]报道一致。
对于IGBC二次手术治疗方案主要取决于初次手术病理T分期。遗憾的是,初次手术仅行单纯的胆囊切除并不能获得准确的T分期,从而限制综合治疗方案的制定[24]。本组病例中,初次胆囊切除术后T1b期53例(31.2%)、T2期19例(11.2%)、T3期98例(57.6%),二次术后T1b期42例(24.7%)、T2期14例(8.2%)、T3期110例(64.7%)、T4期4例(2.4%),上述结果表明,初次术后T分期与患者二次术后T分期存在一定出入,T3期及以上患者比例较高,IGBC不等同于早期胆囊癌。因此,二次术前准确的T分期评估对于制定IGBC综合治疗方案尤为重要。有学者[2]提出,将T3期及以上患者纳入IGBC范畴,容易延误根治手术及辅助化疗时机,导致初次手术创面出现短期复发并加速淋巴及血液转移的进程,是患者不良预后的重要因素,这显示出IGBC规范诊断命名的重要性及临床价值。
病灶残留是指二次术后病理标本中胆囊邻近脏器、脂肪组织、结缔组织及淋巴结等经病理检查发现癌细胞,其能够较好地兼顾肿瘤局部浸润、淋巴结状态及肿瘤生物学行为等特征,从而为IGBC的治疗方案选择提供参考。Ramos等[14]通过回顾性分析59例IGBC患者的临床病理资料发现,30例(50.8%)的患者存在病灶残留,即使二次手术实现R0切除仍预后不良。本研究发现,病灶残留是IGBC早期复发及预后的独立危险因素,本组68例(40.0%)IGBC患者合并病灶残留,随着T分期的增加,病灶残留比例亦升高,其中4例患者为T1b期。因此,病灶残留指标亦为T1b期行根治性切除术的必要性评估提供依据[25]。
在二次手术时间窗方面,目前推荐的二次手术最佳时期为胆囊切除术后4~8周[26]。张宝华教授团队[27]发现,2周内二次手术预后优于>2~4周以及>4周者,这表明二次手术最佳时期仍需进一步研究。本研究结果显示,二次手术时间间隔并非患者早期复发及不良预后的影响因素,但笔者团队[28]既往发现,病灶残留患者二次手术时间在初次胆囊切除4周内可明显改善预后,无病灶残留患者预后与二次手术时间无关。近年来新辅助化疗理念在胆囊癌综合治疗中的应用越来越受到重视,病灶残留的患者新辅助治疗周期延长了二次手术时间窗,但其对于患者预后的影响仍需进一步研究,从而为患者个体化治疗提供依据。
胆囊癌的辅助治疗目前缺乏统一标准,仍存在一定争议,如何筛选出辅助化疗潜在获益的胆囊癌患者仍是胆道外科医生关注热点及难点,适应证主要包括T2期以上、淋巴结阳性或R1切除或合并神经浸润或脉管侵犯等不良预后病理特征者[29-30]。本研究中,26例患者接受GS方案,5例接受GEMOX方案,3例接受GP方案,3例接受AG方案,2例接受SOX方案,无严重不良反应发生,预后多变量分析显示,辅助化疗是患者OS时间的独立保护性因素。分层分析发现,辅助化疗可以改善病灶残留患者预后,亦可以延长早期复发患者术后OS时间。Xiang等[31]也发现辅助化疗可以改善合并有病灶残留的高复发风险的IGBC患者的OS。因此,对于病灶残留患者可以在二次术后行辅助化疗以降低早期复发风险,延长OS时间。
本研究初步发现,病理分化程度、CA19-9及病灶残留与IGBC二次术后早期复发独立相关,术后辅助化疗可以有效改善病灶残留及早期复发患者的预后,但仍存在以下不足:⑴本研究纳入大多数患者为基层医院的转诊患者,初次胆囊切除术中是否完整切除、有无胆汁漏等,病理诊断水平差异及报告不规范等可能造成研究偏倚;⑵ 本研究为单中心回顾性研究,辅助化疗样本量相对较小,仍需多中心、大样本、前瞻性研究进一步评估辅助化疗对于早期复发患者预后的有效性及安全性;⑶ 辅助化疗方案及周期不同可能是影响辅助化疗有效性的潜在因素。
综上所述,病灶残留是IGBC早期复发及预后的独立危险因素,辅助化疗可以改善早期复发患者OS;在有病灶残留的患者中,接受辅助化疗可有助于改善患者RFS及OS。规范IGBC的管理,详细记录初次胆囊切除术中情况,二次手术前进行病理组织标本会诊,明确初次术后肿瘤T分期、肿瘤分化程度、手术切缘、肿瘤细胞类型、有无神经浸润及脉管癌栓等重要病理特征,将为患者综合治疗决策制定提供参考依据,有效改善患者的预后。
利益冲突:所有作者均声明不存在利益冲突。
作者贡献声明:李起、耿智敏设计了这项研究并进行了数据分析、图表绘制和写作;刘恒超、李孟柯、高琦负责数据采集;陈晨、张东、耿智敏负责文章审阅。
