基于AMPK信号通路的附子在不同机体状态下对神经—内分泌—免疫网络的生物学效应表达机制研究
2023-09-08王智威邸松蕊黄鹏力谢辰雨王一帆张建军朱映黎
王智威 邸松蕊 黄鹏力 谢辰雨 王一帆 张建军 朱映黎
机体状态是中药药性生物效应表达的载体,机体状态不同,中药药性作用于机体的生物学效应亦不同[1]。神经—内分泌—免疫(neural-endocrine-immune system ,NEI)网络将神经、内分泌、免疫三大系统相互间的作用作为整体进行研究,以神经递质、激素、细胞因子等全面系统调控人体功能。研究表明,机体状态不同,NEI相关指标亦有不同[2-8]。由此表明,NEI网络对中药基于不同机体状态的生物学效应表达发挥着重要作用。
腺苷酸活化蛋白激酶(AMP-activiated protein kinase,AMPK)被称为细胞的“能量感受器”[9],通过调节下游基因靶点[10]脂肪酸合成酶(fatty acid synthase,FASN)影响中枢神经系统以及神经网络的结构[11-12];通过调控下游靶点[13]6-磷酸果糖激酶-2/果糖-2,6-二磷酸酶3(6-phosphofructo-2-kinase/fructose-2,6-biphosphatase 3,PFKFB3)产生细胞因子调节免疫系统功能[14-16];调节下游靶点固醇调节元件结合蛋白1c (sterol regulatory element binding protein-1c,SREBP-1c)[10],而SREBP-1c又能够进一步调节下游硬脂酰辅酶A去饱和酶1(stearoyl coenzyme A desaturase 1,SCD1)基因表达[17],影响内分泌系统功能[18];除此之外,还可以调节上游靶点[19]胰岛素受体底物2(insulin receptor substrate,IRS2)影响物质代谢,在神经、内分泌、免疫系统中均发挥一定调控作用[20-22]。因此,AMPK信号通路可通过作用于IRS2、FASN、PFKFB3、SCD1基因靶点调节机体NEI网络,是连接NEI网络的主要信号通路之一。
附子为毛茛科乌头属中药,辛、甘,大热,可回阳救逆,补火助阳,散寒止痛,为“回阳救逆第一要药”,临床常用于治疗风寒湿痹疼痛[23]。研究表明,辛热中药附子作用于寒热不同机体状态会引起NEI网络相关指标生物效应不同的改变,但基于AMPK信号通路调节NEI网络相关机制研究尚未见报道。因此,本研究以NEI网络为切入点,对辛热中药附子通过AMPK信号通路调节FASN/PFKFB3/SCD1/IRS2基因作用于寒热不同机体状态小鼠的生物学效应表达机制进行研究。
1 材料与方法
1.1 实验动物
SPF级雄性KM小鼠84只,体质量(20±2)g,购自维通利华实验动物技术有限公司[SCXK(京)2021-0011],饲养于北京中医药大学SPF级实验动物中心。动物房室温为22~26℃,相对湿度60%~70%,光照周期12小时。
1.2 实验药物、试剂与仪器
受试药由中药饮片煎煮浓缩制备:附子(四川同创康能药业有限公司,批号:200701),取500 g附子,10倍量水浸泡1小时,分两次煎煮,每次1.5小时,浓缩后放于4℃冰箱贮存备用。
氢化可的松琥珀酸钠(常州四药制药有限公司,批号:20210811D1);醋酸地塞米松片(上海上药信谊药厂有限公司,批号:501210402)。环腺苷酸(cyclic adenosine monophosphate,cAMP)试剂盒(批号:L211201973)、环鸟苷酸(cyclic guanosine monophosphatec,cGMP)试剂盒(批号:L211228447),以上试剂盒由北京拜尔迪生物技术有限公司提供。去甲肾上腺素(norepinephrine,NE)试剂盒(批号:E20220720-20570A)、多巴胺(dopamine,DA)试剂盒(批号:E20220720-20273A)、5-羟色胺(5-hydroxytryptamine,5-HT)试剂盒(批号:E20220720-24791A)、三碘甲状腺原氨酸(triiodothyronine,T3)试剂盒(批号:E20220720-20591A)、甲状腺素(thyroxine,T4)试剂盒(批号:E20220720-20401A)、补体C3(complement 3,C3)试剂盒(批号:E20220720-20210A)、补体C4试剂盒(批号:E20220720-20211A)、免疫球蛋白G(immunoglobin G,IgG)试剂盒(批号:E20220720-20509A)、免疫球蛋白M(immunoglobin M,IgM)试剂盒(批号:E20220720-20513A),以上检测试剂盒均购自上海酶联生物科技有限公司。RNA提取液(货号:G3013),购自Servicebio。
电子天平(型号:PL-203),梅特勒-托利多仪器(上海)有限公司;酶标分析仪(型号:DR-200BS),无锡华卫德朗仪器有限公司;台式离心机(型号:TGL-16c),上海安亭科学仪器厂;冷冻离心机(型号:neofuge15R),HealForce;全自动生化分析仪(型号:Chemray-240),深圳雷杜生命科技;研磨仪(货号:KZ-Ⅲ-FP),Servicebio;台式高速冷冻型微量离心机(货号:D3024R),DragonLab;荧光定量PCR仪(货号:CFX),Bio-rad。
1.3 分组与给药
适应性喂养7天后,84只小鼠按体质量进行编号,再按照随机数字表法分为7组,每组12只,分别为:空白组、虚热模型组、虚寒模型组、虚热附子低剂量组、虚热附子高剂量组、虚寒附子低剂量组、虚寒附子高剂量组。每日上午(7:00)进行灌胃,虚热、虚寒附子低剂量组给予附子生药量10 g/kg,虚热、虚寒附子高剂量组给予附子生药量20 g/kg,灌胃剂量为1.2 mL/100 g;空白组、虚热模型组和虚寒模型组于灌胃等剂量蒸馏水,连续给药14天。
1.4 造模方法
适应性喂养7 天后,每日下午(16:00)空白组给予等量蒸馏水,虚热组小鼠灌胃醋酸地塞米松(0.35 mg/kg)、虚寒组小鼠灌胃氢化可的松琥珀酸钠(35 mg/kg),制备虚热、虚寒模型,根据体质量调整灌胃剂量,连续造模14天;模型表现同文献一致[24-26],表示造模成功。
1.5 取材方法
实验第15天,采用摘眼球取血,室温静置2小时,在4℃条件下以3000 r/min离心15分钟后取上层血清,留存用于血清指标的检测。冰上取小鼠肾脏称重后快速放于液氮中,后转入-80℃冰箱保存,用于指标检测。
1.6 指标检测
1.6.1 一般观察 实验期间记录各组小鼠造模给药后毛发、精神活动状态以及每3天小鼠体质量的变化。
1.6.2 检测血清cAMP、cGMP指标 采用酶联免疫吸附法,按照ELISA 试剂盒步骤操作进行,完成后置于酶标仪测定吸光值,根据标准曲线计算,检测cAMP、cGMP水平。
1.6.3 血清中神经递质NE、DA、5-HT检测 采用酶联免疫吸附法检测小鼠血清中去甲肾上腺素NE、DA、5-HT含量水平,完成后置于酶标仪测定吸光值,根据标准曲线算出。
1.6.4 血清T3、T4检测 根据试剂盒说明书,酶联免疫吸附法检测小鼠血清中内分泌物质T3、T4含量水平。
1.6.5 血清C3、C4、IgG、IgM检测 采用酶联免疫吸附法检测小鼠血清中C3、C4、IgG、IgM含量水平,具体操作步骤参考试剂盒说明书。
1.6.6 检测心脏组织FASN、SCD1、IRS2、PFKFB3的mRNA表达 利用反转录—荧光定量PCR法(reverse transcript quantitative PCR,RT-qPCR)测定四种基因mRNA表达。具体引物序列见表1。反应体系包含1.0 μL cDNA、10 μmol/L引物0.3 μL,Premix Taq 5 μL,EvaGreen 0.5 μL,加ddH2O补充至10 μL,95℃ 5分钟预变性后,95℃10秒→60℃30秒,40个循环。采用2-ΔΔCt分析相对基因表达差异。

表1 引物序列
1.7 统计学方法
2 结果
2.1 附子对虚热、虚寒机体状态小鼠一般状况及体质量的影响
与空白组比较,虚热模型组小鼠出现毛发偏黄、大便秘结、小便黄、暴躁易怒等现象,虚寒模型组小鼠出现精神萎靡、被毛无光泽、活动减少、抱团等现象。与虚热模型组比较,附子组小鼠症状加重;与虚寒模型组比较,附子组小鼠精神状态有很大程度改善。
与空白组比较,虚热模型组和虚寒模型组小鼠体质量在第7天均开始显著降低(P<0.01,P<0.05);与虚热模型组比较,虚热附子低剂量组小鼠体质量在第14天显著升高(P<0.05),而虚热附子高剂量组小鼠体质量未有改善,变化趋势与虚热模型组相似;与虚寒模型组比较,虚寒附子高剂量组体质量在第14天显著升高(P<0.05)。结果见表2。
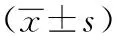
表2 附子对虚热、虚寒机体状态小鼠的影响小鼠体质量的影响
2.2 附子对虚热、虚寒机体状态小鼠血清环核苷酸水平的影响
与空白组比较,虚热模型组cAMP、cAMP/cGMP含量显著升高(P<0.05,P<0.01),虚寒模型组cAMP、cAMP/cGMP含量显著降低(P<0.01),而cGMP含量显著升高(P<0.01)。
与虚热模型组比较,虚热附子低、高剂量组对cAMP、cGMP、cAMP/cGMP有一定的调整作用,但差异无统计学意义(P>0.05);与虚寒模型组比较,虚热附子高剂量组cGMP含量显著降低(P<0.01),而cAMP、cAMP/cGMP含量显著升高(P<0.01)。结果见表3。
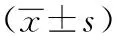
表3 附子对虚热、虚寒机体状态小鼠血清环核苷酸水平的影响
2.3 附子对虚热、虚寒机体状态小鼠神经递质的影响
与空白组比较,虚热模型组NE、DA含量显著升高(P<0.01),5-HT含量显著降低(P<0.01),而虚寒模型组NE、DA、5-HT含量均显著降低(P<0.01)。
与虚热模型组比较,虚热附子低、高剂量组对NE、DA、5-HT有一定的调整作用,但差异无统计学意义(P>0.05);与虚寒模型组比较,虚热附子高剂量组NE、DA、5-HT含量显著升高(P<0.01),附子低剂量组NE、DA、5-HT含量有升高趋势,但差异无统计学意义(P>0.05)。结果见表4。
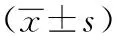
表4 附子对虚热、虚寒机体状态小鼠神经递质的影响
2.4 附子对虚热、虚寒机体状态小鼠内分泌水平的影响
与空白组比较,虚热模型组T3、T4含量显著升高(P<0.01),而虚寒模型组T3、T4含量显著降低(P<0.01)。
与虚热模型组比较,虚热附子低、高剂量组T3含量显著降低(P<0.01),虚热附子低、高剂量组T4含量有降低趋势,差异无统计学意义(P>0.05);与虚寒模型组比较,虚寒附子低、高剂量T3含量显著升高(P<0.01),虚寒附子高剂量组T4含量显著升高(P<0.01),虚寒附子低剂量组T4含量有升高趋势,差异无统计学意义(P>0.05)。结果见表5。
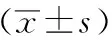
表5 附子对虚热、虚寒机体状态小鼠内分泌的影响
2.5 附子对虚热、虚寒机体小鼠免疫水平的影响
与空白组比较,虚热模型组C3、C4、IgG、IgM含量显著升高(P<0.01),虚寒模型组C3、C4、IgG、IgM含量显著降低(P<0.01);与虚热模型组比较,虚热附子低剂量组C3含量显著降低(P<0.05),虚热附子低、高剂量组C4、IgG、IgM有降低趋势,差异均无统计学意义(P>0.05);与虚寒模型组比较,虚寒附子低剂量组IgG、IgM含量显著升高(P<0.01),虚寒附子高剂量组C3、C4、IgG、IgM含量均显著升高(P<0.01),虚寒附子低剂量组C3、C4含量有降低趋势,差异无统计学意义(P>0.05)。结果见表6。
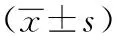
表6 附子对虚热、虚寒机体状态小鼠免疫因子的影响
2.6 附子对虚热、虚寒机体小鼠FASN、PFKFB3、SCD1、IRS2基因mRNA表达的影响
与空白组比较,虚热模型组FASN、PFKFB3、SCD1、IRS2的mRNA表达显著升高(P<0.01,P<0.01,P<0.05,P<0.05),虚寒模型组FASN、PFKFB3、SCD1、IRS2的mRNA表达显著升高(P<0.01,P<0.05,P<0.01,P<0.05);
与虚寒、虚热模型组比较,虚寒附子高剂量组FASN、PFKFB3、SCD1、IRS2的mRNA表达均显著降低(P<0.01,P<0.05,P<0.01,P<0.01),虚热附子高剂量组IRS2的mRNA表达均显著降低(P<0.01),而FASN、PFKFB3、SCD1的mRNA表达有降低趋势,差异无统计学意义(P>0.05)。结果见表7。
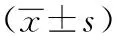
表7 附子对虚热、虚寒机体状态小鼠Fasn、PFKFB3、SCD1、IRS2基因mRNA表达的影响
3 讨论
机体状态是中药药性生物学效应表达的载体,对药物体内代谢生态环境具有重要作用,寒热机体状态不同亦会使同一中药的生物效应表达也不同[1]。NEI网络对于中药基于不同机体状态的生物学效应表达发挥着重要作用。研究表明,AMPK信号通路是连接NEI网络的主要信号通路之一。因此,本文对辛热药附子作用于寒热不同机体状态后NEI网络生物效应不同进行了探察,并通过AMPK信号通路FASN/PFKFB3/SCD1/IRS2基因靶点对其不同生物学效应表达机制进行了深入研究。
现代研究表明,机体寒热状态的产生与神经[2-4]、内分泌[5-6]、免疫[7-8]、环核苷酸水平[27]状态的异常息息相关。环核苷酸系统cAMP和cGMP作为细胞间信息传导的第二信使,与物质代谢中密切相关,在维持机体神经—内分泌—免疫网络的平衡中起重要作用[28]。寒热不同机体状态中环核苷酸的表达有明显的差异,虚热时,cAMP,cAMP/cGMP升高,虚寒时,cAMP、cAMP/cGMP降低[29],为中医微观辨证之一[30]。结果显示,地塞米松组小鼠症状基本符合阴虚(虚热)表观诊断指标;氢化可的松组小鼠症状基本符合阳虚(虚寒)表观诊断指标。辛热中药附子干预虚寒、虚热小鼠后,虚寒小鼠cAMP,cAMP/cGMP含量升高,体质量能够增长至正常水平,状态恢复;而虚热小鼠cAMP,cAMP/cGMP仍处于高水平体质量则出现负增长,精神状态未得到改善。因此表明,附子作用于寒热不同机体状态时,环核苷酸差异性表达,且对于体重与精神状态的改变呈相反趋势。
同时,机体状态不同,NEI网络相关指标亦有不同。研究表明,虚热状态下,交感神经兴奋,NE和DA含量增加、5-HT含量减少[2];而虚寒状态下,中枢神经系统被抑制, NE和DA含量减少,5-HT含量增加或减少,其减少原因可能与5-HT系统受到损坏有关[3-4]。而神经递质水平的异常,则会进一步影响到内分泌与免疫系统。研究表明,虚热状态下,内分泌功能亢进,T3和T4含量增加[5],虚寒状态下,T3和T4含量则会减少[6]。另外,研究发现虚热状态下,IgG、IgM、补体C3均升高,免疫功能呈现为相对亢进状态,其机制可能为阴不制阳,阳气相对亢进,正气处于“虚”的相对亢奋状态[7];虚寒状态时机体免疫力低下,降低IgG、IgM、补体C3的合成[8]。本实验中虚热模型组小鼠神经递质(NE、DA)、内分泌激素(T3、T4)、免疫因子(C3、C4、IgG、IgM)的含量均升高,神经递质5-HT含量降低;表明虚热状态下小鼠的NEI网络异常表现为:中枢神经系统亢奋,内分泌激素分泌增加,免疫功能亢奋[7]。虚寒模型组小鼠神经递质(NE、DA、5-HT)、内分泌激素(T3、T4)、免疫因子(C3、C4、IgG、IgM)含量均降低;表明虚寒状态下小鼠NEI网络异常表现为:中枢神经系统抑制,内分泌激素分泌减少,免疫功能低下。
附子作用于寒热不同机体状态小鼠后,低剂量附子能使虚寒小鼠的T3、IgG、IgM水平得到恢复,高剂量附子能使纠正虚寒证小鼠神经递质水平低下、内分泌系统和免疫功能的紊乱;而虚热证小鼠经附子干预后,小鼠神经递质、内分泌因子和免疫因子仍处于异常水平,表明附子在寒热不同机体状态下对NEI网络系统具有不同的生物学效应。
AMPK信号通路作为连接NEI网络的主要信号通路之一,能够通过FASN、PFKFB3、SCD1、IRS2基因进行调节。研究表明FASN能够影响中枢神经系统[11],以及神经网络的结构方面[12],且在甲状腺功能亢进(虚热)状态下被诱导上调[31]。PFKFB3能够诱导巨噬细胞的糖酵解通量增加,增强M1型巨噬细胞的促炎功能,抗原呈递MHC复合物高表达,在机体免疫应答过程中发挥重要作用[14-16]。另外,SCD1的表达不仅影响内分泌甲状腺[18],且参与炎症反应[32-33]。也就是说,AMPK信号通路通过调节FASN、PFKFB3、SCD1基因靶点参与调控NEI网络的生理功能,本研究结果显示,附子能够显著抑制虚寒小鼠FASN、PFKFB3、SCD1的mRNA表达,而对虚热状态小鼠FASN、PFKFB3、SCD1基因表达无统计学差异。表明,附子作用于寒热不同机体状态下通过调控AMPK信号通路上FASN、PFKFB3、SCD1基因表达进而影响NEI网络的生物学效应的不同。
另外,AMPK信号通路上另一基因靶点IRS2是胰岛素发挥作用的重要基因[34],参与了NEI网络内分泌甲状腺的正常生理过程[20]。除此之外,IRS2还能够介导中枢神经系统内胰岛素信号级联效应[21],文献表明,上调IRS2能够导致巨噬细胞分泌引起胰岛素抵抗的因子,参与神经与免疫相互作用的信号传导过程,同时影响细胞炎症反应,在免疫应答中发挥作用[22]。本研究结果表明,无论是虚寒状态还是虚热状态下,附子均能显著抑制IRS2的mRNA表达,这就提示IRS2可能是附子作用于寒热不同机体状态下发挥“效—毒”双向生物效应的机制之一,值得后续进行深入研究。
综上,依据“药性构成三要素”假说,中药药性是药物成分作用于特定的机体状态,所发生的复杂的、多层次的生物学正负效应的综合表达。本研究基于辛热药性的中药附子作用于不同机体状态机体后其神经—内分泌—免疫网络生物效应表达的机制开展了研究,发现AMPK信号通路上FASN、PFKFB3、SCD1基因位点可能是其“辨证用药”的关键靶点,而IRS2基因可能是附子产生“效—毒”双向作用的机制,还需进一步研究。
