清胰化瘀通腑方治疗急性胰腺炎作用机制的网络药理学和分子对接研究*
2023-09-07蔡锐娜胡仕祥
蔡锐娜 陈 乾 赵 哲 胡仕祥△
(1.河南中医药大学,河南 郑州 450008;2.河南省中医院,河南中医药大学第二附属医院,河南 郑州 450002)
急性胰腺炎(AP)是临床常见急腹症[1],AP 发病急,进展快,常呈自限性,但仍有约20%~30%的患者虽积极治疗发展为单个或多脏器功能障碍,其中死亡率可高达30%~50%[2-3],严重威胁人类的健康。近年来的临床实践与基础研究发现[4-6],中医药对AP 的治疗具有独特优势,西医常规治疗与中医药并用的中西医结合治疗能取得满意的临床疗效。
课题组根据临床治疗AP的经验,总结出中药复方清胰化瘀通腑汤,组方:生大黄10 g(后下),茵陈蒿15 g,芒硝10 g(冲),桃仁10 g,柴胡10 g,厚朴10 g,木香5 g,丹参10 g,红花10 g,延胡索15 g,金银花10 g,连翘10 g。以清热利湿、化瘀通腑为法,应用于临床能有效减轻AP患者不同严重程度的炎症反应,促进患者临床症状恢复。但其治疗AP 的机制因复方成分复杂无法全面阐述,本研究运用网络药理学来探讨清胰化瘀通腑方治疗AP的主要成分及靶点,并利用分子对接技术进行验证,为后续更深层次地探讨清胰化瘀通腑方的主要调控靶点及作用机制提供一定的理论基础。现报告如下。
1 资料与方法
1.1 清胰化瘀通腑方活性成分的筛选和靶点预测 将清胰化瘀通腑方中的药物输入到中医药系统药理学数据库分析平台TCMSP[7]中,筛选条件设置为口服生物利用度(OB)≥30%且类药性(DL)≥0.18[8],从而获得药物活性成分,并根据已有文献报道对筛选结果进行补充,避免遗漏。将药物活性成分导入Pubchem(https://pubchem.ncbi.nlm.nih.gov/)数据库中得到对应的SMILES,再通过SwissTargetPrediction[9]数据库将物种限定为“Homo sapiens”,对清胰化瘀通腑方活性成分进行潜在靶点预测(因TCMSP 中没有矿石类中药,故用BATMAN-TCM[10]数据库补充筛选芒硝的活性成分及靶点)。对上述结果汇总去重并通过UniProt(https://www.uniprot.org/)数据库对靶点信息进行规范,获得清胰化瘀通腑方活性成分的潜在靶点。
1.2 AP 疾病靶基因的筛选 以“AcutePancreatitis”为关键词在GeneCards[11]、DrugBank[12]、OMIM[13]、TTD[14]疾病数据中检索AP 的潜在靶点,将4 个疾病数据库得到的靶点汇总去重后得到AP 靶点。将清胰化瘀通腑方潜在靶点与AP 靶点输入Venny 在线软件,绘制韦恩图获取清胰化瘀通腑方-AP 交集靶点,得到的交集靶点即为清胰化瘀通腑方治疗AP的作用靶点。
1.3 PPI网络的构建与关键靶点的筛选 将清胰化瘀通腑方—急性胰腺炎交集靶点导入STRING 数据库,按物种为“Homo sapiens”,最小互相作用阈值“highest confidence”(>0.9)[15]为检测条件,剔除游离靶点后得到蛋白互作信息,通过Cytoscape3.7.2 软件的Network Analyzer 工具分析其网络拓扑参数,并绘制PPI网络模型。运用CytoNCA[16]拓扑分析各个节点的属性值,包括中介中心性(BC)、接近中心性(CC)、度中心性(DC)、网络中心性(NC)和局部边连通性(LAC),选出同时满足BC、CC、DC、NC、LAC>中位数的所有节点作为关键靶点。
1.4 清胰化瘀通腑方治疗AP 的富集分析 将清胰化瘀通腑方治疗AP 的作用靶点的基因Symbol 通过Uniprot 数据库转换为基因ID,利用R 语言以P≤0.05为筛选条件进行GO和KEGG通路富集分析,并将结果绘制成条形图和气泡图。
1.5 建立清胰化瘀通腑方“药物-活性成分-作用靶点”调控网络 通过Cytoscape3.7.2 构建“药物-活性成分-作用靶点”网络图,运用Network Analyzer 工具拓扑分析活性成分和作用靶点,筛选出发挥药效的核心成分,可供使用的筛选条件包括连接度(Degree)、BC 及CC等。
1.6 分子对接 从PubChem 中下载“药物-有效成分-作用靶点”拓扑分析排名前5 的核心成分的小分子结构,应用Chem3D 软件进行优化,并转换为3D 格式。在PDB 数据库(http://www.rcsb.org/)中筛选PPI网络中拓扑分析排名前5 的核心靶点的蛋白结构,用PyMOL软件对其脱水并剔除原配体,利用AutoDockTools1.5.6和AutoDock Vina 完成分子对接,对部分对接结果用PyMOL软件进行可视化。
2 结 果
2.1 清胰化瘀通腑方有效活性成分筛选及靶点获取 见表1。从TCMSP 中下载大黄、茵陈蒿、桃仁、柴胡、厚朴、木香、丹参、红花、延胡索、金银花、连翘中符合OB 值及DL 值筛选条件的所有活性成分,从BATMAN-TCM 数据库筛选芒硝活性成分,剔除重复值后剩余230 个活性成分。将柴胡、丹参、红花成分标记为A,柴胡、红花、延胡索、金银花、木香共有成分标记为B,柴胡、红花、延胡索、连翘、茵陈蒿、金银花共有成分标记为C,柴胡、红花、连翘、金银花共有成分标记为D,柴胡、茵陈蒿共有成分标记为E,大黄、红花、连翘、桃仁、茵陈蒿、金银花共有成分标记为F,丹参、红花共有成分标记为G,丹参、红花、连翘、金银花共有成分标记为H,红花、金银花共有成分标记为I,连翘、木香共有成分标记为J,连翘、延胡索共有成分标记为K,木香、延胡索共有成分标记为L。通过Swiss Target Prediction预测活性成分的相关靶点(芒硝1 个活性成分的相关靶点通过BATMAN-TCM 数据库补充),对结果汇总去重后剩余734个靶点。

表1 药物中存在的共有活性成分
2.2 AP 相关靶点的预测 见图1。从Genecards、DrugBank、OMIM、TTD 疾病数据库得到AP 靶点个数分别为9 072、6、185、6,汇总去重后得到AP 相关靶点1 269 个。将2.1 得到的清胰化瘀通腑方潜在靶点与AP 靶点输入Venny 在线工具,绘制韦恩图,并获取清胰化瘀通腑方-AP交集靶点179个。

图1 清胰化瘀方通腑方-AP交集靶点韦恩图
2.3 PPI 的构建与核心靶点的筛选 见图2、表2。将清胰化瘀通腑方-AP交集靶点输入STRING数据库,剔除25个游离靶点后得到蛋白互作信息,将其导入Cytoscape3.7.2 软件,PPI 网络模型见图2A,图中共154 个节点,723 条边,节点面积越大、颜色越深Degree 值越高,边越粗相关性越强。经CytoNCA 计算网络中各个节点的属性值,并按中位数进行2 次筛选,得到包括STAT3、PIK3R1、PIK3CA、RHOA、RAC1 等14 个靶点,见图2B,靶点的拓扑分析参数见表2。这些靶点节点大、颜色深,相关性强,可能在清胰化瘀通腑方治疗AP中发挥关键作用。

图2 PPI蛋白互作网络和核心靶点

表2 清胰化瘀通腑方作用AP核心靶点的网络节点特征参数
2.4 GO和KEGG通路富集分析 见图3、图4。将179个作用靶点的Uniprot 号通过Uniprot 数据库转换为entrez 号,然后利用R 语言根据P≤0.05 对GO 的BP(biological process)、CC(celluar component)、MF(molecular function)及KEGG 通路进行富集分析。清胰化瘀通腑方参与的BP 条目主要包含肽基-酪氨酸磷酸化、肽基-酪氨酸修饰和激酶活性的正向调节等2 398 个;CC 条目主要包含膜筏、膜微区、黏着斑等89 个;MF 条目主要包含蛋白丝氨酸/苏氨酸激酶活性、内肽酶活性、跨膜受体蛋白激酶活性等184 个。根据P 值分别选取BP、CC、MF 排名前10 的生物过程绘制条形图。清胰化瘀通腑方参与的通路主要包括PI3K-Akt、脂质和动脉粥样硬化、癌症中蛋白多糖等169 条,选取P 值排名前20的通路绘制气泡图。
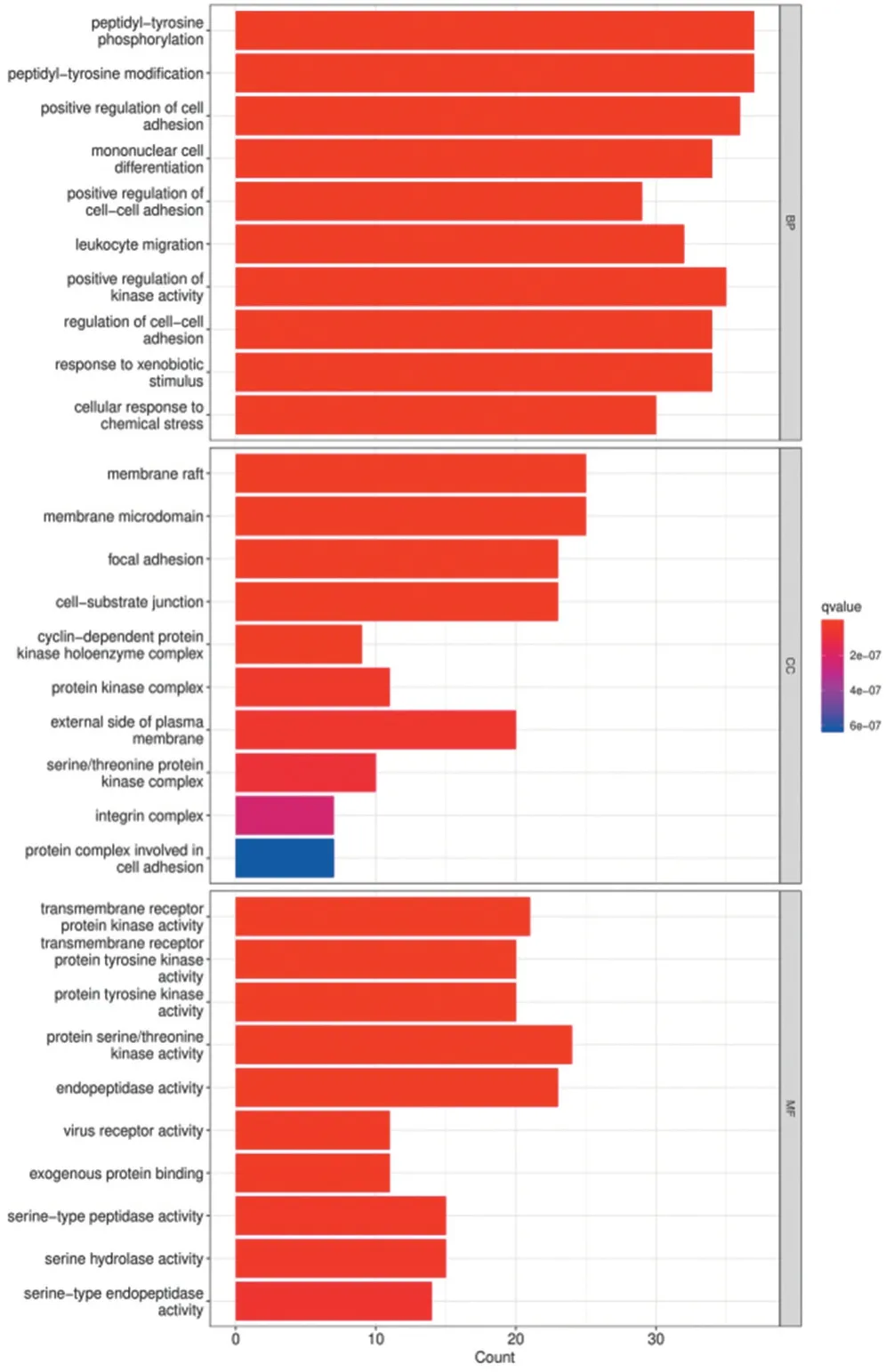
图3 清胰化瘀通腑方治疗AP的GO分析

图4 清胰化瘀通腑方治疗AP的KEGG分析
2.5 清胰化瘀通腑方“药物-活性成分-作用靶点”调控网络的构建 见表3、图5。将药物、活性成分及清胰化瘀通腑方治疗AP 的作用靶点输入CytoScape3.7.2中,得到“药物-活性成分-作用靶点”网络图,并用内置的NetworkAnalyzer 插件分析清胰化瘀通腑方治疗AP的网络拓扑学参数,网络图见图5。图5由345个节点和2280 条边组成,其中药物用圆形节点表示,活性成分以六边形表示,靶点以菱形表示;面积越大、颜色越深说明Degree 值越大,提示该节点越重要。分析结果表明,槲皮素(quercetin)的Degree 值为32,且为柴胡、红花、延胡索、连翘、茵陈蒿、金银花共有成分;山柰酚(kaempferol)的Degree 值为31,且为柴胡、红花、连翘、金银花共有成分;木樨草素(luteolin)的Degree值为30,且为丹参、红花、连翘、金银花共有成分;氧杂蒽酮(Onjixanthone I)的Degree 值为30;异鼠李素(isorhamnetin)的Degree 值为29,且为柴胡、茵陈蒿共有成分,所以预测这5 种药物成分可能为清胰化瘀通腑方治疗AP的核心成分。

图5 药物-活性成分-作用靶点网络图

表3 清胰化瘀通腑方核心成分网络节点特征参数
2.6 分子对接 见图6、图7。将清胰化瘀通腑方核心成分quercetin、kaempferol、luteolin、Onjixanthone I 及isorhamnetin 分别与2.3 中PPI 网络拓扑分析排名前5的核心靶点STAT3、PIK3R1、PIK3CA、RHOA、RAC1 进行分子对接,结合自由能<-5 kcal/mol,表明受体与配体之间具有良好的结合活性,结合活性结果统计如图6 所示,热图中颜色越红,代表结合活性越高。并用PyMOL软件对部分对接结果进行图片展示。

图6 核心成分-核心靶点分子对接热图

图7 核心活性成分与核心靶点部分对接
3 讨 论
中医学并无AP之名,但根据其临床表现及疼痛部位,将其归属于“腹痛”“脾心痛”“胰瘅”等范畴[17],胰腺根据其部位,当属中医六腑范围,按照“六腑以通为用,以降为顺”的理论,将通里攻下法贯穿本病治疗的始终,采用清热通腑、祛瘀通腑、通腑祛湿等治法,不局限于胰腺局部,而是注重于整体功能的调节,不仅可以针对AP 的病因进行治疗,同时可以有效缓解AP 引起的一系列并发症。近年来的临床实践与基础研究发现,西医常规治疗与中医药并用的中西医结合治疗AP能取得满意的临床疗效[18-20]。
课题组总结多年临床经验,综合各医家所长,认为AP患者虽然症状各异,但其病机相同,皆由饮食不节、外感六淫之邪等,导致脾胃健运失司,气机升降失常,腑气不畅,进而逐渐演变成为以热、湿、瘀、毒等蕴结中焦的病变,因此,在疾病早中晚期,毒瘀互结是其主要病机,“毒”为病机,“瘀”为演变。清胰化瘀通腑方清热利湿、化瘀通腑,以大黄、芒硝、茵陈蒿、桃仁为君,大黄、芒硝具有泻热存阴之功,茵陈蒿清利湿热、桃仁活血化瘀,四药共奏通腑泄热、利湿化瘀、釜底抽薪之效;柴胡、厚朴、木香理气并助硝黄通腑,丹参、红花活血化瘀助桃仁解瘀滞共为臣药;金银花、连翘助大黄、芒硝清热解毒、透邪外出,延胡索助桃仁、柴胡活血理气止痛共为佐使药。
本研究中网络药理学初步筛选出清胰化瘀通腑方治疗AP 的活性成分主要包括槲皮素、山柰酚、木樨草素、氧杂蒽酮、异鼠李素等,且部分活性成分多味药物的重复成分,如槲皮素重复6 次,山柰酚、木犀草素重复4 次,异鼠李素重复2 次。研究显示,槲皮素是一类对炎症预防有积极作用的黄酮化合物,调节各种参与致癌和信号转导途径的蛋白,可通过上调miR-216b来抑制肿瘤坏死因子-α(TNF-α)及p38/MAPK 信号通路从而对AP 具有保护作用[21],并抑制表皮生长因子诱导的胰腺癌细胞的迁移活性[22]。山柰酚可抑制NFκB 信号通路的激活来减少炎症因子的产生,减轻AP的炎症反应,改善AP 预后[23],也以剂量依赖的方式抑制人胰腺癌细胞(PANC-1)增值及NF-κB、血管内皮细胞生长因子(VEGF)蛋白表达水平而诱导胰腺癌细胞凋亡并抑制其侵袭[24]。木樨草素通过诱导血红素加氧酶(HO-1)介导的抗炎和抗氧化作用来抑制NFκB 通路的活性、降低脂质过氧化作用、降低TNF-α、丙二醛(MDA)的表达来保护胰腺组织[25-26],也可通过抑制白细胞介素-6(IL-6)、STAT3 通路、EGFR-ras 通路和SOX9 蛋白,从而抑制因AP 诱导的与胰腺癌关系密切的腺泡导管化生、细胞增殖和上皮-间充质转化,减缓胰腺炎进展为胰腺癌的过程[27]。异鼠李素可抑制NF-κB 信号通路的活性、减少炎症因子的释放来发挥抗炎作用[28],并可降低Ras/MAPK 通路中MEK 和ERK的磷酸化水平,阻滞胰腺癌细胞系PANC-1 中的细胞生长,从而预防胰腺癌的发生[29]。由此可见,以槲皮素、山柰酚、木樨草素、异鼠李素为代表的活性成分在清胰化瘀通腑方治疗AP中发挥了重要作用。
在PPI 蛋白互作网络中,筛选出清胰化瘀通腑方治疗AP的核心靶点主要包括STAT3、PIK3R1、PIK3CA等。胰腺组织中STAT3 的活化与AP 的病变危重程度密切相关[30],STAT3 在包括胰腺癌在内的多种癌症中呈现出过表达,并导致肿瘤细胞的生长、侵袭和转移[31],且AP 可激活IL-6 和TNF-α 诱导的STAT3 信号通路,促进炎症反应、胰腺纤维化和细胞凋亡[32],导致肺损伤甚至多器官功能障碍[33-35],抑制STAT3 活性是缓解AP 进展的潜在靶标[35]。PI3K 所参与的PI3K/Akt信号通路可通过调控腺泡细胞的炎症反应、凋亡、自噬、氧化应激等,对AP 的发生发展及治疗起重要作用[36],而分别编码PI3K 催化亚基p110α、调节亚基p85α 的PIK3CA 和PIK3R1 均参与PI3K/Akt 通路,两个基因的功能缺陷均可导致PI3K/Akt 通路异常[37-38]。富集分析作用靶点的结果显示,清胰化瘀通腑方治疗AP 可能通过PI3K/Akt、脂质和动脉粥样硬化、癌症中蛋白多糖等信号通路。PI3K/Akt控制着多种信号传导通路,以往的许多实验中已证实了其在炎症反应中的作用,而且它与NF-κB、IL-6 也密切相关[39],是AP 发生发展过程中的重要信息通路。PI3K 通过影响AP 疾病过程中胰蛋白酶原激活、钙超载和NF-κB 通路,从而对胰腺腺泡细胞的病理反应进行调控[40],并通过调节促炎细胞因子密切影响着AP 的严重程度[41]。激活PI3K/Akt 下游通路NF-κB 可引起腺泡细胞发生氧化应激反应,并诱导细胞自噬[42],加强胰腺损伤和坏死程度[43-44]。而抑制PI3K/Akt 信号通路的激活可抑制NF-κB 通路,阻止细胞凋亡,减轻炎症反应[45-46],同时阻止活性氧(ROS)的产生,减轻AP 中甲状腺的损伤[47]。故推测清胰化瘀通腑方可能通过抑制PI3K/Akt 信号通路来治疗AP。本研究分子对接结果显示,槲皮素、山柰酚、木樨草素、异鼠李素与STAT3、PIK3R1、PIK3CA等均具有良好的结合活性。
本研究发现,清胰化瘀通腑方可能通过槲皮素、山柰酚、木樨草素等多种活性成分,调控STAT3、PIK3R1、PIK3CA 等多个靶点,干预PI3K/Akt 等多条信号通路,从抗炎、抗细胞凋亡、抗氧化应激等方面来治疗AP,为临床应用清胰化瘀通腑方治疗AP 提供了科学依据。后续将在此基础上继续深入研究,进行动物或细胞实验验证,更深层次地探讨清胰化瘀通腑方的主要调控靶点及作用机制,以期为开发利用中医药治疗AP提供新思路。
