新型匹维溴铵多晶型的性能分析
2023-09-06沈意周陈正国庄江海庄程瀚张朝霞张国庆
沈意周 陈正国 庄江海 庄程瀚 张朝霞 张国庆


摘 要: 为分析匹维溴铵的多晶型以及不同晶型之间性能的差异,通过溶剂介导的悬浮搅拌结晶技术分别在二氧六环、异丙醇、丙酮、乙腈/水(1/1,v/v)体系中制备出了4种晶型,利用X射线粉末衍射仪(XRPD)、掃描电子显微镜(SEM)、热重分析仪(TGA)、差示扫描量热仪(DSC)和傅里叶红外光谱(FT-IR)对其进行结构和性能表征;在pH值为1.2和6.8的条件下比较了4种晶型的溶解度,并在高温高湿、研磨和压力的条件下分析不同晶型的稳定性。结果表明:匹维溴铵的4种晶型分别具有不同的X射线特征峰以及热力学性能,其中晶型Ⅰ、晶型Ⅱ和晶型Ⅲ是无水晶型,晶型Ⅳ是一种二水合物;晶型Ⅳ在pH值1.2中平衡溶解度最低,仅有1.47 mg/mL,而在pH值6.8中最高,达到了13.83 mg/mL,相比于传统晶型Ⅰ,晶型Ⅳ在强酸条件下损耗更少而在中性条件下具有更优的溶解性能;稳定性研究结果表明晶型Ⅰ和晶型Ⅳ均具有较为良好的稳定性能。该研究制备了新型的匹维溴铵,丰富了匹维溴铵的多晶型产品,对开发新型匹维溴铵的活性药物成分具有重要意义。
关键词: 匹维溴铵;多晶型;二水合物;溶剂介导;X射线粉末衍射;平衡溶解度
中图分类号: R917 文献标志码: A 文章编号: 1673-3851 (2023) 03-0206-07
引文格式:沈意周,陈正国,庄江海,等. 新型匹维溴铵多晶型的性能分析[J]. 浙江理工大学学报(自然科学),2023,49(2):206-212.
Reference Format: SHEN Yizhou, CHEN Zhengguo, ZHUANG Jianghai,et al. Performance analysis of new pinaverium bromide polymorphs[J]. Journal of Zhejiang Sci-Tech University,2023,49(2):206-212.
Performance analysis of new pinaverium bromide polymorphs
SHEN Yizhou1, CHEN Zhengguo1, ZHUANG Jianghai2, ZHUANG Chenghan2, ZHANG Zhaoxia1, ZHANG Guoqing1
(1. School of Materials Science & Engineering, Zhejiang Sci-Tech University, Hangzhou 310018, China; 2. Zhejiang Apeloa Jiayuan Pharmaceutical Co., Ltd., Dongyang 322100, China)
Abstract: In order to analyze the polycrystalline forms of pinaverium bromide and the differences in properties between different crystalline forms, four crystalline forms were prepared by solvent-mediated suspension-stirring crystallization in dioxane, isopropanol, acetone and acetonitrile/water (1/1,v/v) systems, respectively, and their structures and properties were characterized by X-ray powder diffraction (XRPD), scanning electron microscopy (SEM), thermogravimetric analysis (TGA), differential scanning calorimetry (DSC) and Fourier infrared spectroscopy (FT-IR). The solubility of the four crystalline forms were compared at the pH values of 1.2 and 6.8, and the stability of the different crystalline forms was analyzed under high temperature and high humidity, grinding and pressure conditions. The results show that the four crystalline forms of pinaverium bromide have different X-ray characteristic peaks as well as thermodynamic properties. Specifically, crystalline form I, crystalline form Ⅱ and crystalline form Ⅲ are crystal-free and crystalline form Ⅳ is a dihydrate; crystalline form Ⅳ has the lowest equilibrium solubility at pH 1.2 with only 1.47 mg/mL and the highest at pH 6.8 with 13.83 mg/mL, and compared with the traditional crystalline form I, crystalline form Ⅳ has less loss under strong acid conditions and better solubility under neutral conditions; the stability study results show that both crystalline form I and crystalline form IV have good stability performance. We prepare a new form of pinaverium bromide, which has enriched the multi-crystalline products of pinaverium bromide and is of great siginificance for the development of new active pharmaceutical ingredients of pinaverium bromide.
Key words: pinaverium bromide; polymorph; dihydrate; solvent-mediated; X-ray diffractometer; equilibrium solubility
0 引 言
對晶型的研究贯穿药物开发的整个过程[1-3]。多晶型现象在固体药物中普遍存在[4];药物多晶型通常用来描述一种药物可以以不同的晶相存在的现象,其对药物质量和疗效的影响,引起了人们极大的兴趣[5-7]。多晶型药物通常包括稳定型、亚稳定型、不稳定型、溶解型和非晶型[8],各种多晶型的药物可能表现出不同的物理和化学特性,包括溶解度、溶出率、生物利用度、熔点、密度、压缩性、流动性和化学稳定性[9-11]。因此,在药物研究过程中应尽可能多地发现新晶型,对这些新晶型进行评估并从中选择一种有效且质量可控的药物晶型极其重要[12]。目前应用最广泛的多晶型筛选方法之一是将药物放在各种溶剂中重结晶。根据Ostwald [13]提出的阶段性规则,在不同溶剂中重结晶时容易获得可转移的多晶型。由于溶剂的影响,溶质分子会表现出不同的溶解度,从而改变溶质和溶剂分子之间的作用力,如氢键和范德瓦尔斯力[14-15],因此溶剂介导的悬浮搅拌结晶技术被开发出来,并广泛用于筛选最稳定的多晶型[16]。在一个典型的饱和溶液中,稳定的晶型将在反复溶解和沉淀过程中形成,该过程一般分为三步:第一步是起始晶型的溶解,第二步是稳定晶型的成核,第三步是稳定晶型的生长。在药物的晶型研发中,科研人员通过溶剂介导的悬浮搅拌结晶技术发现了许多稳定的药物多晶型,使该技术广泛应用于药物多晶型研发生产中。
匹维溴铵,化学名称为N(2-溴-4,5-二甲基苄基)-N(2[双甲基-2-去甲基蒎烷基]乙氧基)乙基)吗啉溴,是一种非抗胆碱能的肌肉解痉剂,自1977年以来一直作为口服药用于肠道治疗。目前,关于匹维溴铵晶型的报道只有晶型Ⅰ和无定形[17-18],其中晶型Ⅰ为目前匹维溴铵的药用晶型。匹维溴铵作为肠道用药物,其在体内作用过程应该具有一定的选择性,特别是相比于在胃部环境中,匹维溴铵在肠道环境中应具有更好的溶解性能。
本文通过溶液介导的悬浮搅拌结晶法制备了4种匹维溴铵晶型产品(晶型Ⅰ、晶型Ⅱ、晶型Ⅲ和晶型Ⅳ),通过X射线粉末衍射(XRD)、差示扫描量热法(DSC)、热重分析(TGA)、傅里叶变换红外光谱(FT-IR)和扫描电子显微镜(SEM)对其进行了表征分析,研究了4种晶型在不同pH值下的溶解性能,探索了4种晶型的稳定性,为后续匹维溴铵的制剂生产提供了一定的理论指导。
1 实验部分
1.1 实验材料
匹维溴铵化合物原料由浙江普洛家园药业有限公司提供;1,4-二氧六环(化学纯度≥99.7%)、异丙醇(化学纯度≥99.7%)和丙酮(化学纯度≥99.5%)购自杭州双林化学试剂有限公司;去离子水(电导率1 μS/cm)实验室自制。
1.2 多晶型制备
采用溶剂介导的悬浮搅拌结晶法制备新晶型,溶剂及对应的晶型如表1所示。具体制备过程:在搅拌状态下向4 mL二氧六环、异丙醇、丙酮或乙腈/水(1/1, v/v)中加入200 mg的匹维溴铵化合物原料配置成悬浮液,搅拌12 h后,将悬浮液过滤后得到滤饼,将滤饼在40 ℃下干燥24 h,最后得到多晶型样品。
1.3 测试与表征
1.3.1 晶型测试
使用D8 Advance衍射仪(Bruker,德国)对样品进行X射线粉末衍射测试。取30~50 mg的样品置于玻璃片上,压至平整后放入仪器进行测试,设置条件Cu-Kα辐射,管电压和管电流分别设置为40 kV和40 mA,2θ范围为3°~40°,扫描速度为3(°)/min。
1.3.2 表观形貌观测
使用Gemini SEM-500场发扫描电子显微镜(Zeiss,德国)观察匹维溴铵多晶型的表观形貌。将3~5 mg的样品均匀洒在导电胶上,利用离子衍射仪进行镀金(10 mA,1 min),然后在3 kV的工作电压下进行观察。
1.3.3 热性能测试
主要通过差示扫描量热仪(DSC)和热重分析仪(TGA)对样品的热力学性能进行测试。
使用Q2000差示扫描量热仪(美国TA公司)进行DSC实验。将3~8 mg的样品密封在铝盘中,在N2氮气保护气体的条件下(流量为50 mL/min)以10 ℃/min的速度从室温升到200℃。
使用Pyris 1热重分析仪(PerkinElmer,美国)进行TGA分析。将3~8 mg的样品置于坩埚中,设置范围从25~400 ℃,在N2为保护气体的条件氮气保护下(流量为50 mL/min)以10 ℃/min的速度升温。
1.3.4 分子结构测试
采用FT-IR光谱仪(Thermo Nicolet,美国)KBr透射模式收集样品的红外光谱。将样品与KBr按照1∶100的体积比混合研磨,在15 MPa的压力条件下进行压片,随后进行检测。每个样品在4000~400 cm-1范围内扫描,分辨率为4 cm-1。
1.3.5 平衡溶解度测试
使用静态重量法[19-20]在37℃下不同pH值的磷酸盐缓冲溶液中测定匹维溴铵晶型I、Ⅱ、Ⅲ和Ⅳ的溶解度。首先取一个烧瓶,在其中加入1 mL磷酸盐缓冲液,放入40 ℃烘箱中烘干,取出后进行称量直至质量不再发生改变,此时记为M1。取新的空瓶,将待测样品和pH 1.2或pH 6.8的磷酸盐缓冲液分别进行混合振荡,振荡24 h后用0.22 μm滤膜过滤出澄清液,取1 mL澄清液放入空瓶中,在40 ℃烘箱中烘干,取出后再对瓶子进行称量直至质量不再发生改变,记为M2。溶解度计算如式(1)所示:
S=(M2-M1)/V(1)
其中:S为药物的溶解度,mg/mL;M2为加入药物和磷酸盐缓冲液烘干溶剂后瓶子的质量,mg;M1为只加入磷酸盐缓冲液烘干溶剂后瓶子的质量,mg;V为澄清液体积,mL。每个样品都进行3次平行实验,计算出平均值和标准偏差。
pH值1.2磷酸盐缓冲液的配置:量取9 mL浓盐酸,加水稀释至1000 mL。pH值6.8磷酸盐缓冲液的配置:称量6.800 g磷酸二氢钾与0.896 g氢氧化钠,随后加水溶解转至容量瓶,稀释至1000 mL。
1.3.6 稳定性表征
通过将样品放置在不同的温度、湿度、研磨和压力条件下来研究匹维溴铵4种晶型的稳定性能。温度湿度稳定性实验条件如下:将100 mg样品储存在温度为40 ℃、相对湿度为75%的密闭环境中3个月,每隔1个月取出部分样品进行XRD测试。
通过在研钵中分别研磨100 mg晶体样品1、3 min和5 min来测试研磨稳定性,用XRD对研磨后的样品进行分析,以监测其晶体结构的变化。对于压力稳定性测试,将100 mg的晶体样品放在一个模具中,分别在5 、10 MPa和15 MPa的压力下压制1 min,然后取出样品进行XRD测试。
2 结果与讨论
2.1 X射线粉末衍射分析
分子在晶格中的不同排列方式会导致其在XRD图谱中的衍射峰产生明显差异,因此X射线粉末衍射仪是鉴别药物多晶型最有效的方法[21]。匹维溴铵4种晶型的XRD图谱如图1所示,晶型Ⅱ、晶型Ⅲ、与晶型Ⅳ的XRD图与之前Quintana等[17]报道的晶型I的XRD图不同,晶型Ⅱ在6.119°、14.074°、16.517°、18.411°、18.635°、19.758°、23.939°、24.167°、24.674°和25.449°出现了特征衍射峰,而晶型Ⅲ在5.527°、10.545°、14.415°、17.702°、19.579°、20.170°、20.311°、23.634°、24.208°和25.082°出现了特征峰,晶型Ⅳ则在5.875°、12.256°、13.830°、15.803°、17.967°、19.597°、21.718°、24.002°、24.614°和24.980°出现了特征峰。XRD表征证实了匹维溴铵的新晶型的存在,通过XRD衍射图谱,匹维溴铵的晶型Ⅰ、晶型Ⅱ、晶型Ⅲ和晶型Ⅳ可以很容易地相互区分。
2.2 扫描电子显微镜分析
晶体在不同溶剂中的生长显然会导致不同的形态[22],通过扫描电子显微镜可以观察晶体的微观形貌,图2为4种晶型的扫描电镜图。晶型Ⅰ是不规则的小块聚集,单个小块的大小约为1~4 μm;晶型Ⅱ具有明确的块状形态,表面相对光滑,尺寸为10~20 μm;晶型Ⅲ主要由块状棒状物组成,长度约为4~10 μm,宽度为2~4 μm;晶型Ⅳ表现出小棒和小块的不规则堆积状态,大小约为20~60 μm。晶体形态变化主要是由于4种晶体是从不同溶剂中析出的,导致其具有不同的晶习,最终使产品的形貌产生差异[23]。
2.3 热性能分析
图3为匹维溴铵4种晶型的DSC和TGA图。由图3可知,4种晶型均表现出不同的热力学性能。晶型Ⅰ的DSC曲线显示167 ℃时有一个尖锐的吸热峰,TGA曲线显示167 ℃之后过程中有明显的质量损失,与文献中报道的数据[17]一致;晶型ⅡDSC曲线上在141.0 ℃和167 ℃有两个放热峰,由于TGA曲线在141 ℃时没有明显的质量损失,可能141.0 ℃的放热峰为晶型相转变导致;将晶型Ⅱ加热到150 ℃时发生了转晶现象,晶型Ⅱ转变成了晶型Ⅰ,同时在166.7 ℃的峰刚好是晶型Ⅰ的熔点,这也印证了晶型Ⅱ在加热过程中转化为晶型Ⅰ;晶型Ⅲ的DSC曲线在164 ℃处出现一个吸热峰,与晶型Ⅰ出现的167 ℃有明显差异,进一步证明了它是一种新的晶体形式。晶型Ⅳ的DSC图与其他晶型显著不同,分别在90 ℃和167 ℃有两个吸热峰,代表了溶剂蒸发和熔点;此外,晶型Ⅳ的TGA曲线在100 ℃前显示出明显的重量损失,由于在加热过程中晶格中的水分子蒸发导致,表明晶型Ⅳ是一种水合物,通过对TGA图中晶型Ⅳ的重量损失计算得知晶型Ⅳ中水的质量损失约为5.64%,与二水合物的理论值5.73%非常接近。综上所述,晶型Ⅳ是二水合物。对晶型Ⅱ和晶型Ⅳ进行热处理分析其晶型转变,将两种晶型加热到150 ℃并保溫1 min,然后进行XRD测试以确定在加热过程中是否发生转晶。结果发现,晶型Ⅱ和晶型Ⅳ在热处理后最终都转变为晶型Ⅰ,晶型Ⅱ转变为晶型I是由于分子晶格重排,而晶型Ⅳ是由于失水造成的。
2.4 傅里叶红外光谱分析
红外光谱是物质定性的重要的方法之一,光谱中吸收峰的位置、强度和形状可用于确定分子结构和分子间的相互作用[24]。图4中的FT-IR光谱显示了匹维溴铵4种晶型的性质,4种晶型的图谱均具有其典型的官能团吸收峰,对应的C—H的振动峰出现在2996~2946 cm-1,CC(芳香族)的振动峰出现在1601 cm-1,C—O—C的伸缩振动峰出现在1219 cm-1,C—N拉伸振动峰出现在1173 cm-1,C—Br的振动峰出现在885 cm-1,表明4种晶型具有相同的分子结构,在重结晶过程中没有发生任何副反应。另外,4种晶型在均带有一定的吸附水,吸附水的吸收峰出现在3435 cm-1附近;从晶型Ⅳ的红外谱图中还可观察到结晶水3300 cm-1处的伸缩振动峰以及1670 cm-1处的弯曲振动峰,这再次表明结晶水的存在。
2.5 平衡溶解度分析
药物的溶解度是考虑药物能否使用这种结晶形式作为原料药的一个重要指标[25],对于许多药物来说,有必要根据其溶解度来选择合适的替代给药途径。考虑到匹维溴铵是一种肠道药物,在不同的pH值环境中会呈现出不同的溶解性能,本文模拟胃液和肠道环境,评估了4种晶型在pH值分别为1.2和6.8的缓冲液中的平衡溶解度,其溶解度数据如表2和图5所示。匹维溴铵的4种晶型在pH值6.8的磷酸盐溶液中均表现出良好的溶解性能,在溶解度8.00~12.00 mg/mL,溶解性能排序晶型Ⅳ、晶型Ⅲ、晶型Ⅱ、晶型Ⅰ;在pH值1.2的模拟胃液环境中,4种晶型的溶解度下降到5.00 mg/mL以下,顺序为晶型Ⅰ、晶型Ⅱ、晶型Ⅲ、晶型Ⅳ。以上结果表明,新的晶型比已报道的晶型Ⅰ表现出更好的溶解行为,其中晶型Ⅳ相比于其他晶型,其在pH值从胃部到肠道的环境变化中具有更加良好的溶解性能,这使得更多的药物分子在肠道环境中发挥作用。
2.6 穩定性分析
对匹维溴铵的4种晶型进行了关于温湿度、研磨和压力条件的稳定性实验。在稳定性实验前后收集了样品的XRD衍射图。图6为在温度40 ℃、相对湿度75%条件下储存3个月的4种晶型的XRD结果,经过3个月的储存后可以发现,晶型Ⅰ、Ⅲ和Ⅳ一直保持稳定,XRD图没有变化,而晶型Ⅱ在储存2个月后开始显现晶型I的特征峰,形成了晶型Ⅰ和晶型Ⅱ的混晶。上述结果表明,晶型Ⅰ、Ⅲ和Ⅳ具有良好的湿热稳定性,而部分晶型Ⅱ在高温高湿条件下会转化为晶型Ⅰ。
4种晶型研磨实验结果的XRD图如图7所示,从图中可以看出,晶型Ⅰ、Ⅲ和Ⅳ都很稳定,研磨一定时间后,特征峰都未发生改变。但晶型Ⅱ在研磨1 min之后,XRD图谱显示晶型Ⅱ完全转变成了晶型Ⅰ。上述结果表明,在研磨条件下,晶型Ⅰ和晶型Ⅳ都具有良好的稳定性,而晶型Ⅱ在经过一定时间的研磨后会转化为晶型Ⅰ。
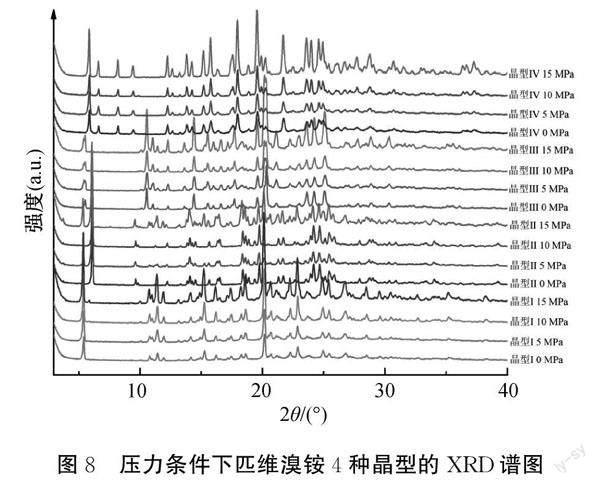
在5 、10 MPa和15 MPa的压力条件下,分别对匹维溴铵的4种晶型进行了压力稳定性测试,结果如图8所示。4种晶型在不同压力条件下的XRD图谱与未处理过的样品基本一致,未发生转晶现象(见图8),说明4种晶型在压力条件下可以保持稳定。
综上所述,晶型Ⅱ在外部条件的影响下会出现转晶现象,而晶型Ⅰ、晶型Ⅲ和晶型Ⅳ在各种条件下都表现出很好的晶体结构稳定性。特别是晶型Ⅳ,作为二水合物,有希望在后续的药物配方中使用。
3 结 论
本文通过溶剂介导的悬浮搅拌结晶法,制备了匹维溴铵的4种晶型,主要结论如下:
a)通过在二氧六环、丙酮、异丙醇以及乙腈和水的混合溶剂中悬浮搅拌获得匹维溴铵的4种晶型,其中晶型Ⅱ、晶型Ⅲ和晶型Ⅳ(二水合物)为匹维溴铵的新晶型,并具有不同的物理和化学特性。
b)匹维溴铵晶型Ⅱ、晶型Ⅲ和晶型Ⅳ与已报道的晶型Ⅰ相比,都具有更优的溶解度,特别是晶型Ⅳ(二水合物),在pH值6.8时平衡溶解度最高,而在pH值1.2时最低。
c)晶型Ⅳ在各种储存条件下都具有良好的稳定性,未发现有转晶以及结晶性下降的现象,有望成为新的制剂药用晶型。
参考文献:
[1]Lopes C S D, Bernardes C E S, Piedade M F M, et al. A new polymorph of 4-hydroxyvalerophenone revealed by thermoanalytical and X-ray diffraction studies[J]. European Physical JournalSpeccial Topics, 2017, 226(5): 849-855.
[2]Tao W, Zavalij P Y, Zachariah M R. Crystal structure of a new polymorph of iodic acid, δ-HIO3, from powder diffraction[J]. Powder Diffraction, 2017, 32(4): 261-264.
[3]Sharma K, Kalita A C, Murugavel R. Five different pseudo-polymorphs of 4-aminoarylphosphate: supramolecular aggregation in organophosphates[J]. CrystEngComm, 2017, 19(7): 1058-1070.
[4]冒莉,郑启泰,吕扬. 固体药物多晶型的研究进展[J]. 天然产物研究与开发,2005,17(3):371-375.
[5]Shi Q, Chen H B, Wang Y N, et al. Recent advances in drug polymorphs: Aspects of pharmaceutical properties and selective crystallization[J]. International Journal of Pharmaceutics, 2022, 611: 121320.
[6]Haleblian J, McCrone W. Pharmaceutical applications of polymorphism[J]. Journal of Pharmaceutical Sciences, 1969, 58(8): 911-929.
[7]Sarma B, Chen J, Hsi H Y, et al. Solid forms of pharmaceuticals: Polymorphs, salts and cocrystals[J]. Korean Journal of Chemical Engineering, 2011, 28(2): 315-322.
[8]Pindelska E, Sokal A, Kolodziejski W. Pharmaceutical cocrystals, salts and polymorphs: Advanced characterization techniques[J]. Advanced Drug Delivery Reviews, 2017, 117: 111-146.
[9]Chieng N, Rades T, Aaltonen J. An overview of recent studies on the analysis of pharmaceutical polymorphs[J]. Journal of Pharmaceutical and Biomedical Analysis, 2011, 55(4): 618-644.
[10]Singhal D, Curatolo W. Drug polymorphism and dosage form design: a practical perspective[J]. Advanced Drug Delivery Reviews, 2004, 56(3): 335-347.
[11]Li Y, Chow P S, Tan R B H. Quantification of polymorphic impurity in an enantiotropic polymorph system using differential scanning calorimetry, X-ray powder diffraction and Raman spectroscopy[J]. International Journal of Pharmaceutics, 2011, 415(1/2): 110-118.
[12]杨世颖,周健,张丽,等. 我国化学药物晶型研究现状与进展[J].医药导报,2019,38(2):177-182.
[13]Ostwald W. Studien über die bildung und umwandlung fester krper[J]. Zeitschrift Für Physikalische Chemie, 1896, 22U(1): 289-330.
[14]Du D, Ren G B, Qi M H, et al. Solvent-mediated polymorphic transformation of famoxadone from form II to form I in several mixed solvent systems[J]. Crystals, 2019, 9(3): 161.
[15]Gu C H, Young V Jr, Grant D J W. Polymorph screening: influence of solvents on the rate of solvent-mediated polymorphic transformation[J]. Journal of Pharmaceutical Sciences, 2001, 90(11): 1878-1890.
[16]Rodríguez-hornedo N, Murphy D. Significance of controlling crystallization mechanisms and kinetics in pharmaceutical systems[J]. Journal of Pharmaceutical Sciences, 1999, 88(7): 651-660.
[17]Quintana Mendoza J H, Aparicio A P, Henao J A. Powder diffraction data and preliminary spectroscopic and thermal characterization of pinaverium bromide, a drug used for functional gastrointestinal disorders[J]. Powder Diffraction, 2021, 36(1): 20-24.
[18]周浩辉,林国良,耿玉先,等. 无定形态的匹维溴铵:201410322869.8 [P]. 2016-02-10.
[19]Guo Y M, Hao Y H, Zhou Y N, et al. Solubility and thermodynamic properties of vanillyl alcohol in some pure solvents[J]. The Journal of Chemical Thermodynamics, 2017, 106: 276-284.
[20]Qin Y J, Wang H S, Yang P, et al. Measurement and correlation of solubility and dissolution properties of flunixin meglumine in pure and binary solvents[J]. Fluid Phase Equilibria, 2015, 403: 145-152.
[21]Jia L N, Li Z H, Gong J B. Two new polymorphs and one dihydrate of lenalidomide: solid-state characterization study[J]. Pharmaceutical Development and Technology, 2019, 24(9): 1175-1180.
[22]代帅,朱建政,梁陈静,等.晶体微结构对恩格列净溶出性能的影响[J].浙江理工大学学报(自然科学版),2022,47(3):357-362.
[23]Bommaka M K, Chaitanya Mannava M K, Rai S K, et al. Entacapone polymorphs: crystal structures, dissolution, permeability, and stability[J]. Crystal Growth & Design, 2021, 21(10): 5573-5585.
[24]Xu J, Gong X F, Li P, et al. Mifepristone polymorph with enhanced solubility, dissolution and oral bioavailability[J]. Steroids, 2020, 159: 108649.
[25]Purvis T, Mattucci M E, Crisp M T, et al. Rapidly dissolving repaglinide powders produced by the ultra-rapid freezing process[J]. AAPS PharmSciTech, 2007, 8(3): E58.
(責任编辑:张会巍)
收稿日期: 2022-10-11网络出版日期:2022-12-05网络出版日期
基金项目: 国家自然科学基金项目(22075252)
作者简介: 沈意周(1998— ),男,浙江嘉兴人,硕士研究生,主要从事药物晶型方面研究。
通信作者: 张国庆,E-mail:zgq@zstu.edu.cn
