16p13.11 微重复包含NDE1 基因的变异性质在产前诊断中的研究
2023-09-06张苗苗方玉琴唐俊湘王朝红孙玉秀朱健生
张苗苗 方玉琴 唐俊湘 王朝红 孙玉秀 朱健生
安徽医科大学附属妇幼保健院(合肥 230000)
随着检测技术的提高,染色体微阵列分析(chromosome microarray analysis,CMA)逐渐扩展到产前诊断领域,成为先天性异常和神经发育障碍的一线检测[1]。因此,发现了越来越多的拷贝数变异(copy number variations,CNVs)。16 号染色体含有很多的低拷贝重复序列,其p 臂10%的区域是由高度同源的片段组成,这些重复片段介导的非等位基因同源重组易形成CNVs。16 号染色体p 臂的复杂结构表明它是新的微重复综合征的候选区域[2-3]。
16p13.11 属于神经易感区域,包含14 个已知的编码蛋白质的基因,其中NDE1 是与神经系统表型相关的最强候选基因[4]。因此,16p13.11 微重复常见的表型为语言迟缓、智力低下、颅面畸形和行为异常,骨骼系统、循环系统、泌尿和消化系统的异常较少见[5-10]。然而,在表型正常的个体中也发现了该重复的携带者。有证据表明,16p13.11 微缺失是致病的,而其复制是良性变异[11],也有学者认为,该重复在表型上存在性别差异,男性携带者的病变率高于女性[4]。虽然这个区域的缺失是明确与精神障碍性疾病相关,但重复的病例却很少见导致它的临床表现达成共识是一个很大的挑战,并且报道多见于产后病例,而针对产前的较少。因此,本研究旨在探讨16p13.11 微重复的基因型-表型的相关性,综合分析临床和细胞遗传学,并评估其在产前诊断中的致病性质,以期为遗传咨询提供帮助。
1 资料与方法
1.1 研究对象 本研究共纳入2017年1月至2022年8 月在安徽医科大学附属妇幼保健院遗传中心接受CMA 检测的6 722 例样本(6 312 份羊水和410 份外周血)。排除517 例具有明确致病表型的变异病例,在排除的病例中未检测到16p13.11 微重复。剩余6 205 例根据不同的产前诊断指征分为3 组:(1)神经认知障碍患者组,包括61 例精神障碍患者(发育迟缓、智力低下等),但无神经系统结构异常;(2)神经系统异常产前组,包括356 例B 超显示胎儿神经系统异常(小头畸形、侧脑室增宽等)的孕妇;(3)神经系统无异常产前组,包括5 788 例因其他原因(无创产前检查高风险、产妇高龄等)行CMA 检测的孕妇。所有家庭在检测前都接受了遗传咨询,并签署了知情同意书。本研究得到安徽省妇幼保健院伦理委员会的批准(伦理批号:2207560)。
1.2 检测方法
1.2.1 CMA 检测 在孕妇进行羊膜腔穿刺术时抽取羊水,同时从疑似异常的患者中抽取外周血进行CMA 检测。根据制造商说明书[12],使用Affymetrix CytoScan 750K(Affymetrix,USA)进行SNP 检测,并使用Affymetrix CytoScan 750K 微阵列分析平台进行分析。查阅DGV、Decipher、OMIM、UCSC、ISCA和PubMed 等公共数据库,评估检测结果的临床意义,参考已发表的病例报告和病例对照研究进行全面分析。
1.2.2 随访 对携带16p13.11 微重复的胎儿及父母进行了电话随访,并查阅电子医疗记录。随访标准参照Gesell 量表、Wechsler 成人智力量表和0 ~6 岁儿童神经心理发育量表[13],身高和体重以《儿科学》第八版儿童生长曲线为依据。
1.3 统计学方法 数据使用SPSS 20.0 版(IBM,USA)进行分析,采用χ2检验确定重复病例的概率。P<0.05 为差异有统计学意义。
2 结果
2.1 CMA 检测结果 神经认知障碍患者组和神经系统异常产前组均无16p13.11 微重复病例。神经系统无异常产前组中共检出13 例(case1-13)携带16p13.11 微重复的胎儿,所有病例都有相似的该重复,涉及全部的NDE1 基因(chr16:14,892,975-18,172,468)。13 例孕妇的产前诊断指征主要为:唐氏和爱德华氏综合征高风险(7/13),其中3 例父母进行了CMA 验证,结果显示1 例(病例5)变异是新发突变,另外两例(病例3 和11)是遗传自表型正常的母亲(表1 和图1 和图2)。

图1 染色体16P13.11 微重复区域的表示Fig.1 Scale representation of the microduplication region of chromosome 16P13.11

图2 染色体16P13.11 微重复胎儿(病例3、5、11 和13)的家族谱系Fig.2 Family pedigree of fetuses(case 3,5,11 and 13)with microduplications of chromosome 16P13.11
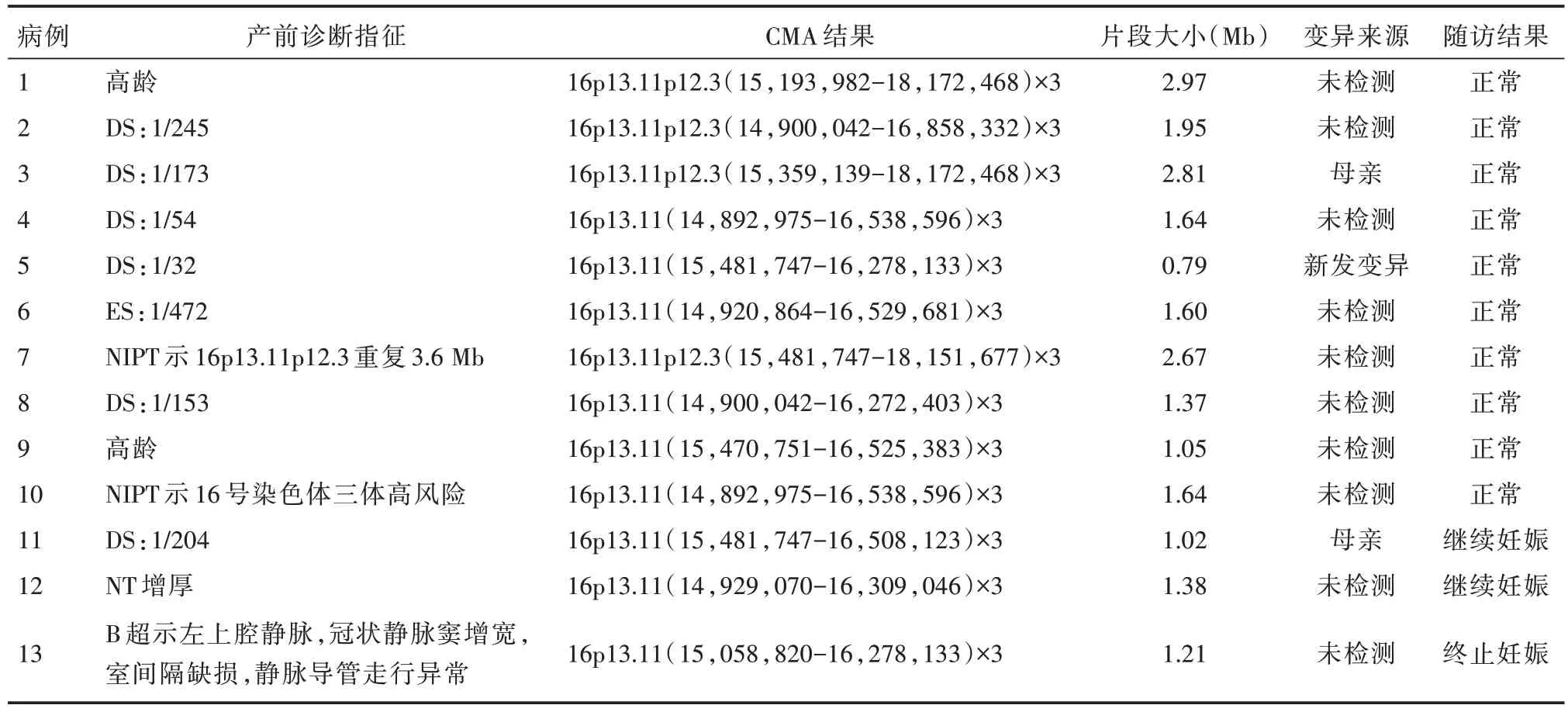
表1 在神经系统无异常产前组中13 例携带16p13.11 微重复的病例信息Tab.1 Information of the 13 cases with 16p13.11 microduplication in the prenatal group without abnormal nervous system
2.2 随访结果 随访13 例携带16p13.11 微重复胎儿的妊娠结局。病例13 的父母因为胎儿心脏异常而选择终止妊娠,病例11 和病例12 的父母继续妊娠中,且在后期的产检中未观察到其他结构异常。其余10 例胎儿(病例1-10)足月出生。我们对胎儿的产后健康进行追踪,主要关注神经心理发育、颅面畸形、先天性缺陷和骨骼异常等。在这些胎儿中未观察到明显的异常,并且他们的生长和发育符合同龄标准,但仍需长期的随访调查(表1)。
2.3 16p13.11 微重复检出率的比较 在神经认知障碍患者组和神经系统异常产前组中未检测到16p13.11 微重复。神经认知障碍患者组(0.00%)与神经系统无异常产前组(0.22%)的检出率进行比较,差异无统计学意义(P= 0.711)。由于患者组的样本量较小,我们将神经系统无异常产前组的检出率与文献[4,14]中的患者组进行比较(P=0.489),两组间的差异也无统计学意义(表2)。
3 讨论
CMA 具有高分辨率,准确性高,不需要进行组织培养从而缩短实验时间的特点,因此特别适合产前检测[15]。但CMA 的临床应用存在一定局限性,由于基因型和表型不完全对应,特定CNV 的潜在功能意义可能是未知的,被称为临床意义不明(variants of uncertain significance,VOUS)的变异体,最初将3 个区域(16p13.11、15q13bp1-5 和近端1q21)的重复序列归类为VOUS[16]。由于复杂的临床异质性以及在“看似”正常的个体中发现相似或相同的微重复,导致在家系研究后,16P13.11 微重复的临床表型尚存在争议。因此,本研究通过对病例队列和对照人群的大数据分析比较,将特定基因组区域与疾病联系起来,这将极大地提高我们对整个基因组和中枢神经系统功能重要性的认识,并且据我们所知,这是第一篇关于16p13.11 微重复在产前检测中的临床致病性报道。
从分子角度来看,NDE1 是16p13.11 片段上与神经系统表型相关的最强候选基因,它是由10 个外显子组成,编码中心体蛋白,该蛋白质参与大脑发育过程中的有丝分裂、神经元迁移,在人脑的皮质生长过程中发挥关键作用。该蛋白质含有自结合结构域、LIS1 相互作用结构域和C 端保守结构域[17]。NDE1/LIS1/NDEL1 复合物介导细胞内转运活动,是精神分裂症通路的一部分[18]。NDE1 基因突变会导致无脑畸形,这是一种以大脑皮层缺乏褶皱、严重脑萎缩、小头畸形和严重认知障碍为特征的疾病。然而FUJITANI 等[19]通过NDE1 和FOPNL 的过表达,进行功能获得性实验,发现它们的过表达未改变皮质脑室下区,径向胶质细胞或基底祖细胞的数量。虽然这些基因的拷贝数缺失已经导致了动物模型的神经学表现,但拷贝数增加的表型后果仍然不清楚。因此,这些基因的重复在行为和认知障碍中的作用只是推测,进一步描述这些基因的潜在影响将增强我们对相关临床表型的理解。
从临床表型来看,16p13.11 微重复患者具有广泛的临床表型并且严重程度不同[20-24]。一项研究总结了10 例携带16p13.11 微重复患者的临床表型显示,5 例患有运动和语言发育迟缓,6 例患有行为异常,2 例患有社交障碍[5]。然而,关于16p13.11 微重复与临床的相关性不确定,因为携带者可能异常,也可能完全正常。HANNES 等[11]发现该变异与正常表型相容,并认为该重复可能是真正的良性变异。我们的发现与其一致,因为在我们的研究中,神经认知障碍患者组或神经系统异常产前组中未检测到16p13.11 微重复。相反,13 例16p13.11 微重复的携带者属于神经系统无异常产前组。此外,患者组和对照组之间的检出率没有显著差异。由于本研究中患者组的样本量较小,我们将神经系统无异常产前组的检出率与文献中患者组的检出率进行比较,差异也无统计学意义。特别是1 ~10 例胎儿在出生后未观察到特异的临床表型,这支持了我们的假设,即产前检测到的16p13.11 微重复可能是良性的。这可能与环境因素、不完全外显率或可变表达有关。但是,我们在产前就发现了这些微重复,需要长期的随访来确认该重复是否会有其他临床症状。
我们的病例中有1 例因为胎儿心脏异常而引产。SHIMOJIMA 等[25]描述了1 例并发19p13.3 微缺失的婴儿,在3 个月大时患有室间隔和主动脉瓣缺损,但在16p13.11 片段上尚未发现与这些疾病相关的基因。16p13.11 微重复临床表型的多样性可能与“二次打击”学说相关,或调节元件microRNA(hsa-miR1972 和hsa-miR484)与其他基因修饰物相互作用导致的[5]。由此可见,16p13.11微重复的致病性复杂,但具体机制尚不清楚。在本研究中,我们将6 722 例样本汇聚在一起,以确定16p13.11 微重复携带者会有哪些临床表型。具有以下优势:(1)这是第一篇关于16P13.11 微重复在产前诊断的研究,在孕妇进行遗传咨询时,我们的研究有一定的参考价值。(2)我们不仅探讨了16p13.11 微重复的临床表型,并且将临床表型与分子机制联系起来,以期帮助对此片段进行更深层次的遗传学研究。本研究的局限性:(1)缺乏对因心脏异常而引产胎儿的病理学研究,探讨其潜在的分子机制。(2)由于父母的焦虑情绪,我们无法获得更多的样本进行父母验证。在后续的研究中,我们将会更加注重样本的留取和保存,以期在分子机制上有更进一步的研究和发现。
综上所述,我们在产前检测中发现了13 例携带16p13.11 微重复包含NDE1 基因的胎儿,除1 例引产外,其余12 例均健康。鉴于16p13.11 微重复的低外显率特征,我们认为16p13.11 微重复很可能是良性的。然而,16p13.11 微重复的可变表达是复杂的,需要进一步研究。此外,尽管所有分娩的婴儿在撰写本文时仍保持健康,但这些个体需要持续随访。
【Author contributions】ZHANG Miaomiao performed the experiments and wrote the article.FANG Yuqin performed the experiments.TANG Junxiang and WANG Chaohong revised the article.SUN Yuxiu and ZHU Jiansheng designed the study and reviewed the article.All authors read and approved the final manuscript as submitted.
