平衡针联合低频rTMS 对卒中后失眠患者睡眠质量的影响
2023-08-31安富刘佳宁谷凌云于淑萍张晓明黄伟
安富,刘佳宁,谷凌云,于淑萍,张晓明,黄伟
(1.中国人民解放军总医院第七医学中心,北京 100700;2.湖北中医药大学针灸骨伤学院,武汉 430061)
中风是全球第2 大死亡原因,也是致残的主要原因,已成为血管疾病发生率和死亡率增加的主要原因之一[1]。中国每年有200 多万人中风[2]。失眠是睡眠觉醒周期中最常见的疾病,影响大约50%的中风患者[3]。失眠被定义为在开始或维持睡眠或早起时反复出现困难,并伴有日间功能损害[4]。在某些情况下,青年时期出现的失眠可能比后出现的失眠更容易导致中风[5]。另一方面,失眠可能直接源于中风期间的脑缺血或缺氧,或住院病房的环境条件,或与中风相关的医疗条件,或疼痛、抑郁、感染、药物引起的不良反应等[6-7]。中风后失眠会恶化认知和身体功能,导致康复期间病情加重[8]。目前,美国睡眠医学学会制定的指南建议将认知行为疗法作为失眠症的一种治疗方法,但并不容易广泛使用[9]。同时,催眠药物的不良反应(如嗜睡、疲劳和头晕)限制了其在中风后睡眠障碍患者中的使用[10]。因此,在全球范围内,包括中医药在内的替代疗法治疗失眠症的不良反应均较少。
平衡针通过针刺身体某一穴位,达到人体自身的阴阳平衡。平衡针法主要通过对神经递质的重新分配治疗失眠[11]。 重复经颅磁刺激(repetitive transcranial magnetic stimulation, rTMS)作为一种相对较新的康复治疗方法,是一种无痛苦、无创的改变大脑兴奋性的方法。卒中患者在健侧半球接受低频rTMS可能比在患侧接受高频rTMS更有利[12],低频rTMS已成为非致残性失语或慢性中风患者神经康复和语言康复的潜在治疗工具。本研究采用平衡针联合低频rTMS 治疗缺血性卒中后失眠患者,观察其对患者睡眠质量及血清5-羟色胺(5-hydroxytryptamine, 5-HT)、去甲肾上腺素(noradrenaline, NE) 和褪黑素(melatonin, MLT)水平的影响。
1 临床资料
1.1 一般资料
采用PASS11.0多组比较计算样本量,取α=0.05及β=0.2,求得4组总样本量为150例,按照最大脱落率20%,计算得总样本量为188例。选取中国人民解放军总医院第七医学中心2021年8月至2022年2月收治的缺血性卒中后失眠患者作为研究对象,将188例患者按入院号进行编号,采用随机数字表法分为4组,对照组、平衡针组、低频rTMS组和联合组,每组47例。有163例患者因服用中药或镇静安神类药物而进入为期1周的洗脱期,洗脱期结束后即入组开始治疗。治疗期间,对照组脱落2例,平衡针组脱落4例,低频rTMS组脱落5例,联合组脱落5例,4组脱落原因均为患者由于个人原因无法继续治疗。4组一般资料比较,差异无统计学意义(P>0.05),具有可比性,详见表1。本研究已获得中国人民解放军总医院第七医学中心伦理委员会批准(批号2023-73)。
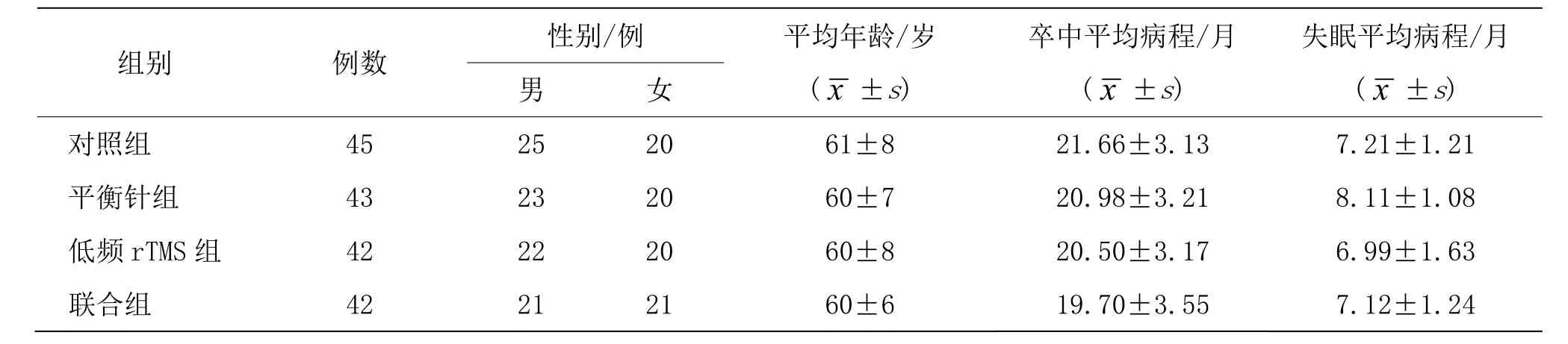
表1 4 组一般资料比较
1.2 诊断标准
卒中诊断标准参照《中国急性缺血性脑卒中诊治指南2018》[13]中相关内容。卒中分期标准参照《中国缺血性中风中成药合理使用指导规范》[14]中后遗症期的内容,即发病6个月后。失眠的诊断标准参照《中国成人失眠诊断与治疗指南》[15]中的相关内容。
1.3 纳入标准
符合上述诊断标准;年龄40~80 岁;患者同意参与本研究,并签署知情同意书。
1.4 排除标准
在卒中发病前有失眠症者;不配合相关检查者;认知功能严重受损者;合并严重系统疾病者;心、肺、肝、肾等重要脏器器质性损害者;既往有晕针史或惧怕针刺者;有rTMS 治疗禁忌者。
1.5 脱落标准
疗程未满4 周或失访者(因疗效满意,经受试者与研究者一致认可,疗程未满4 周停止治疗,不属于脱落病例);由于个人原因(例如出国、其余重大疾病等因素)无法继续治疗者。
1.6 剔除和中止标准
不符合纳入标准而被纳入者;符合排除标准而未被排除者;违背本研究规定治疗方案者;在试验期间接受了其他针对本疾病的治疗方法,以致于影响本试验疗效评估者;发生严重不良事件,不宜继续接受试验者;研究期间出现其他急重症,需采取紧急措施者;不合作、不服从治疗或主动要求中途退出者。
2 治疗方法
4 组均接受常规基础治疗。
2.1 对照组
予艾司唑仑(山东信谊制药有限公司,国药准字H43020696,1 mg),每晚睡前 口服,每次1 mg,持续4 周。
2.2 平衡针组
予平衡针针刺治疗。取失眠穴[16](位于前臂掌侧面,腕横纹正中央桡侧端)以及健侧偏瘫穴(位于耳尖上1.5 寸)、肩痛穴(位于足三里下2 寸,腓骨小头和外踝连线中上1/3 处)、膝痛穴(位于肘关节背侧正中)和臀痛穴(位于肩峰至腋后皱襞1/2 处)。患者取仰卧位,常规消毒穴位处皮肤。采用0.35 mm×40 mm 无菌针灸针垂直快速刺入失眠穴约0.5 寸,行上下提插,以出现放射性针感(麻胀感为主)为宜,旋转出针,不留针。采用 0.35 mm×75 mm 无菌针灸针,直刺偏瘫穴 2 寸(以患者感酸麻胀痛为准),直刺肩痛穴2 寸(行上下提插,以有触电针感向足背传导为宜),直刺膝痛穴2 寸(以针感向腕关节背侧放射为准),直刺臀痛穴2 寸(行上下提插,以针感向腕关节放射为准),上述穴位均不留针。隔日治疗1 次,持续4 周。
2.3 低频rTMS 组
予低频rTMS 治疗。采用经颅磁刺激仪(武汉依瑞德公司)治疗。8 字线圈,频率1 Hz,磁感应强度0.05 T,治疗靶点为右额叶背外侧区,刺激强度为80%~120%运动阈值。每日治疗1 次,持续4 周。
2.4 联合组
予平衡针联合低频rTMS 治疗。平衡针针刺治疗同平衡针组,低频rTMS 治疗同低频rTMS 组。每日治疗1 次,持续4 周。
3 治疗效果
3.1 观察指标
3.1.1 匹兹堡睡眠质量指数(Pittsburgh sleep quality index, PSQI)评分
于治疗前和治疗后采用PSQI 评分评估患者的睡眠质量。PSQI 由日间功能障碍、催眠药物、睡眠障碍、睡眠质量、睡眠时间、睡眠效率、入睡时间7 个项目组成,每个项目0~3 分,得分越高表示睡眠质量越差。
3.1.2 多导睡眠系统监测
采用多导睡眠系统监测总睡眠时间(total sleep time, TST)(即多导睡眠图记录的总卧床时间)、睡眠觉醒时间(sleep awake, SA)(即多导睡眠图记录的觉醒时间)和睡眠效率(sleep efficiency, SE)(即总睡眠时间占总记录时间的百分比)。
3.1.3 血清5-HT、MLT 和NE 的水平
治疗前和治疗后,分别于清晨采集4 组患者空腹状态下的外周静脉血5 mL,分离后取上清液储存于﹣80 ℃待用。用酶联免疫吸附法检测血清中5-HT 和NE 的水平。治疗前和治疗后,分别于凌晨3:00 在光线昏暗的环境中采集4 组患者外周静脉血5 mL 检测夜间血清MLT 的水平,以减少光线对褪黑素分泌的影响。所有操作严格按照试剂盒说明书进行。
3.1.4 不良反应发生情况
治疗过程中,记录4 组出现的不良事件及处理方法,包括晕针、滞针、局部血肿、感染、过敏、恶心、心悸、眩晕、腹部不适等。不良反应分为轻度、中度和重度。治疗中偶发轻微症状且持续时间小于0.5 h为轻度,治疗后或一段时间后出现的轻微症状且持续时间小于2 h 为中度,针刺后即发的较重症状且持续2 h 以上为重度。
3.2 统计学方法
采用SPSS22.0 统计软件进行数据分析。符合正态分布的计量资料以均数±标准差表示,多组间比较用方差分析,组间两两比较采用SNK-q检验;不符合正态分布的计量资料比较用非参数检验。P<0.05 表示差异具有统计学意义。
3.3 治疗结果
3.3.1 4 组治疗前后PSQI 评分比较
4 组治疗前PSQI 评分比较,差异无统计学意义(P>0.05)。与同组治疗前比较,4 组治疗后PSQI 评分均降低,差异具有统计学意义(P<0.05)。4 组治疗后PSQI 评分比较,差异有统计学意义(P<0.05)。治疗后组间两两比较,平衡针组和低频rTMS组PSQI评分均高于对照组和联合组(P<0.05);联合组PSQI 评分和对照组的差异无统计学意义(P>0.05);平衡针组和低频rTMS 组 PSQI 评分组间比较,差异无统计学意义(P>0.05)。详见表2。提示4 组的疗法均可改善睡眠质量,对照组和联合组改善睡眠质量的效果优于平衡针组和低频rTMS 组,联合组和对照组改善睡眠质量的效果相当,平衡针组和低频rTMS 组的效果相当。
表2 4 组治疗前后PSQI 评分比较(±s)单位:分
注:与同组治疗前比较1)P <0.05;与对照组比较2)P<0.05;与联合组比较3)P<0.05。
组别 例数 治疗前 治疗后对照组 45 14.44±2.17 7.62±2.041)平衡针组 43 14.66±2.09 9.94±1.331)2)3)低频rTMS 组 42 13.99±2.47 9.95±1.281)2)3)联合组 42 13.78±2.79 7.41±1.021)
3.3.2 4 组治疗前后TST、SE 和SA 比较
4 组治疗前TST、SE 和SA 比较,差异无统计学意义(P>0.05)。与同组治疗前比较,4 组治疗后TST 和SE 升高(P<0.05),SA 降低(P<0.05)。4 组治疗后TST和SE 比较,差异有统计学意义(P<0.05)。治疗后组间两两比较,平衡针组和低频rTMS 组TST 和SE 均低于对照组和联合组(P<0.05);联合组TST、SE 和SA 与对照组比较,差异无统计学意义(P>0.05);平衡针组和低频rTMS 组TST、SE 和SA 比较,差异无统计学意义(P>0.05)。详见表3。提示对照组和联合组在改善总睡眠时间和睡眠觉醒时间的效果优于平衡针组和低频rTMS 组,但联合组疗法和对照组的效果相当。
表3 4 组治疗前后TST、SE 和SA 比较(±s)
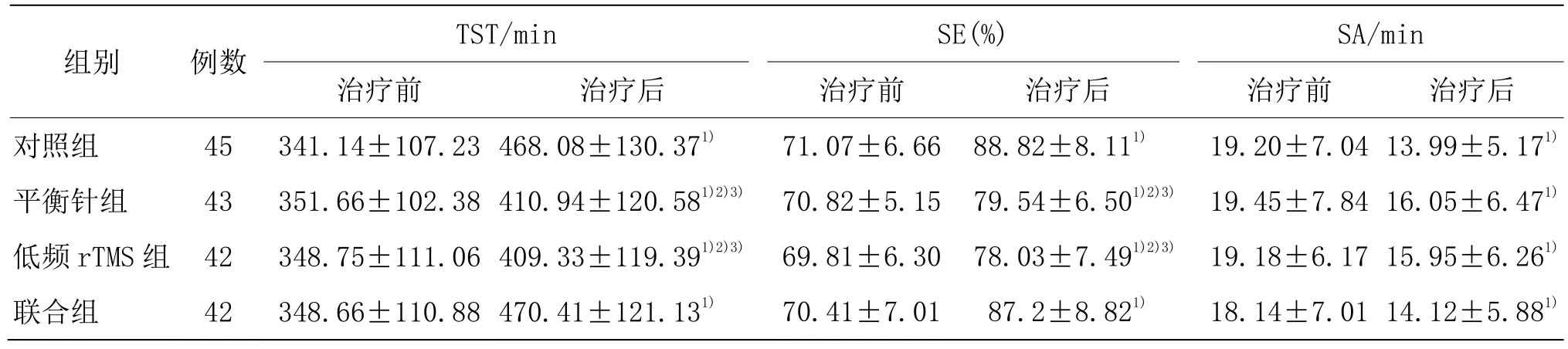
表3 4 组治疗前后TST、SE 和SA 比较(±s)
注:与同组治疗前比较1)P<0.05;与对照组比较2)P<0.05;与联合组比较3)P<0.05。
组别 例数 TST/min SE(%) SA/min治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 45 341.14±107.23 468.08±130.371) 71.07±6.66 88.82±8.111) 19.20±7.04 13.99±5.171)平衡针组 43 351.66±102.38 410.94±120.581)2)3) 70.82±5.15 79.54±6.501)2)3) 19.45±7.84 16.05±6.471)低频rTMS 组 42 348.75±111.06 409.33±119.391)2)3) 69.81±6.30 78.03±7.491)2)3) 19.18±6.17 15.95±6.261)联合组 42 348.66±110.88 470.41±121.131) 70.41±7.01 87.2±8.821) 18.14±7.01 14.12±5.881)
3.3.3 4 组治疗前后血清5-HT、MLT 和NE 的水平比较
4 组治疗前血清5-HT、MLT 和NE 水平比较,差异无统计学意义(P>0.05)。4 组治疗后血清5-HT 和MLT水平高于同组治疗前(P<0.05),NE 水平低于同组治疗前(P<0.05)。4 组治疗后血清5-HT、MLT 和NE 水平比较,差异有统计学意义(P<0.05)。治疗后组间两两比较,平衡针组和低频rTMS 组血清5-HT 和MLT 水平低于对照组和联合组(P<0.05),NE 水平高于对照组和联合组(P<0.05);联合组血清5-HT、MLT 和NE 水平与对照组比较,差异无统计学意义(P>0.05);平衡针组和低频rTMS 组血清5-HT、MLT 和NE 水平比较,差异无统计学意义(P>0.05)。详见表4。提示4 组的疗法均可上调患者外周血血清5-HT 和MLT 水平,下调血清NE 水平;对照组和联合组的疗法对血清5-HT、MLT 和NE 水平的影响优于平衡针组和低频rTMS 组,联合组与对照组对上述指标的影响相当。
表4 4 组治疗前后血清5-HT、MLT 和NE 的水平比较(±s)
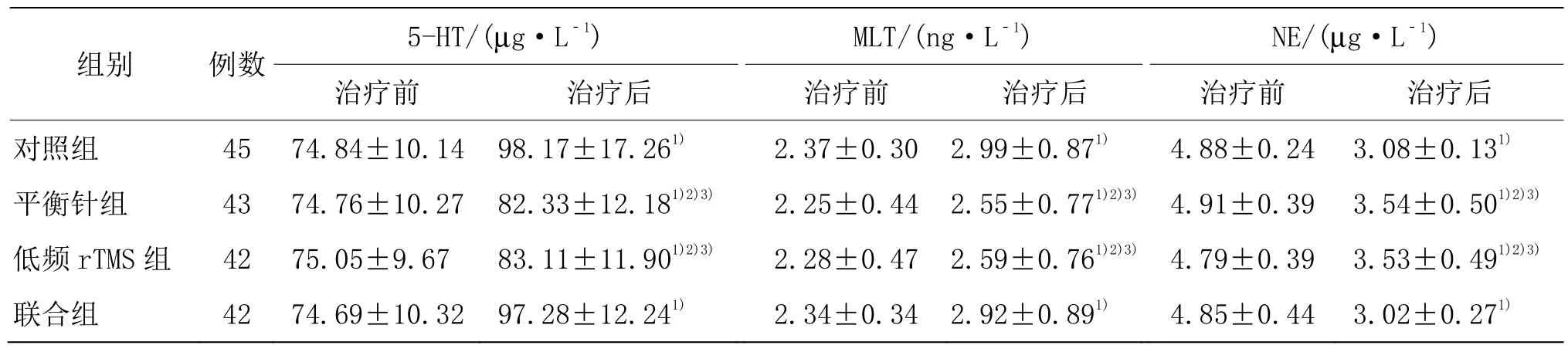
表4 4 组治疗前后血清5-HT、MLT 和NE 的水平比较(±s)
注:与同组治疗前比较1)P<0.05;与对照组比较2)P<0.05;与联合组比较3)P<0.05。
组别 例数 5-HT/(µg·L﹣1) MLT/(ng·L﹣1) NE/(µg·L﹣1)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 45 74.84±10.14 98.17±17.261) 2.37±0.30 2.99±0.871) 4.88±0.24 3.08±0.131)平衡针组 43 74.76±10.27 82.33±12.181)2)3) 2.25±0.44 2.55±0.771)2)3) 4.91±0.39 3.54±0.501)2)3)低频rTMS 组 42 75.05±9.67 83.11±11.901)2)3) 2.28±0.47 2.59±0.761)2)3) 4.79±0.39 3.53±0.491)2)3)联合组 42 74.69±10.32 97.28±12.241) 2.34±0.34 2.92±0.891) 4.85±0.44 3.02±0.271)
3.4 安全性评价
纳入的180 例患者治疗前后生命体征指标均未见明显异常。治疗过程中,对照组发生中度不良反应1 例,轻度1 例,不良反应发生率为4.4%;平衡针组发生中度不良反应2 例,不良反应发生率为4.7%;低频rTMS 组发生轻度不良反应2 例,不良反应发生率为4.8%;联合组发生轻度不良反应1 例,中度不良反应1 例,不良反应发生率为4.8%。中度不良反应予对症处理,轻度未予特殊处理且自行好转。4 组不良反应发生率比较,差异无统计学意义(P>0.05)。
4 讨论
失眠通常分为继发性和原发性。慢性原发性失眠的特点是长期难以维持和启动睡眠、早起、情绪不佳、疲劳、注意力不集中和生活质量差[17]。长期失眠会增加心血管疾病的风险,如脑血管疾病、高血压、糖尿病和痴呆[18]。在原发性失眠中,血清5-HT、NE 和MLT 水平可能在睡眠抑制或激活系统中的睡眠调节中发挥关键作用[19-20]。研究显示,5-HT2A 受体的选择性逆激动剂可显著改善原发性失眠患者的睡眠维持[21]。补充MLT可改善中年原发性失眠症睡眠障碍,如总睡眠时间、快速眼动百分比和清晨醒来时间[20]。缺血性卒中后失眠是常见的继发性失眠类型之一。失眠对中风患者的预后有很大影响[22],因为它会增加中风的复发率,导致心理障碍和认知障碍,加重身体症状,严重影响康复过程和日常生活[23]。在中风的任何阶段改善失眠对短期和长期恢复都是积极的[24]。镇静和催眠药物通常用于缺血性卒中后失眠的临床症状治疗[25]。
在失眠的复杂病因中,脑内神经递质的紊乱被广泛认为与失眠有关。5-HT、NE 和MLT 在维持清醒和嗜睡中起着重要作用[26],是公认的神经中枢递质“致眠因子”。5-HT 是一种哺乳动物大脑和神经突触组织中广泛分布的抑制性神经递质。5-HT 的主要功能是促进清醒和抑制快速眼动睡眠。中枢神经系统中5-HT 释放减少,突触间隙5-HT 含量下降诱发了失眠发生。循环5-HT 浓度的变化亦可反映睡眠与精神的变化。因此,人血清中5-HT 的检测对失眠具有重要科研意义[27]。NE作为儿茶酚胺类神经递质,主要由交感节后神经元和脑肾上腺素能神经末梢合成和分泌,是后者释放的主要递质。NE 水平与睡眠系统的正常运行密切相关[28]。
5-HT 作为一种单胺类抑制性神经递质,与中枢NE均可激活肾上腺素能受体可作用于心血管、精神活动、觉醒等的调节。缺血性卒中患者睡眠和觉醒系统受损时,脑内的5-TH、NE 等多种神经递质的分泌和作用会受到影响,导致睡眠障碍的发生[29]。有研究[30-31]表明针刺治疗可以影响下丘脑及海马内5-HT1A、5-HT2A 受体表达引起下丘脑及海马内5-HT 含量的改变,降低血清NE 水平,从而改善中枢抑制功能,从而改善失眠症。MLT 是松果体分泌的一种激素,夜间分泌达到高峰,MLT 协调昼夜节律并调节睡眠功能[32]。由于MLT 的合成通过大脑中的神经通路和环境光/暗循环进行调节,并通过大脑中血管释放到循环中,研究发现睡眠不足患者伴随着MLT 分泌受损[33]。有学者发现,MLT 的异常分泌可能与中风患者的失眠有关[34-35],针灸增加了MLT的分泌,减少了失眠和焦虑[36]。由此,检测缺血性卒中后失眠患者外周血清5-HT、NE 和MLT 浓度,证实了平衡针联合低频rTMS 疗法可通过调节“致眠因子”分泌和缓解失眠而发挥有益作用。
本研究有以下局限性。由于有许多潜在的影响因素,如卒中患者用药基线、患者的针灸经验等[37],这些因素是后续高质量随机对照临床试验的重点。尽管大多数针刺和rTMS 研究显示了积极的疗效,但缺乏更有力的循证证据,无法得出一般性结论或明确结论。本研究没有对患者进行随访,限制了结论的普遍性。本研究仅进行了主观指标的评价(PSQI、TST、SE 和SA 评分),在未来研究中,更多地使用客观指标(如多导睡眠检测)来评估睡眠质量,提倡主观和客观指标共用[38]。
