内镜辅助下经椎间孔病灶清除椎间融合术治疗腰椎布鲁杆菌脊柱炎11例*
2023-08-23李启超王永峰刘儒星徐朝健
李启超 王永峰 陕 楠 刘儒星 赵 斌 原 杰 徐朝健
(山西医科大学第二医院脊柱外科,太原 030001)
布鲁氏菌病是一种人畜共患疾病,全球每年报告新增病例约50万例,我国将其列为二类动物疫病,华北、西北、东北为高发地带[1]。该病10%~85%的局部并发症涉及肌肉、骨骼系统,腰椎最常受累[2~4],即腰椎布鲁杆菌脊柱炎(lumbar brucellus spondylitis,LBS)。该病尚未有统一治疗标准,规范化抗菌治疗无效且症状严重者可选择手术。对比全椎板切除、病灶清除术,经椎间孔病灶清除椎间融合术(transforaminal lumbar interbody debridement and fusion,TLIDF)可保留后方韧带复合体(posterior ligament complex,PLC)结构[5],术后脊柱稳定性更好,但会对多裂肌造成过度破坏。多裂肌参与脊柱的背伸与侧向旋转[6],保留该结构可更早进行术后康复锻炼,对老年人极为重要,避免长期卧床出现并发症。内镜辅助下经椎间孔椎间融合术(transforaminal lumbar interbody and fusion,TLIF)与开放TLIF比较,不仅可保留PLC结构,也更好地实现对多裂肌的保护[7,8],在治疗腰椎退行性变时疗效可靠,但治疗LBS鲜有报道。我院2021年3月~2022年9月对11例LBS行内镜辅助下TLIDF,临床疗效满意,现报道如下。
1 临床资料与方法
1.1 一般资料
本组11例,男4例,女7例。年龄41~74岁,(59.9±8.8)岁。主诉为腰部疼痛、活动受限,同时有发热、盗汗,体温36.8~38.4 ℃,8例出现神经症状,表现为单或双侧下肢感觉障碍及肌力减弱。病程2~10个月,(5.9±2.6)月。11例均有牛、羊接触史,6例有长期牛羊鲜奶饮用史。4例在当地诊断为腰椎结核。单节段病变8例:L2/31例,L3/43例,L4/53例,L5/S11例;多节段病变3例:L1~L31例,L4~S12例。影像学分期[9]:中期改变6例,晚期改变5例(图1,2)。术前红细胞沉降率(erythrocyte sedimentation rate,ESR)16~100 mm/h,(44.6±24.4)mm/h;C反应蛋白(C-reactive protein,CRP)17.3~95.7 mg/L,(40.5±21.7)mg/L;血白细胞(white blood cell,WBC)3.68×109/L~9.58×109/L,(6.3±1.8)×109/L;中性粒细胞百分比34.4%~83.5%,(54.3±11.8)%。11例布鲁杆菌标准试管凝集试验(standard tube agglutination test,SAT)均≥1∶160。除2例合并原发性高血压外,余9例无合并症。
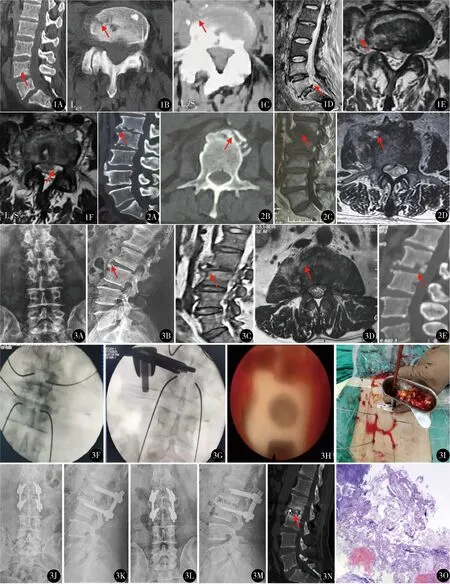
图1 A.CT三维重建示L4/5、L5/S1终板间有小溶骨性破坏;B,C.CT示椎体前缘、椎体有溶骨性破坏;D.MRI矢状位T2抑脂像,显示L4/5、L5/S1椎间、椎体炎性信号,椎管内少量脓肿;E,F.MRI轴位示L4/5、L5/S1椎旁、椎管内局限性脓肿图2 A.CT三维重建示L1/2、L2/3椎间隙变窄,溶骨性破坏与成骨共存,椎体前缘骨赘增生、硬化;B.CT示L1周缘呈“花边样”外观;C.MRI矢状位T1像,L1/2椎间、椎体明显炎性信号;D.MRI轴位示L1~2椎旁、椎管内高低混杂脓肿信号,椎体呈“花边样”外观 图3 PELIF典型病例:男,53岁,病变节段L2/3 A,B.X线片示腰椎退行性变,L1/2、L2/3椎间隙变窄,椎体前方增生骨赘;C,D.术前MRI示L2/3椎间、椎体炎性信号,椎间盘破坏;E.术前CT示L2/3终板骨质破坏,椎体炎性骨赘增生与溶骨破坏;F~I.C形臂下导针定位、置入方形套管、植入混有利福平的自体骨、融合器镜下观;J,K.术后即刻腰椎X线片示L2/3内固定位置好;L~N.术后1年DR示内固定位置好,固定有效,CT示L2/3椎间骨性融合,骨小梁连接(EckⅠ级);O.显微镜下见纤维软骨组织形成,有炎性细胞浸润,符合炎性病变(HE染色 ×100)
病例选择标准[10,11]:SAT≥1∶160且已明确诊断;标准化药物治疗>6周后腰痛或下肢神经功能障碍未见好转,手术指征明确。排除标准:一般情况差,无法耐受手术;其他导致相似症状的疾病,如腰椎结核、化脓性脊柱炎、脊柱肿瘤等。
1.2 方法
术前按《布鲁氏菌病诊疗指南》[12]的推荐用药治疗6周(多西环素 100 mg/次,2次/d+利福平600 mg/次,1次/d+新诺明1000 mg/次,2次/d),同时行保肝治疗,加强营养,有发热症状的患者待体温降至正常后2 d再进行手术。2例合并原发性高血压,心内科会诊处理后正常手术。
11例规律抗菌药物治疗6周后腰部疼痛及下肢神经功能障碍未见好转,且进行性加重,采用内镜辅助下一期后路手术,主要依据病变节段进行术式选择。L1/2、L2/3椎间孔较大,在置入“方型”套管时骨质破坏更少,对出口根的干扰程度小,采用内镜辅助经皮椎间融合术(percutaneous endoscopic lumbar interbody fusion,PELIF)。L4/5、L5/S1节段由于存在高髂嵴阻挡及椎间孔较小,采用单侧双通道内镜椎间融合术(unilateral biportal endoscopic lumbar interbody fusion,UBE-LIF)更安全;因合并腰椎滑脱导致椎间孔形变者,更适用于UBE-TLIF。L3/4节段2种术式操作难度相似,但PELIF可在局麻+强化下进行,依据患者意愿及术前一般状况进行选择。
内镜辅助下PELIF:以L2/3为例。俯卧位。C形臂定位L2、L3双侧椎弓根体表投影点,局部浸润麻醉后各做一约1 cm长切口,穿刺针穿刺后导丝固定。再次C形臂定位L2/3棘突体表位置,在其左侧旁开8 cm记做进针点,局部浸润麻醉后做1 cm长切口。逐级扩张后置入工作套管,环锯切除L3上关节突腹侧,椎间孔成形后退出套管,置入内镜[德国SPINENODS脊柱内镜(SP081375.030),批文号:国械注进20163062295],行黄韧带切除、病灶清理、神经松解等减压操作。透视引导下将尾侧开口的专用“方形”工作套管定位在椎间隙,继续镜下清创、刮除上下终板软骨,将利福平与植骨颗粒(同种骨植入材料,山西奥瑞生物材料有限公司,批文号:国械注准20163130428)混合后植入椎间隙,最后放置融合器(上海三友医疗器械股份有限公司,PEEK材料,批文号:国械注准20143132375,依据术中试模大小来进行融合器尺寸的选择)。完成后退出内镜及工作套管,留置引流后缝合。经皮置入椎弓根螺钉,C形臂再次确认融合器与内固定位置后,留置引流、缝合。见图3。
UBE-LIF:以L4/5为例。全麻后取俯卧位。C形臂定位L4、L5椎弓根右侧体表投影,标记为切开线。消毒铺单后上下2处各切开1.5 cm长切口,置入导棒,建立三角关系,扩张套管逐级扩张,形成工作通道及观察通道。关节镜[美国Stryker 30°关节镜系统(BL-OE),批文号:国械注进20183061803]监视下切除L4右侧下关节突,显露黄韧带、硬膜囊及L5神经根。神经拉钩保护硬膜囊及神经根,清理病变的椎间盘,使用骨锉、刮匙仔细处理椎板间隙,将利福平与植骨颗粒混合后植入椎间隙,最后放置融合器,留置引流后缝合。见图4。

图4 ULIF典型病例:女,73岁,病变节段L4/5 A,B.腰椎正位X线片示退行性改变,L4、L5椎体前方骨密度增高,侧位可见L4椎体前滑脱,L4/5、L5/S1椎间隙变窄;C,D.MRI矢状位STIR序列可见L4、L5椎体炎性改变,轴位示L4/5节段椎旁脓肿;E,F.CT三维重建示L4/5椎间终板有小溶骨破坏灶及增生硬化,L4椎体前缘溶骨性破坏;G~K.病变组织、处理后的椎板间隙、融合器镜下观、C形臂确认融合器位置、留置引流;L,M.术后即刻X线片示内固定位置良好,椎体复位好;N,O.术后2个月X线片复查,内固定位置好,融合器无移位,椎体无滑脱;P.术后6个月X线片复查,L4/5椎间可见骨小梁连接,初步融合(EckⅡ级);Q.腰椎间隙组织病理显微镜下可见纤维软骨组织形成,大量炎性细胞浸润,符合炎性病变(HE染色 ×400)
术后处理:切口常规留置引流,引流量<30 ml/d时拔管。根据患者每日饮食情况调整补液量。拔除引流后即可佩戴腰围活动。术后鼓励患者积极进行腰背肌功能锻炼,帮助恢复。所有患者腰围需至少佩戴8周,期间避免弯腰提重物等不良姿势。术后继续规律口服抗布氏杆菌药物6周,剂量同术前。出院标准:引流管拔除;术后连续3 d无体温异常;患者精神状态好,可在家属协助下佩戴腰围下地活动。出院时嘱定期来我院复查,待ESR、CPR指标正常后停药。
1.3 观察指标
术前及末次随访时ESR、CRP变化;术前及术后1、3个月和末次随访时腰背部与腿部疼痛视觉模拟评分(Visual Analogue Scale,VAS)、Oswestry功能障碍指数(Oswestry Disability Index,ODI);采用改良MacNab标准[13]评价临床疗效;采用美国脊髓损伤协会(American Spinal Injury Association,ASIA)测定表[14]评估下肢神经功能状态:A级,完全性损伤(在脊髓损伤平面以下,包括S4/5无任何运动及感觉功能保留);B级,不完全性损伤(在脊髓损伤平面以下,包括S4/5有感觉功能保留,但无任何运动功能保留);C级,不完全性损伤(在脊髓损伤平面以下有运动功能保留,但损伤平面以下有一半以上的关键肌肌力<3级);D级,不完全性损伤(在脊髓损伤平面以下有运动功能保留,但损伤平面以下有一半以上的关键肌肌力≥3级);E级,正常(感觉和运动功能正常)。采用Eck分级[15]评估末次随访骨融合情况(依据X线片/CT):Ⅰ级,明确融合(融合器模糊,可见大量骨小梁连接和结构重塑);Ⅱ级,部分融合(融合器清晰可见,可见少量骨小梁连接);Ⅲ级,可能未融合(融合器清晰可见,未见骨小梁连接);Ⅳ级,没有融合(融合器发生塌陷,未见骨小梁连接);Ⅴ级,无法评估。
1.4 统计学处理
2 结果
11例顺利完成手术,其中PELIF 3例,UBE-LIF 8例,无中转开放手术。术后切口均1期甲级愈合,无感染及窦道形成,随访期内均未发现与手术有关的严重并发症。3例PELIF分别随访6、14、18个月;8例UBE-LIF随访6~13个月(表1)。术前11例ESR、CRP均大于正常值,末次随访均恢复至正常。术后1、3个月及末次随访腰腿痛VAS评分和ODI与术前相比有显著性差异(表2)。末次随访11例SAT均为阴性。末次随访腰椎X线/CT均示椎间植骨融合良好,未发生内固定移位、松动及断裂,6例Eck Ⅰ级融合(PELIF 2例,UBE-LIF 4例),见图3,5例Eck Ⅱ级融合(PELIF 1例,UBE-LIF 4例),见图4。11例末次随访依据改良MacNab标准,优7例(PELIF 2例,UBE-LIF 5例),良3例(PELIF 1例,UBE-LIF 2例),可1例(UBE-LIF 1例),优良率90.9%(10/11);ASIA分级术前D级8例(PELIF 1例,UBE-LIF 7例),E级3例(PELIF 2例、UBE-LIF 1例),末次随访11例均为E级。

表1 11例术中、术后情况
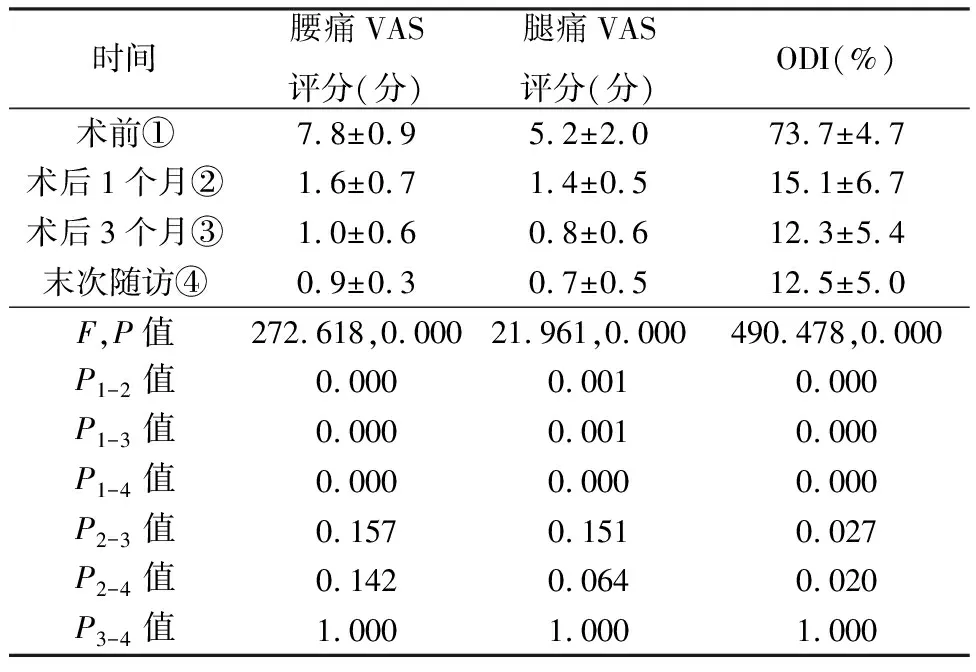
表2 术前后腰腿痛VAS评分、ODI比较(n=11)
3 讨论
3.1 早期诊断与治疗
布鲁氏菌病作为一种人畜共患的疾病,常常侵袭骨与关节,腰椎为易感染部位[3,4]。抗菌药物是治疗LBS的基础,推荐用药方案[13]:多西环素 100 mg/次,2次/d+利福平600 mg/次,1次/d+新诺明1000 mg/次,2次/d,连续使用6周。早期LBS仅侵及椎体上下缘,椎间盘未受累,同时无椎旁脓肿出现[9],药物治疗预后较好。因此,LBS的早期诊断在治疗中尤为重要。早确诊、早用药可以延缓其进展,甚至多数患者可治愈。本组11例在经过规律抗菌药物治疗后症状均未见缓解,且有明显进展,因此,采取手术治疗。
本病临床表现与腰椎结核相似,因此,误诊率较高[10]。从以下几点进行鉴别[4]:①腰椎结核患者多为午后低热,腰背部疼痛症状较轻,LBS患者多因明显腰背部疼痛就诊,且多为午后高热。②在传染源方面,牛、羊、猪及犬型布鲁杆菌均可使人患病,临床多见牛、羊致人感染。Shen等[16]报道96%(64/67)的LBS患者有明确的牲畜接触史。本组11例在患病前均有牛羊接触史,其中6例有长期牛羊鲜奶饮用史,因此,对有腰痛、午后发热等症状且有长期牛、羊等家畜及生鲜奶制品接触史者,应高度怀疑有布氏杆菌感染。③LBS中腰椎最常受累,主要为L4、L5椎体,胸椎、颈椎次之;脊柱结核最常受累椎体为胸椎,腰椎、颈椎次之。本组4例当地误诊为腰椎结核,因此,根据症状与影像学检查,怀疑布氏杆菌感染者,应尽早完善实验室检查协助诊断。
3.2 治疗策略
对存在严重腰痛或下肢痛、椎间脓肿以及药物治疗无效的LBS患者,多采用手术治疗[17~20]。目前,LBS的手术治疗方案尚未形成统一意见。主要术式根据入路不同可分为:前路清创植骨融合,后路椎板减压、植骨融合内固定,前路清创植骨融合联合后路内固定[21]。前路视野开阔,病灶清除和神经减压更为彻底,但易发生大血管损伤及术后肠梗阻等并发症[22],且无法为病椎提供坚强的内固定。后路远离腹腔,避免一些严重的并发症,但Joaquim等[23,24]认为后路全椎板减压破坏了脊柱正常的PLC结构,导致远期脊柱不稳定,发生腰椎后凸畸形及滑脱。
LBS作为一种细菌感染性疾病,清创后病椎是否需行内固定、椎间是否放置融合器仍有争论。有学者认为后路内固定会降低抗生素的疗效,同时细菌黏附于钉棒系统导致新的感染。然而Chang等[25]认为钛合金相较于聚甲基丙烯酸甲酯与不锈钢材料,更不容易发生细菌定植。在彻底清创联合长期、规律用药的前提下,钛合金钉棒系统在脊柱感染的治疗中是可靠的。Chen等[26]认为若病椎破坏较大(>50%)无法为椎弓根螺钉提供支持时,应延长至少一个节段进行固定。杨新明等[27]对经病椎固定与跨病椎固定进行了研究,认为符合病椎置钉条件者,均可行病椎置钉;对是否行椎间融合器植骨融合,他们认为此时融合效率较低,且容易导致融合器塌陷于病椎内。然而,若仅进行后路内固定而无椎间融合器支撑,病椎间会因上下弹性不稳而影响远期融合效率。我们前期研究[5]显示TLIDF术在清创、减压时保留脊柱PLC结构,同时坚强的内固定系统维持了术后脊柱稳定性,为椎间融合器植骨融合提供基础,辅以药物治疗取得较好的远期疗效,随访期内无断钉、融合器塌陷及复发现象。
3.3 术中体会
与开放术式相比,内镜辅助下椎间融合、经皮置钉在减少椎旁肌损伤及术后医源性不稳方面更具优势,有出血少、住院时间短、恢复快的优点[28,29]。镜头贴近病灶区域,视野显露清晰,对与神经粘连严重的病灶进行剥离效率高,在清创时最大程度避免神经损伤。炎性感染不同于退变性疾病,LBS镜下可见炎性肉芽组织与正常组织交织,轻微出血即可导致镜下视野模糊,因此,持续的生理盐水冲洗配合射频止血对维持术野清晰尤为重要,但水流速度不易过快,避免水压过高刺激硬膜囊,按一台手术时间镜下操作90 min为准,我们术中约使用3000 ml盐水4袋。同时应避免过度追求术野清晰度而频繁射频止血,会增加神经损伤的可能性,不造成视野遮挡的渗血均可接受。在行椎间隙清创时,应着重在有下肢神经刺激症状一侧操作,一般仅进行单侧清创、减压,避免造成术中病灶的播散。由于内镜手术产生的可移植骨量较少,同时为彻底清创,部分学者主张将增生骨质彻底清除。但LBS椎体改变以增生、硬化为主,病椎间多形成骨刺或骨桥,我们认为术中不应过度追求清创的彻底性而进行大面积的骨质破坏,保留部分骨质可协助后路钛合金内固定系统为融合器提供相对稳定的融合环境。我们术中仅在后路开窗、扩孔时切除部分骨质,然后使用刮匙清除炎性组织,配合术中对病灶区域的持续盐水冲洗,最后椎间置入混有利福平的同种异体骨颗粒进行植骨融合,随访期内无复发病例,无严重并发症出现,在随访期内未发生融合器移位、塌陷,且在末次随访时椎间融合程度令人满意。
本组11例均采用经皮置钉,通过1~1.5 cm切口进行,术后切口容易护理,不易出现大面积渗出,这也是切口均Ⅰ期甲级愈合的原因。随访期间未发现内固定断裂,配合足量、规律使用抗菌药物,未发现与钉棒系统有关的感染,可初步认为经皮置钉是可靠的。
在规范化抗菌药物治疗的基础上,内镜辅助PELIF在治疗LBS时较好地保护多裂肌,保留PLC结构及大量骨性结构,配合后路内固定系统及椎间融合器,为脊柱提供良好的生物力学稳定性,患者早期回归工作、生活,临床疗效肯定。但该技术学习曲线长,需术者熟练掌握常规脊柱内镜技术后方可开展。由于LBS患病率较低,本组纳入样本量少,对于内镜辅助下PELIF治疗LBS的远期疗效仍需大样本、多中心进行研究。
