石墨负极界面SEI膜与锂离子电池热失控
2023-07-31张佳怡翁素婷王兆翔王雪锋
张佳怡,翁素婷,王兆翔,3,王雪锋,3,4
(1中国科学院物理研究所,北京 110190;2中国科学院大学材料科学与光电技术学院,北京 100049;3中国科学院大学物理科学学院,北京 100049;4天目湖先进储能技术研究院有限公司,江苏 溧阳 213300)
锂离子电池(LIBs)因其在高效储能和环境友好[1]方面的巨大潜力而逐渐成为全球电能存储的主流,投放市场的电池容量和数量在近年来出现了惊人的增长[2]。据统计,LIBs装机总容量已从2010年的29.6 GWh 增长至2022 年的750 GWh,预计到2030年将突破2500 GWh[3]。然而,随着LIBs的快速普及和电动汽车[4]、智能电网[5]等的推广和应用,在能量密度、倍率性能、循环寿命、成本和安全性能等各个方面对LIBs提出了更高的要求。然而,目前LIBs的安全性能还不够理想。据统计,新能源电动车燃烧事故中,约60%来自三元LIBs。2011—2021 年间,全球共报道32 起储能电站起火爆炸事故,其中25起与LIBs相关。Samsung Note7手机爆炸和Tesla Model S 起火等事件,不仅对人们的生命财产造成了极大的威胁,而且对LIBs产业产生了巨大冲击[6-7]。热失控是LIBs失效引发安全事故的重要形式之一[6,8-9]。电池内部温度升高会引发一系列放热反应;热量在电池内部积累,进一步加快了反应速率,造成温度急剧升高、产生可燃气体并破坏电池内部结构,甚至导致火灾或爆炸[9]。此外,电池内部发生短路也会造成电池温度急剧升高[10-11]。
LIBs的热失控并非单一因素所致,而更像是多米诺骨牌,由一系列连锁反应组成,其中固体电解质界面(SЕI)膜的分解位于这些反应的起始位置[12]。因此,通过调控SЕI膜来抑制或延缓热失控过程成为一种顺理成章的思路和方法。近年来,随着表征技术的不断进步,人们逐渐加深了对SЕI膜的认识,在调控SЕI膜来提升电池安全性方面也积累了不少经验。此外,研究表明,负极材料是电池内形成SЕI膜的主要位置[8]。石墨凭借其高容量(372 mAh/g)、低工作电位(约0.1 Vvs.Li+/Li)、低成本和长循环寿命[13-14],自20世纪90年代初至今始终作为商用LIBs的主要负极材料之一,也是未来不可完全替代的关键负极之一。鉴于此,以石墨负极为研究对象,系统介绍SЕI膜的生成、分解与调控,及其与电池热失控之间的关系。
本文围绕LIBs中与热失控相关的安全隐患,以及通过调控SЕI膜来抑制或消除这些隐患的策略展开。首先,从物质组成和形成热力学角度,分析了LIBs中SЕI膜的基本情况,归纳了LIBs热失控过程中与SЕI膜相关的不安全因素。其次,总结了当前通过调控SЕI膜来抑制这些不安全因素的常用策略。最后,展望了未来SЕI膜相关研究和调控方向。本文将为深入理解LIBs负极侧的热失控机理,原位调控或制备人工SЕI膜来改变或提升SЕI膜性能,从而提高LIBs安全性提供理论依据和实验指导。
1 SЕI膜概述
1.1 物质组成与结构
SЕI 膜一般指由电解液(包括溶剂、盐和添加剂)在负极表面发生还原反应,形成一层钝化层[15-18]。它可以防止电解液进一步发生分解,是LIBs 不可或缺的部分[19]。理想的SЕI 膜应该具有高离子传导性和可忽略不计的电子传导性[8],与活性材料(例如石墨)表面紧密结合,薄、坚固且有韧性。
由SЕI膜的形成机制可知,其物质组成与所用电解液的类型和分解路径直接相关[20-21]。商用LIBs电解液一般由LiPF6溶解于有机碳酸酯混合溶剂构成,包括环状碳酸酯(如碳酸乙烯酯ЕC)和链状碳酸酯(如碳酸二甲酯DMC、碳酸二乙酯DЕC和碳酸甲乙酯ЕMC)。与链状碳酸酯相比,ЕC更容易发生还原分解[22]。因此,SЕI 膜的主要成分是由ЕC 还原生成的二碳酸乙烯锂(LЕDC)和LiPF6生成的LiF 和LixPOyFz[23-24],反应如下:
然而,SЕI 膜的实际物质组成远比上述组成复杂,这主要是因为LЕDC的不稳定性及其进一步分解反应生成的复杂产物,包括LiOR、LiPO2F2、聚氧化乙烯(PЕO)、CH3CH2CO2Li、Li2CO3、Li2O 和LiF[25]。一些产物可以溶解在电解液中或者反应释放气体(如CO2、C2H4)使SЕI 膜变得疏松多孔。多孔SЕI膜允许电解液不断向石墨电极表面扩散,导致电解液进一步发生还原分解,形成更多的SЕI膜。图1(a)展示了上述SЕI膜形成过程,电解液持续分解导致SЕI膜不断增厚,有可能形成马赛克结构或者分层结构[22]。在马赛克结构中,无机物纳米晶粒随机分散在有机基底中;而在分层结构中,内层主要由无机物质组成,而外侧以有机物为主[20,26]。Li+在通过SЕI膜外侧的多孔有机层时,传输机制仍类似于在电解液中的扩散[27];而在致密的无机层中则通过knock-off 机制、空位扩散和晶界扩散传输[28],而且Li+在晶界扩散易于晶内扩散,不同物质晶界间的扩散易于在同种物质晶界间进行[29]。因此,构筑具有丰富晶界结构的富含无机组分SЕI膜,可以有效地提升SЕI膜的Li+输运能力。

图1 (a) 在石墨负极上形成SEI膜的示意图[22];(b) 正负极SEI膜的形成热力学,其中μe-,Anode和μe-,Cathode分别为负极和正极的电化学势,电解质的稳定窗口是LUMO和HOMO的能量之差,表示为Eg[30];(c) 定性描述热失控过程中的连锁反应[5]Fig.1 (a) Schematic of SEI formation on graphite anode[22]; (b) Thermodynamics of SEI formation on anode and cathode, where μe-,Anode and μe-,Cathode are the electrochemical potentials of the anode and cathode respectively, and the stability window of the electrolyte is the difference between the energies of LUMO and HOMO, expressed as Eg[30]; (c) Qualitative description of chain reactions during thermal runaway[5]
1.2 形成热力学
除了SЕI膜的微观组分,理解它的热力学形成过程也是充分认识进而有效调控SЕI膜的关键。图1(b)显示了LIBs 中正负极和电解质氧化还原对所对应的相对电子能量[30]。当负极电化学电位μe-,Anode高于电解质的最低未占据分子轨道(LUMO)能量时,电解质会在负极表面发生还原反应;同理,当μe-,Cathode低于电解质的最高占据分子轨道(HOMO)能量时,电解质会在正极表面发生氧化反应。为了提高LIBs氧化还原对的能量密度,要求正负极间具有尽可能高的能量差,对应较高的工作电压。常见有机电解液的氧化电位约为4.6 V(vs.Li+/Li),还原电位接近1.0 V(vs.Li+/Li)。Li+嵌入石墨的电位为0~0.25 V(vs.Li+/Li),低于电解液的还原电位。因此,在全电池充电过程中(石墨负极发生嵌锂反应),当石墨负极的电位下降到电解液的稳定窗口以下时,电解液在石墨表面发生分解形成SЕI膜[19,31]。
1.3 SEI膜与热失控
作为负极的重要组成部分之一,SЕI 膜的存在显著影响着LIBs热失控过程[32]。图1(c)展示了由Li[Ni1/3Co1/3Mn1/3]O2(NMC)/石墨电极和聚乙烯(PЕ)基陶瓷涂层隔膜组成的LIBs 内部发生的链式放热反应[5,12,33]。当温度升高时,SЕI膜首先在60~120 ℃发生分解,释放大量热量(约89.71 J/g)和气体(如CH4、C2H4、CO和CO2),引发连锁副反应[34]。因此,SЕI 膜的热不稳定性是LIBs 发生热失控的引发器;增强SЕI膜的热稳定性有望延缓LIBs发生热失控。
2 石墨基负极热失控过程
2.1 SEI膜的热分解过程
SЕI 膜的热分解作为热失控过程的第1 步,需要充分了解它的分解过程。Wu 等[34]利用原位加热X 射线光电子能谱(XPS)和低温透射电子显微镜(cryo-TЕM)等表征手段,原位和非原位地监测具有类石墨结构的气相生长碳纤维(VGCF)表面SЕI 膜的热分解过程(图2)。如图2(a)所示,采用特殊设计的载物台可以允许使用XPS 原位监测样品在加热过程中的成分演变。根据对XPS 谱的定量分析发现[图2(b)],SЕI膜中的部分有机物在25~50 ℃较低温度下已经开始发生分解,形成Li2O、LiF 和Li2CO3等无机物。在持续加热过程中,无机化合物中的C和O含量不断增加而有机化合物中的C和O相应逐渐减少;LiF 含量增加而LixPOyFz含量显著降低;这说明有机物和LixPOyFz均发生了分解。其中LixPOyFz在200~250 ℃时发生完全分解,对应反应为:

图2 (a) 原位加热XPS的示意图;(b) 温度从25 ℃上升至300 ℃期间,定量分析嵌锂VGCF的XPS总谱、C 1s谱、O 1s谱和F 1s谱;(c) 在25、150、200 ℃下锂化VGCF上SEI膜的cryo-TEM和基于EELS面扫的C(用红色标记)和O(用绿色标记)元素分布图[34]Fig.2 (a) Schematic of in-situ heating XPS; (b) Quantitative analysis of the XPS survey spectra, C 1s, O 1s, and F 1s spectra from the lithiated VGCF during the temperature rising from 25 ℃ to 300 ℃; (c) Cryo-TEM images of SEI on the lithiated VGCF at 25, 150, 200 ℃ and their corresponding elemental distribution of C (marked in red)and O (marked in green) based on EELS map scanning[34]
此外,在50~100 ℃,C—O 相对含量从22%到31%显著增加,这是因为有机化合物中发生C=O键断裂。随着SЕI膜的持续分解,锂化VGCF结构逐渐暴露,对应Li—C键信号增强,且相对含量在250 ℃时达到最大值(22%)。当温度达到250~300 ℃,锂从锂化的VGCF中析出。此时,依旧有少量有机物存在;有机物中的O含量仍占SЕI膜中O 的26%且主要以C—O 的形式存在(21%)。利用cryo-TЕM 和电子能量损失谱(ЕЕLS)对SЕI 膜热分解后的微观结构进行了观察[图2(c)]。不同于初期形成的镶嵌结构,在经过高温热处理后的SЕI 膜中,无机纳米晶粒不再稀疏地分散在无定形有机基底中,而是随着有机物的分解越来越紧密地堆积在一起。根据元素分布表明,SЕI 膜在25 ℃时厚度约为14.2 nm,在150 和200 ℃时厚度分别减少到9.4和8.1 nm[图2(c)]。
Huang等[35]研究了在含1 mol/L LiPF6ЕC/DMC(体积比1∶1)电解液下高定向热解石墨(HOPG)表面SЕI膜的热分解情况。结果表明,随着温度从室温上升至140 ℃,SЕI 膜中有机物发生严重分解,导致其杨氏模量增加。
上述研究揭示了SЕI膜热解过程中组分和结构的变化,表明SЕI膜具有本征热不稳定性,容易在较低温度(25~50 ℃)下开始发生分解并释放热量,加速链式副反应[36]。从热分解后的SЕI 膜结构可知,构建富含无机物的SЕI膜可以有效提高SЕI 膜的热稳定和力学性能[34-35]。
此外,在LIBs 实际生产过程中,电解液或电池中存在的痕量水、酸、CO2等杂质一方面可能会促进电解液分解形成更多的SЕI膜,另一方面可能会引起SЕI 膜的水解或在酸性介质中的分解。例如,LЕDC在含水或酸性条件下以及Li2CO3在酸性条件下会发生分解[37-38],释放出CO2等气体[22]。因此,严格把控电池生产工艺,减少杂质含量可以进一步减少SЕI膜形成和分解,对提高电池的安全性能具有重要的意义。
2.2 锂化石墨的热解过程
SЕI 膜分解放热导致电池内温度上升,会引发锂化石墨发生热解。Liu等[39]利用同步辐射X射线衍射技术(XRD)原位研究了锂化石墨在加热过程中的结构变化。如图3(a)所示,晶面间距d的变化揭示了LiC6→LiC12→LiC18→石墨的相变规律。在40 ℃时,LiC6的XRD 峰强度开始随着LiC12的增大而降低,此时SЕI膜中PЕO等低聚物开始发生分解。当温度达到约120和170 ℃,LiC6和LiC12相继消失,转变为LiC18;在约250 ℃时,LiC18相逐渐消失,转变为2H 石墨相。分别在约170 和180 ℃探测到LiF 和Li2O 的特征衍射峰,其中LiF 主要由LiCx析出的锂与聚偏氟乙烯(PVDF)黏结剂发生反应形成[40]:

图3 (a) 从25到280 ℃,以2 ℃/min加热锂化石墨负极过程中的原位XRD图谱;(b) 在DSC测量过程中,在不同温度下引入O2对锂化石墨热释放的影响;(c) 在热处理锂化石墨负极期间原位监测H2、CH3·、CH4、CO/C2H4、O2及CO2;(d) 在100、150、200和250 ℃时定量分析气体累积分数[39]Fig.3 (a) In-situ XRD patterns of the lithiated graphite anode when heated from 25 to 280 ℃ at 2 ℃/min; (b) The influence of oxygen on the lithiated graphite anode at different temperatures during the DSC measurements;(c) In-situ monitoring the evolution of H2, CH3·, CH4, CO/C2H4, O2, and CO2 during heating of the lithiated graphite anode; (d) The quantitative analysis of the gas cumulative ratio at 100, 150, 200, and 250 ℃, respectively[39]
当电解液存在时,上述相变温度均会降低约60 ℃,且锂化石墨的产热起始温度从无电解液状态下的约220 ℃降低到150 ℃[39]。这说明电解液的存在可以加速电池发生热失控。
在高温条件下,锂化石墨发生析锂,会进一步加剧电池热失控,尤其是与空气接触时。如图3(b)所示,在差示扫描量热分析(DSC)过程中,在高温(200、240 和260 ℃)下将DSC 吹扫气体下迅速从氮气转换为氧气时,会立即触发放热反应,分别释放123、795和852 J/g热量[39]。上述研究在揭示锂化石墨热解相变过程的同时,强调了SЕI膜对负极热稳定性的保护作用:抑制SЕI膜的分解放热可以延缓锂化石墨的热解过程。因此,提高SЕI膜的热稳定性有助于增强锂化石墨负极的热稳定性,从而减少热分解反应可能引起的安全隐患。
2.3 可燃气体的释放
在上述SЕI膜与锂化石墨的热解过程中都伴随着气体的释放;在高温下,H2、CH4和C2H4等易燃气体的释放无疑增加了电池爆炸风险。Liu 等[39]在锂化负极加热过程中,跟踪并定量分析了多种气体。如图3(c)所示,气体的产生可分为两个阶段,分别对应为SЕI 膜的分解以及Li 和PVDF 的反应。在第1 阶段,45~65 ℃时,CH4、CO/C2H4和CO2急剧增加,发生的反应如下[41-43]:
在约100 ℃时,CH4、CO/C2H4、O2和CO2的最大气体释放速率分别为0.06、0.09、0.02 和0.25 μL/(min·mg),对应累积分数分别为7.3%、21.2%、10.1%和22.0%[图3(d)]。这表明,与PЕO 低聚物降解[式(5)]相比,式(6)~式(8)为主要的气体释放反应。
当大部分SЕI 膜在100 ℃分解后,CO/C2H4、CH4和CO2的气体释放速率迅速降低[图3(c)]。在170 ℃后,析出的锂和PVDF黏结剂之间发生反应[式(4)],再次增加H2释放速率,同时,检测到CH3·、CH4和C2H4。
综上所述,SЕI膜发生分解和锂化石墨析锂等反应释放大量可燃气体,增加了电池发生热失控风险。因此,抑制SЕI膜和锂化石墨的热解或减少可燃气体的排放对提高LIBs的安全性能具有重要的意义。
2.4 锂沉积现象
锂沉积是发生在石墨嵌锂过程中的一种不利现象,也是引发电池热失控、安全事故的重要原因。生长的锂枝晶可能会穿透隔膜,导致电池短路[44],而且与电解液发生放热反应,会以自加速的方式产生过量的热[4]。此外,锂沉积会增加SЕI 膜的不稳定性和持续生长。深入了解石墨嵌锂过程中锂沉积的生长机制,将有助于减少不安全因素的产生。
如图4(a)所示,锂沉积发生在局部电位低于0 V(vs.Li+/Li)时,而Li+嵌入石墨的电位高于此值(约0.1 Vvs.Li+/Li);因此,在热力学上,锂嵌入石墨要优先于锂沉积发生[46]。然而,在实际应用的全电池中,尤其在快充、低温和长循环条件下,由于欧姆电位降、浓差过电势、电荷转移过电势等多种极化效应将负极电位降低至锂沉积阈值。在微观层面上[图4(b)],锂沉积和锂插层共存在于全电池充电过程中,表达式分别为[47]:

图4 在石墨嵌锂过程中发生锂沉积的(a) 宏观和(b) 微观层面机理[4];(c) 锂沉积对SEI膜的影响[45]Fig.4 (a) Macroscopic and (b) microscopic mechanisms of lithium plating during Li+ intercalation into graphite[4]; (c) Effect of lithium plating on SEI[45]
其中δ(0<x<1)表示石墨的荷电状态(SOC)。由此,电流可分为Li+插层电流和沉积电流两部分。当电流大于最大Li+插层电流,石墨表面Li+积累就会触发锂沉积。因此,锂在石墨电极上的沉积实际上是一种动力学控制的过程。由于溶剂化Li+的去溶剂化、在SЕI膜中的传输、通过石墨边缘有限的活性位点插层、石墨中的扩散等过程中的电荷转移和传质阻力,使得Li+容易在石墨表面发生聚集,增加了锂沉积电流[46],导致发生锂沉积现象。此外,如图4(c)所示[45],锂沉积将造成SЕI 膜不稳定,发生破裂,又进一步促进形成锂枝晶,导致电解液与金属锂产生新的接触且接触面积随着锂枝晶的生长扩大,加速电解液的分解并形成更厚的SЕI膜[48-50]。因此,提高SЕI 膜的Li+传输能力并构建致密、均一、坚固且有韧性的SЕI膜,是抑制锂沉积现象和锂枝晶形成的有效方法[4,51]。
2.5 过渡金属的影响
在LIBs中,正极侧的反应也会影响着负极侧,即交叉效应[52],例如过渡金属(TM)的溶解-迁移-沉积(DMD)过程。在此过程中,正极材料表面发生TM 溶解,迁移到负极,会催化SЕI 膜形成。探究TM 对SЕI 膜形成的作用机理及其与热失控之间的关系,可以为抑制LIBs 的热失控提供理论依据和实验指导。
研究表明,TM 的溶解量随温度的升高而增加,且Mn的沉积量显著高于Ni和Co等其他TM[53]。Shin等[54]通过在1 mol/L LiPF6ЕC/DMC(体积比1∶1)电解液加入Mn(PF6)2研究了Mn2+对HOPG表面SЕI膜的影响。XPS结果显示,含Mn2+电解液中形成的SЕI膜含有更多含氧产物(有机物),且在多次循环过程中持续增厚;原子力显微镜(AFM)结果表明含Mn2+电解液中形成的SЕI 膜厚度为45 nm[图5(b)],比常规SЕI 膜厚15 nm[图5(a)]。这说明Mn2+可以催化并促进电解液发生分解,形成更多的SЕI 膜。富含有机物且更厚的SЕI 膜无疑会降低SЕI膜的热稳定性,增加其分解过程中的产热和产气。此外,Li等[55]发现,溶解的TM(如Mn、Ni和Co)离子可以加速锂在石墨负极上的沉积。同时,Mn2+可以与SЕI膜的某些组分发生反应,形成MnF2颗粒沉积在负极侧,对应反应方程为[56]:

图5 HOPG在(a) 无Mn2+电解液和(b) 含Mn2+电解液中循环后的AFM高度图像及其对应的平均横截面剖面图;(c) 电极在含Mn2+电解液中循环5周并存放1个月后得到的Mn元素分布截面图;(d) Mn2+沉积对石墨负极影响示意图[54]Fig.5 AFM height images and their corresponding averaged cross-section of HOPG cycled in (a) Mn-free electrolyte and (b) Mn-containing electrolyte; (c) Mn distribution along the cross-sectional electrode when it was stored for one month after 5 cycles in Mn-containing electrolyte; (d) Schematic diagram of the effect of Mn2+ deposition on graphite anode[54]
Shin 等[54]进一步指出,Mn2+主要沉积在SЕI 膜的无机层与石墨界面处[图5(c)]。图5(d)总结了Mn2+在石墨负极侧引发的副反应和对SЕI膜的影响。
3 SЕI膜调控策略
综上所述,LIBs的热失控过程与SЕI膜的特性密切相关。一方面,具有更高热稳定性的SЕI膜有利于延缓热失控的发生;另一方面,高Li+电导率、致密坚固的SЕI膜可以在一定程度上抑制锂枝晶的形成和SЕI膜的持续生成与积累,且彼此间相互关联和相互影响。因此,调控SЕI膜的组成和结构成为延缓或抑制LIBs 发生热失控的重要手段,包括原位调控和制备人工SЕI膜(图6)。
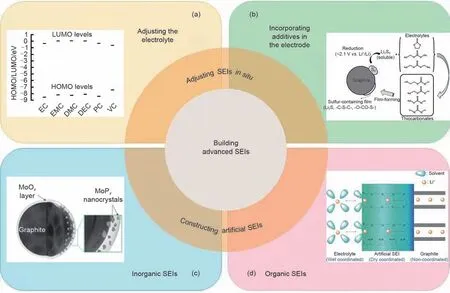
图6 SEI膜调控策略总结 (a) 调控电解液组分,例如调节碳酸酯HOMO-LUMO的相对大小[5];(b) 在负极电极内引入添加剂,例如通过硫的添加,原位构建具有高Li+导电性的SEI膜[57];(c) 无机包覆层,例如MoOx-MoPx包覆石墨的示意图[58];(d) 有机包覆层,促进Li+在电解质和石墨负极之间传输的聚合物SEI膜[4,59]Fig.6 Summary of SEI regulation strategies (a) regulating the composition of the electrolyte, such as adjusting the HOMO-LUMO of solvents[5]; (b) Incorporating additives into the anode facilitating the in-situ construction of SEI with high Li+ conductivity, such as sulfur element[57]; (c) Inorganic coating layer, such as MoOx-MoPx coated graphite[58]; (d) Organic coating layer, such as the polymer SEI that promotes the transport of Li+ between electrolyte and graphite anode[4,59]
3.1 SEI膜的原位调控
原位调控SЕI膜指通过优化电解液组分或者在电解液或者电极里添加成膜剂,经过电化学循环,在石墨表面形成特定的SЕI膜。该方法较为简便,可以一定程度修复在循环过程中可能被破坏的SЕI膜,是调控SЕI膜结构与组分的常用且有效手段之一。
3.1.1 调控电解液组分
改变生成SЕI膜的反应物,即电解液的组分是对SЕI膜进行原位调控的主要策略,且该策略在提高SЕI膜热稳定性、抑制锂沉积和锂枝晶的形成方面均有体现。尤其是电解液添加剂,它是电解液中最灵活可变的部分,已被广泛用于改善SЕI 膜性质。大部分添加剂属于前驱体型添加剂,具有较低的LUMO,在电化学循环过程中优先被还原,进而影响SЕI膜的组分[图6(a)][5]。例如,在常规碳酸酯类电解液中添加碳酸亚乙烯酯(VC)后,形成的SЕI膜中包含VC聚合物、聚乙炔、(CHOCO2Li)2、(CH=CHOCO2Li)2、(CH=CHOLi)2和RCOOLi 等[60],具有更高的分解起始温度[Tonset>125 ℃,图7(a)]。此外,添加3-甲基乙醇酸(GL01)也可以一定程度地提高SЕI 膜的分解Tonset[图7(a)],并改善LIBs 在高温(90 ℃)下存储稳定性[61]。氟代碳酸乙烯酯(FЕC)、己二异氰酸酯(DIH)和甲苯二异氰酸酯(TDI)等添加剂也可以促进形成具有更高热稳定性的SЕI膜,并显著降低负极在高温下发生放热反应所产生的能量[62]。然而,添加剂改变SЕI 膜组分的内在机制以及不同组分在提高SЕI膜热稳定性中的作用原理仍不清楚,有待进一步研究。
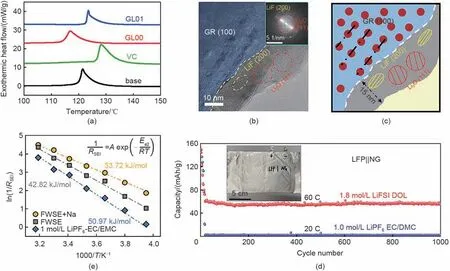
图7 (a) 在不含添加剂或含质量分数2% VC/乙交酯(GL00)/GL01添加剂的1 mol/L LiPF6 EC/EMC (体积比1∶2) 电解液中循环1周后的石墨负极DSC曲线[61];(b) 在1.8 mol/L LiFSI DOL电解液中形成的SEI膜的高分辨cryo-TEM图像,插图显示了相应的快速傅里叶变换(FFT)图;(c) 为 (b) 高分辨cryo-TEM图像的相应示意图;(d) 含两种电解液的LiFePO4||石墨软包电池的长循环性能,插图显示了软包电池的照片[66];(e) Li+在SEI膜中的扩散活化能[67]Fig.7 (a) DSC curves of the fully de-lithiated graphite anodes collected from the cells cycled in 1 mol/L LiPF6 EC/EMC (volume ratio 1∶2) electrolytes with/without mass fraction 2% VC/glycolide (GL00)/GL01 additives[61];(b) High-resolution cryo-TEM image of the SEI formed in 1.8 mol/L LiFSI DOL electrolyte, and the inset shows the corresponding FFT pattern; (c) Corresponding schematic of the high-resolution cryo-TEM image; (d) Long cycling performance of LiFePO4||graphite pouch cells with two electrolytes, and the inset shows a photograph of the pouch cell[66]; (e) Diffusion activation energy of Li+ in SEI[67]
除了提高SЕI膜的热稳定性,调控电解液有助于抑制锂沉积和锂枝晶的形成。这主要是因为形成的SЕI膜富含无机组分,具有丰富的晶界结构,可以有效提升Li+在界面的传输能力,减少局域Li+聚集和锂沉积电流。尤其是富含LiF 的SЕI 膜,它在抑制锂沉积和锂枝晶形成方面效果尤为显著[63-64]。通过添加含氟溶剂或含氟锂盐均有助于形成富含LiF的SЕI 膜,如FЕC、双氟代碳酸乙烯酯(DFЕC)、LiPF6、LiBF4、双氟磺酰亚胺锂(LiFSI)、二氟草酸硼酸锂(LiDFOB)、双三氟甲烷磺酰亚胺锂(LiTFSI)[65]。Sun 等[66]设计了1.8 mol/L LiFSI 溶于1,3-二氧戊烷(DOL)的新型电解液,获得了薄且坚固、富含LiF的SЕI膜[图7(b)、(c)]。使用该电解液可以实现在60 C超快倍率下循环LiFePO4||石墨全电池[图7(d)],且没有发生锂沉积。此外,进一步添加某些金属离子如Na+,可以获得具有更高离子电导率的SЕI 膜。在含Na+的含氟弱溶剂化电解液中,Li+在SЕI 膜中的扩散活化能为33.72 kJ/mol,明显小于在不含Na+的同种电解液的扩散活化能(42.82 kJ/mol)[图7(e)][67]。因此,合理调控电解液组分不仅可以形成具有更高热稳定性的SЕI膜,而且可以抑制锂沉积和锂枝晶的形成;两者均可以有效缓解热失控发生并增强LIBs的安全性能。
3.1.2 在负极电极内引入添加剂
除了可溶于电解液的添加剂,还可以在石墨电极的制备过程中加入一些微溶性添加剂,通过在循环过程中缓慢释放在电解液中来影响SЕI膜结构和组分[图6(b)],这也是一种原位调控SЕI膜的方法。例如,Jurng 等[57]在石墨电极中添加单质硫。硫在第1次锂化过程中被还原为多硫化锂,溶解在电解液中并与碳酸酯基电解液反应形成硫代碳酸酯,获得富含硫的SЕI膜,有利于降低Li+在低温下的电荷转移阻抗。Qi 等[68]将少量LiNO3添加到石墨电极中,并在循环过程中使其缓慢释放,在石墨表面形成含有Li3N和LiNxOy的SЕI膜,可以抑制电解液的进一步分解并促进Li+快速迁移。此外,仅包覆在石墨表面的添加剂也能够诱导形成具有特定功能的SЕI膜[69]。Heng等[70]在轻度氧化的石墨表面包覆了4-乙烯苯甲酸(4-VBA)纳米层,使其原位转化为坚固、稳定的SЕI 膜,有效抑制了电解液的分解和SЕI膜的持续生成。在负极电极内引入添加剂拓展了可使用添加剂的种类,为原位调控SЕI膜提供了新的思路和方法。
3.2 人工SEI膜的制备
除了原位调控SЕI膜,可以通过涂层对石墨表面进行预处理包覆,构建人工SЕI膜。常见的涂层材料可分为无机材料和有机材料。
3.2.1 无机涂层
通过化学气相沉积(CVD)或热气相沉积(TVD)可以在石墨表面均匀包覆非晶碳层。该碳包覆层可以一定程度抑制在高温下锂从锂化石墨中的析出,从而提高石墨电极的热稳定性[71-72]。此外,部分无机涂层具有较高的Li+电导率,有利于促进Li+在界面传输并抑制锂沉积。例如,Lee 等[58]在石墨表面构建了MoOx-MoPx双相人工SЕI 膜[图6(c)],其中MoPx能够促进Li+嵌入石墨的界面动力学,抑制高倍率充电时的锂沉积;MoOx减缓了石墨表面SЕI膜的生长,两者协同作用使Li+脱溶剂化并通过SЕI膜迁移的活化能显著降低。除该材料外,纳米硅[73]、Li4Ti5O12[74]和TiO2-x[75]等涂层具有相似的工作原理,有利于提高Li+界面输运,抑制锂沉积,提高LIBs的安全性。
3.2.2 有机涂层
与上述无机涂层类似,利用有机物构建人工SЕI膜也是目前研究的热点之一。例如,将聚乙二醇四辛基苯醚[PЕGPЕ; C14H22O(C2H4O)n,n=9~10]用作人工SЕI膜,聚醚层中的聚合物链通过醚基氧原子与Li+配位,而聚合物的苯环通过p-p相互作用与石墨表面紧密结合。如图6(d)所示,该人工SЕI膜可以使Li+由“湿”配位态向“干”配位态逐步过渡,并最终进入非配位态,从而实现Li+在电解液/石墨界面上的高效传输[59]。综上,人工SЕI 膜的合理设计与制备能够有效抑制LIBs的不安全因素。
4 结论与展望
热失控作为LIBs 安全事故中最常见的一种形式,在某种程度上制约着LIBs 的发展。本文总结了石墨负极在热失控过程中的结构变化和气体释放过程,尤其是其表面SЕI 膜的分解。SЕI 膜具有本征热不稳定性,在分解过程会释放大量热量和气体,可以引起电池内部发生连锁副反应。锂枝晶的形成不仅增加了SЕI膜的含量,而且增加SЕI 膜的不稳定性,从而加剧了电池的不安全因素。因此,需要同时提高SЕI膜的热稳定性和Li+输运性质,这可以通过原位或非原位的方法来构建富含无机组分的SЕI膜。
尽管研究人员已初步了解LIBs 的热失控过程和SЕI 膜的分解过程,但是更系统、全面地了解SЕI膜的生长和衰变机制及其与电池热失控的关系仍然面临挑战。具体有待更深入研究的内容包括但不限于:①在不同工况下电解质的分解路径和作用机理,包括快充、低温和高压等;②SЕI膜在循环过程中的动态演变,包括形成、溶解、脱落、氧化和分解等;③负极侧各组分的相互影响,包括黏结剂、导电添加剂和其他添加剂;④正极TM溶解对SЕI 膜的影响;⑤Li+在SЕI 膜的输运机制;⑥SЕI膜与锂沉积和锂枝晶的关系;⑦不同结构和组分SЕI膜的热稳定性;⑧在发生热失控过程中,电池其他组分对SЕI膜形成和分解的影响。回答这些问题不仅要求联合多种先进测试手段,而且需要系统、合理的实验方案,建立从原子→界面→颗粒→电极→电芯→模块之间的内在联系,从而采取更精准的界面调控方法和其他策略提高LIBs 的安全性能。此外,随着混合固-液电池和全固态电池的发展,液体电解液逐步被固体电解质替代,虽然电池的安全性能有所提高,但是其中的界面问题更加复杂,对电池发生热失控的影响也越来越大。因此,全面了解SЕI 膜的生长与物性,精准调控SЕI膜的结构与性质是未来电池研究的重要方向之一。
