基于FTO-PANI-Pt/Fe2O3的新型电化学传感器快速检测过氧化氢*
2023-07-27王小花苏丽霞刘冰倩
杨 迪,王小花,苏丽霞,刘冰倩
(贵州大学药学院,贵州省合成药物工程实验室,贵州 贵阳 550025)
过氧化氢(H2O2)具有较强的氧化性可作为氧化剂、漂白剂等试剂,而被广泛应用于日常生活、工业生产、生物加工、绿色能源化学、采矿加工及临床医药等领域[1-2]。正常情况下,H2O2分解生成水和氧气,对人体和环境不会造成危害。当水体、环境和食品中及生物体内的 H2O2超过一定量时,容易造成水体、环境污染及生物体受损中毒或致癌等。因此,过氧化氢的检测对人体健康以及环境资源保护需引起重视。目前,氧化氢的检测方法主要包括化学发光法[3]、高效液相色谱法[4]、荧光法[5]和电化学法[6]等。这些方法选择性及灵敏度都具有一定优势,但不足之处也十分明显:专一性不强,大型仪器价格贵重,操作不便,需要专业人员进行培训后使用等。因此,建立一种低成本、高灵敏、快速检测H2O2的方法十分迫切。
近年来,迅速发展的电化学传感器因具有响应速度快、操作简单、灵敏度高、成本较低且选择性好等优点,在食物安全检测、环境监测、药物分析领域得到了广泛应用。虽然H2O2在普通电极上可以被还原,但灵敏度较低且易被干扰。为提高检测H2O2的选择性和灵敏度,需对电极进行修饰。金属氧化物通常较便宜且可重复使用,但其活性低于贵金属催化剂。一种常见的策略是将贵金属负载到金属氧化物上以合成负载型催化剂。该载体不仅有助于实现贵金属颗粒的高度分散,而且通过强金属参与反应,提高催化活性。赤铁矿(α-Fe2O3),因其良好的热稳定性、环境友好性和低成本而备受青睐[7-8],特别是 α-Fe2O3纳米晶体在不同的反应环境中具有较高的表面效应,是一种良好的催化剂。Fe2O3作为一种还原氧化物,可以与贵金属形成较强相互作用,Fe2O3与 Pt 通过 Fe-O-Pt 键锚定 Pt 纳米颗粒,有效减缓团聚,α-Fe2O3/Pt 催化剂通常在不同的化学反应和检测上表现出显著的催化性能,如甲醛催化氧化、H2O2氧化还原和丙酮气体氧化[9]。
基于纳米金属材料与聚苯胺(PANI)的优良特性,首次制备具有良好导电性的新型 FTO-PANI-Pt/Fe2O3复合电极电化学传感器,利用贵金属及金属氧化物良好的协同催化性能,增强了检测灵敏度,拓展了贵金属负载到金属氧化物材料在电化学传感领域的应用。
如图1所示,使用传统三电极系统,将FTO-PANI-Pt/Fe2O3复合电极作为工作电极,构建检测H2O2的电化学传感器。当目标物H2O2存在时,基于复合电极催化H2O2发生氧化还原反应产生电子,从而将化学量转化为电学量,由转换器经过转换或放大处理得到可识别的电信号,最终反映到显示装置,由此可对 H2O2进行定量分析。这可能是因为H2O2被氧化时会将电子传递给复合材料,而复合材料上具有良好导电性的Pt/Fe2O3和PANI会迅速地将电子传递给FTO电极,从而增强电流信号。根据电流强度与目标物浓度成正相关,可以定量分析H2O2。该电化学传感器制备简单且检测速度快,实现简单、快速、灵敏的检测H2O2。

图1 基于PANI/Pt/Fe2O3电化学传感器检测 H2O2 原理图
1 实 验
1.1 试剂与仪器
氯铂酸,上海化学试剂一厂;过氧化氢(纯度=30%)、铁氰化钾(纯度≥99.5%)、过硫酸铵(纯度≥98.0%)、苯胺(纯度≥99.5%)均购自成都金山化学试剂有限公司;碳酸氢钠(纯度≥99.5%)、六水三氯化铁(纯度≥99.0%)均购自天津市永大茂化学试剂厂;磷酸氢二钠,天津市科密欧化学试剂有限公司;聚乙烯吡咯烷酮PVP-40,上海源叶生物科技有限公司;氢氧化钠(纯度≥96.0%),天津市科密欧化学试剂有限公司;盐酸(纯度:36%~38%),重庆川东化工有限公司;其它试剂均为国产分析纯;实验用水为二次水。
101-1A 电热鼓风干燥箱,天津天泰仪器有限公司;UV-5500PC 紫外-可见分光光度仪,上海元析仪器有限公司;CHI650E A17314电化学工作站,上海辰华仪器有限公司;掺杂氟的SnO2导电玻璃(FTO),武汉晶格太阳能科技有限公司;ST3100 pH计,奥豪斯仪器有限公司;TGL-20 W/S台式高速离心机,金坛市城东盛联实验仪器厂;QUINTIX35-1CN 型sartorius电子天平。
1.2 电极的制备和测试
1.2.1 Pt/Fe2O3的合成
参照文献[10],取 25 mL 无水乙醇、0.676 g FeCl3·6H2O和1.8 g NaHCO3依次加入 100 mL 圆底烧瓶中,强磁搅拌约 30 min。然后将得到的溶液转移到离心管中分别用蒸馏水和乙醇多次洗涤,离心后室温干燥得到Fe2O3固体。取 0.02084 g 制备的 Fe2O3分散于 20 mL 去离子水中,磁搅拌。然后依次加入 1 mL H2PtCl6(19.3 mM)水溶液、0.010 g 聚乙烯吡咯烷酮(PVP,PVP-40)和 0.01580 g 硼氢化钠(NaBH4)。在 100 ℃下加热回流 3 h 后,将沉淀离心收集,用去离子水洗涤 4 次。最后,将 Pt 纳米颗粒修饰的 Fe2O3(记作Pt/Fe2O3)在 60 ℃的烘箱中干燥 6 h[11],加去离子水超声混匀,即得 0.85 mg/mL Pt/Fe2O3溶液。
1.2.2 PANI的合成
参照文献,取 3.4 mL 浓盐酸缓慢滴入装有 20 mL 去离子水的圆底烧瓶中,再加入 450 μL 苯胺,并在磁力搅拌器加热搅拌 30 min。取 0.09 g 过硫酸铵溶于 10 mL 去离子水中溶解 10 min,作为阴离子源,将该溶液缓慢滴加到阳离子前躯体中搅拌 1 h 形成聚苯胺,溶液最初呈微红金黄色,最后呈绿色,说明聚苯胺完全聚合形成[12]。
1.2.3 传感器的制备
制备传感器之前,用棉花蘸取乙醇擦拭 FTO,再用乙醇和二次水分别超声 10 min,于 60 ℃下烘干备用。 然后制备电极,如图1所示,使用移液枪吸取 10 μL PANI 溶液滴涂在 FTO 表面,在 37 ℃烘箱中进行干燥,然后继续滴涂 30 μL Pt/Fe2O3,晾干后备用,修饰的 FTO 电极作为工作电极(FTO-PANI-Pt/Fe2O3)。
1.2.4 电化学测试
在0.01 mol/L磷酸盐缓冲溶液 (PBS)中组成三电极体系,以新制的FTO (25 mm2)为工作电极,Ag/AgCl电极为参比电极,铂电极为对电极。用循环伏安法 (cyclic voltammetry,CV)探索实验可行性,扫描电压0~0.8 V,扫描速率为0.05 mVs-1。
1.3 实际样品的处理
1.3.1 牛奶
将 20 mL 1 mol/L H2SO4与 80 mL 牛奶混合离心(20 min,8000 r/min),上清液用 1 mol/L NaOH 调整 pH 到 6.5,得到处理后牛奶标准溶液。用 0.1 M PBS 稀释 5 倍,在稀释的牛奶样品中掺入不同浓度的 H2O2,然后进行电化学检测[13]。
1.3.2 湖水
首先使用 0.22 μM 过滤膜将湖水过滤,除去颗粒杂质,调 pH 至 6.5,再用 0.1 M PBS(pH=6.5)稀释 5 倍得到湖水标准溶液。在稀释的湖水样品中掺入不同浓度的 H2O2,然后进行电化学检测。
2 结果与讨论
2.1 FTO-PANI-Pt/Fe2O3的形貌和结构表征
通过SEM,如图2A所示,Fe2O3呈球状,如图2B所示,Pt/Fe2O3有小颗粒附着在球状Fe2O3上,说明Pt均匀的覆盖在Fe2O3上,说明Pt/Fe2O3制备成功[14]。如图2C所示,滴凃在FTO上的PANI为短枝叉形状[15]。图2D为FTO-PANI-Pt/Fe2O3图像,可以看出Pt/Fe2O3在PANI上很好的分散,这进一步表明复合材料的成功合成。通过 EDS 表征材料的元素组成,如图2F所示,FTO-PANI-Pt/Fe2O3复合电极上含有C、N、O、Fe和Pt元素。图2E为FTO-PANI-Pt/Fe2O3放大 2000 倍的SEM图,由于放大倍数较小,形貌特征不是很明显。图2G 为与之对应的 EDS 元素映射图像。从图2G中可以看到C、N、O、Fe和Pt元素分布均匀。
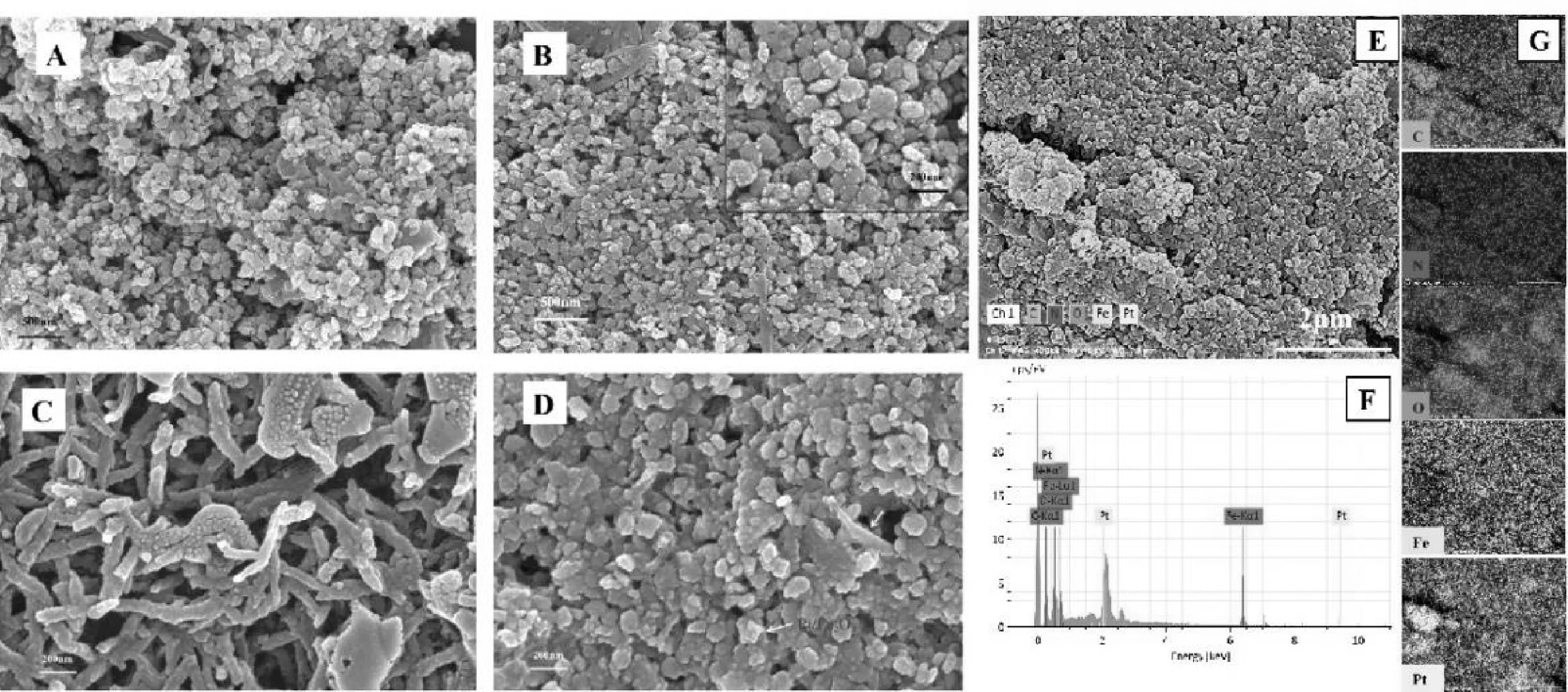
图2 Fe2O3(A)、 Pt/Fe2O3(B)、PANI(C)、PANI-Pt/Fe2O3(D)的SEM 图;PANI-Pt/Fe2O3的EDS 图 (F),SEM 图 (E)和对应的 EDS 元素映射图像 (G)
图 3(A)显示了PANI、Fe2O3、Pt/Fe2O3材料在 4000~400 cm-1区域的红外光谱。从图 3(A)中可以看到PANI的红外光谱,在3413 cm-1处宽带对应于 -OH 伸 缩 振 动 峰,在 1627、1550、1494、1182 和 1003 cm-1处的其他红外波段分别对应于C=N、C=C 伸缩模式、苯环的 C=C 伸缩模式、及在平面弯曲模式下 C-H 的伸缩模式。此外,在1920 cm-1处是环戊烷的特征吸收峰[16];Fe2O3的特征吸收峰在 472 cm-1和 560 cm-1处对应于 Fe-O 伸缩振动,吸收峰在 1625 cm-1处可能是由于纳米颗粒中有机分子的 C-C 键的存在;Pt/Fe2O3复合材料的-OH 伸缩区的振动峰从 3413 cm-1红移至 3448 cm-1,峰值为 1112 cm-1是 C-O 的吸收峰[17]。在 557 cm-1处的吸收带对应于 Pt-Cl 的拉伸不对称振动[18]。从 Pt/Fe2O3纳米复合材料的光谱中,可以找到 Pt 和 Fe2O3的所有特征峰,表明纳米复合材料制备成功。
图3(B)为合成材料的紫外可见吸收光谱图。从图3(B)中可以看到,PANI(曲线“a”)在330~360 nm和500~700 nm范围内存在2个特征吸收峰,分别是PANI的芳香族C-C键和醌族C-C键的π-π*跃迁引起的[19]。Fe2O3(曲线“b”)在550 nm处有特征吸收峰[20]。Pt/Fe2O3与之相比在400~500 nm区域观察到两个较宽的吸收峰,对应Fe2O3纳米材料和Pt纳米粒子的共振模式。以上各表征结果均表明FTO-PANI-Pt/Fe2O3复合电极成功制备。
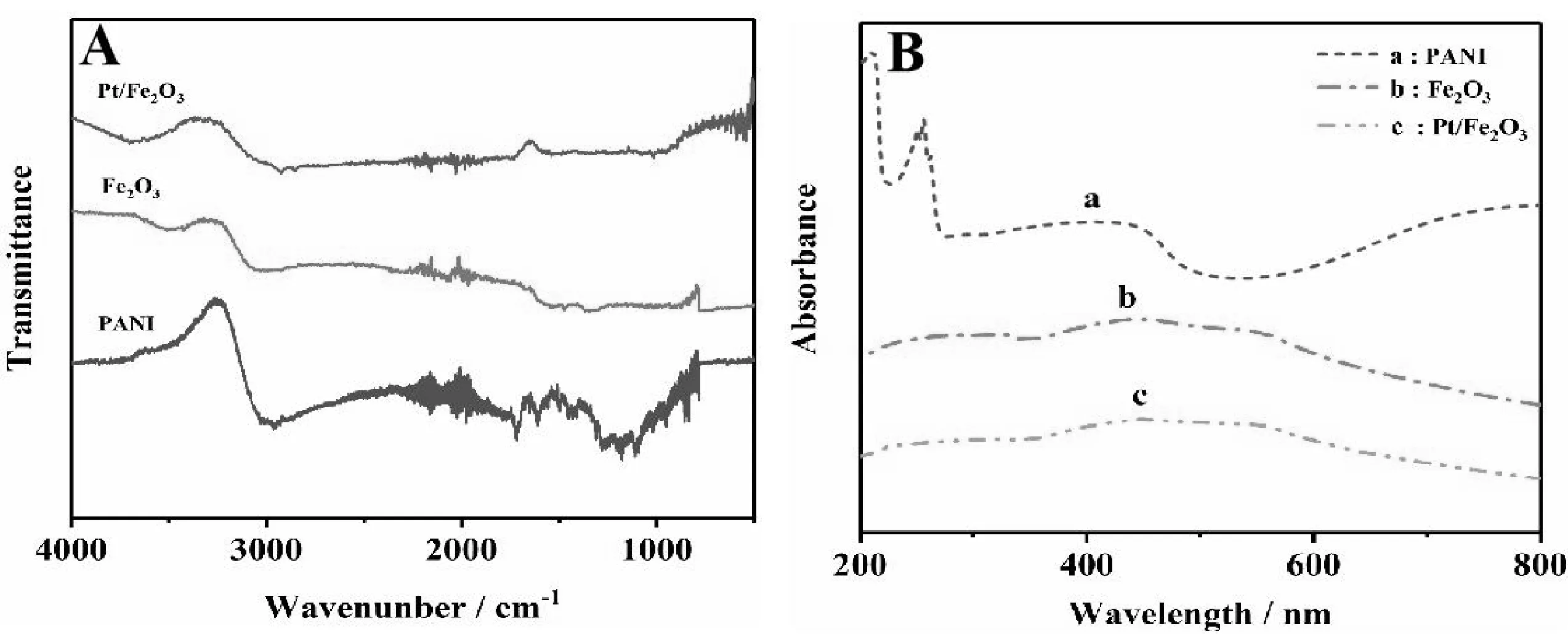
图3 (A)Fe2O3、Pt/Fe2O3、PANI的红外光谱图(B)PANI(a)、Fe2O3 (b)、Pt/Fe2O3(c)的紫外可见光谱图
2.2 可行性探究
为确保基底材料成功修饰于玻璃电极(FTO)上,在相同的条件下,利用CV和EIS来 来研究不同修饰组分在电极表面的电化学行为。如图4(A)所示,在裸 FTO 电极(曲线“a”)上观察到 [Fe(CN)6]3-/4-氧化还原反应对应的一对氧化还原峰,Fe2O3(曲线“c”)以及 PANI 修饰的 FTO (曲线“b”)其峰值电流有所上升,有聚苯胺及双金属复合材料 (Pt/Fe2O3)修饰的 FTO 电极(曲线“d”)的峰值电流最大,这表明其具有很强的电催化氧化性能。此外,图4(B)为不同修饰电极的电化学交流阻抗谱图(EIS),其半圆直径表示电子转移电阻,由图4可看出 FTO-PANI-Pt/Fe2O3电极(曲线“d”)半径最小,其对应的电阻最小,导电性最佳,表明 Pt/Fe2O3可以给电极和电解质之间提供一个良好的电子通路,加快电子传输速率。这与 CV 测量结果一致。
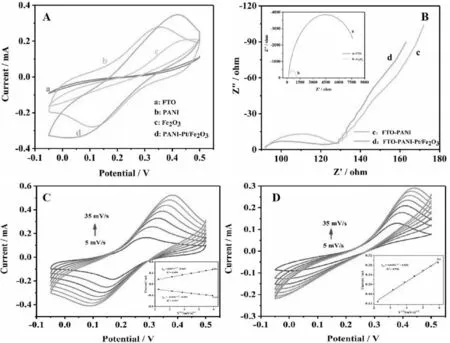
图4 不同修饰电极的循环伏安(CV)图(A);不同修饰电极的交流阻抗图(B);FTO-PANI-Pt/Fe2O3复合电极在不同扫速(5~35 mV/s)下循环伏安 (CV)图(C)(内置图:阳极峰电流(Iox和 Ired)值与扫速的线性相关性);
为进一步研究复合电极的动力学过程,实验采用循环伏安法考察了FTO-PAN-Pt/Fe2O3电极在不同扫描速率下的影响。如图 4(C)所示:随着扫描速率从 5 mV/s 增加到 35 mV/s,相比于裸电极FTO(图4(D))FTO-PAN-Pt/Fe2O3的阳极峰和阴极峰峰电流逐渐增加,且阳极峰峰电位正移,阴极峰峰电位负移。随后得到了峰值电流与扫描速率平方根的良好线性关系,其对应回归方程分别为 Iox (mA)=0.097 v1/2-0.0492(R2=0.9995)和 Ired (mA)=-0.0601 v1/2-0.0588(R2=0.9968),表明了该电极上的基底材料的氧化还原反应是一个扩散控制过程。故而证明经一体化诱导成型所构建的双金属复合物修饰聚苯胺电极(FTO-PANI-Pt/Fe2O3)具备较好的的电化学行为。
为了探索该实验的可行性,在相同的条件下,利用CV比较4种材料电催化氧化H2O2的活性。从图5(C)可看出,复合材料修饰的电极(曲线“e”)的电催化氧化能力远高于裸电极 FTO (曲线“a”)、FTO-PANI(曲线“b”)、FTO-Fe2O3(曲线“c”)、FTO-PANI-Fe2O3(曲线“d”),表明该复合材料修饰的电极具有协同催化氧化性。为了验证复合材料对 H2O2的催化效果,用CV研究了 FTO-PAN-Pt/Fe2O3对 H2O2的电催化活性。从图5(A,B)中可以看出,随着过氧化氢浓度增加响应电流值显著增强,说明复合电极 FTO-PANI-Pt/Fe2O3对 H2O2有显著的电流响应。因此,以上实验证明一体化诱导成型所构建的双金属复合物修饰聚苯胺电极构建的电化学传感器是可行的。

图5 (A,B)复合电极 FTO-PANI-Pt/Fe2O3 电极在含有或不含有 H2O2 的循环伏安图(A)及柱状图(B);
2.3 实验参数的优化
(1)不同检测液的选择
为了研究 FTO-PANI-Pt/Fe2O3电极在不同电解液中检测过氧化氢(H2O2)的电化学行为,本实验选取四种溶液作为电解液用于配制 H2O2溶液,并用CV进行测试。其结果如图 6(A)所示,发现由 PBS 做电解液的催化材料较另外三者的催化效果明显。因此选取 PBS 做电解液用于电化学检测。
(2)pH优化
溶液的pH值对H2O2的电化学检测有着重要影响,为了使FTO-PANI-Pt/Fe2O3复合电极电化学效果达到最佳,需对检测溶液的pH值进行优化。由图6(B)可知,当 pH 为 6.5 时,复合电极对 H2O2的催化效果达到最大;随着 pH 的继续增大,其催化效果反而降低。所以选择检测液的pH值为6.5。
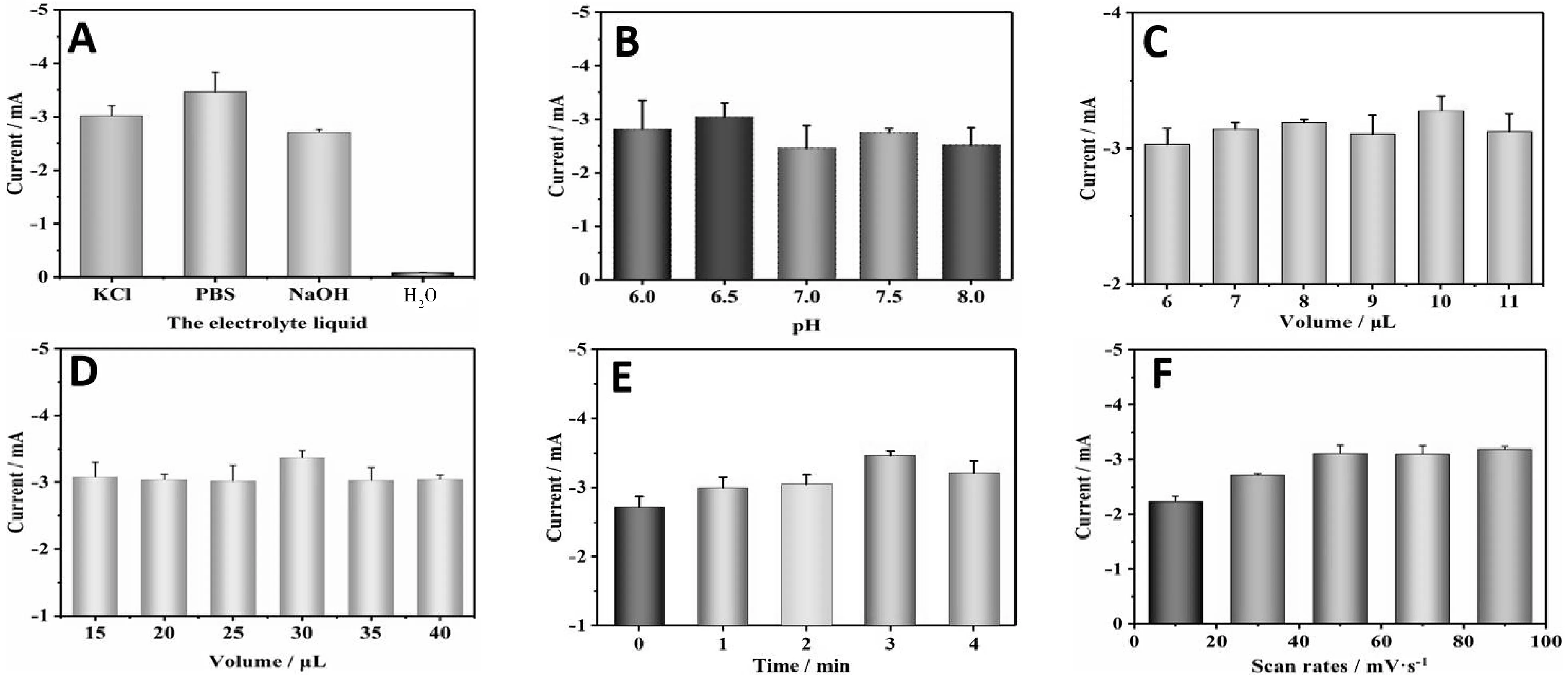
图6 不同电解液配制的 3 mg/mL H2O2与电流的关系(A);不同 pH 下的3 mg/mL H2O2 与电流的关系(B);不同体积PANI 制备的电极下 3 mg/mL H2O2 与电流的关系(C);不同体积 Pt/Fe2O3 复合材料制备电极下 3 mg/mL H2O2 与电流的关系(D);不同催化时间下的3 mg/mL H2O2 与电流的关系(E);不同扫描速度下的3 mg/mL H2O2 与电流的关系(F)
(3)PANI 用量的优化
当电极上修饰材料过多时,容易造成工作电极上的复合材料脱落,而当用量过少时,不易成膜且可能不足以支撑对 H2O2的还原,因此,选定合适的涂覆量对于构建复合电极是极其有必要的。采用不同滴涂量的PANI,在相同条件下运用CV检测,其结果如图 6(C)所示,通过图上催化性能可以看出当PANI体积为10 μL 时,FTO-PANI-Pt/Fe2O3复合电极对 3 mg/mL H2O2的催化性能达到最佳,故后续实验均选取 10 μL PANI 用于制备电极进行电化学检测。
(4)Pt/Fe2O3用量的优化
复合材料 Pt/Fe2O3的浓度对H2O2的电化学检测也有着重要影响,如图6(D)所示,通过图上催化性能可以看出当 Pt/Fe2O3复合材料为 30 μL 时,FTO-PANI-Pt/Fe2O3复合电极对 H2O2的催化性能达到最佳,但当浓度逐渐增大时,可能由于电阻增大,阻碍了电子传递,导致氧化峰电流变小。因此将30 μL Pt/Fe2O3复合材料作为最佳复合材料浓度。
(5)检测时间的影响
反应时间是影响复合电极催化过氧化氢的重要因素,通过改变 FTO-PANI-Pt/Fe2O3电极催化H2O2的时间,进一步考察 FTO-PANI-Pt/Fe2O3电极还原H2O2的电化学性能。其结果如图 6(E)所示,当反应时间为 3 min 时,其催化效果达到最佳。
(6)扫描速率的优化
由于 FTO-PANI-Pt/Fe2O3电极催化 H2O2的电化学性能受扫描速度的影响。本实验通过改变扫描速度,进一步考察 FTO-PANI-Pt/Fe2O3电极还原 H2O2的电化学性能。其结果如图6(F)所示,随着扫描速度增加,峰电流增大,当扫速为50 mV/s时,复合电极对 H2O2的催化效果达到最大;随着扫速的继续增大,其催化效果接近。因此选取50 mV/s为最佳扫描速率进行电化学检测。
2.4 H2O2的定量分析性能
在最佳优化条件下,利用该传感器对不同浓度的H2O2进行CV检测。如图7(A,B)和图7(C,D)所示,随着H2O2浓度的增大,峰电流值逐渐增大,H2O2浓度在 0.2~1.2 mg/mL 和 1.2~3.6 mg/mL 范围内,响应电流与 H2O2的浓度呈现出两段良好的线性关系,校准曲线分别为y=-1.9892x-0.1499(R2=0.9991)和y=-0.4703 x - 1.9653(R2=0.9956),最低检测限 (LOD)为 0.4 mM(S/N=3)。与文献报道检测H2O2的其他方法比较 (表1),虽然检测限没有明显优势,但其优势在于检测快速,便捷。

表1 H2O2检测方法的比较

图7 FTO-PANI-Pt/Fe2O3 复合电极在0.2~1.2 mg/mL H2O2 溶液中的循环伏安 (CV)图(A)及线性图(B);FTO-PANI-Pt/Fe2O3 复合电极在1.2~3.6 mg/mL H2O2 下的 0.1 M PBS(pH=6.5)溶液中的循环伏安 (CV)图(C)及线性图(D)
在检测H2O2的线性范围内,研究该传感器的选择性。如图8(A)所示,该传感器仅对H2O2有明显的响应,2.5倍浓度的干扰离子 (甘氨酸(Gly)、维生素C(VitC)、葡萄糖(Glucose)、盐酸多巴胺(DA)、组氨酸(His)、尿素(Urea)、谷氨酸(Glutamic acid))引起的信号变化极其微弱,表明该传感器具有良好的选择性。平行制备5个 FTO-PANI-Pt/Fe2O3电极,检测其对 3 mg/mL H2O2的电催化活性,评价其重现性。其结果如图 8(B)所示,其相对标准偏差 RSD 为 2.99%,证实其优良的重现性。此外,通过CV测试了电极基材的稳定性,见图8(C),结果表明,复合电极具有良好的稳定性,提高了检测的准确性。利用同批次和不同批次制备电极,对该方法重现性进行评估,首先,用同一批制备得的修饰电极在 1.2 mg/mL H2O2溶液中进行 3 次 CV 平行测试,结果如图 8(D)所示,检测不同批次其相对标准偏差(RSD)为 1.03%。此外,在相同条件下,用不同批制备的修饰电极分别对上述所用溶液进行平行测定(图 8(E)),其相对标准偏差(RSD)为 1.52%,结果表明该修饰材料的电化学分析法具有可接受的再现性。为了研究 FTO-PANI-Pt/Fe2O3电化学传感器的稳定性,将合成的复合材料 Pt/Fe2O3和 PANI 放置在 4 ℃ 的冰箱中保存一段时间后,再用同样方法制备电极,对所合成的材料的稳定性进行探究。根据不同储存天数下催化性能的变化来鉴别该传感器的稳定性。取三支同一条件下合成的复合电极 FTO-PANI-Pt/Fe2O3,在对应天数同一时刻对 1.2 mg/mL H2O2进行测试,其结果图 8(F)所示,30 天后计算其稳定性依然能达到初始值的 101.67%,相对标准偏差 RSD 为 0.99%,表明合成的材料具有较好的稳定性。

图8 电化学传感器的选择性(A,H2O2浓度为0.3 mg/mL,其他干扰离子浓度为0.75 mg/mL);电化学传感器的重现性(B,H2O2浓度为1.2 mg/mL);电化学传感器的稳定性(C,10 mV/s 扫描速率循环 15 次CV);
2.5 实际样品检测
为了研究 FTO-PANI-Pt/Fe2O3传感器的实际应用,使用标准加入法对牛奶、湖水样品中的 H2O2进行CV 检测。检测结果列于表2。用于牛奶样品检测的回收率为 89.3%~102.8%,相对标准偏差(RSD)小于 2.4%;对湖水样品的加标回收率为 101.2%~109.7%,多次检测结果的 RSD 小于 3.7%。结果表明,所制备的 FTO-PANI-Pt/Fe2O3传感器适用于检测真实水样和牛奶中的 H2O2。

表2 传感器对实际样品中H2O2测定的回收率
3 结 论
本文首次制备了一体化诱导成型所构建的双金属复合物修饰聚苯胺电极,以此作为工作电极构建了新型电化学传感器,用于快速、灵敏的H2O2检测。实验证明优异的灵敏度源于Pt/Fe2O3修饰的聚苯胺电极可以给电极和电解质之间提供一个良好的电子通路,从而加速电化学反应过程的电子传输。更重要的是,该电极材料稳定、修饰过程简单、检测响应快,实现了快速测定H2O2。本研究不仅开发了一个性能优异的电化学传感H2O2的电极材料制备方法,还为贵金属及金属氧化物材料电化学领域的应用提供了新的方法。
