土壤中砷和硒生物有效态的联合提取
2023-07-13吴梅赵家宇刘怡田兴磊倪润祥刘永林
吴梅,赵家宇,刘怡,田兴磊,倪润祥,刘永林*
(1.重庆师范大学GIS应用研究重点实验室,重庆 401331;2.重庆师范大学地理与旅游学院,重庆 401331;3.山东省地质科学研究院,济南 250013;4.农业农村部农业生态与资源保护总站,北京 100125)
硒(Se)是人与动物生长发育所必需的微量元素,其摄入过少或过量均会危害健康[1]。砷(As)是被国际癌症研究机构划分为一类致癌物的类重金属[2-4]。人体主要通过食物链摄取硒和砷,而农作物是食物链的重要组成部分[1,5-6]。农作物中硒和砷的含量既受到土壤中硒和砷总量影响,更受到土壤中硒和砷的生物有效性的制约[7-8]。有研究表明,硒与砷的化学性质近似,且土壤中硒与砷的伴生关系明显[9]。植物中硒与砷之间存在拮抗作用,即硒能缓解砷对植物的毒害作用[10]。目前,农作物中硒与砷的交互和拮抗作用已被广泛关注[10-12]。若能同时提取土壤中生物有效态硒与砷,将对进一步研究土壤中硒与砷的迁移转化、交互关系以及对植物中硒和砷含量的交互影响具有重要价值。除此之外,联合提取实验可以减少实验步骤,节约时间与物质成本,具有较好的实际意义。
目前,关于联合消煮测定土壤中砷、硒全量的研究较多[13-15],但对联合提取测定土壤中生物有效态砷与硒的研究较少。在前人研究工作中,提取土壤生物有效态硒时多采用K2HPO4、KH2PO4、KH2PO4-K2HPO4和NaHCO3等作为浸提剂[16-17];提取土壤生物有效态砷时多采用NaHCO3、HCl 和NaH2PO4作为浸提剂[7,18-19]。但以上浸提剂均为分开提取土壤生物有效态硒与砷,以致实验步骤多,效率较低。因此,需找到一种化学浸提剂,用以联合提取土壤中生物有效态硒和砷,以提高实验效率。前人研究表明,硒与砷在化学性质上具有相似的原子数和电子层数,常以含氧酸根形式存在[20]。因此,理论上可以找到一种化学浸提剂将土壤中生物有效态硒与砷同时提取。
在土壤生物有效态硒的常用浸提剂中,NaHCO3和K2HPO4的水溶液呈碱性,KH2PO4的水溶液呈酸性。前人研究表明,这3 种浸提剂不仅能提取土壤水溶态硒和可交换态硒(这两种形态硒合称生物有效态硒),还能提取其他形态硒,如酸性的KH2PO4提取剂也可将土壤中少量的碳酸盐结合态硒提取出来。KH2PO4-K2HPO4缓冲溶液呈中性,可以有效提取土壤中有效态硒,同时也可避免对其他形态硒的提取[16],因此,使用KH2PO4-K2HPO4缓冲溶液提取土壤中的生物有效态硒效果最好[21-23]。张传琦等[24]、张克斌等[25]认为,0.1 mol·L-1稀HCl 对土壤生物有效态砷的提取效果较好。黄瑞卿等[18]对比研究了0.1 mol·L-1HCl、0.5 mol·L-1NaH2PO4和0.5 mol·L-1NaHCO3提取土壤生物有效态砷,结果显示3 种浸提剂都能较好地提取土壤中的生物有效态砷。肖玲等[26]认为,0.5 mol·L-1NaHCO3是提取土壤生物有效态砷最适宜的浸提剂。基于此,本研究将综合对比0.5 mol·L-1NaHCO3、0.5 mol·L-1KH2PO4、0.1 mol·L-1HCl 和0.1 mol·L-1KH2PO4-K2HPO44 种化学浸提剂对土壤中生物有效态硒与砷的联合提取实验效果,旨在达到以下研究目的:①阐述4 种化学浸提剂所提取的土壤生物有效态硒和砷与土壤总硒和总砷的相互关系;②用植物指示法验证4种浸提剂联合提取土壤生物有效态硒与砷的实验效果,以确定最佳浸提剂。
1 材料与方法
1.1 实验仪器
万分之一分析天平:BSA124S-CW 型[赛多利斯科学仪器(北京)有限公司];调速多用振荡器:HY-4型(常州天瑞仪器有限公司);电动离心机:LD-5 型(金坛区西城新瑞仪器有限公司);电热板:DS24-45F型(莱玻特瑞科技有限公司);氢化物发生原子荧光光度计(HG-AFS):AFS-9700 型(北京海光仪器有限公司);硒与砷空阴极灯:HAF-2 型(北京海光仪器有限公司)。
1.2 实验试剂
实 验 所 需 试 剂:NaHCO3、HCl、HNO3、HClO4、KH2PO4、K2HPO4、硫脲、抗坏血酸和氢氧化钠均为优级纯,硼氢化钠为分析纯,以上样品均购买于重庆川东化工有限公司;砷标准溶液(GNM-SAS-002-2013)和硒标准溶液(GNM-SSE-003-2013)采购自国家有色金属及电子材料分析测试中心。实验所需混合溶液:HNO3和HClO4混合溶液,HNO3∶HClO4(体积比)=5∶1;硫脲+抗坏血酸溶液,2.5 g硫脲和2.5 g抗坏血酸溶于100 mL超纯水;1µg·mL-1砷和硒的标准储备液,用1 mol·L-1HCl 将10µg·mL-1砷、硒标准溶液稀释至1 µg·mL-1;还原剂(现配现用),2.5 g 氢氧化钠和7 g硼氢化钠溶于500 mL超纯水。
1.3 实验样品处理与测试
1.3.1 土壤与玉米样品采集和前处理
随机采集成土母岩和土壤类型相同的9 件玉米根系土壤,并采集对应成熟的玉米根和玉米籽。土壤样品在室内自然风干后剔除其中的瓦块、碎石、植物根系,过2 mm 孔径的尼龙筛(10 目),采用四分法取10目土样,用玛瑙研钵充分研磨后过0.15 mm 孔径的尼龙筛(100 目),保存在塑料瓶中,待测。玉米籽与玉米根的处理参考《土地质量地球化学评价规范》(DZ/T 0295—2016)进行。将采集的玉米根与土壤剥离,玉米脱粒后保留玉米籽,用超纯水将玉米根和玉米籽反复清洗干净后按编号顺序放置在实验台面上,将剪成0.5~1.0 cm 的玉米根系和玉米籽一起放置在85~90 ℃烘箱中烘烤1 h,再在70 ℃条件下烘干至质量恒定。用不锈钢粉碎机将其粉碎后过60 目尼龙筛,保存在塑料瓶中,待测。
1.3.2 土壤生物有效态硒与砷的提取过程
4 种浸提剂提取土壤生物有效态硒与砷的详细步骤见表1。其中0.1 mol·L-1KH2PO4-K2HPO4提取时振荡和离心分两次进行,第一次振荡240 min 后离心10 min,将上清液倒入聚乙烯瓶中。在离心管剩余样品中加入10 mL 超纯水继续振荡240 min 后离心10 min,将上清液倒入聚乙烯瓶中与上一步的0.1 mol·L-1KH2PO4-K2HPO4溶液混合均匀。

表1 4种提取剂分别提取土壤生物有效态砷与硒的步骤[13-14]Table 1 Steps of extracting bioavailable arsenic and bioavailable selenium with four extractants respectively in soils[13-14]
提取液中砷和硒的测试步骤:①分别取5 mL 4种提取剂所得浸提液至100 mL 烧杯,加入2 mL HNO3和HClO4混合溶液,在180 ℃的电热板上消煮至冒出大量浓白烟,取下,冷却至室温;②加入2 mL 6 mol·L-1HCl,继续消煮至冒出大量浓白烟,取下,冷却至室温。③用超纯水少量多次冲洗烧杯内壁和表面皿内侧,将所得溶液转移至20 mL试管,加入1 mL 12 mol·L-1HCl,定容,摇匀,上机测定提取液中硒浓度。④准确吸取测定硒浓度后的消解溶液3 mL,加入2 mL 硫脲+抗坏血酸和HCl混合液(硫脲+抗坏血酸和HCl的体积比为1∶1),定容至15 mL,静置40 min,测定提取液中砷浓度。称取0.5 g 左右玉米籽和玉米根测定其总硒和总砷,称取0.1 g 土壤样品,测定其总硒和总砷,具体消煮和测定方法见文献[27]。
1.3.3 硒、砷标准溶液配制和标准曲线标定
分别取0.5 mL 1 µg·mL-1的硒或砷标准储备液,加入5 mL 12 mol·L-1HCl,定容至50 mL,摇匀,此时标准液中硒、砷的浓度为10µg·L-1。以5%(体积比)的HCl溶液为载流,氢氧化钠和硼氢化钠混合溶液为还原剂。待仪器稳定后用标准曲线测量法测定样品中硒、砷含量。
1.3.4 实验质量控制与检出限
实验过程中所用烧杯、试管等均在20%HNO3中浸泡超过24 h。土壤总硒和总砷测定中使用两组土壤标准物质(GBW07404a 和GBW07406a)控制;土壤生物有效态硒与砷测定中使用两组平行样品以确保实验操作可靠。玉米标准物质(GBW10012)用于控制玉米根和玉米籽中总硒和总砷的实验质量。实验中所有标准物质的硒、砷的测定含量相对标准偏差均小于10%。硒标准曲线:c=0.012IF+0.023,r=0.999 9(c为浓度,IF为荧光强度);砷标准曲线:c=0.039IF+0.129,r=0.999 4。硒和砷的检测限分别为0.01µg·L-1和0.05 µg·L-1。土壤总砷、总硒与玉米根和玉米籽砷、硒的加标回收率均在93%~106%之间。
1.4 仪器工作条件
实验仪器工作参数:振荡器250 r·min-1,离心机4 000 r·min-1,电热板180 ℃。HG-AFS 工作条件见表2。
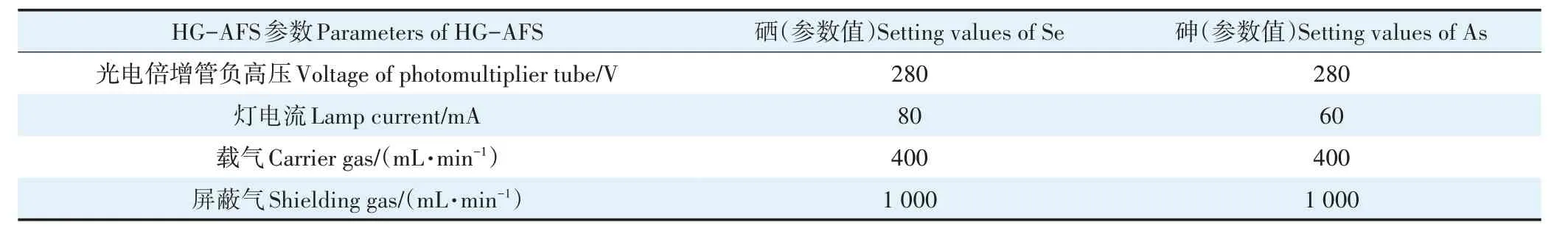
表2 仪器工作条件Table 2 Instrument operating conditions
2 结果与讨论
2.1 土壤生物有效态砷含量
Kruskal-Wallis 非参数检验结果显示,4 种提取剂所提取的土壤中生物有效态砷含量具有显著差异(P<0.05)。0.5 mol·L-1NaHCO3、0.5 mol·L-1KH2PO4、0.1 mol·L-1HCl和0.1 mol·L-1KH2PO4-K2HPO4提取的土壤生物有效态砷含量均值分别为0.119、0.478、0.548 mg·kg-1和0.343 mg·kg-1(表3)。0.5 mol·L-1KH2PO4和0.1 mol·L-1HCl 提取的土壤生物有效态砷含量与土壤总砷含量无显著相关性。0.5 mol·L-1NaHCO3(r=0.794,P<0.01)和0.1 mol·L-1KH2PO4-K2HPO4(r=0.788,P<0.01)提取的土壤生物有效态砷含量与土壤总砷含量均呈显著正相关。

表3 4种提取剂分别提取的土壤生物有效态砷含量和土壤、玉米总砷含量(mg·kg-1)Table 3 Four extractants extract the bioavailable arsenic content in soil and total arsenic content in soils and corns(mg·kg-1)
4种提取剂中仅0.1 mol·L-1KH2PO4-K2HPO4所提取的土壤生物有效态砷含量与玉米籽(r=0.901 8,P<0.01)和玉米根(r=0.848 1,P<0.01)总砷呈显著正相关,其余均无显著相关性(图1)。虽然同为磷酸根的0.5 mol·L-1KH2PO4所提取土壤生物有效态砷含量高于0.1 mol·L-1KH2PO4-K2HPO4所提取的生物有效态砷含量,但其提取量与玉米籽和玉米根总砷无显著相关性,因此相对来说0.1 mol·L-1KH2PO4-K2HPO4更适用于土壤生物有效态砷的提取。
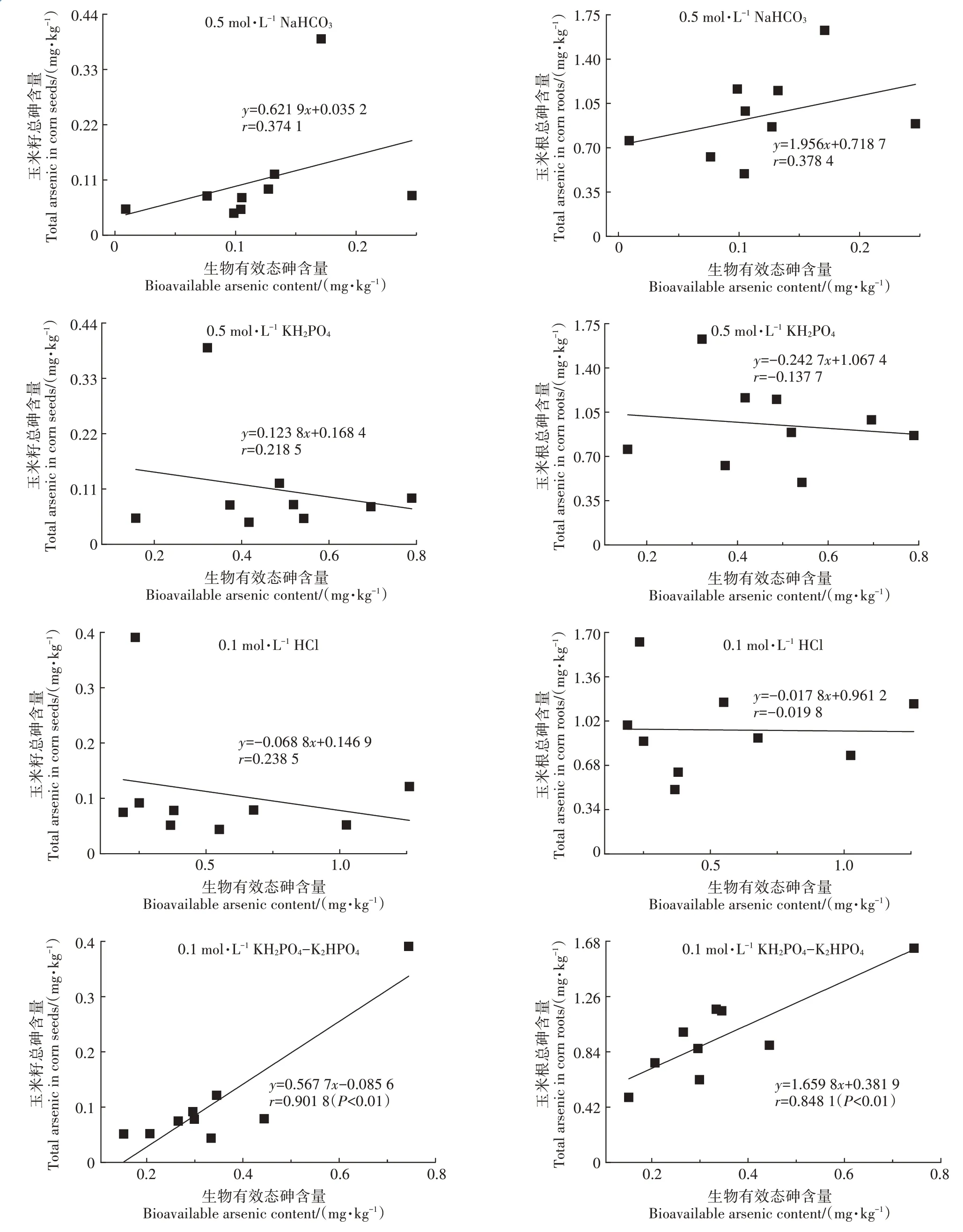
图1 4种提取剂提取的土壤生物有效态砷含量与玉米籽、玉米根中总砷含量相关性Figure 1 Correlation between bioavailable arsenic content extracted by four extractants in soils and total arsenic content in corn seeds and roots
2.2 土壤生物有效态硒含量
Kruskal-Wallis 非参数检验结果显示,4种提取剂所提取的土壤生物有效态硒含量具有显著差异(P<0.05),0.5 mol·L-1NaHCO3、0.5 mol·L-1KH2PO4、0.1 mol·L-1HCl 和0.1 mol·L-1KH2PO4-K2HPO4提取的土壤生物有效态硒含量均值分别为0.023、0.015、0.009、0.023 mg·kg-1(表4)。除0.1 mol·L-1HCl 外,0.5 mol·L-1NaHCO3(r=0.648,P<0.05)、0.5 mol·L-1KH2PO4(r=0.627,P<0.05)和0.1 mol·L-1KH2PO4-K2HPO4(r=0.707,P<0.05)提取的土壤生物有效态硒含量均与土壤总硒含量呈显著正相关。

表4 4种提取剂分别提取的土壤生物有效态硒含量和土壤、玉米总硒含量(mg·kg-1)Table 4 Four content extractants extract the bioavailable selenium and total selenium content in soils and corns(mg·kg-1)
4 种提取剂提取的土壤生物有效态硒含量与玉米籽总硒含量均无显著相关性,但与玉米根总硒含量均呈显著正相关(图2),r分别为0.818 3(P<0.01,0.5 mol · L-1NaHCO3)、0.717 5(P<0.05,0.5 mol · L-1KH2PO4)、0.731 3(P<0.05,0.1 mol·L-1HCl)、0.822 1(P<0.01,0.1 mol·L-1KH2PO4-K2HPO4)。综合来看,0.1 mol·L-1KH2PO4-K2HPO4和0.5 mol·L-1NaHCO3都能有效将土壤中的生物有效态硒提取出来,这与周菲等[28]和周越等[29]的研究结果一致。
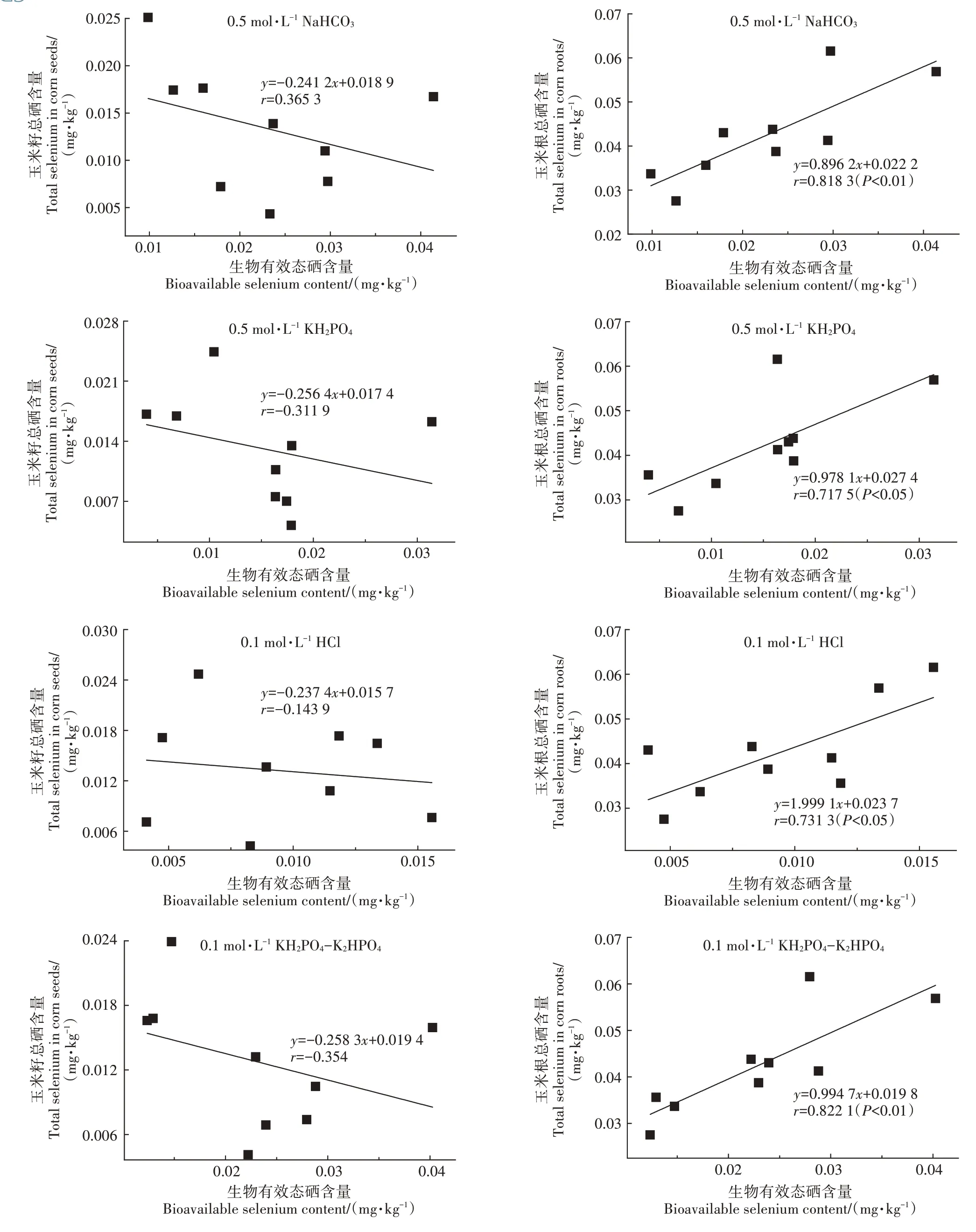
图2 4种提取剂提取土壤生物有效态硒含量与玉米籽、玉米根总硒含量相关性Figure 2 Correlation between bioavailable selenium content extracted by four extractants in soils and total selenium content in corn seeds and roots
2.3 0.1 mol·L-1 KH2PO4-K2HPO4对土壤生物有效态砷与硒的联合提取
4种提取剂中0.1 mol·L-1KH2PO4-K2HPO4提取土壤生物有效态砷的效果最佳(表3和图1)。原因是磷与砷的电子排布相似,且均形成三元酸,但磷酸根半径较砷酸根和亚砷酸根小,具有更强的电荷密度,因此,磷酸根易将吸附在土壤颗粒表面的砷替换下来[30-31]。在化学性质上,磷酸盐与砷酸盐也具有许多相似性,磷酸盐缓冲溶液不仅可以提取土壤吸附的砷,而且对于部分存在于土壤颗粒晶格中的砷也可提取,从而增加了提取量[32-33]。通气性良好的土壤中,砷主要以砷酸根和亚砷酸根形态存在,它和磷酸根有很大的相似性。在大多数自然土壤中,As(Ⅴ)可以被氧化铁、氧化铝和氧化钙吸附固定,与As(Ⅴ)相似,磷酸盐在土壤中也会被上述物质强烈地吸附固定[34]。Alam 等[35]比较了磷酸钾、硫酸钾、氯化钾、硝酸钾和高氯酸钾对土壤砷的提取率,发现磷酸钾的提取率比其他几种盐的提取率高得多,土壤对磷酸根的吸附选择性高于砷酸根,因此,磷酸根可以有效地将土壤吸持的砷酸根和亚砷酸根提取出来。
0.1 mol·L-1KH2PO4-K2HPO4和0.5 mol·L-1NaHCO3提取土壤中生物有效态硒的效果均较好(表4 和图2),但由于0.5 mol·L-1NaHCO3对土壤生物有效态砷的提取效果较差,因此0.1 mol·L-1KH2PO4-K2HPO4更适合于联合提取土壤生物有效态硒与砷。0.1 mol·L-1KH2PO4-K2HPO4可以提取土壤中的水溶态、可交换态及部分有机结合态的硒[21],以上3 种赋存形态的硒是评价土壤中硒生物有效性的适宜指标[22-23]。吴少尉等[16]试验了不同提取剂对于土壤中有效态硒的提取效果,其中NaHCO3、KH2PO4、K2HPO4、KH2PO4-K2HPO4的浸提率均较高。由于NaHCO3、K2HPO4的水溶液呈碱性,KH2PO4的水溶液呈酸性,都使提取液中不仅只含有有效态硒,而使用呈中性的KH2PO4-K2HPO4缓冲溶液提取可避免对其他形态硒的提取[36]。
硒与砷具有相似的原子数和电子层数,在化学结构上相似,常以含氧酸根形式存在[9,20]。0.1 mol·L-1KH2PO4-K2HPO4提取土壤生物有效态硒与砷的原理是阴离子交换作用,磷酸根能将土壤中被其他化合物,例如氧化铁、氧化铝所吸附的砷酸根、亚砷酸根、硒酸根、亚硒酸根提取出来[16,18]。因此,从化学理论和实验结果均可得出,0.1 mol·L-1KH2PO4-K2HPO4可作为土壤中生物有效态硒与砷联合提取的浸提剂,此浸提剂即可简化实验操作步骤、节约化学试剂,也对综合评价土壤中砷与硒的生物有效性具有重要意义。
3 结论
(1)4 种提取剂中仅0.1 mol·L-1KH2PO4-K2HPO4
提取的土壤生物有效态砷与土壤总砷(r=0.788,P<0.01)、玉米籽砷(r=0.902,P<0.01)和玉米根砷(r=0.848,P<0.01)呈 显 著 正 相 关,因 此0.1 mol·L-1KH2PO4-K2HPO4对土壤生物有效态砷提取效果最好。
(2)4 种提取剂中0.1 mol·L-1KH2PO4-K2HPO4和0.5 mol·L-1NaHCO3提取的生物有效态硒含量与土壤总硒(r=0.707,P<0.05;r=0.648,P<0.05)、玉米根硒(r=0.822,P<0.01;r=0.818,P<0.01)呈显著正相关,但0.5 mol·L-1NaHCO3对土壤生物有效态砷的提取效果较差。
(3)本研究建立了土壤中生物有效态砷与硒联合提取的实验方法——0.1 mol·L-1KH2PO4-K2HPO4联合提取法。