纳米碳溶胶配施尿素对土壤N2O排放的影响
2023-07-13纪程孙玉香孟圆徐聪汪吉东张永春
纪程,孙玉香,孟圆,徐聪,汪吉东,3*,张永春,3
(1.江苏省农业科学院农业资源与环境研究所,南京 210014;2.江苏大学环境与安全工程学院,江苏 镇江 212013;3.南京农业大学,南京 210095)
氧化亚氮(N2O)是大气中重要的温室气体之一,大气中N2O 浓度的空前升高是全球气候变化的重要驱动因素[1]。当前大气中N2O 体积分数已达到3.32×10-7,与1750 年工业革命前相比,增长率达23%[2]。农业、工业、生物质燃烧以及活性氮淋溶和大气沉降的间接排放是N2O 的主要人为排放源[3]。其中,农业土壤N2O 排放占重要地位,氮肥的广泛使用推动了土壤N2O 排放量的增长。据估算,农业源排放的N2O 可占全球人为排放的60%~70%[4]。
国内外科研工作者一直致力于探索如何通过农田氮管理实现土壤N2O 减排。一方面通过优化氮肥管理实现N2O减排[5-6],另一方面通过提高氮肥利用率减少气态氮(N2O和NO等)损失[7-8]。近年来纳米碳材料在改良土壤、提高肥料利用率以及节肥增产上表现出较好效果[9-11]。纳米材料配施氮肥可以发挥其表面效应和小尺寸效应,既能够增强肥料的吸附性能,减少肥料的流失,又可以改善土壤理化性质,尤其是在碱性土壤pH和养分的改良方面[12-13]。学者们也逐渐关注到纳米碳材料对土壤N2O排放的影响。研究发现,纳米碳可以通过吸附土壤中的铵态氮而降低N2O排放[14]。然而,也有研究表明添加纳米碳能够提高土壤N2O排放,可能的原因是纳米碳促进了土壤微生物活性[15]。这些有关纳米碳材料对N2O排放影响相互矛盾的结果可能与纳米碳和土壤之间复杂的相互作用有关。
土壤硝化和反硝化作用是产生N2O 的关键过程,施加纳米碳材料既可以影响土壤硝化过程,也可以影响反硝化过程。我们推测施加纳米碳材料条件下土壤N2O 的排放取决于其对硝化和反硝化过程的净效应。因此,检测纳米碳材料作用下土壤硝化和反硝化潜势的变化有助于揭示纳米碳材料对N2O 排放的影响。本文选用纳米碳溶胶为供试材料,研究其对两种处理土壤N2O 排放的影响,以期为纳米碳溶胶的推广应用以及减少农业源N2O排放提供理论基础。
1 材料与方法
1.1 试验材料
纳米碳溶胶采用通电电解双石墨电极板制成,由沈阳美华农业有限公司提供,纳米碳粒子粒径为10~100 nm。供试土壤采集于江苏省滨海界牌镇的小麦-玉米轮作种植区(33°43'N,119°37'E),该地区处于暖温带和亚热带季风气候的过渡地带,年平均气温和降水量分别为14.1 ℃和942.6 mm,土壤类型为黄河冲积物发育而来的潮土。秸秆还田是改善该地区农田土壤质量的重要措施之一,且已在该种植区大面积推广。目前已实行麦玉双季秸秆还田2 a,获取上一季作物的全量秸秆后,将秸秆机械粉碎至5~10 cm,再用旋耕机旋入土壤耕层(0~20 cm)。每年小麦秸秆的还田量约为5 000 kg∙hm−2,玉米秸秆的还田量约为6 000 kg∙hm−2。同时设置秸秆离田处理,该田块收获的秸秆不还田。本试验土壤样品采集于秸秆还田和秸秆离田田块。根据S 点法布点,每个田块采集5 份耕层土壤(0~20 cm),土样混匀后带回实验室,自然风干后过2 mm 筛,去除可见的根和有机残留物。取部分风干土样测定土壤基本理化性质,其余风干土样用于开展培养实验。初始土壤性质及纳米碳溶胶的性质详见表1。
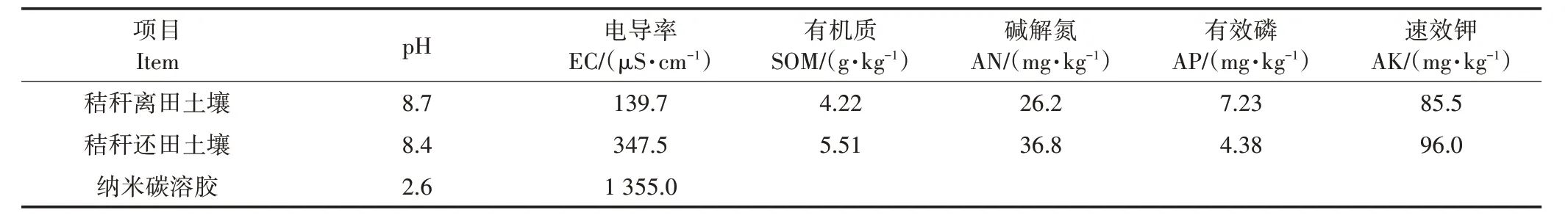
表1 供试土壤及纳米碳溶胶的基本理化性质Table 1 Basic physico-chemical properties of soils used in the study
1.2 培养实验设计
称取80 g 土样(按干土计)置于250 mL 培养瓶,用去离子水调节土壤水分至50% 最大持水量(WHC),在25 ℃黑暗条件下预培养一周,以恢复土壤微生物活性。秸秆离田和秸秆还田土壤均设置4 个处理,分别是:①不施尿素和纳米碳溶胶的对照(CK);②单施纳米碳溶胶(C);③单施尿素(N);④混施尿素和纳米碳溶胶(NC)。每个处理设置3次重复。尿素(以N计)施用量为每千克土200 mg,纳米碳溶胶施用量为2%(干土质量)。正式培养时,用去离子水将土壤水分调节至80%WHC,此时为兼性厌氧环境,土壤硝化和反硝化反应均可发生,具有最大的N2O 净排放潜力[16-18],每隔2 d 通过称重法用去离子水补充培养瓶内损失的水分。所有培养瓶(4个处理×2种土壤类型×5 个时间点×3 个重复=120 个培养瓶)采用完全随机区组排列,于25 ℃黑暗环境中培养21 d。此外,在正式培养开始的第1、3、8、15、21 天破坏性采集土壤,用于测定土壤理化性质和硝化、反硝化潜势。
1.3 气体与土壤样品分析
正式培养前8 d 每天收集和分析气体一次,之后的第9天到第21天取气频率为每隔3 d一次。每次采气前去掉保鲜膜用吹风机通空气5 min,之后用橡胶塞密封培养瓶,使用注射器采集瓶内气体作为N2O 的初始浓度。密封培养瓶2 h后再次采集瓶内气体。气体中的N2O 浓度利用配有电子捕获检测器(ECD)的安捷伦7890A(Agilent 7890A,美国)气相色谱仪测定,载气为含95%氩气和5%甲烷的混合气。N2O 排放通量由密封前后2 h 内累积的气体浓度计算,具体公式为:
其中:F是指N2O 排放通量,µg·kg-1·h-1;ρ是指在标准温度和压力下N2O 的密度,kg·m-3;V是指锥形瓶的容积,m3;W是指培养所用土壤的干质量,kg;ΔC/Δt是指在给定时间(2 h)内密封锥形瓶后N2O 浓度的变化,10-9h-1;T是指锥形瓶内的温度,℃。
利用密封2 h 前后的N2O 浓度计算得到的N2O 排放量代表采样当天的N2O 日平均排放量。根据每两个相邻采样日的排放通量,按顺序累积计算得到培养期内N2O排放总量。
利用紫外分光光度计(HITACHI,UV-2900,Tokyo,日本)测定土壤硝态氮和铵态氮含量,分别利用双波长紫外分光光度法和靛酚蓝法。采用复合玻璃电极仪(PHS-3C mv/pH detector,Shang-hai,中国)测定土壤pH 值,测定时的土水比为1∶5。土壤可溶解性有机碳(DOC)含量由TOC 分析仪(TOC Vcph,Shimadzu,Kyoto,日本)测定。土壤硝化潜势利用氯酸盐抑制法测定[19],具体步骤:称取5 g 鲜土于100 mL 培养瓶,向瓶中加入含20 mL 1 mmol·L-1硫酸铵[(NH4)2SO4]的磷酸盐缓冲液(NaCl 8.0 g·L-1,KCl 0.2 g·L-1、Na2HPO40.2 g·L-1、NaH2PO40.2 g·L-1,pH 7.4),并加入5 mL 10 mmol·L-1氯酸钾(KClO3)溶液抑制亚硝酸盐的氧化;将培养瓶放入恒温(25 ℃)振荡培养箱中遮光培养24 h,然后加入5 mL 2 mol·L-1氯化钾(KCl)溶液浸提亚硝态氮(NO-2-N);NO-2-N 含量用紫外分光光度计在540 nm 波长下测定,显色剂为N-(1-萘基)-乙二胺;硝化潜势根据单位时间内单位土壤样品增加的NO-2-N 含量计算。土壤反硝化潜势利用乙炔抑制方法测定[20],具体步骤:称取5 g 鲜土于250 mL 培养瓶,向瓶中加入25 mL 溶液[1 mmol·L-1葡萄糖和1 mmol·L-1硝酸钾(KNO3)],斡旋混匀,盖上橡胶塞,用真空泵抽真空后充入高纯氮气,反复抽洗3 次,再用乙炔将瓶内10%的氮气置换,并使瓶内外气压一致;将培养瓶放入恒温(25 ℃)培养箱中培养3 h,3 h 后用注射器采集瓶内气体;利用气相色谱仪分析气体样品中N2O 浓度,土壤反硝化潜势根据单位时间内N2O 的产生量计算。
1.4 数据统计分析
所有数据基于烘干土质量计算。利用配对分析T检验分析两种土壤各处理间理化性质、硝化和反硝化潜势的显著性差异。利用双因素方差分析检验纳米碳溶胶与尿素施用对两种处理土壤N2O 排放量的影响(LSD 检验,P<0.05)。本研究中所有数据结果以平均值加减标准误差(Mean±SE)表示,n=3。所有数据处理与分析使用SPSS 20.0软件进行。
2 结果与分析
2.1 尿素与纳米碳溶胶作用下的土壤理化性质
秸秆还田显著改变了土壤理化性质,主要表现为秸秆还田显著提高了土壤电导率、有机质和碱解氮含量,同时显著降低了土壤pH(P<0.05)。
施加尿素短期内显著增加了土壤NH+4-N 含量,秸秆离田和秸秆还田土壤的NH+4-N 含量均在培养的第3 天最高,之后持续下降,到第14 天左右下降到较低水平(图1a和图1c)。施加尿素后土壤的NO-3-N 含量在整个培养期内呈上升趋势(图1b和图1d)。配对T检验结果表明(表2),施加纳米碳溶胶显著增加了施氮条件下秸秆离田土壤的NH+4-N 含量,而显著降低了秸秆还田土壤的NH+4-N 含量。同时,施加纳米碳溶胶显著降低了施氮条件下秸秆离田土壤的含量,显著提高了秸秆还田土壤的含量(P<0.05)。如图2a 和图2c 所示,培养期内土壤pH 呈现下降趋势。施加尿素处理的土壤pH 在培养初期增加。同时,施加纳米碳溶胶显著降低了秸秆还田土壤的pH(P<0.05,表2)。如图2b和图2d所示,施加尿素显著增加了两种土壤的DOC 含量,施加纳米碳溶胶显著增加了秸秆还田土壤第3天的DOC含量,但对第21天的DOC含量无显著影响。
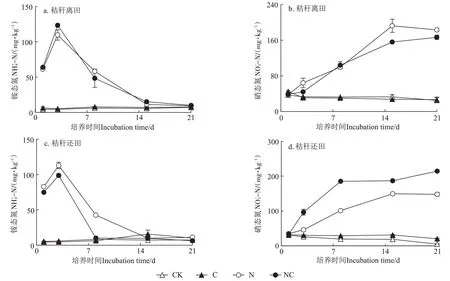
图1 秸秆离田和秸秆还田土壤铵态氮和硝态氮含量的动态变化Figure 1 Dynamic variations ofandcontents from the straw-removal and straw-return soils

图2 秸秆离田和秸秆还田土壤pH和可溶性有机碳含量的动态变化Figure 2 Dynamic variations of pH and DOC contents from the straw-removal and straw-return soils
2.2 尿素与纳米碳溶胶作用下的土壤N2O排放
如图3 所示,尿素施用下秸秆离田与秸秆还田土壤的N2O 排放速率均在第一周内迅速升高,直至出现峰值后下降,然后趋于平稳。纳米碳溶胶和尿素对土壤N2O 排放具有显著的交互作用(P<0.05),且对不同处理土壤的影响结果不同。与CK 相比,单施纳米碳溶胶对土壤N2O 排放无显著影响。施氮条件下,添加纳米碳溶胶显著增加了秸秆离田土壤的N2O 排放,而显著降低了秸秆还田土壤的N2O 排放,减排效率达63%(P<0.05,图3d)。

图3 秸秆离田和秸秆还田土壤N2O排放通量和累积排放量Figure 3 Dynamic variations of N2O fluxes and cumulative N2O emissions from the straw-removal and straw-return soils
2.3 尿素与纳米碳溶胶作用下的土壤硝化和反硝化潜势
本研究中,纳米碳溶胶显著提高了施氮条件下秸秆离田土壤和秸秆还田土壤的硝化潜势(P<0.05,表2),比例提高16%和25%(图4a)。然而,两种土壤的反硝化潜势对纳米碳溶胶的响应不同,施氮条件下添加纳米碳溶胶显著降低了秸秆还田土壤的反硝化潜势,但秸秆离田土壤的反硝化潜势对纳米碳溶胶无显著响应(图4b)。

图4 秸秆离田和秸秆还田土壤的硝化潜势和反硝化潜势Figure 4 Rates of the potential nitrification and denitrification from the straw-removal and straw-return soils
3 讨论
3.1 纳米碳溶胶对土壤理化性质的影响
纳米碳材料对土壤养分具有一定的固持或活化作用[21]。本研究中,施用纳米碳溶胶能够显著增加秸秆离田土壤含量和秸秆还田土壤的含量,显著降低秸秆离田土壤的和秸秆还田土壤的含量,表明纳米碳溶胶可以活化和固持土壤中的无机氮。纳米碳溶胶作为一种高C/N 的碳源,可以同时对微生物的同化作用和矿化作用产生刺激,因此,纳米碳溶胶引起土壤氮素的变化取决于两种作用的净效应。研究发现,施用纳米碳溶胶能够降低碱性土壤的pH[13],这可能与纳米碳的特殊性能——外包膜带有的负电荷以及本身的笼形芳香结构有关[22]。在本研究中,施加纳米碳溶胶显著降低了秸秆还田土壤的pH,但秸秆离田土壤的pH 对纳米碳溶胶无显著响应。培养第3 天时,在施用尿素基础上添加纳米碳溶胶显著提高了秸秆离田和秸秆还田土壤的DOC 含量,这与生物质炭对土壤DOC 含量的影响类似。外源碳投入能够提高土壤微生物活性,导致土壤有机养分被微生物快速分解[23]。同时,添加外源碳可能促进了土壤中老碳的分解,从而增加了土壤DOC含量。
3.2 纳米碳溶胶对土壤硝化和反硝化潜势及N2O 排放的影响
本研究中,在施用尿素基础上添加纳米碳溶胶显著增加了秸秆离田土壤的N2O 排放量,这可能与纳米碳施入对土壤硝化反应的促进作用有关(图4)。氨氧化过程是土壤硝化反应的关键步骤,该过程主要由氨氧化微生物驱动。一般情况下,氨氧化细菌在碱性土壤的硝化反应中占据主导地位,尤其是本研究的高铵环境[24]。原因是氨氧化古菌普遍适宜生长在含量较低且酸性环境,而氨氧化细菌更偏向于底物丰富的环境[25]。本研究中,纳米碳溶胶施加后土壤C/N 的升高可能会增加土壤氨氧化细菌数量。研究表明,氨氧化细菌与土壤C/N 具有显著正相关关系[26],土壤C/N 可以通过改变氮的相对可利用性影响氨氧化微生物丰度,从而调控硝化作用[27]。此外,纳米碳溶胶的施入提高了土壤有效碳含量,这可能会造成异养微生物和自养硝化菌之间对NH+4的竞争[28],而在氮底物充足的条件下,这种竞争关系会促进硝化反应,导致N2O 排放量升高。然而,也有研究发现,纳米碳材料可能通过吸附无机氮底物而抑制土壤硝化作用[15]。以上研究结果表明,纳米碳材料对土壤氮素转化的影响具有一定的复杂性,并且表现出土壤特异性。
尽管施用纳米碳溶胶显著提高了秸秆还田土壤的硝化潜势,但其显著降低了施氮条件下该土壤的N2O 排放,表明纳米碳溶胶对土壤硝化反应的促进作用不是其减排N2O 的原因。我们推测纳米碳溶胶对秸秆还田土壤反硝化过程的抑制作用是其减少N2O排放的原因之一。相比于秸秆离田土壤,秸秆还田土壤的有机碳含量较高,土壤中异养微生物活性较高,土壤有效碳含量的提高将促进微生物对无机氮的同化作用[29-30]。因此,施加纳米碳溶胶可能通过激发秸秆还田土壤异养微生物对底物无机氮的同化而降低土壤反硝化速率。此外,纳米碳的输入还可能通过促进土壤彻底反硝化过程而降低N2O 排放。研究表明,土壤碳含量能够改变反硝化过程还原剂和氧化剂的相对有效性,反之也会影响反硝化的最终产物,即NO、N2O 和N2[31-32]。外源碳输入通过刺激微生物代谢,增加对O2的消耗,进而为彻底反硝化创造有利条件[33]。此外,碳底物组分的复杂性也会显著影响土壤反硝化作用及其N2O 产物[34]。本研究中,纳米碳溶胶对两种处理土壤N2O 排放影响的不一致性可能与土壤本底碳含量有关。此外,该条件下有机碳组分与N2O排放的耦联效应需进一步探究。
4 结论
纳米碳溶胶对土壤N2O 排放的影响与氮肥添加和土壤类型有关。氮肥施用条件下,施加纳米碳溶胶能够显著增加秸秆离田土壤的N2O 排放,而显著降低秸秆还田土壤的N2O 排放。因此,将施加纳米碳溶胶作为调控土壤氮素水平的措施时,应考虑到其增加N2O排放的可能性。