基于滤纸片上浮法探究pH和底物浓度对H2O2酶促反应的影响
2023-07-06董路遥王颖张志祥
董路遥 王颖 张志祥


摘要 优化教材实验“探究 pH 对H2O2酶活性的影响”,并测量了不同浓度的H2O2底物对酶促反应的影响,利用滤纸片上浮法测定酶促反应速率,简化实验步骤、放大实验现象,提高了实验成功率。结果显示:H2O2酶的最适 pH在6.0左右,pH2.0环境下其活性完全丧失,pH10.0环境下活性降低且重新置于适宜 pH 环境后可部分恢复。一定范围内,酶促反应速度与 H2O2浓度呈正比。
关键词 滤纸片上浮法酶活性 H2O2酶
中图分类号 G633.91 文献标志码 B
文件编号:1003-7586(2023)03-0070-03
“探究 pH 對 H2O2酶活性的影响”是人教版《必修1·分子与细胞》中“降低化学反应活化能的酶”的重要实验,但教材只提出使用 H2O2酶和 H2O2作为实验材料,未具体说明实验如何操作、气体如何收集等问题。浙教版教材则利用排水法收集气体,通过不同 pH 下 O2释放量来表征酶活性大小。然而,学生在实际操作中常会出现滤纸片粘贴不牢、气体收集困难、组间现象差异不明显等问题,实验成功率较低。
为使学生观测到更明显的实验现象,以人教版教材“叶圆片上浮法探究光合作用强度”实验为基础,将 H2O2酶通过吸附法固定在圆形滤纸片上,利用滤纸片上浮法探究酶促反应速率。相比于排水集气法,滤纸片上浮法将O2的生成速度转化成滤纸片上浮速度,学生通过录制视频就能实现对多组实验结果的观察记录,同时也能克服由于装置气密性、学生集气熟练度等因素带来的干扰。并且滤纸片形状固定,材质统一,可吸附的酶量相对恒定,实验的平行性较好,可重复性强。
1 材料与方法
1.1制备磷酸缓冲液和 H2O2溶液
将0.2 mol/L 磷酸二氢钠、0.2 mol/L 磷酸氢二钠和蒸馏水按一定比例配制成 pH 为2.0、4.0、5.0、6.0、7.0和10.0的磷酸缓冲液。将30%的 H2O2原液分别用蒸馏水稀释至1.5%、2%和3%。
1.2酶的提取和固定化
将200 g 马铃薯和400 mL 20 mmol/L 磷酸二氢钾置于破壁机中榨汁并过滤,滤液即为粗酶液。向含粗酶液的培养皿中投入直径为1 cm 的圆形滤纸片,浸泡1 min,然后夹起滤纸片,靠在洁净的试管壁上。
1.3酶促反应的测定
1.3.1不同pH对H2O2酶活性的影响
取5个200 mL 规格的烧杯编号1~5,分别倒入50 mL pH 为4.0~8.0的磷酸缓冲液,再倒入等量1.5% H2O2溶液。向各烧杯中轻轻放入8片含酶滤纸片并用秒表计时。观察滤纸片在烧杯内的位置变化,记录每片滤纸片从入水到出水的全部时长。
1.3.2不同浓度的H2O2对酶促反应速率的影响
取3个200 mL 烧杯编号Ⅰ~Ⅲ,分别倒入50 mL 1.5%、2%和3%的 H2O2溶液,再倒入等量 pH 为6.0的磷酸缓冲液,向各烧杯中加入8片含酶滤纸片,记录滤纸片的上浮时长。
1.3.3探究过酸或过碱对酶的影响是否可逆
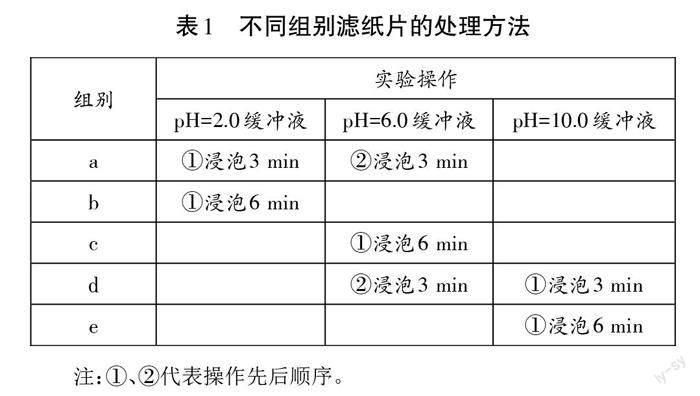
取5个200 mL 烧杯编号 A~E,向各烧杯中均加入50 mL pH 为6.0的缓冲液和50 mL H2O2溶液。将含酶的滤纸片平均分为五组(每组8片),分别编号为a~e组,如表1进行相关操作。接着,将a~e组滤纸片依次倒入 A~E 号烧杯中,记录每片滤纸片上浮时长。
1.4数据处理
用Excel计算每组滤纸片上浮的平均时间及标准差,并绘制曲线图和柱形图。
2 结果与分析
2.1不同 pH 对H2O2酶活性的影响
由表2可知,22.3 s 时,pH 6.0组的滤纸片率先上浮,其余组的第一片滤纸片也在接下来的2~4秒内上浮。在pH 4.0~8.0范围内,随着pH 上升,滤纸片上浮的时间先下降后上升,说明 H2O2酶活性先升高后下降,当pH为6.0时,滤纸片上浮时间最短,因此H2O2酶的最适pH在6.0左右。
基于实验数据,学生利用 Excel 软件绘制上浮时间-pH 曲线图(图1),在提高数据处理能力的同时,通过认别坐标图中横纵坐标含义、曲线趋势等关键图表元素增强了学生的识图分析能力和逻辑推理能力,这为深入分析pH对酶活性的影响奠定了基础。
2.2不同 H2O2浓度对反应速率的影响
当 H2O2浓度为1.5%-3%时,滤纸片上浮时间与 H2O2浓度成反比,即 H2O2浓度越高,酶促反应速度越快(图2)。这是因为当底物浓度较低时,酶分子的活性中心未被底物全部饱和,所以随着底物浓度的增加,反应速率逐渐增大。
2.3探究过酸或过碱对酶的影响是否可逆
随着实验的深入,有学生提出疑问:将过酸过碱条件下的酶重新置于最适 pH,其活性能否恢复?为进一步研究酶的作用机理,学生组建兴趣小组,增设了一组拓展实验。
表3数据显示:(1)含酶滤纸片经pH为2.0的缓冲液处理后未上浮,恢复至最适pH后也未能浮起。(2)含酶滤纸片经 pH 为10.0的缓冲液处理后仍有少量上浮,但上浮时间增加。恢复至最适pH后,滤纸片上浮数量增加,上浮时间缩短。但这些组的酶促反应速率均低于 C 组,说明 H2O2酶在pH6.0时活性最强,在pH 为2.0条件下完全失活,但在pH 为10.0条件下相对耐受,恢复至合适pH 以后,其活性可以部分恢复,此结论与葛暄等的实验一致。
天然态酶分子(N)会经过一系列相对稳定的中间态 U1、U2等,最终过渡到变性状态,中间状态时仍具部分活性,而且是可逆过程,只要除去不利因素,酶活性就可以恢复到原有状态。本实验中,当酶处于pH 为10.0的碱溶液中时,酶的空间结构发生一定程度的改变,只具有部分酶活性,但是此时仍处于相对稳定的中间态,没有达到变性态。因此将酶从 pH 为10.0的溶液中转移至pH为6.0的溶液后,酶活性有一定程度的恢复,酶促反应速度加快。而 A、B 组的酶置于 pH 为2.0的缓冲液后,酶分子越过中间态,直接到达变性态,完全失活,即使重新置于最适pH 中,酶活性也不能恢复。
3 实验反思
3.1优化滤纸片处理,拍摄视频回看计时
滤纸片上浮法相比排水集气法操作更简单,现象更直观。但由于滤纸片上浮速度较快,计时可能出现误差;不同组别先后处理产生的时间差也可能使土豆片久置,导致初始酶活性产生变化。因此可将所有滤纸片分别处理后分组晾挂在试管外壁上,实验开始时,将所有晾有滤纸片的试管同时浸入 H2O2溶液中,利用相机拍摄滤纸片从杯底上浮至液面的全过程,实验结束后回看视频对各组进行分别计时(图3)。视频计时保证了计时的准确性和初始酶活性的一致性,也为教师的课堂教学提供了宝贵的实录素材。
3.2合理确定固定化时间
固定化时间对酶活性的作用具有两重性。延长固定化时间能增加H2O2酶的固定效果,使酶更充分的吸附在滤纸片上。然而,固定化时间过长,土豆匀浆中 H2O2酶被微生物分解,活性则会大大降低。因此,控制合理的固定化时间对于提高酶的吸附效率具有重要意义。土豆中的多酚氧化酶会引起多酚类物质的逐渐氧化,使匀浆出现褐变现象,随固定时间的延长,褐色逐渐加深。因此在实际操作中,可根据土豆匀浆的颜色来确定何时终止固定过程。当土豆匀浆颜色变为浅红棕色时,固定化效果最好。
3.3自主学习合作探究
实验过程中,教师引导学生围绕学习目标展开由浅入深,由表及里的探究活动,实现自主学习和合作探究的高度统一。预习时学生提问:为何将滤纸片浸泡在酶液中?教师可引导学生查阅选修中的固定化技术及相关资料对固定化方法进行自主预习;实验后学生提问:过酸过碱条件下酶活性是否可逆?教师可引导学生自行设计实验方案,合作开展探究,同时鼓励学生自学Excel等软件,小组互助对实验数据展开分析和解读。由于课堂时间限制,学生只测量了 H2O2浓度为1%、2%和3%时的酶促反应速度,具体的饱和底物浓度可由兴趣小组在课后进行深入探索。总之,学生在课堂上出现的任何问题都可以成为课堂生成的资源,真正体现了以学定教,动态生成的教学理念。
参考文献:
[1]王桔红,谢莉,万紫微,魏梓欣.“比较过氧化氢在不同条件下的分解”实验材料探索与改进[J].中学生物教学,2019(24):62-63.
[2]徐彤.滤纸圆片在提升学生 STEM 素養中的应用——以“不同pH对酶活性的影响”实验设计教学为例[J].中学生物教学,2019(17):35-38.
[3]陈加敏.酶浓度和底物浓度对酶活性影响因素的教学探讨[J].生物学教学,2020,45(09):78-80.
[4]葛暄,徐海丽.探究pH对过氧化氢酶活性恢复的影响[J].安徽教育科研,2019(06):98-100.
