艾司氯胺酮与右美托咪定和七氟烷复合麻醉用于中小手术的可行性
2023-06-28任羽佳冯伟王培周霞
任羽佳 冯伟 王培 周霞

[摘要] 目的 探讨艾司氯胺酮与右美托咪定和七氟烷复合用药行无阿片麻醉(OFA)用于中小手术的可行性。
方法 选取行中小型手术病人60例,随机分为OFA组和传统阿片类药物麻醉组(OA组),每组30例。主要观察指标:入室时(T0)、插管前3 min(T1)、插管后3 min(T2)、切皮时(T3)、切皮后5 min(T4)、切皮后10 min(T5)、切皮后15 min(T6)、气管拔管时(T7)、清醒时(T8)的平均动脉压(MAP)和心率(HR)。次要观察指标:病人术后视觉模拟评分法(VAS)评分及术后24 h内氟比洛芬酯使用情况,术中血管活性药物使用情况,气管拔管、麻醉清醒、麻醉后监护治疗室(PACU)停留的时间,术后不良反应发生率,术中脑电双频指数(BIS)。
结果 OFA组的MAP和HR在T2~T6时高于OA组,T7、T8时低于OA组(F=5.146~44.145,P<0.05)。OFA组麻醉清醒即刻、术后4 h及24 h的VAS评分低于OA组(F=6.318~20.332,P<0.05),术后24 h内氟比洛芬酯使用率低于OA组(χ2=5.963,P<0.05)。OFA组阿托品和麻黄碱的使用率低于OA组(χ2=4.812、7.925,P<0.05),气管拔管、麻醉清醒、PACU停留的时间均长于OA组(t=2.015~4.354,P<0.05),术后24 h内恶心呕吐、拔管后呼吸抑制的发生率和拔管后躁动评级低于OA组(χ2=11.882、6.667,t=-3.268,P<0.05)。OFA组术中BIS值高于OA组(F=86.485~298.646,P<0.05),两组病人均未发生术中知晓和术后谵妄。
结论 艾司氯胺酮、右美托咪定、七氟烷复合用药OFA在中小手术中的应用是安全可行的,其术后不良反应少,可促进病人术后康复。
[关键词] 无阿片麻醉;艾司氯胺酮;右美托咪定;七氟烷;小外科手术
[中图分类号] R614
[文献标志码] A
[文章编号] 2096-5532(2023)02-0259-05
doi:10.11712/jms.2096-5532.2023.59.069
[开放科学(资源服务)标识码(OSID)]
阿片类药物具有强效的镇痛效果,是目前临床麻醉中广泛应用的药物,但该类药物的诸多不良反应如术后恶心呕吐、呼吸抑制、谵妄、疼痛过敏、慢性术后疼痛等,不利于病人康复。因此,基于多模式镇痛理念,ELKASSABANY等提出了无阿片麻醉(OFA)。目前,OFA已在减体质量、胸外科、妇科腹腔镜、乳癌、结直肠等手术中成功应用。本研究通过查阅大量相关文献和预试验拟定了以艾司氯胺酮、右美托咪定和七氟烷为主的复合麻醉方案,探究其用于中小手术的可行性及优势,以期为临床麻醉提供更优的选择。
1 资料与方法
1.1 样本量估算
本研究以平均动脉压(MAP)为主要结局指标,利用PASS 15软件(NCSS,Kaysville,Utah,USA)来计算所需样本量。根据预试验结果,OFA组干预后MAP为(12.9±1.2)kPa,OA组MAP为(11.7±1.3)kPa,取双侧检验α值为0.05、Power为0.90,输入PASS 15软件Two-Sample T-Tests Allowing Unequal Variance中可算得至少需要入组24例,考虑有20%的脱落率,最终每组需至少入组30例。
1.2 研究对象及分组
选取在我院择期行中小手术(二、三级手术)的气管插管全身麻醉病人60例。納入标准:①年龄18~65岁;②美国麻醉医师协会分级Ⅰ~Ⅱ级;③心、肺、肝、肾功能无明显异常。排除标准:①麻醉药物过敏者;②长期使用阿片类药物者;③合并精神疾病者。手术类型涉及泌尿外科(经尿道前列腺切除术、腹腔镜下肾囊肿摘除术)、血管外科(大隐静脉主干激光闭合术)、口腔颌面外科(颌骨囊肿摘除术、腮腺病损切除术、颌下腺病损切除术、上颌骨骨折切开复位内固定术、下颌骨病损切除术)。采用随机数字表法将入选病人分为OFA组和传统阿片类药物麻醉组(OA组),每组30例。本研究经医院医学伦理委员会批准,病人均签署知情同意书。
1.3 麻醉方法
病人入室后给予监测无创血压、心率(HR)、心电图、脉搏氧饱和度、脑电双频指数(BIS)。开放外周静脉,滴注乳酸林格液并给予抗胆碱药盐酸戊乙奎醚0.01 mg/kg静脉推注。
OFA组病人麻醉诱导前以右美托咪定(江苏恒瑞医药股份有限公司,规格为2 mL:200 μg)0.5 μg/
kg作为负荷量,10 min内泵完。麻醉诱导:艾司氯胺酮(江苏恒瑞医药股份有限公司,规格为2 mL:50 mg)0.5 mg/kg+丙泊酚1~2 mg/kg+顺苯磺酸阿曲库铵0.2~0.3 mg/kg静脉推注。麻醉维持:艾司氯胺酮0.5 mg/(kgh)静脉泵注,右美托咪定0.3 μg/(kgh)静脉泵注,七氟烷(上海恒瑞医药有限公司,规格为120 mL)持续吸入,顺苯磺酸阿曲库铵0.04~0.06 mg/kg间断静脉推注。
OA组麻醉诱导:舒芬太尼(宜昌人福药业有限公司,规格为1 mL:50 μg)0.3~0.4 μg/kg+丙泊酚1~2 mg/kg+顺苯磺酸阿曲库铵0.2~0.3 mg/kg静脉推注。切皮前5 min给予病人舒芬太尼0.3~0.4 μg/kg静脉推注。麻醉维持:舒芬太尼0.15~0.30 μg/kg间断静脉推注,七氟烷持续吸入,顺苯磺酸阿曲库铵0.04~0.06 mg/kg间断静脉推注。
两组病人术中根据BIS值及时调整七氟烷的吸入浓度,维持BIS值在40~60之间以保证适当的麻醉深度。缝皮结束前30 min停用右美托咪定和肌松药,结束前20 min停用艾司氯胺酮,结束前5 min停止吸入七氟烷。病人自主呼吸恢复后,潮气量>5 mL/kg、呼吸频率>12 min-1时转入麻醉后监护治疗室(PACU),清醒配合后给予吸痰拔管。
两组病人术中MAP<8.0 kPa伴HR<60 min-1时给予麻黄碱6 mg,术中MAP<8.0 kPa伴HR>60 min-1时给予去甲肾上腺素8 μg,HR<50 min-1时给予阿托品0.5 mg。术后24 h内视觉模拟评分法(VAS)评分≥5分时,给予氟比洛芬酯50 mg。病人出现恶心呕吐时,给予昂丹司琼8 mg。
1.4 观察指标
1.4.1 主要观察指标 围手术期不同时间点的MAP、HR,即入室时(T0)、插管前3 min(T1)、插管后3 min(T2)、切皮时(T3)、切皮后5 min(T4)、切皮后10 min(T5)、切皮后15 min(T6)、气管拔管时(T7)、清醒时(T8)的 MAP和HR。
1.4.2 次要观察指标 病人麻醉清醒即刻、术后4 h和24 h的VAS评分(0分为无痛,10分为剧痛)及术后24 h内氟比洛芬酯的使用情况,术中血管活性药物使用情况,气管拔管、麻醉清醒、PACU停留的时间,术后24 h内恶心呕吐和拔管后呼吸抑制(呼吸频率≤10 min-1,血氧饱和度<90%)的发生率,术后躁动评级(1级:平静安睡;2级:清醒安静;3级:激惹,但易使之安静;4级:无法克制的哭闹,不易使之安静;5级:谵妄、反抗、兴奋定向障碍),术后谵妄(术后连续3 d采用3D-CAM量表评估)的发生率,T4、T5、T6时的BIS值与术中知晓发生率。
1.5 统计学处理
采用SPSS 23.0软件进行统计学处理。正态分布的计量资料以±s表示,两组间比较采用独立样本t检验,重复测量数据比较采用重复测量方差分析;计数资料以例数和百分比表示,组间比较采用卡方检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较
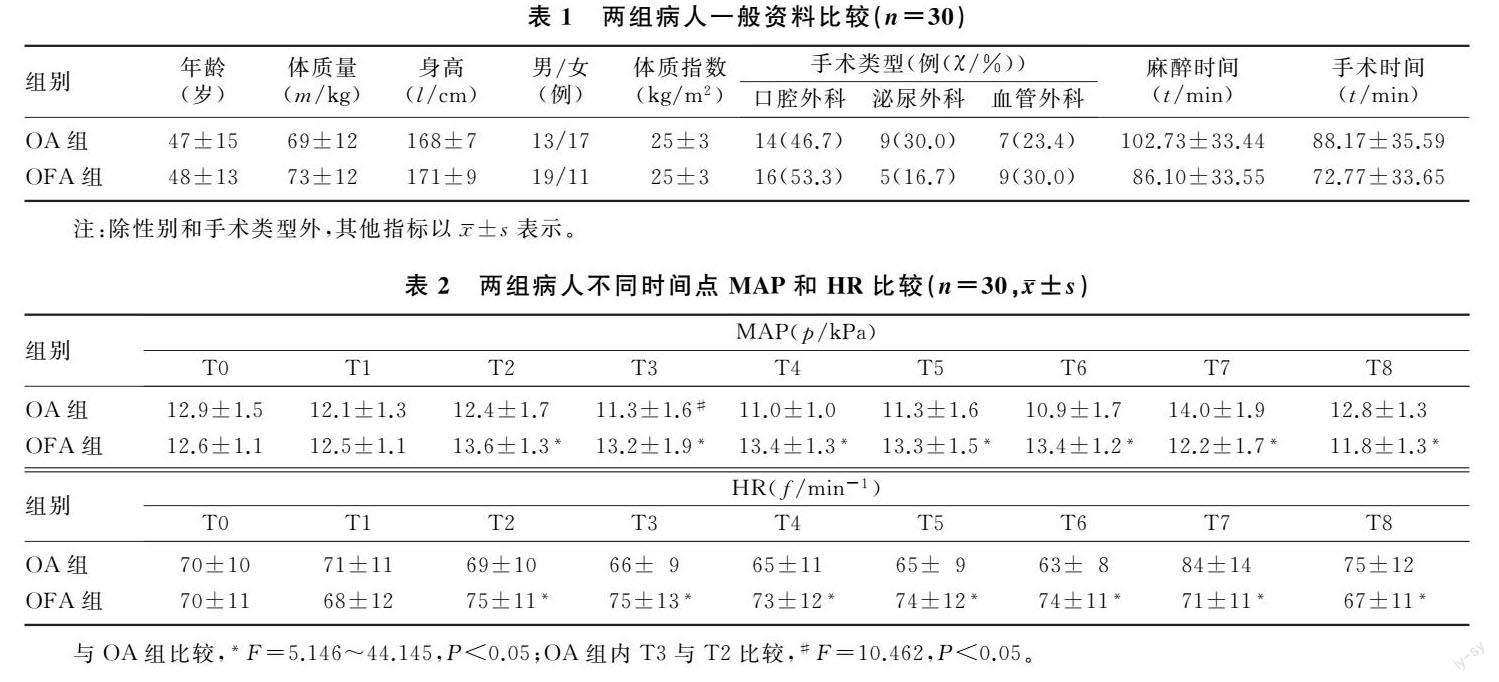
两组病人的年龄、体质量、身高、性别、体质指数、手术类型、麻醉时间和手术时间比较,差异均无统计学意义(P>0.05)。见表1。
2.2 两组各时间点MAP和HR比较
两组病人各时间点MAP比较,组间、时间、交互效应差异均有统计学意义(F组间=12.466,F时间=5.233,F组间×时间=9.050,P<0.05)。两组病人各时间点HR比较,组间效应差异无显著意义(F组间=1.271,P>0.05),时间和交互效应差异均有统计学意义(F时间=3.916,F组间×时间=5.821,P<0.05)。T0、T1时,两组病人MAP、HR比较差异无统计学意义(P>0.05);T2~T6时,OFA组的MAP、HR均高于OA组(F=5.146~44.145,P<0.05);T7、T8时,OFA组的MAP、HR均低于OA组(F=6.054~17.416,P<0.05)。在T2~T6时段内,OFA组的MAP和HR后一时间点与前一时间点比较差异无统计学意义(P>0.05);OA组T3时的MAP较T2时变化较大(F=10.462,P<0.05),其余时间点的MAP和HR与前一时间点比较差异均无统计学意义(P>0.05)。见表2。
2.3 两组术后VAS评分及氟比洛芬酯使用率比较
两组病人术后各时间点VAS评分比较,组间、时间、交互效应差异均具有统计学意义(F组间=18.334,F时间=27.438,F组间×时间=7.028,P<0.05);与OA组相比,OFA组病人麻醉清醒即刻、术后4 h以及24 h 的VAS评分均显著降低(F=6.318~20.332,P<0.05)。OFA組病人术后24 h内氟比洛芬酯使用率低于OA组(χ2=5.963,P<0.05)。见表3。
2.4 两组术中血管活性药物使用情况比较
OFA组病人术中阿托品和麻黄碱的使用率低于OA组(χ2=4.812、7.925,P<0.05),两组病人术中去甲肾上腺素使用率差异无统计学意义(P>0.05)。见表4。
2.5 两组气管拔管、麻醉清醒及PACU停留时间比较
OFA组气管拔管时间、麻醉清醒时间及PACU停留时间显著长于OA组(t=2.015~4.354,P<0.05)。见表5。
2.6 两组术后不良反应比较
OFA组拔管后呼吸抑制及术后24 h内恶心呕吐的发生率均低于OA组(χ2=6.667、11.882,P<0.05),术后躁动评级也低于OA组(t=-3.268,P<0.05)。两组病人均未发生术后谵妄。见表6。
2.7 两组术中BIS值及知晓发生率比较
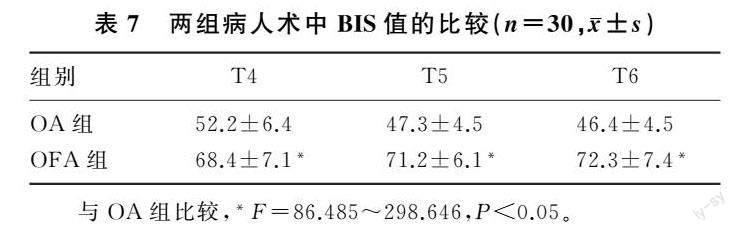
两组病人术中各时间点BIS值比较,组间、交互效应差异有显著意义(F组间=450.143,F组间×时间=8.745,P<0.05),时间效应差异无显著意义(F时间=0.437,P>0.05);与OA组相比,OFA组术中BIS值均显著高于OA组(F=86.485~298.646,P<0.05)。两组病人均未出现术中知晓。见表7。
3 讨论
右美托咪定是临床上常用的镇痛、镇静药物,兼具抗心律失常、抗焦虑的功能。麻醉诱导前持续泵注右美托咪定,可以减少其他麻醉药物的使用,使诱导过程平稳,插管刺激轻。但该药作为高选择性α2肾上腺素能受体激动剂,能抑制交感神经兴奋,长时间泵注会诱发血压和HR的降低。因此,本研究复合使用艾司氯胺酮,利用艾司氯胺酮的拟交感作用中和右美托咪定的交感神经抑制,从而达到循环的稳定。值得一提的是右美托咪定的“可唤醒镇静”作用,长时间泵注后其半衰期延长,会产生一种能被语言和微小刺激唤醒的近似生理性的睡眠状态,这种镇静状态在停药后,可以持续较长一段时间。七氟烷和丙泊酚都是临床常用的麻醉维持药物,因丙泊酚对呼吸循环抑制较明显,本研究优选七氟烷。七氟烷对自主呼吸影响小,不刺激呼吸道,使用时起效极快,诱导迅速,病人苏醒快,麻醉深度也更容易控制。
本文研究结果显示,OFA组病人气管插管阶段的血流动力学指标波动在正常范围之内,说明麻醉诱导前右美托咪定的负荷量和麻醉诱导时的艾司氯胺酮剂量足以消除气管插管时的疼痛刺激。在插管后3 min到切皮后15 min的时间段内,OFA组的MAP、HR显著高于OA组,这与阿片类药物抑制应激反应的效果更强有关,也与艾司氯胺酮兴奋交感神经的作用有关。通过在该时间段OFA组内MAP、HR波动的前后比较可发现,OFA组的血流动力学较为平稳,且OFA组术中血管活性药物的使用率明显低于OA组。在麻醉恢复阶段,OA组拔管后血压和HR出现反跳现象,拔管后躁动评级较高,病人依从性差。相反,OFA组在拔管时和麻醉清醒时的血压和HR无明显波动,这得益于右美托咪定长时间输注后产生的“可唤醒镇静”作用,使病人呈近似非快动眼睡眠的状态,有效避免了气管拔管时的呛咳反应诱发的心血管不良事件,使整个恢复过程平静无躁动。但OFA组病人的拔管、麻醉清醒和PACU停留时间明显长于OA组,病人的定向力恢复所需时间较长。
疼痛和恶心呕吐是最常见的术后不良反应,与病人的就诊满意度降低相关。有研究结果表明,术中艾司氯胺酮、右美托咪定的使用可明显降低病人术后疼痛评分,减少术后镇痛药物使用,避免形成痛觉过敏,且这两种药物均不影响胃肠道。本研究中,OFA组病人术后各时间点的VAS疼痛评分、术后24 h内氟比洛芬酯使用率及术后24 h内恶心呕吐发生率均显著低于OA组,表明OFA有利于病人的术后恢复。术后呼吸抑制是阿片类药物麻醉最为严重的不良反应之一。艾司氯胺酮的前体氯胺酮可松弛支气管平滑肌,缓解支气管痉挛,且不减弱咽喉保护性反射,有助于病人围手术期的气道保护。右美托咪定呼吸抑制作用轻微。本研究中OFA组病人未发生术后呼吸抑制,且病人术毕拮抗残余肌松药后自主呼吸恢复速度很快,表明OFA消除了病人术后呼吸抑制的安全隐患,在术后呼吸管理方面优势明显。
本研究局限性为,艾司氯胺酮的应用使得BIS值相对OA组明显升高,数值波动在65~75之间,使麻醉深度无法得到精确判断。相关研究显示,艾司氯胺酮可以升高BIS值,且不同剂量的艾司氯胺酮对脑电波的影响不同,继而使得BIS值的变化范围不同。但目前尚无可以指导艾司氯胺酮应用的麻醉深度监测指标。因此,本研究在参考BIS值的同时,严密监测镇静药物用量及血流动力学变化,术后随访显示两组病人均未出现术中知晓。
综上所述,艾司氯胺酮、右美托咪定、七氟烷复合用药的OFA在口腔外科、泌尿外科、血管外科等中小手术中的应用是可行的,其应用使病人在术中、拔管、麻醉清醒阶段血流动力学更平稳,有效避免了阿片類药物带来的术后恶心呕吐、术后疼痛、拔管后呼吸抑制与躁动等不良反应,可帮助病人更安全舒适地度过围手术期。
[参考文献]
ELKASSABANY N M, MARIANO E R. Opioid-free anaesthesia-what would inigo montoya say Anaesthesia, 2019,74(5):560-563.
ZIEMANN-GIMMEL P, GOLDFARB A A, KOPPMAN J, et al. Opioid-free total intravenous anaesthesia reduces posto-
perative nausea and vomiting in bariatric surgery beyond triple prophylaxis. British Journal of Anaesthesia, 2014,112(5):906-911.
DEVINE G, CHENG M, MARTINEZ G, et al. Opioid-free anesthesia for lung cancer resection: a case-control study. Journal of Cardiothoracic and Vascular Anesthesia, 2020,34(11):3036-3040.
MASSOTH C, SCHWELLENBACH J, SAADAT-GILANI K, et al. Impact of opioid-free anaesthesia on postoperative nausea, vomiting and pain after gynaecological laparoscopy-A randomised controlled trial. Journal of Clinical Anesthesia, 2021,75:110437.
MUZII L, GALATI G, DI TUCCI C, et al. Medical treatment of ovarian endometriomas: a prospective evaluation of the effect of dienogest on ovarian reserve, cyst diameter, and associated pain. Gynecological Endocrinology: the Official Journal of the International Society of Gynecological Endocrinology, 2020,36(1):81-83.
KELLER D S, ZHANG J Y, CHAND M. Opioid-free colorectal surgery: a method to improve patient & financial outcomes in surgery. Surgical Endoscopy, 2019,33(6):1959-1966.
PANCHGAR V, SHETTI A N, SUNITHA H B, et al. The effectiveness of intravenous dexmedetomidine on perioperative hemodynamics, analgesic requirement, and side effects profile in patients undergoing laparoscopic surgery under general anesthesia. Anesthesia, Essays and Researches, 2017,11(1):72-77.
QIU G L, WU Y, YANG Z Y, et al. Dexmedetomidine activation of dopamine neurons in the ventral tegmental area attenuates the depth of sedation in mice. Anesthesiology, 2020,133(2):377-392.
张春艳,刘保江. 七氟醚的临床应用现状. 医学综述, 2008,14(7):1092-1094.
MION G, VILLEVIEILLE T. Ketamine pharmacology: an update (pharmacodynamics and molecular aspects, recent fin-
dings). CNS Neuroscience & Therapeutics, 2013,19(6):370-380.
EBERHART L H, MAUCH M, MORIN A M, et al. Impact of a multimodal anti-emetic prophylaxis on patient satisfaction in high-risk patients for postoperative nausea and vomiting. Anaesthesia, 2002,57(10):1022-1027.
MENDOLA C, CAMMAROTA G, NETTO R, et al. S(+)-ketamine for control of perioperative pain and prevention of post thoracotomy pain syndrome: a randomized, double-blind study. Minerva Anestesiologica, 2012,78(7):757-766.
ZHANG B H, WANG G F, LIU X P, et al. The opioid-spa-
ring effect of perioperative dexmedetomidine combined with oxycodone infusion during open hepatectomy: a randomized controlled trial. Frontiers in Pharmacology, 2017,8:940.
PELTONIEMI M A, HAGELBERG N M, OLKKOLA K T, et al. Ketamine: a review of clinical pharmacokinetics and pharmacodynamics in anesthesia and pain therapy. Clinical Pharmacokinetics, 2016,55(9):1059-1077.
LIN N, VUTSKITS L, BEBAWY J F, et al. Perspectives on dexmedetomidine use for neurosurgical patients. Journal of Neurosurgical Anesthesiology, 2019,31(4):366-377.
樊青珠,李燕爽,代輝,等. 不同剂量艾司氯胺酮对咪达唑仑镇静患者脑电双频指数的影响. 中国新药与临床杂志, 2022,41(6):362-366.
(本文编辑 马伟平)
