机器人辅助下远端胃癌根治术操作技巧与经验
2023-06-22王启飞,王刚,邓正明,潘华峰,刘江,王海锋,江志伟
王启飞,王刚,邓正明,潘华峰,刘江,王海锋,江志伟


摘 要 目的:分析总结应用达芬奇机器人辅助下远端胃癌根治术的操作技巧与经验。方法:回顾性分析2019年11月—2022年1月在南京中医药大学附属医院应用达芬奇机器人辅助远端胃癌根治术治疗82例患者的临床资料。结果:所有患者均顺利完成手术,无中转开腹。手术时间(211.2±31.2)min,出血量(33.1±18.2)ml,淋巴结清扫数目(28.6±13.7)枚,术后住院时间(6.7±7.3)d。并发症发生患者4例,其中吻合口瘘1例、肺部感染1例、切口感染 2例,均采用保守方法治愈,未出现腹腔内出血及吻合口狭窄等情况。结论:达芬奇机器人辅助远端胃癌根治术是安全、可行的,此术式具有术野清晰度高、解剖更精细以及患者术后恢复快等优势,且科学的手术步骤和操作技巧能够缩短术者学习曲线、降低手術难度,使患者从中受益。
关键词 机器人辅助手术;远端胃癌根治术;操作技巧
中图分类号 R735.2 文献标识码 A 文章编号 2096-7721(2023)05-0485-07
Analysis of surgical skills and experience of robot-assisted radical gastrectomy for distal gastric cancer
WANG Qifei, WANG Gang, DENG Zhengming, PAN Huafeng, LIU Jiang, WANG Haifeng, JIANG Zhiwei
(Department of General Surgery, the Affiliated Hospital of Nanjing University of Chinese Medicine, Nanjing 210029, China)
Abstract Objective: To analyze and summarize the surgical skills and experience of Da Vinci robot-assisted radical gastrectomy for distal gastric cancer. Methods: The clinical data of 82 patients who underwent Da Vinci robot-assisted radical gastrectomy for distal gastric cancer in the Affiliated Hospital of Nanjing University of Chinese Medicine from November 2019 to January 2022 were retrospectively analyzed. Results: All patients successfully completed the surgery without conversion to laparotomy. The operative time was (211.2±31.2)min, with the bleeding volume of (33.1±18.2)ml, the number of lymph node dissection of (28.6±13.7), and the postoperative hospital stay of (6.7±7.3)d. Complications occurred in 4 cases, including 1 case of anastomotic fistula, 1 case of pulmonary infection and 2 cases of incisional infection, all of which were treated by conservative methods without intraperitoneal bleeding bleeding or anastomotic stenosis. Conclusion: Da Vinci robot-assisted radical gastrectomy for distal gastric cancer is safe and feasible, with the advantages of high image clarity, more precise anatomy, and quick postoperative recovery. In addition, the scientific surgical procedures and skills could shorten the learning curve of the surgeon and reduce the difficulty of surgical procedures.
Key words Robot-assisted surgery; Radical gastrectomy for distal gastric cancer; Operation technique
目前胃癌作为最常见的消化道恶性肿瘤之一,严重威胁人类的生命健康。根据2022年国家癌症中心发布的最新全国癌症统计数据[1],我国胃癌发病率和死亡率均位列恶性肿瘤发病率与死亡率的第3位。目前根治性手术仍然是胃癌最主要的治疗方案,南京中医药大学附属医院作为全国较先开展达芬奇Xi机器人辅助手术的单位之一,在长期的临床实践中积累了较多的手术经验以及围手术期治疗和护理的相关经验。迄今为止,本中心应用达芬奇机器人手术系统已完成300余例胃癌手术,并在淋巴结清扫技巧和助手协助配合等方面积累了大量经验,本文详细阐述达芬奇机器人辅助远端胃癌根治术中操作技巧及经验,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2019年11月—2022年1月在南京中医药大学附属医院行达芬奇机器人辅助下远端胃癌根治术的82例患者临床资料。其中男性55例,女性27例;年龄(58.5±11.9)岁;术前 CT 分期:Ⅰ期 38例,Ⅱ期 29例,Ⅲ期 15例。纳入标准:①术前胃镜及病理检查结果显示为胃恶性肿瘤患者;②同意行机器人辅助远端胃癌根治术患者;③肿瘤无远处转移患者。排除标准:①胃良性疾病患者;②中转开腹患者;③心、脑、肺严重合并症者;④严重精神疾病患者。
1.2 患者体位与Trocar位置
手术采用静吸复合麻醉,患者取头高足低30°体位。术中采用五孔法,于脐下3cm置入8 mm Trocar作為观察孔C,气腹压力设定为12 mmHg。在镜头引导下分别于右侧锁骨中线平脐、右侧腋前线肋下2 cm、左侧腋前线肋下2 cm分别置入8 mm Trocar,左侧锁骨中线平脐处置入12 mm Trocar作为助手操作孔A,右肋下Trocar、右脐旁Trocar、镜头Trocar、左肋下Trocar分别连接机器人机械臂R1、R2、C、R3(如图1);R1、R2连接抓钳,R3连接超声刀。
1.3 手术操作步骤与要点
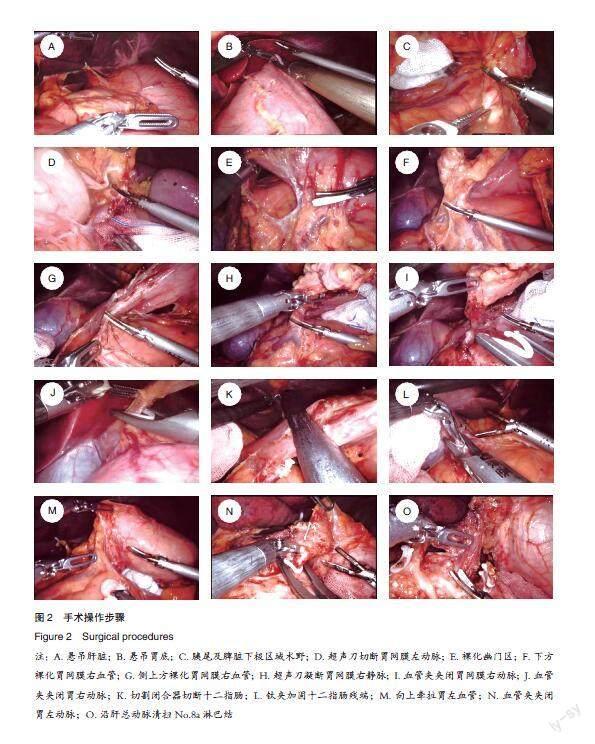
①悬吊肝脏:于肝脏下缘打开小网膜至贲门右侧,经剑突左下方穿入荷包缝合针,荷包线绕过肝圆韧带,经剑突右下方穿出,将荷包线固定于贲门右侧肝胃韧带,体外牵拉固定悬吊肝脏(如图2A),暴露术野。②清扫No.4sb淋巴结:超声刀沿横结肠上缘无血管区分离胃结肠韧带至胰尾附近停止,再沿胃大弯血管弓内裁剪大网膜至第一支胃短动脉,将胃大弯向左上牵拉至悬吊肝脏的荷包线处,锁扣夹固定(如图2B),暴露胃后部及胰腺;R1臂抓钳将大网膜向左上牵拉,使胰尾、胃网膜左血管、脾脏下极区术野良好显露(如图2C);R2臂抓钳和助手形成三角牵拉,沿结肠向脾门分离,游离网膜左系膜,分离胃网膜左动脉,在根部以Hem-o-lock夹闭后用超声刀离断(如图2D),清扫No.4sb淋巴结。③裸化幽门区:R1臂抓钳向上牵引小网膜,助手向下牵胃窦部,超声刀打开幽门区及十二指肠球部上无血管区至胃右血管;R1抓钳提起胃,R2抓钳向下牵拉大网膜,在胃大弯血管弓内游离幽门下大网膜及网膜右系膜至胰腺上缘水平,裸化幽门区(如图2E)。④清扫No.4d、No.6淋巴结:超声刀继续向右分离胃结肠韧带,逐层打开融合筋膜,紧贴胰头表面分离暴露胃网膜右动静脉,此处可从大网膜上、下两个方向显露胃网膜右血管并进行裸化,同时分离胃胰韧带并显露胃十二指肠动脉(如图2F~2G),超声刀凝断胃网膜右静脉,血管夹夹闭胃网膜右动脉后切断(如图2H~2I),清扫No.4d、No.6淋巴结。⑤清扫No.5、No.12a淋巴结:R1抓钳提起小网膜,切开肝十二指肠韧带,沿胃十二指肠动脉及肝总动脉分离充分显露肝固有动脉及胃右动脉,于胃右动脉根部血管夹夹闭后离断(如图2J),继续沿肝固有动脉向肝门分离,清扫No.5和No.12a组淋巴结。⑥离断十二指肠:直线切割闭合器离断十二指肠(如图2K),多枚钛夹加固十二指肠残端(如图2L)。⑦清扫No.11p、No.7、No.8a、No.9淋巴结:将大网膜牵至左侧,胃向左上翻,R1抓钳在胃后壁靠近胃左血管处向上牵拉(如图2M),沿胰腺上缘打开胰腺前被膜,R2抓钳提起已分离的脂肪组织,助手持“花生米”下压胰腺,分离暴露脾动脉,清扫No.11p淋巴结。超声刀继续向胃左动脉及腹腔干游离,显露腹腔动脉干,分离胃左动脉,在胃左动脉根部夹闭后离断,清扫No.7、No.9淋巴结(如图2N),超声刀凝断胃左静脉,继续向右扩展,沿肝总动脉清扫No.8a淋巴结(如图2O)。⑧清扫No.1、No.3淋巴结:游离胃小弯及贲门右侧,清扫No.3、No.1淋巴结。
1.4 消化道重建与标本取出
本研究中53例患者取上腹部正中切口5~7 cm,完成肿瘤切取及消化道重建。29例患者在机器人辅助下采用“双针四步”法完成消化道重建[2],于耻骨联合上方2横指处取3~4 cm切口,取出标本。
2 结果
所有患者均顺利完成手术,无中转开腹。手术时间为(211.2±31.2)min,出血量为(33.1±18.2)ml,淋巴结清扫数目为(28.6±13.7)枚,术后住院时间为(6.7±7.3)d。53例行小切口取出、吻合,29例在机器人辅助下完成消化道重建,术后病理Ⅰ期34例,Ⅱ期20例,Ⅲ期23例,Ⅳ期5例。其中发生并发症4例,其中吻合口瘘1例、肺部感染1例、切口感染2例(见表1),均采用保守方法治疗,未出现腹腔内出血及吻合口狭窄。
3 讨论
手术机器人作为微创外科领域的新设备,凭借其独特的优势在临床已被广泛认可[3]。与传统的腹腔镜手术相比,达芬奇机器人手术系统具有10~15倍的高清三维立体图像,能够使术者更精确地辨认微小解剖结构;同时机器人手术系统可自动过滤生理震颤,避免了腹腔镜术野震颤等问题;手术机器人器械臂可540°旋转,使得术中操作更加灵活、精细,且主刀医生在术中可自行控制镜头与机械臂的角度与位置,降低与助手在术中默契配合的要求;此外,有研究表明,外科医师学习机器人手术系统操作的曲线较短,更容易掌握规范的机器人辅助下胃癌手术操作技能[4-5]。自2002 年 Hashizume M等人[6]首次报道达芬奇机器人辅助胃癌根治术的成功案例以来,机器人辅助胃癌根治术已逐步应用于临床,并取得了良好的临床疗效[7-9]。本中心自2019年11月开展达芬奇机器人辅助外科手术,现已有大量临床数据证实了机器人辅助胃癌手术的安全性及有效性,并积累了丰富的手术临床经验及技巧,希望本中心在机器人辅助胃癌根治术方面总结的经验能够帮助初步开展达芬奇机器人辅助远端胃癌根治术的外科医师倍道而进,造福广大患者。
3.1 淋巴结清扫技巧
机器人辅助远端胃癌根治术的淋巴结清扫路径和顺序与传统腹腔镜手术略有不同,根据《机器人胃癌手术中国专家共识(2021版)》中的肿瘤整块切除原则行分区域淋巴结清扫术,即No.4sb→No.6→No.5、12a→No.11p、8a、7、9→No.1、3[10]。胃周淋巴结的分布和流动走向是与胃周围血管的分布相联系的,所以淋巴结清扫的过程也是胃周血管显露的过程[11]。本中心对于No.6及No.4sb淋巴结清扫较传统方式有所改进,尤其对于网膜肥胖患者,No.6及No.4sb淋巴结的清扫是难点,术野暴露不清,容易出血;利用手术机器人高清三维的清晰视野,将幽门区小网膜、大网膜开窗,使胃窦及十二指肠球部裸化,提起胃窦区,从胃窦上、下两个方向清扫淋巴结,使No.6淋巴结清扫空间及术野更加开阔,同时能减少大网膜多次翻动,减少助手暴露操作,从而使出血及渗出可控,让清扫更加容易,大大缩短手术时间;同理切开部分大弯及胃底侧网膜,使No.4sb淋巴结清扫更加便捷。
3.2 充分发挥机器人辅助下超声刀的优势
达芬奇机器人手术系统具有10~15倍的高清三维立体图像,能够使术者更精确地辨认微小解剖结构,机器人辅助远端胃癌根治术应充分利用手术机器人高清3D视野的优势,做到细小血管超声刀精细夹闭、离断,尤其在清扫淋巴结时,超声刀钳夹大块组织时会使血管夹夹闭不全,夹持力变弱,应遵循“小步快走”的理念,辨清细小血管,避免出血及反复止血;同时也应充分利用超声刀凝断血管的功能,在无张力状态大胆离断小于5 mm的血管,避免反复夹闭血管耗费时间、增加手术费用,尤其对于脾门区血管丰富,盲目使用血管夹夹闭,易导致出血。
3.3 R1抓钳的使用
与腹腔镜手术相比,机器人辅助手术除了主刀医生可自行操控术野,更重要的是术中多了一个操作臂,R2抓钳、R3超声刀或电钩与腹腔镜的操作大同小异,R1臂的使用是机器人辅助手术中不可忽视的一部分,R1抓钳的作用无疑是显露术野,而术野暴露主要由主刀医生完成,因此R1抓钳的操作尤为重要。术中减少R1抓钳的频繁变动,使术野显露清晰以及充分利用有限的空间开展精细化操作是术中操作的要点,部分中心在进行达芬奇机器人辅助手术时采用“3+2”或“3+1”孔的模式,这种模式虽对机器人辅助手术的初学者友好,但对助手的水平要求更高。本研究总结了手术机器人R1臂抓钳显露术野的关键:①清扫No.4sb淋巴结将大网膜向左上牵拉;②游离胃结肠韧带、分离大网膜及清扫No.6淋巴结时,将胃体向头侧上牵;③清扫No.5、No.12淋巴结时提拉小网膜;④清扫No.11p、No.7、No.8a、No.9淋巴结时将胃后壁靠近胃左血管处向上牵拉,以上几步在操作缺少张力时R1抓钳需适当微调。
3.4 “花生米”的制作与使用
达芬奇机器人手术助手在手术操作强度上较腹腔镜助手有所降低,但机器人手术助手更需要与主刀医生相机行事的默契配合。助手应熟练使用各种手术器械并在术中顺畅转换,在关键部位协助主刀医生进行术野暴露,这才能使整个手术过程流畅,手术效率及手术质量大大提高。在机器人辅助胃癌淋巴结清扫过程中,助手需经常下压胰腺及血管并给予张力,协助主刀医生完成术野显露,此过程通常用吸引器或抓钳协助完成,但吸引器及抓钳下压胰腺极容易对胰腺造成损伤,尤其对于新手掌握不好力度,甚至容易引发胰瘘。吸引器下压血管或抓钳钳夹、牵拉血管时如果力道过小,摩擦力不够,易导致血管滑脱,影响主刀操作;如果反复牵拉下压血管或力度过大易致出血,严重影响手术进程。“花生米”的制作方法:将1/4腔镜纱布用生理盐水浸湿,卷成条状,将其对折,持针器夹持(如图3),以自制“花生米”替代吸引器及抓钳,既能增大器械与组织间的摩擦力,又不易损伤胰腺、血管,让术中操作变的简单,术野暴露更加良好,自制“花生米”在下压胰腺及血管时是不可或缺的器械。
4结论
机器人辅助手术是微创外科发展的方向,目前我国开展达芬奇机器人辅助胃癌手术的医疗机构逐渐增多,其临床技术仍需精进,技术创新任重道远。机器人辅助技术可以安全、有效地完成胃癌根治术[7-8,12],它在淋巴结清扫数、减少出血量、重建消化道方面有显著优势,希望本中心的技巧经验可以帮助学习曲线内的同行,使广大患者受益。
参考文献
[1] ZHENG R S, ZHANG S W, ZENG H M, et al. Cancer incidence and mortality in China, 2016[J]. Press Corrected Proof, 2022, 2(1): 1-9.
[2] 刘江, 王刚, 程伟, 等. 达芬奇机器人镜下手工吻合技术在远端胃切除毕Ⅱ式吻合中的应用[J]. 腹腔镜外科杂志, 2020, 25(6): 412-416.
[3] 阚明韵, 柳欣欣, 江志伟. 机器人胃癌根治术的现状与展望[J].机器人外科学杂志(中英文), 2022, 3(4): 337-342.
[4] Kim M S, Kim W J, Hyung W J, et al. Comprehensive learning curve of robotic surgery: discovery from a multicenter prospective trial of robotic gastrectomy[J]. Annals of Surgery, 2021, 273(5): 949-956.
[5] 秦倩, 时飞宇, 孙祺, 等. 达芬奇机器人手术系统辅助胃癌根治术的学习曲线[J].中华消化外科杂志, 2019, 18(5): 459-465.
[6] Hashizume M, Shimada M, Tomikawa M, et al. Early experiences of endoscopic procedures in general surgery assisted by a computerenhanced surgical system[J]. Surgical Endoscopy, 2002, 16(8): 1187-1191.
[7] 王剛, 潘华峰, 刘江, 等. 达芬奇Xi系统在完全机器人根治性远端胃大部切除术中的应用[J].山东大学学报(医学版), 2020, 58(5): 51-55.
[8] 刘召, 谢毅, 朱含放. 机器人与腹腔镜行胃癌D2根治性淋巴结清扫术近期疗效对比的Meta分析[J].机器人外科学杂志(中英文), 2022, 3(4): 295-310.
[9] 周岩冰.机器人手术系统在胃癌治疗中的应用[J].中华消化外科杂志, 2022, 21(3): 348-354.
[10] 中国研究型医院学会机器人与腹腔镜外科专业委员会, 中国抗癌协会胃癌专业委员会. 机器人胃癌手术中国专家共识(2021版)[J].中华消化外科杂志, 2022, 21(1): 1-9.
[11] Kumamoto T, Kurahashi Y, Niwa H, et al. Laparoscopic suprapancreatic lymph node dissection using a systematic mesogastric excision concept for gastric cancer[J]. Annals of Surgical Oncology, 2020, 27(2): 529-531.
[12] 余佩武, 李政焰.中国胃癌机器人手术开展的现状与思考[J].中华胃肠外科杂志, 2020, 23(4): 332-335.
