臭氧催化氧化联合曝气生物滤池工艺对炼化二级出水中污染物的去除效果
2023-06-15张雪英雍晓雨
马 骏,李 丹,张雪英,雍晓雨,任 云,周 俊
(1.南京工业大学 环境科学与工程学院,江苏 南京 211800;2.南京工业大学 生物与制药工程学院,江苏 南京 211800;3.南京市市政设计研究院有限公司,江苏 南京 210008)
石油化工企业的化工原料生产、石油炼制技术、有机材料合成等越来越趋向于多样性,因此产生的污染物越来越复杂,处理难度也越来越大[1-3]。江苏省最新的《化学工业水污染物排放标准》在2020年3月1日实施,规定化学需氧量(COD)排放限值小于50 mg/L,提高了对炼化废水处理的要求。炼化废水常用的深度处理主要通过物理法、化学法和生物法3道工序完成[4-5]。其中,化学法主要依靠高级氧化技术产生大量的自由基[6-8],进而矿化废水中的有机污染物,增加废水的可生化性,随后生物法矿化后的污染物更容易被生物反应池的微生物利用[9],提高对炼化废水中难降解有机物的去除效率,使废水达标排放[10]。
臭氧催化氧化作为高级氧化技术的一种,具有反应快速、高效、无选择性、无二次污染等优点,在工业废水处理中有着广泛应用[11]。臭氧催化氧化对有机污染物的降解主要通过两种途径:一种是O3在水中分解产生大量的自由基,通过自由基矿化废水中的有机污染物;另一种是O3分子直接攻击水中的污染物,与污染物发生反应达到降解作用[12-14]。曝气生物滤池(BAF)的优点:占地面积小,投资少;不需要回流,流程短;技术简单,可以处理大规模废水[15],是炼化废水深度处理最常用的方法之一。BAF对于污染物的去除原理主要包括截留过滤和生物降解:截留过滤主要依托BAF填料的多孔特点和形成的致密生物膜,将水中的悬浮物拦截;生物降解主要通过BAF生物膜上丰富的菌群去除废水中的污染物[16-17]。炼化二级废水在进入深度处理时,水中大部分易降解有机物已被去除,单用臭氧催化氧化处理残留的难降解有机物需要加大投加量才能处理达标,成本很高;单独用BAF处理,效果并不理想。但若两者联用,采用臭氧催化氧化前置处理,将难降解的大分子有机物矿化为易于微生物利用的小分子有机物,提高废水可生化性,降低有机负荷后进入BAF,可显著提升废水处理效果[18-21]。
目前,在实际使用臭氧催化氧化联合BAF(O3-BAF)工艺处理炼化二级出水的应用中,存在2个问题:①不同催化剂与不同废水的适配性不同,有机物的矿化率低,导致臭氧催化氧化效率低;②由于炼化废水有机物种类繁多,自然驯化的BAF生物膜微生物多样性不高且O3-BAF的协同性差,导致整体处理效率不高,不能保证COD、总氮(TN)长期稳定达标排放[22-23]。本文针对某特定石化公司的炼化二级出水,为了提高臭氧催化氧化效率,缩短BAF的驯化时间,提升BAF系统的污染物去除效率,选择自主研发的专门针对该废水的催化剂以及课题组筛选出来的混合菌群,研究臭氧催化氧化和BAF各阶段对废水中污染物去除的机制,为炼化废水的深度处理提供技术支撑。
1 材料与方法
炼化二级出水取自南京某石化公司污水处理厂,基本性质见表1。

表1 炼化二级出水基本性质
1.1 装置与实验材料
实验装置示意图如图1所示,实验装置由曝气泵、臭氧发生器、流量计、蠕动泵、储水桶、臭氧催化氧化柱和BAF等构成。臭氧发生器以空气为气源,采用气体流量计控制O3投加量和BAF气水比,通过调节蠕动泵来控制O3接触时间。臭氧催化氧化柱由高55 cm、内径3 cm的有机玻璃制成,BAF反应柱由高28 cm;内径6 cm的有机玻璃制成。臭氧催化氧化柱选择Al2O3基催化剂,O3接触时间为40 min,O3投加量为40 mg/L,采用下进上出的进水方式。
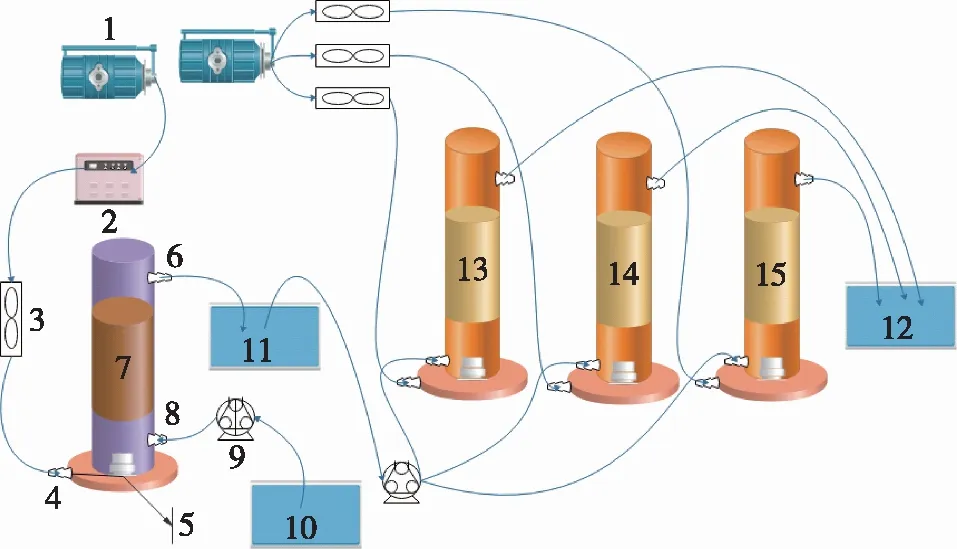
1—曝气泵;2—臭氧发生器;3—转子流量计;4—入气口;5—曝气头;6—出水口;7—臭氧催化氧化柱(臭氧柱);8—入水口;9—蠕动泵;10—炼化二级出水储水桶;11—臭氧柱出水储水桶;12—BAF出水储水桶;13—BAF 1号柱(BAF1);14—BAF 2号柱(BAF2);15—BAF 3号柱(BAF3)
BAF反应柱选用陶粒作为填料,驯化阶段设置BAF气水比为4∶1(体积比),水力停留时间(HRT)为4 h。实验设置3组并联的BAF,由同一臭氧催化氧化柱出水为BAF进水,均采用下进上出的进水方式,3组BAF的对比条件:①投加菌剂和活性污泥(BAF1);②投加活性污泥(BAF2);③自然驯化(不添加菌剂和活性污泥)(BAF3)。驯化投加的污泥为原厂BAF的污泥,投加的菌剂为课题组在活性污泥中筛选出来的混合菌群,主要包括Alcaligenes和Methylobacterium,占比超过80%,大部分Alcaligenes可以同时进行硝化反硝化作用,从而达到去除废水中TN的效果,Methylobacterium可用葡萄糖或者其他复杂有机物作为碳源。污泥和菌剂的投加量均为BAF反应器容积的5%。
1.2 方法
1.2.1 水质基本检测方法
COD使用重铬酸钾法测定;NH3-N含量(质量浓度,下同)使用纳氏试剂比色法测定;TN含量使用碱性过硫酸钾法测定;TP含量使用钼锑抗分光光度法测定[24];TOC含量使用岛津TOC测定仪测定。
1.2.2 三维荧光检测方法
水样过0.45 μm微滤膜后通过三维荧光光谱仪(F-7000型,日本日立公司)检测,激发光谱从200 nm增到450 nm,发射光谱从250 nm增到550 nm,狭缝宽度均为5 nm,扫描速率为12 000 nm/min,光电倍增管电压400 V,将减去纯水修正拉曼峰干扰后的数据绘出色谱的二维等值图,采用荧光区域积分(FRI)法对荧光有机物的相对含量进行定量分析[25-26]。
1.2.3 分子量检测方法
选择分子量小于500、500~1 000、1 000~3 500、3 500~7 000和大于7 000这5种规格的透析袋,剪成20 cm左右的独立小段。0.292 g的乙二胺四乙酸(EDTA)溶于1 L的蒸馏水,并将pH调到8.0左右,然后将事先准备好的透析袋在此溶液中并于沸腾情况下煮10 min;用蒸馏水将透析袋冲洗干净,装入待测溶液后夹紧;将透析袋浸入5 L的蒸馏水中透析24 h,透析完成后通过测量TOC含量表征分子量变化情况。
1.2.4 有机物检测方法
取300 mL水样,注入500 mL的分液漏斗中,用盐酸调节pH到2.0以下,分3次共注入15 mL二氯甲烷,收集下层萃取液。上层水相用10%的NaOH调节pH到12.0以上,分3次注入15 mL二氯甲烷,收集下层萃取液。将2次收集到的萃取液混合,通过干燥的无水硫酸钠柱收集滤液。通过旋转蒸发仪将滤液蒸干后,用甲醇洗脱并定容到1 mL,采用气相色谱质谱(GC/MS)(7890/5975c型,美国安捷伦公司)检测[27]。
1.2.5 微生物多样性分析
在BAF驯化中期和稳定期取各个组别的生物膜样品,然后将样品由上海美吉生物公司进行凝胶电泳和高通量测序,最后通过上海美吉生物公司的数据分析平台进行物种多样性分析和群落结构的统计分析。
2 结果与讨论
2.1 不同处理系统进出水水质分析
2.1.1 COD含量和去除率的变化
O3-BAF工艺整个运行周期COD含量的变化情况如图2所示。由图2可知:BAF启动1~7 d内,系统处于挂膜阶段,滤料表面附着的微生物量较少,仅依靠滤料本身的截留吸附作用和水中原有污泥中的少量微生物降解作用,COD几乎没有变化;在10~40 d内,3组O3-BAF系统对COD的去除率都稳步上升,在第40天左右,3组O3-BAF系统依次达到稳定阶段;在40~49 d期间,BAF的1、2、3号柱出水COD平均质量浓度依次为24、28和33 mg/L,COD去除率依次为71%、67%和61%。在49~77 d内,每隔7 d改变一次装置运行条件,考察不同HRT和气水比对O3-BAF系统COD去除率的影响,结果见图2。由图2可知:在气水比4∶1、HRT为4 h的情况下,3组O3-BAF系统的COD平均去除率依次为68%、64%和58%;在气水比4∶1、HRT为2 h的情况下,3组O3-BAF系统的COD平均去除率依次为66%、60%和55%。在不改变气水比的情况下,HRT为4 h时COD的去除效果最优,即随着HRT的减小,COD去除率有所下降。在气水比3∶1、HRT为4 h的情况下,3组O3-BAF系统的COD平均去除率依次为74%、69%、64%;在气水比2∶1、HRT为4 h的情况下,3组O3-BAF系统的COD平均去除率依次为69%、66%和58%。在保持HRT为4 h的情况下,气水比为3∶1时COD的去除率最优。溶解氧是影响出水水质和微生物生长的重要因素,气水比的大小决定了BAF反应器中溶解氧的含量,合适的气水比为BAF系统的运行提供O2,同时促进老化生物膜的脱落;当气水比进一步增大时,BAF系统中的溶解氧过多导致BAF系统内稳定状态的破坏,进而降低污染物的去除效果,同时能耗较高;当气水比减小时,过低的溶解氧含量不能满足BAF系统中微生物的代谢,进而降低污染物的去除效果。综上可知,当HRT为4 h、气水比为3∶1时,O3-BAF系统对COD的去除效果最佳。
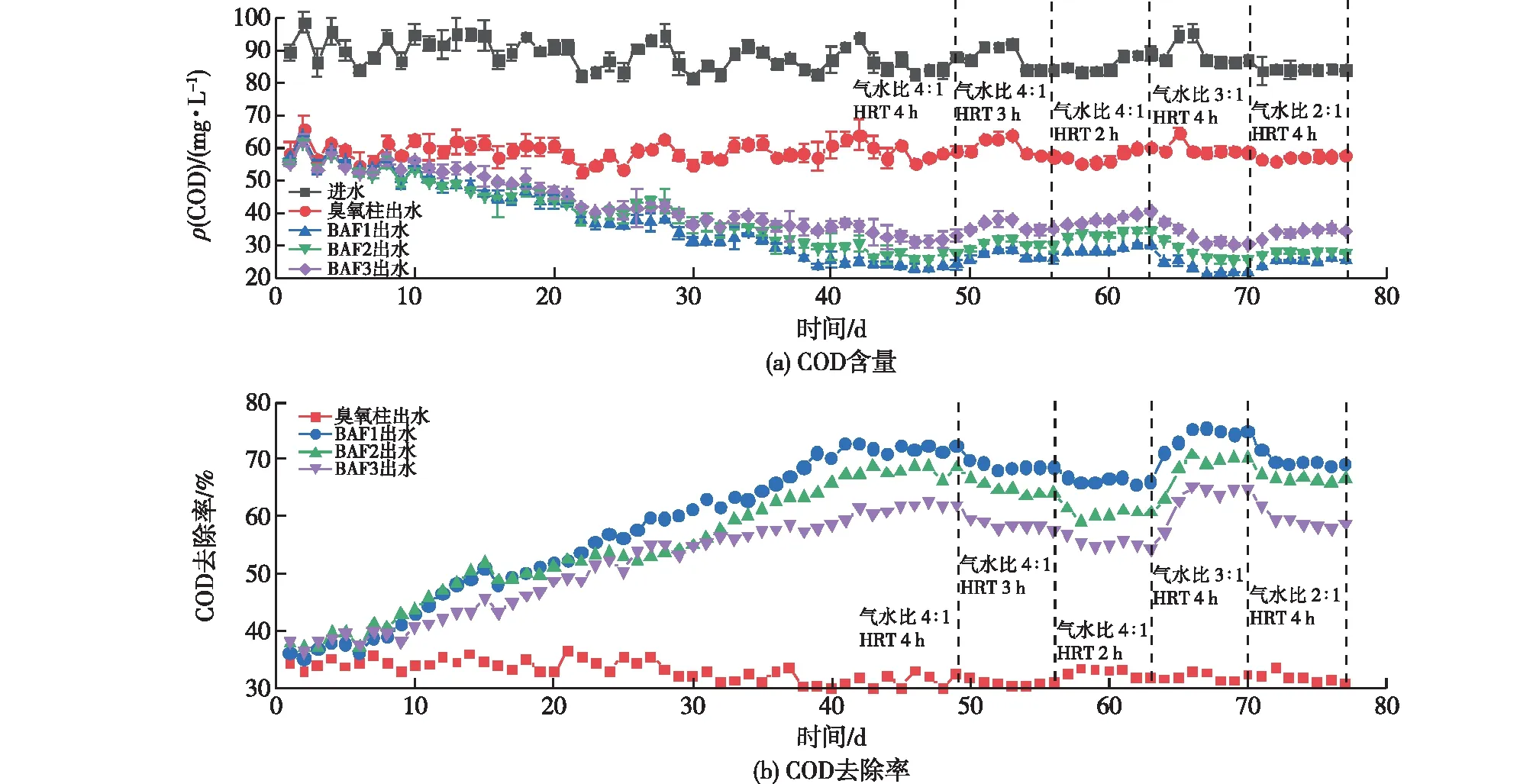
图2 COD含量和去除率的变化
2.1.2 NH3-N含量和去除率的变化
图3为NH3-N含量和去除率的变化曲线。由图3可知:BAF启动1~7 d内,NH3-N含量变化较大;随后3组O3-BAF系统NH3-N去除率皆稳定上升并达到稳定运行阶段;在40~77 d期间,出水NH3-N平均质量浓度都低于1.0 mg/L,NH3-N去除率都大于80%。O3-BAF1系统对NH3-N的去除效果相较于另外2组更好,这是由于投加的菌剂驯化良好,导致NH3-N去除效率提升。在49~77 d内,每隔7 d改变1次装置运行条件,3组O3-BAF系统对NH3-N去除率的影响都较小,说明O3-BAF对NH3-N的去除效果较为稳定且效果较好,不会因为条件的改变产生很大的变化,运行阶段不需要考虑专门针对NH3-N调整运行参数。
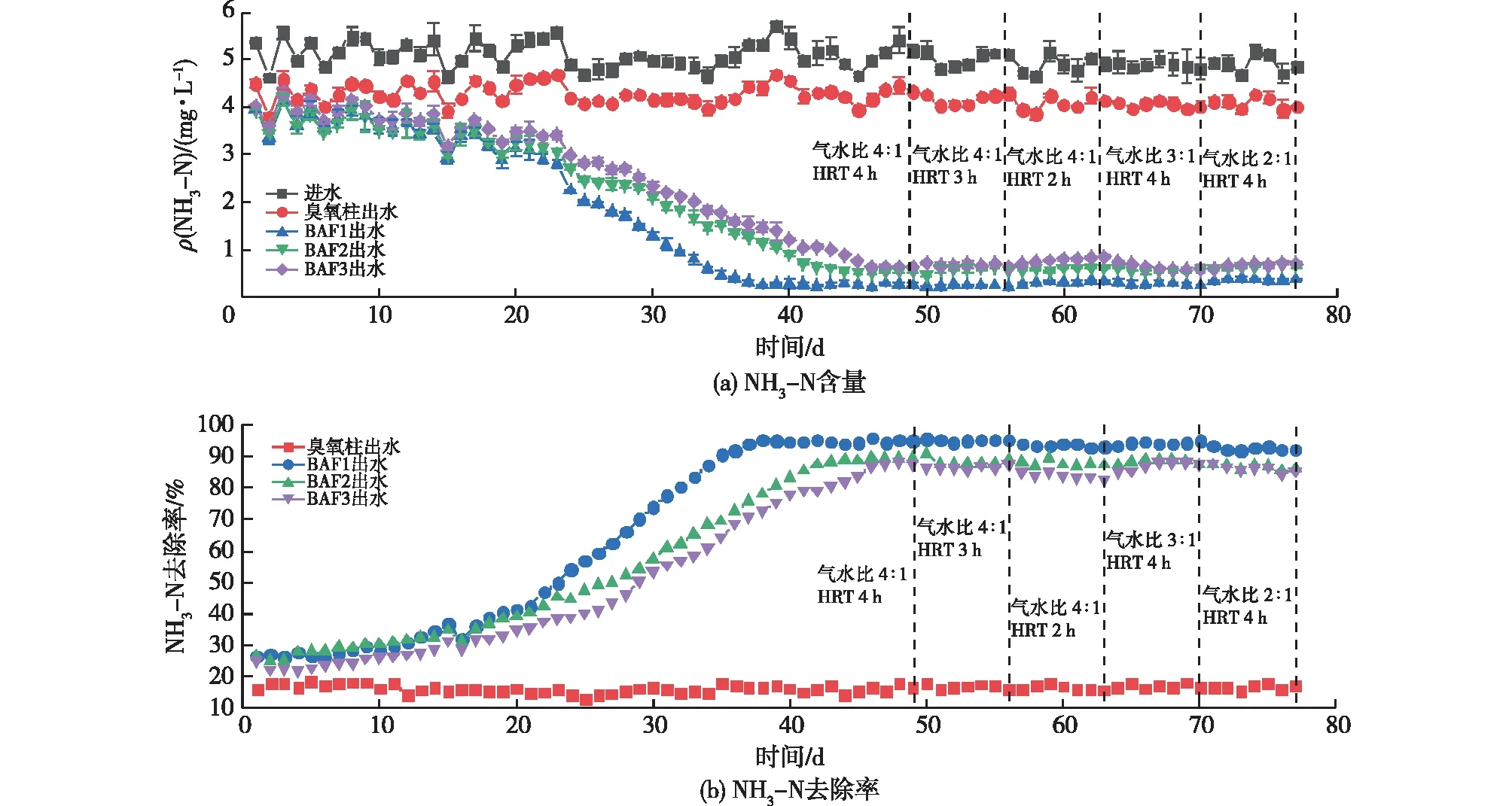
图3 NH3-N含量和去除率变化
2.1.3 TN含量和去除率的变化
图4为TN含量和去除率的变化曲线。由图4可知:BAF启动1~40 d内,3组O3-BAF系统皆处于驯化阶段,对TN的去除率均稳步上升;在40~45 d内,3组系统都达到稳定阶段,且在此稳定阶段,HRT和气水比对TN含量影响不大,O3-BAF1系统出水TN平均质量浓度为3.5 mg/L,平均去除率约为65%;其他2组出水TN平均质量浓度为4.2 mg/L,平均去除率仅约为54%,这是由于BAF1投加的菌剂提高了整体的脱氮效果。
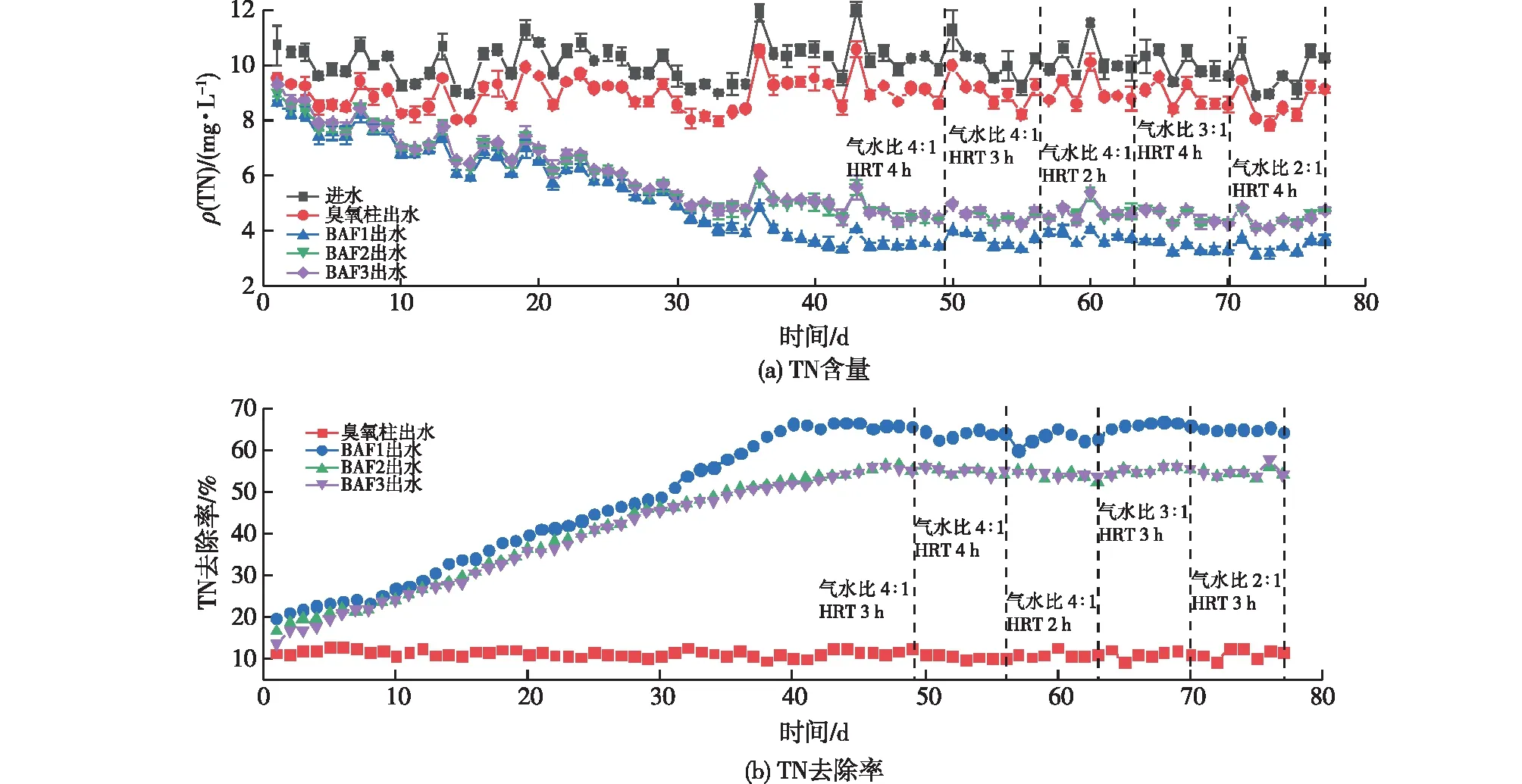
图4 TN含量和去除率的变化
2.1.4 TP含量和去除率的变化
图5为O3-BAF工艺出水TP含量和去除率的变化曲线。由图5可知:炼化二级出水中TP质量浓度约为0.07 mg/L,在驯化20 d时TP质量浓度接近0 mg/L。
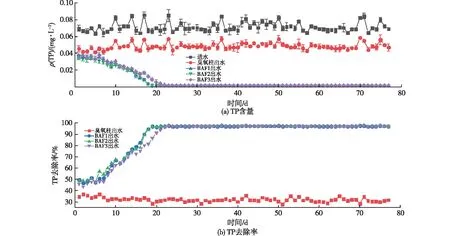
图5 TP含量和去除率变化
2.2 不同阶段进出水中有机物的三维荧光分析
不同阶段进出水中有机物的三维荧光分析如图6所示。由图6可知:炼化二级出水中的主要污染物为类色氨酸芳香族蛋白质物质(区域Ⅱ)和类溶解性微生物代谢产物类物质(区域Ⅳ);通过臭氧催化氧化和BAF处理后,3组O3-BAF系统出水的三维荧光图谱都发生了明显的变化,原本荧光强度最高的类色氨酸芳香族蛋白质峰(发射光谱:350 nm;激发光谱:230 nm)和第二高的类溶解性微生物代谢产物峰(发射光谱:350 nm;激发光谱:230 nm)均有着明显的减弱,说明这两类物质都得到了明显的去除;3组O3-BAF系统按总体峰强度从弱到强依次为O3-BAF1、O3-BAF2、O3-BAF3,按类色氨酸芳香族蛋白质峰强度从弱到强依次为O3-BAF1、O3-BAF2、O3-BAF3,按类溶解性微生物代谢产物峰强度从弱到强依次为O3-BAF2、O3-BAF1、O3-BAF3,造成O3-BAF1溶解性微生物代谢产物峰强度大于O3-BAF2的原因是BAF1中有更加丰富的菌群,导致类溶解性微生物代谢产物类物质去除效率略低于BAF2。

图6 三维荧光图谱
O3-BAF进出水中有机物三维荧光强度体积积分变化如图7所示。由图7可知:炼化二级出水、臭氧柱出水、3组BAF出水中有机物的三维荧光强度体积积分占比和组成相似,总体而言,按荧光强度体积积分占比由小到大依次为类色氨酸芳香族蛋白质物质(区域Ⅱ)、类富里酸物质(区域Ⅲ)、类溶解性微生物代谢产物类物质(区域Ⅳ)、类腐殖酸物质(区域Ⅴ)、类酪氨酸芳香族蛋白质物质(区域Ⅰ)。炼化二级出水的类色氨酸芳香族蛋白质物质主要为杂环化合物、含苯环的化合物等,约占水体荧光类有机物总量的46%。经过臭氧催化氧化后,区域Ⅱ和Ⅰ的占比分别上升到52%和7%,区域Ⅲ、Ⅳ和Ⅴ的占比皆有所下降;臭氧催化氧化出水经BAF的处理后,区域Ⅱ的占比皆有所上升,区域Ⅳ的占比皆进一步下降。
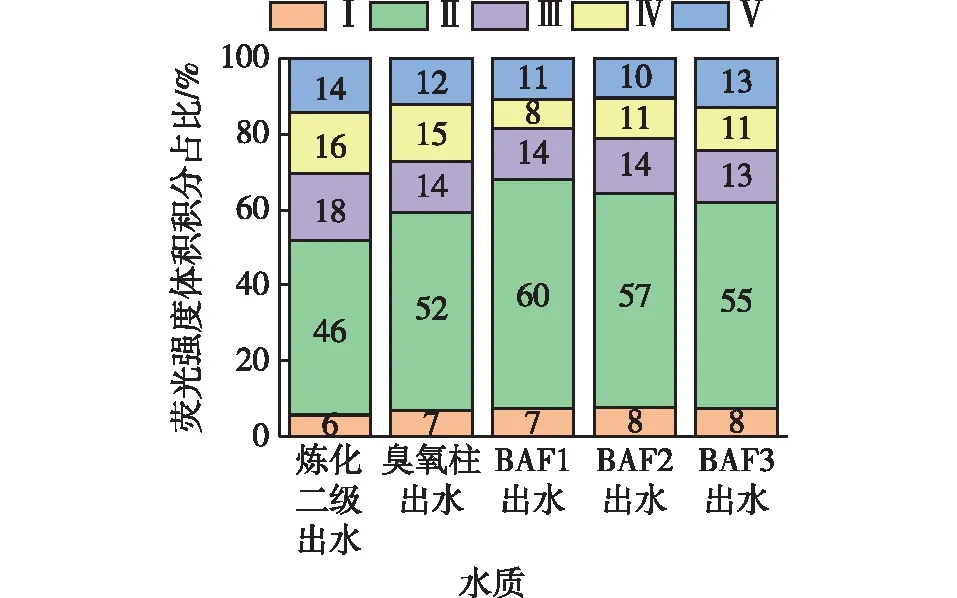
图7 O3-BAF进出水中有机物三维荧光强度体积积分变化
2.3 不同阶段进出水中有机物分子量分析结果
O3-BAF进出水中有机物的分子量变化如图8所示。由图8可知:炼化二级出水经过臭氧催化氧化后,废水中分子量1 000以下的有机物占比由原来的45%上升到71%,分子量3 500以上的有机物占比有所下降,大量难降解的大分子有机物被分解为易降解的小分子有机物,大部分易降解的小分子有机物在进入BAF系统后有利于被反应器内的微生物利用。3组BAF出水中分子量在1 000以下的有机物占比均有很大程度的下降,BAF1、BAF2和BAF3对应的占比分别下降到23%、28%和30%。分子量大于3 500的有机物占比明显增加,说明通过臭氧催化氧化的矿化作用,使炼化二级出水的矿化率有着明显的提升,提高了废水的可生化性[28]。
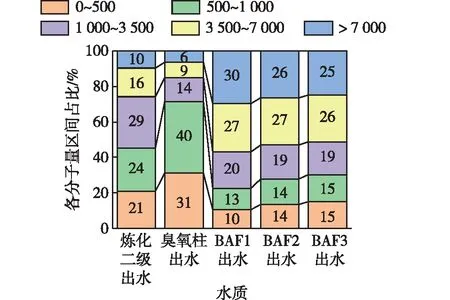
图8 O3-BAF进出水中有机物的分子量变化
2.4 微生物多样性分析
3组BAF系统中微生物的稀释曲线如图9所示,除了BAF3中微生物种类略低外,BAF1和BAF2的较为相似。驯化和稳定运行阶段3组BAF系统中微生物的维恩图如图10所示。由图10可知:驯化期间,BAF1、BAF2、BAF3分别有516、513、484种菌,其中331种是共同存在的;稳定运行阶段,BAF1、BAF2、BAF3分别有840、749、611种菌,其中446种是共同存在的;说明经过BAF处理,无论是菌种种类还是数量都有一定程度的增加,由于BAF1投加了微生物菌剂,在每个阶段都比其他2组的微生物数量大,更加丰富多样的微生物有利于废水的处理。
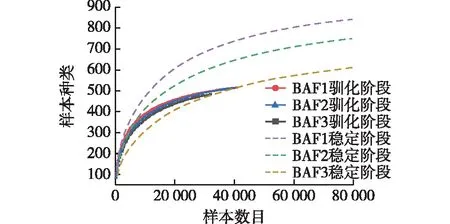
图9 驯化和稳定运行阶段3组BAF系统中微生物的稀释曲线
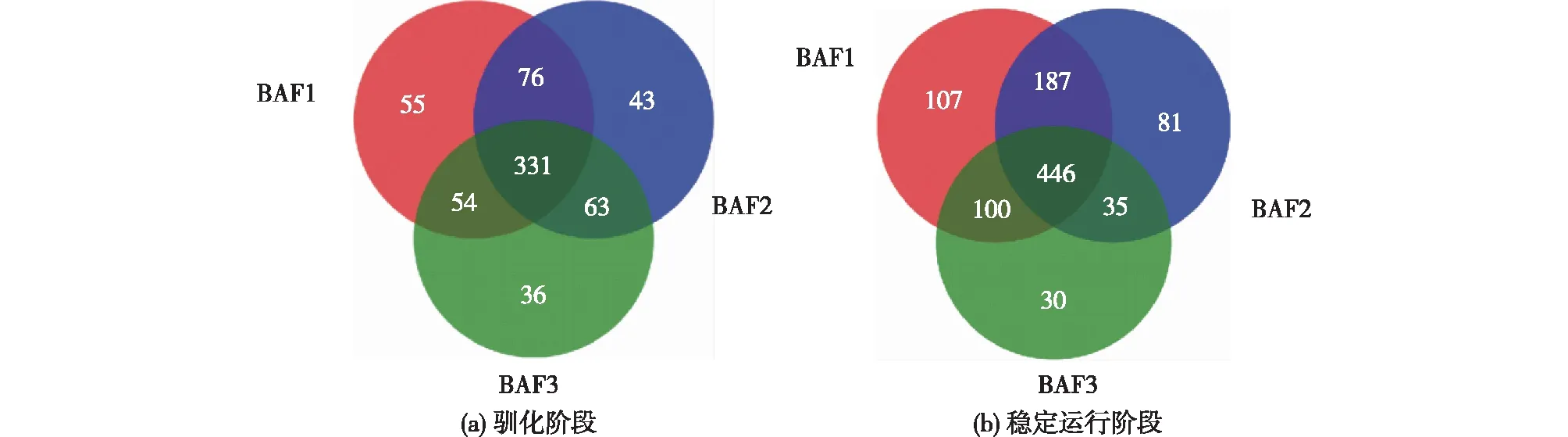
图10 驯化和稳定运行阶段3组BAF系统中微生物的维恩图
3组BAF系统门水平上的组成和属水平上的微生物组成如图11所示。由图11可知:3组BAF稳定运行期间微生物在门水平上主要细菌菌群包括变形菌门(Proteobacteria)、放线菌门(Actinobacteria)、拟杆菌门(Bacteroidetes)、绿弯菌门(Chloroflexi)等,其中,变形菌门、放线菌门、拟杆菌门和绿弯菌门是优势菌门,优势菌门的丰度总和占到微生物总量的80%以上。在3组的样品中丰度始终保持最高的是变形菌门,分别占48%、51%和54%,其中变形菌门和放线菌门作为主要菌种,在生物活动过程中能降解大量的有机物,去除氮和磷;拟杆菌门是严格的需氧化学有机营养体,可降解水中的很大部分有机物。BAF1驯化阶段投加菌剂使放线菌门所占比例约为其他2组的2倍左右,因此BAF1中COD和TN的去除率要优于其他2组。在属水平上,主要菌群包括鞘脂菌属(Sphingobium)、红球菌属(Rhodococcus)、氢噬菌属(Hydrogenophaga)、厌氧绳菌科某细菌(norank_f_Anaerolineaceae)等,鞘脂菌属能够降解低环多环芳烃等杂环化合物[29],红球菌属常见于炼油废水的处理[30],氢噬菌属于反硝化菌的一种[31]。相较于其他2组主要属组成,BAF1中产碱杆菌属(Alcaligenes)和甲基杆菌属(Methylobacterium)的丰度明显提高,说明投加的生物菌剂中的主要功能菌成功地生长于BAF1系统中,丰富了BAF1的微生物多样性,提升了其脱氮除碳的效率。

图11 3组BAF系统的微生物组成
3 结论
1)在气水比为3∶1、HRT为4 h时,BAF1对COD和NH3-N的处理效果达到最优,此时臭氧催化氧化和BAF1联用的出水COD质量浓度能够稳定在25 mg/L以下,NH3-N质量浓度稳定在0.5 mg/L以下,TN质量浓度稳定在4.0 mg/L以下,TP完全去除。
2)炼化二级出水中类色氨酸芳香族蛋白质物质(区域Ⅱ)和类溶解性微生物代谢产物类物质(区域Ⅳ)为主要污染物,经过臭氧催化氧化联合BAF工艺处理后,荧光强度有着明显的下降。
3)炼化二级出水经过臭氧催化氧化后,废水中分子量低于1 000的有机物占比由原来的45%上升到71%,经过BAF处理后下降到30%以下。
4)3组BAF稳定期的微生物组成整体相差不大,BAF1投加的主要功能菌成功生长在BAF1系统中,缩短了驯化时间,增加了微生物多样性和丰度,提升了系统脱氮除碳的效率,对相关工程项目的运行有良好的指导意义。
