直接法合成碳酸二甲酯的催化剂研究进展
2023-06-15魏振浩黄益平倪泽雨岳昌海黄晶晶孙玉玉冯能杰
魏振浩,黄益平,倪泽雨,岳昌海,黄晶晶,孙玉玉,吴 丹,冯能杰
(1.中建安装集团有限公司 工程研究院,江苏 南京 210023;2.南京工业大学 化工学院,江苏 南京 211800)
几十年来,天然气、煤炭、石油等传统化石燃料已广泛应用于交通、发电、化工和钢铁等行业,其需求量随着社会的发展进步而急剧增加,同时也导致CO2的排放量逐年猛增,据统计,2021 年世界CO2的排放总量高达363亿t。近年来,由CO2引发的温室效应对人类生存环境产生了越来越严重的威胁,在《巴黎协定》框架下,碳中和已成为各国应对气候变化行动的新标杆,控制和减少CO2的排放成为当今各国政府及科学界亟待解决的共同问题[1]。为了解决这一问题,科研人员加大了对CO2捕集利用与封存(CCUS)技术的研发和合作,CCUS技术也逐步驶入高速发展的快车道[2]。将CO2作为原料转化为高附加值的化学品被认为是CCUS的终极解决方案,其不仅能够实现碳减排,还能将CO2“变废为宝”,对解决温室效应并实现碳中和具有重要意义。CO2作为原料,具有来源丰富、价廉易得的优点,然而其难以活化的特性让资源化利用充满了挑战,目前一些有价值的化学品,如甲醇、水杨酸、碳酸二甲酯(DMC)、聚碳酸酯多元醇和尿素等,已成功通过CO2直接或间接地转化得到[1]。其中,只有少数技术在经济上是可行的且实现了商业化,如以CO2为原料生产尿素和聚碳酸酯多元醇,然而,大部分技术仅停留在实验阶段,未能实现工业化推广应用,如完全以CO2为碳源生产甲醇(CH3OH)和以CO2为原料直接合成DMC等[1]。据估计[1],到2050年,全球每年须通过以CO2为原料生产化学品的途径消耗约为6亿t CO2,目前CO2最大规模的利用途径是生产尿素,但是每年只能利用约1.4亿t CO2,可以看出,CO2资源化利用任重而道远。
由于DMC具有良好的化学反应性、高含氧量、低毒和优良的溶解性等独特性能,激发了巨大的市场需求。DMC是近年来备受关注的环保型绿色化学品,被形象地誉为有机合成领域的“新基块”[3]。DMC分子中含有—CH3、—OCH3、—OCO—、—CO—和—COOCH3官能团,因而可替代多种高毒性的化合物(如光气、硫酸二甲酯、氯甲酸甲酯等)进行羰基化、甲基化和甲氧基化等反应,广泛应用于医药、农药和材料合成等领域;DMC能以任何比例与有机溶剂-醇、酮、酯等互溶,可作为绿色溶剂在医药、胶黏剂、清洗和涂料等领域使用;最重要的是,DMC具有较高的含氧量(质量分数为53.3%),可替代甲基叔丁基醚(质量分数为18.2%)作为汽油和柴油添加剂,其能够有效地改善燃油的辛烷值,大幅降低燃油废气中的总碳氢化合物、CO和颗粒物[4]。以柴油添加剂的市场规模为例,全球每年约消耗5 300亿L柴油燃料,按照DMC添加量为4%计算,DMC的需求量约为1 680万t/a,同时DMC的使用也能够减少因化石燃料燃烧产生的CO2排放量(约为5 200万t/a)[1,4]。
综上所述,DMC从生产过程到作为产品使用均能发挥减碳作用,因此,以CO2为原料直接合成DMC被认为是最有应用前景和市场前景的研究领域。
迄今为止,DMC主要有3种成熟的生产工艺:光气法、甲醇氧化羰基化法和酯交换法。其中,光气法使用剧毒的光气为原料且产物中HCl气体会对设备造成严重腐蚀,因此该法已基本被淘汰[5]。甲醇氧化羰基化法是以CH3OH、CO和O2为反应物,以Cu、Pd、Co、Se等金属化合物作催化剂[6],在高压反应釜中制备DMC,该法主要存在设备腐蚀和爆炸危险等缺点。酯交换法先利用CO2和环氧乙烷(或环氧丙烷)进行环加成,再与CH3OH进行酯交换得到DMC,同时副产多元醇。该方法存在工艺复杂、精制能耗大且副产物难以处理等缺点[7]。
目前,直接法合成DMC处于实验阶段,以CO2和CH3OH为原料,直接反应制备DMC的反应式见式(1)。
CO2+2CH3OH→CH3OCOOCH3+H2O
(1)
该法避免使用剧毒反应原料,副产物只有水,原子利用率为100%,符合绿色化学理念。另外,该法不仅能够实现CO2资源化利用,还能极大地提高产品附加值,在碳资源利用和碳减排方面具有重要意义,符合可持续发展要求[8]。因此,该合成方法受到了国内外学者的广泛关注,具有极大的研究价值和深远的社会意义。
1 热力学研究
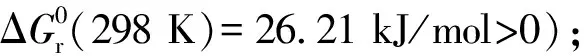
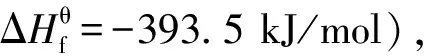
通过上述分析可知,CO2难以活化且该反应受热力学平衡限制是其面临的主要技术瓶颈,因此开发高活性催化剂,降低反应能垒,提高反应物活化分子数量,同时将产物不断移出反应体系以促进反应的正向进行,才能获得理想的反应转化率和DMC收率。
2 催化剂研究
目前,该反应的催化剂主要有离子液体催化剂、碳酸盐类催化剂、过渡金属氧化物催化剂、杂多酸催化剂和负载型催化剂。其中离子液体催化剂和碳酸盐类催化剂为均相催化剂,过渡金属氧化物催化剂、杂多酸催化剂和负载型催化剂为非均相催化剂。
2.1 离子液体催化剂
以咪唑类、季铵盐类或吡啶类阳离子为基础的离子液体催化剂[11-14],具有热稳定性好、难燃、不易挥发、毒性小、可调性好和易于产品纯化等优点,是近年来该反应中催化剂领域的研究热点之一。
赵浩岩[11]设计制备了一系列新型羟基功能化碱性离子液体,如二(或单)烷基二(或三)羟乙基氢氧化铵、氢氧化四羟乙基铵和氢氧化烷基羟乙基或二羟乙基咪唑等,并考察了它们在直接法合成DMC反应中的催化性能。结果发现,氢氧化二羟乙基甲基苄基铵的催化性能最优,在140 ℃和CO2压力3.0 MPa的条件下,反应3 h,甲醇转化率可达1.5%,DMC选择性为99.7%,该催化剂可以重复使用3次以上且催化活性几乎不变。在前人研究的基础上,他们根据自己的实验结果提出了碱性功能化离子液体的催化反应机制,如图1所示。CO2和CH3OH在强碱性OH-介质中容易被吸收和活化,形成活性CO2-和CH3O-阴离子;与此同时,通过配位作用在OH-阴离子、羟基、CO2与CH3OH分子之间形成了丰富的氢键网络,从而进一步促进CO2与 CH3OH分子中C—O与H—O键的极化;含有2个羟乙基的氢氧化二羟乙基甲基苄基铵具有较强的氢键酸性,在上述体系中很容易生成CH3+阳离子,即存在碱性位、氢键网络和氢键酸性的反应体系极大地促进了CH3OH直接羰基化反应的速控步骤;其结果是CH3O-进攻活性CO2-产生CH3COO-中间体,CH3COO-进一步与CH3+阳离子形成产物DMC。
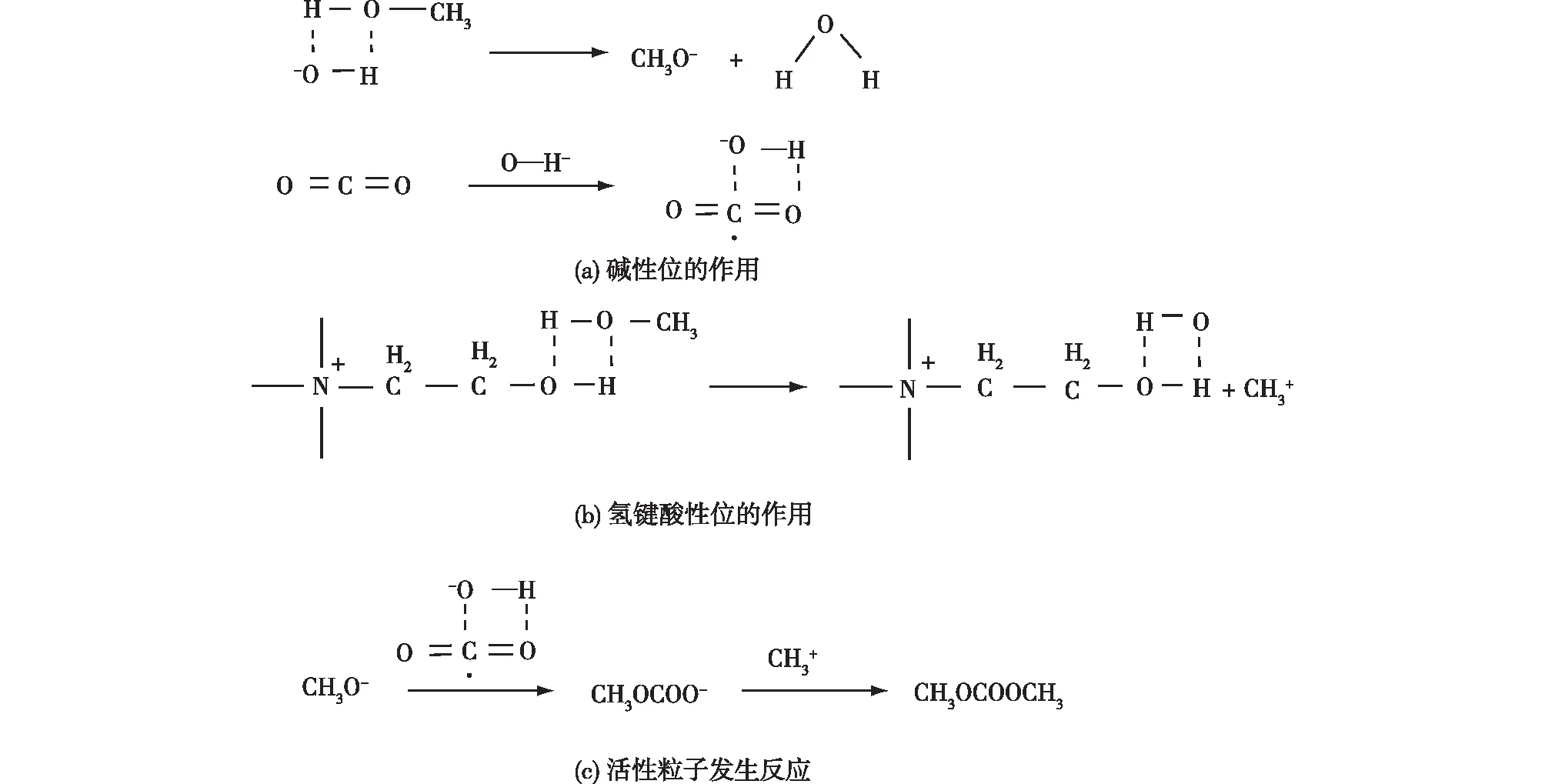
图1 碱性功能化离子液体的催化反应机制[11]
Tamboli等[12]将壳聚糖生物聚合物溶解在1-甲基-3-(甲基磺酰基)-1H-咪唑-3-鎓氯化物(ILs)中制得两元催化剂体系,该催化剂体系能够为CO2的捕获提供丰富的羟基(亲核基团)和胺基(CO2吸附位)。此外,壳聚糖能够改善CO2在催化体系中的溶解度并提高活性位点的利用率。结果表明,该催化体系能够有效地催化CO2和CH3OH生成DMC,在100 ℃和7.5 MPa的条件下,其甲醇转化率高达16.9%,DMC选择性可达98.7%。
为了在更温和的反应条件下获得理想的DMC产品收率,Liu等[13]设计制备了以1,8-二氮杂二环十一碳-7-烯(DBU)为活化剂、二溴甲烷(CH2Br2)和乙腈(CH3CN)为溶剂、离子液体1-乙基-3-甲基咪唑六氟磷酸盐(C6H11F6N2P)为促进剂的催化剂体系。探究了离子液体的作用机制并优化了直接法合成DMC的反应条件:离子液体通过促进反应中间体的转化以提高DMC的收率;在最优的反应条件下(60 ℃和0.25 MPa)反应12 h,甲醇转化率高达83%,DMC收率可达81%。
Zhao等[14]合成了咪唑碳酸氢离子液体([CnCmIm][HCO3])并用于催化CO2和CH3OH直接合成DMC。结果发现,以[C1C4Im][HCO3]为代表的离子液体在合成DMC过程中既作催化剂又作脱水剂,具有活性高、DMC选择性高和可循环使用的优点;在室温和CO2压力1.0 MPa的条件下,甲醇转化率高达74%,DMC选择性为97%。认为催化和脱水的协同作用是[CnCmIm][HCO3]具有优异甲醇转化性能的关键,据此提出了催化脱水反应机制,结果见图2。在离子液体中,[CnCmIm][HCO3]与咪唑羧酸氢(CnCmIm—CO2)之间存在平衡;CnCmIm—CO2可以促进CO2和CH3OH生成DMC和H2O;同时,CnCmIm—CO2也可以与H2O反应,促使平衡向生产DMC的方向进行。
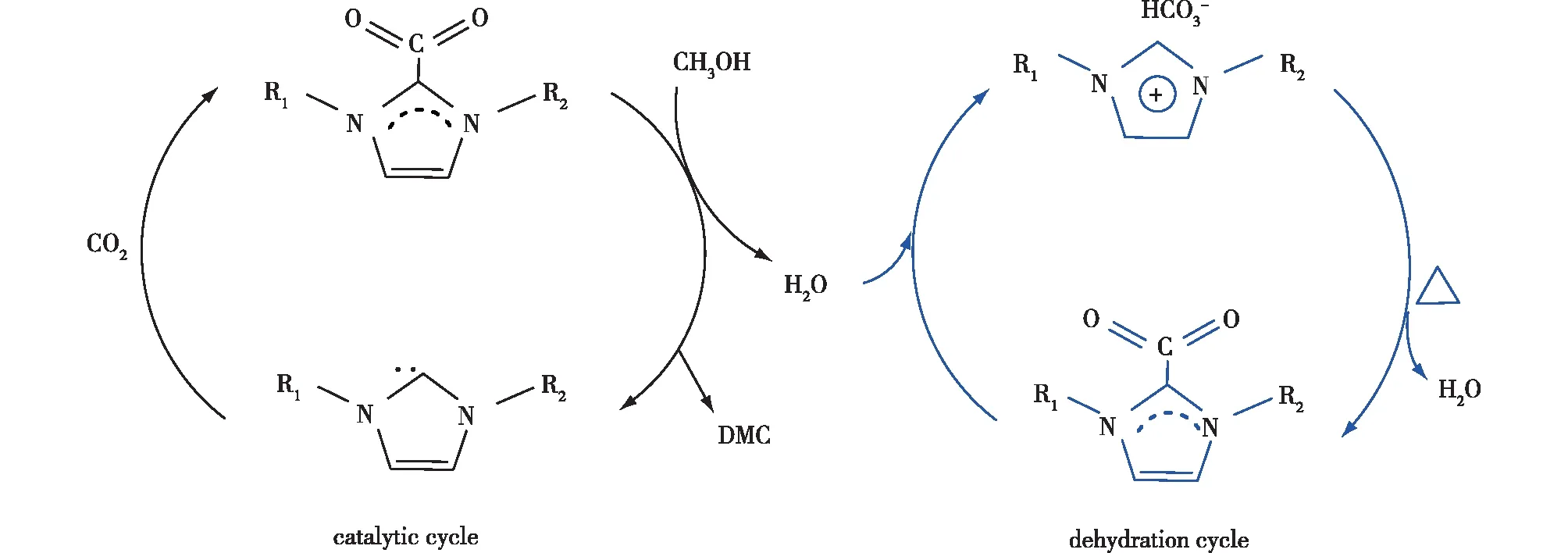
图2 [CnCmIm][HCO3]的催化脱水机制[14]
离子液体催化剂具有反应活性高、DMC选择性高(≥90%)且三废排放少的优点,然而其组成复杂(通常至少由两种组分组成)、价格昂贵且制备过程繁琐,因此一直未能实现工业化应用。近年来,兼具脱水作用的离子液体催化剂被开发,其甲醇转化率是普通离子液体催化剂的数十倍,具有更广阔的应用前景。
2.2 碳酸盐类催化剂
一些有机碱和无机碱可以催化CO2和CH3OH直接合成DMC,这类催化剂通常需要外部提供甲基(采用甲基化试剂,如卤代烃)。有机碱类有四甲基氢氧化铵[(CH3)4NOH]、三乙胺(Et3N)和三丁铵(Bu3N)等,无机碱类有K2CO3、Na2CO3、NaOH和K3PO4等。上述碱类催化剂中催化效果最好的是K2CO3,其通常需要CH3I 提供甲基才能发挥最佳的催化性能。K2CO3/CH3I的催化反应机制如图3所示[15]。首先,K2CO3活化CH3OH生成CH3O-;随后,CH3O-与CH3I 和CO2分别形成二甲醚(CH3OCH3)或[CH3OCH2]-;最终,[CH3OCH2]-与H+在K2CO3/CH3I环境下生成DMC和HI。
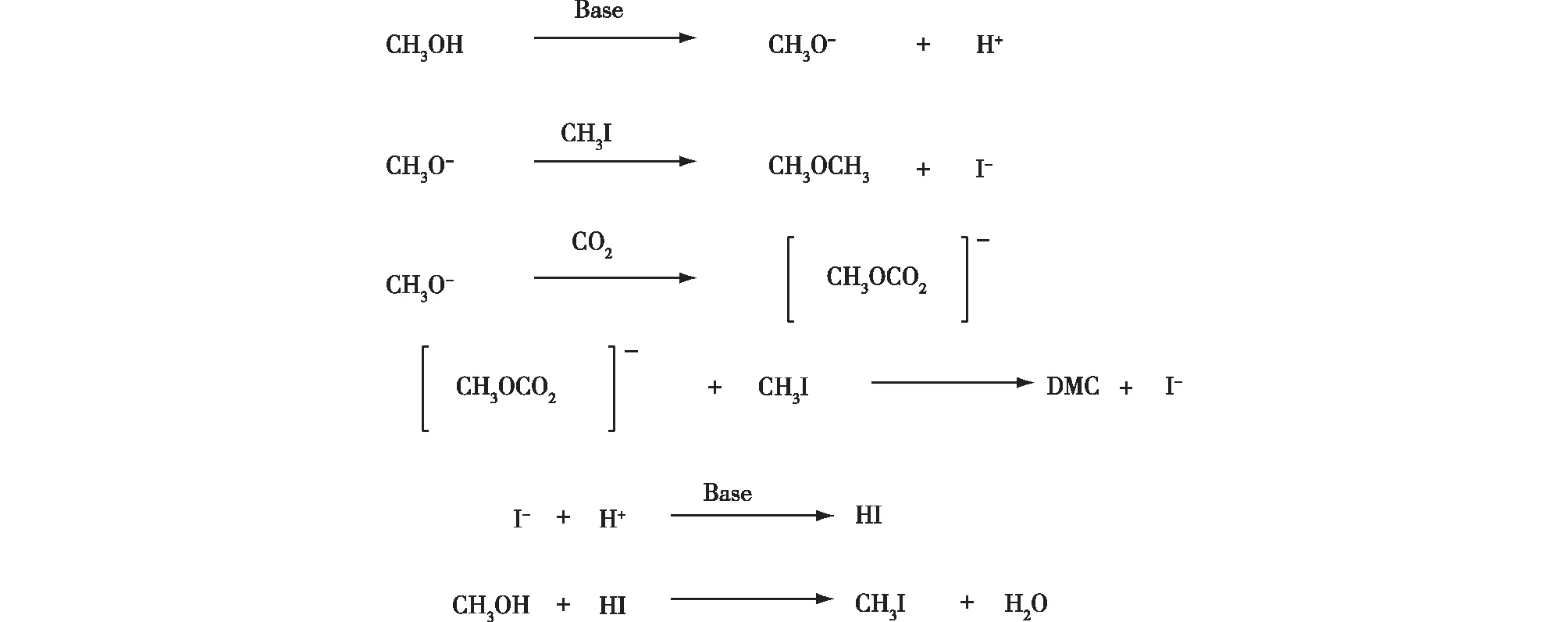
图3 K2CO3/CH3I的催化反应机制[15]
Fujita等[15]评估了一系列碱性催化剂(K2CO3、KHCO3、Na2CO3、Li2CO3、(NH4)2CO3、BaCO3和CaCO3)在直接法合成 DMC反应中的催化性能。他们发现K2CO3的催化性能最优,在70 ℃和CO2压力8 MPa的条件下,其甲醇转化率为4.1%,DMC选择性为81.8%。
Yang等[16]在CO2和CH3OH反应体系中加入氧化环己烯,考察了K2CO3的催化反应性能。研究表明,在150 ℃和CO2压力为2.6 MPa的条件下,甲醇转化率为16.2%,DMC选择性为38.7%。相较于Fujita等[15]使用的K2CO3-CH3I催化剂体系,K2CO3-氧化环乙烯催化剂的甲醇转化率提高了约4倍,但其DMC选择性却大幅降低。
上述催化剂体系的主要优点是采用价廉易得的K2CO3作为主催化剂,然而在反应过程中通常需要昂贵的CH3I协助。CH3I具有腐蚀性且在反应过程中被消耗,这无疑增加了催化剂的使用成本。另外,与其他类型催化剂相比,碱性催化剂的DMC选择性较低。
2.3 过渡金属氧化物催化剂
过渡金属氧化物能够提供Lewis酸碱活性位,因此CH3OH在邻位Lewis酸碱活性位的共同作用下吸附并活化,然后CO2插入反应,所得的单碳酸酯与在酸活性位上活化的CH3OH结合生成DMC。大量研究表明,在直接法合成 DMC反应中,CeO2和ZrO2为代表的催化剂表现出良好的活性和稳定性,是该反应领域研究最多且机制研究最充分的催化剂。
Tomishige等[17]以具有邻位酸碱活性中心的ZrO2为催化剂,在不添加任何助剂的情况下,由CO2和CH3OH直接合成DMC。他们研究了煅烧处理对ZrO2活性的影响,结果表明,在400 ℃下煅烧的ZrO2催化剂表现出最优的催化性能。认为ZrO2表面的单斜相和邻位酸碱活性中心对催化活性具有促进作用,但是平衡反应的存在致使甲醇转化率不高(只有约1%)。在后续的研究中[18],发现对ZrO2进行H3PO4改性能够明显提高甲醇转化率(约为4.5%),而且反应能在较低的温度(比未经H3PO4改性前降低了40 ℃)下进行。将这归因于弱Brønsted酸位(四方相Zr与P原子间相互作用而形成)对CH3OH的活化作用。
Wang等[19]用密度泛函理论(DFT)计算方法研究了CH3OH和CO2在立方(c)、四方(t)和单斜(m)ZrO2相上直接合成DMC的反应机制[20](图4)。结果表明,3种晶面的最优路径均为CH3OCO中间体路径,催化活性由大到小的顺序为:t-ZrO2、m-ZrO2、c-ZrO2。此外,ZrO2表面的酸碱性质和电子结构决定其催化活性,即表面 Lewis 酸碱性越强,带隙越小,催化活性越高。
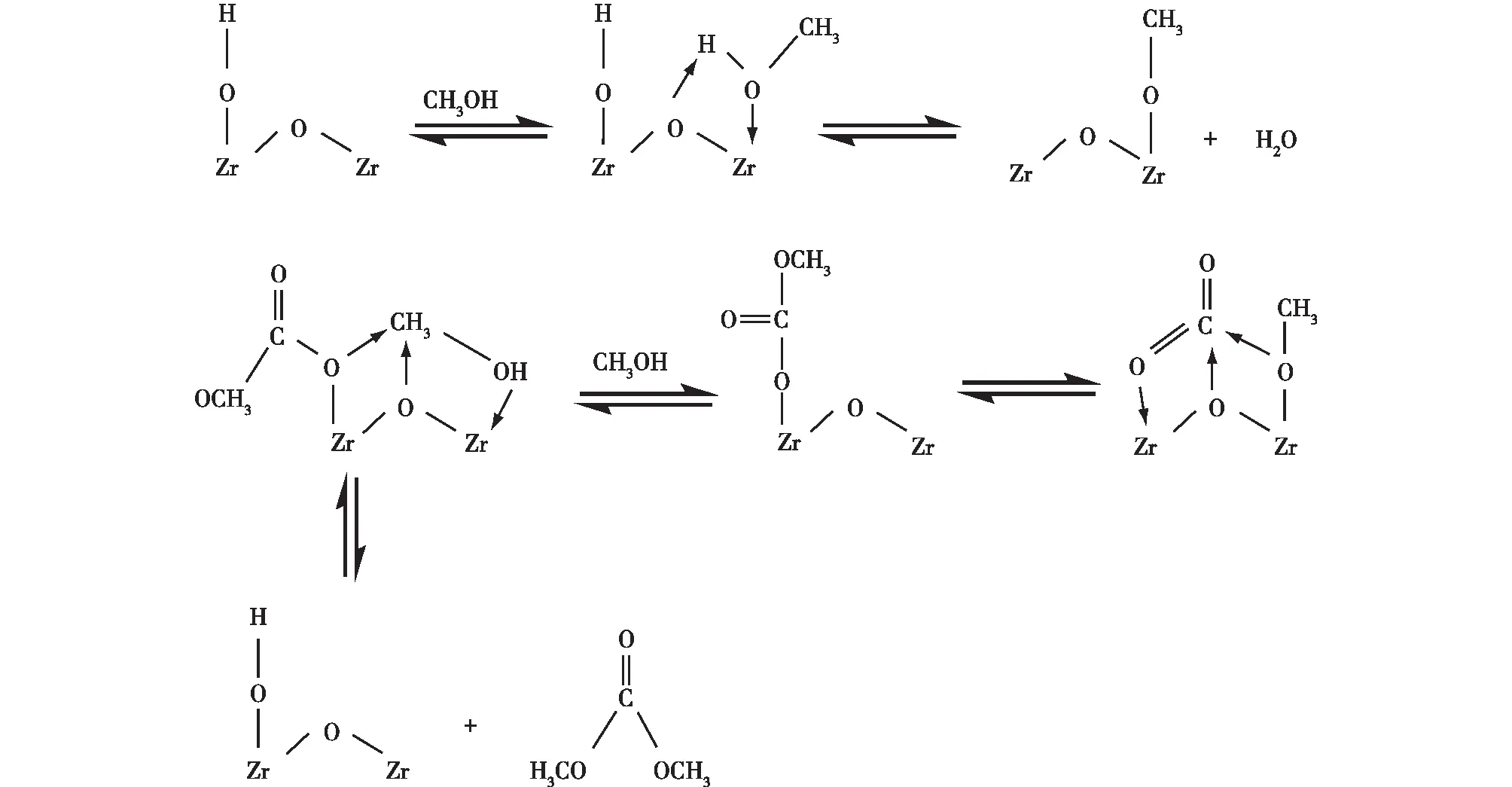
图4 ZrO2的催化反应机制[20]
Kumar等[21]以CeO2作催化剂、3A分子筛作脱水剂,考察了其在直接法合成DMC反应中的催化性能。在120 ℃和CO2压力15 MPa的条件下,甲醇转化率可达0.66%,DMC选择性为100%。为了提高CeO2的催化活性,Fu等[22]采用先进的溶剂热法合成了超一维CeO2纳米线,并考察了H2表面还原对其催化活性的影响。研究发现,经H2还原后,CeO2纳米线表面上产生了更多的酸碱位点,催化活性大大提高;500 ℃下还原的CeO2纳米线具有最高的催化活性,在120 ℃和CO2压力5 MPa的条件下,其甲醇转化率为1.97%,DMC选择性为100%。
CeO2与ZrO2相似,其独特的自生固溶性及丰富的酸碱位点与氧空位,赋予它优异的DMC选择性(大多情况下为100%),然而其催化效率低导致甲醇转化率不高。鉴于双金属氧化物催化剂的特殊氧空位催化机制和双金属界面协同效应,研究人员探索添加第二组分金属氧化物以制备双属氧化物催化剂,以期望实现催化剂性能的提升[23-25]。
Zheng等[26]对比研究了掺杂不同金属离子的M/ZrO2(M=Al、Ca、Ce、Pr和Y)催化剂的催化性能。结果表明,Ce掺杂的ZrO2催化剂具有最高的催化活性,在170 ℃和 17.5 MPa的条件下,Ce0.1Zr0.9O2纳米棒催化剂的甲醇转化率为0.64%,DMC选择性为100%;当采用3A分子筛作脱水剂时,该催化剂的甲醇转化率高达14.3%,选择性为100%。
刘斌[27]利用原位红外技术研究了CO2、CH3OH和DMC 在Zr0.1CeO2上的吸附行为,并以此提出表面催化反应机制,结果如图5所示。首先,CO2在Lewis酸碱对的作用下吸附活化形成双齿碳酸酯结构;然后,CH3OH在邻位Lewis酸位上吸附活化生成甲氧基吸附物种;随后,双齿碳酸酯与甲氧基反应生成甲基碳酸酯;最后,甲基碳酸酯与另一个CH3OH反应得到DMC。
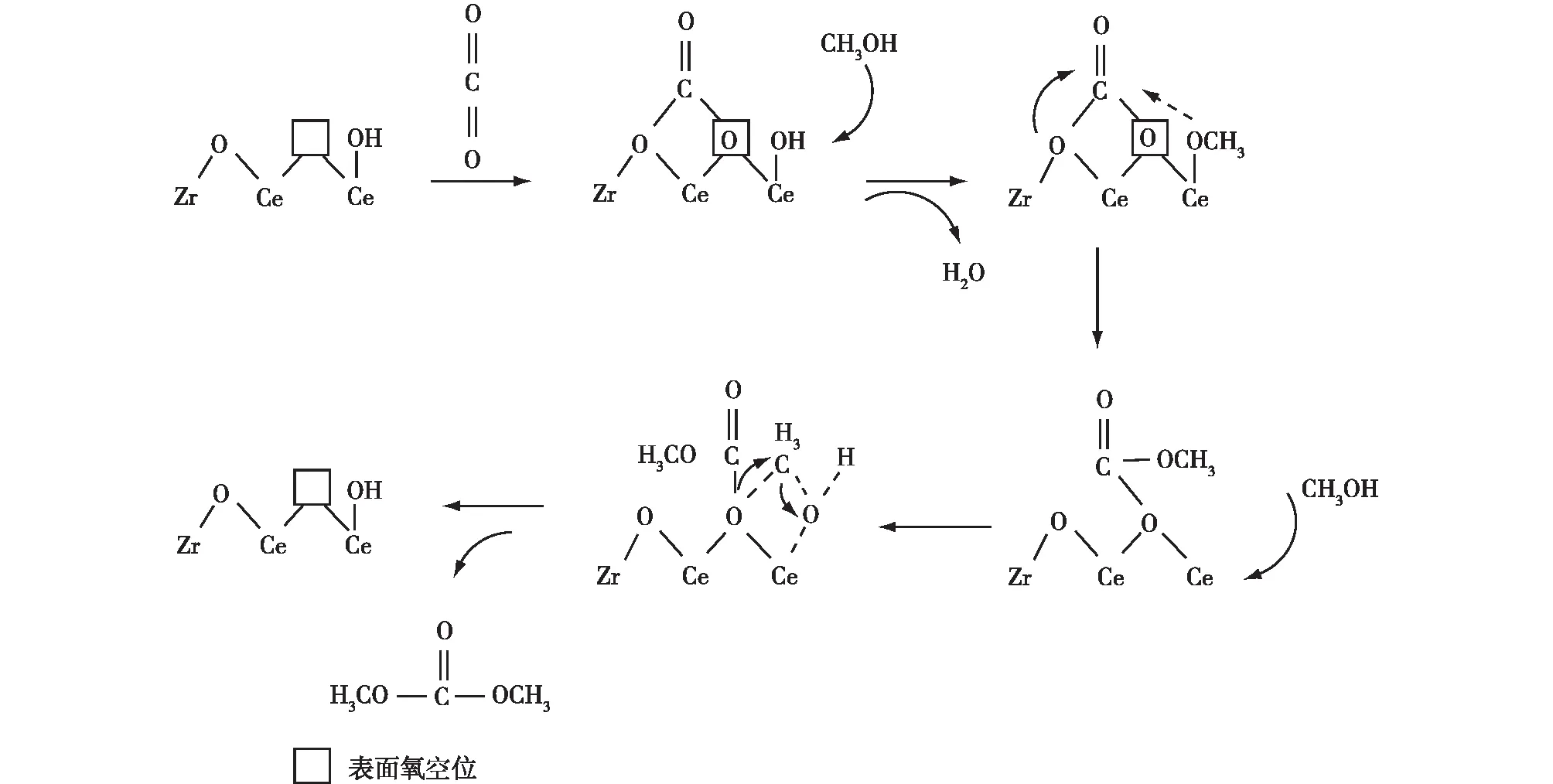
图5 Zr0.1CeO2的表面催化反应机制[27]
尽管研究者付出了不懈努力,在不添加脱水剂的情况下,铈锆氧化物催化剂的甲醇转化率仍然较低。不过,铈锆氧化物催化剂的DMC选择性可达100%,这能够使产品的分离提纯工艺得以简化。另外,铈锆氧化物催化剂的物化性质稳定,便于长期储存,具有较好的工业应用前景。
2.4 杂多酸催化剂
杂多酸是一种含氧桥的金属-氧簇化合,其特殊的笼状结构赋予它“假液相”行为,作为催化剂使用,可以有效地提高反应活性和产品选择性。杂多酸的酸强度通常高于一般的无机含氧酸,具有Brønsted酸位、氧化还原性和光电催化特性,因此在催化领域备受关注。
Chiang等[28]采用溶胶-凝胶法制备了H3PW12O40/ZrO2催化剂,并优化了直接法合成DMC的反应条件。结果发现,在最优的反应条件下(170 ℃和 5.0 MPa),其甲醇转化率为4.45%,DMC选择性为89.93%。
Aouissi等[29]以Co1.5PW12O40为催化剂、在气相和液相体系中进行了直接法合成DMC反应的对比研究。液相实验结果证实甲醇的转化率主要受压力影响,高压有利于DMC的生成,而DMC的选择性主要受温度影响。与液相实验结果不同,气相实验结果表明甲醇转化率和DMC选择性主要取决于温度,低温有利于DMC的生成。以Co1.5PW12O40为催化剂、在200 ℃和常压条件下,甲醇转化率为7.6%,DMC选择性为86.5%。
Chiang等[30]通过溶胶-凝胶法合成了Keggin型杂多酸H3PW12O40/Ce0.1Ti0.9O2催化剂,并研究了其在直接法合成DMC反应中的催化性能。结果表明,在170 ℃、5 MPa和CO2/N2体积流量比为1/7的条件下, 甲醇转化率为5.5%,DMC选择性为91.4%。此外,基于氧空位理论,他们提出H3PW12O40/Ce0.1Ti0.9O2的催化反应机制,这一反应机制从氧空位和晶体缺陷的角度解释了H3PW12O40/Ce0.1Ti0.9O2催化活性的本质,结果如图6所示。由于晶体结构缺陷,H3PW12O40/Ce0.1Ti0.9O2表面存在大量的氧空位,这些氧空位构成了催化反应所需的Lewis酸位;CO2分子的氧原子填充一个空位,随后CH3OH分子的氢原子填充另一个空位;然后,另一个CH3OH分子也被吸附到这些已填补空位的相邻氧空位上,形成一个大而不稳定的中间体;最后,中间体裂解生成DMC和水,并从表面的氧空位上解吸以完成一个催化循环。
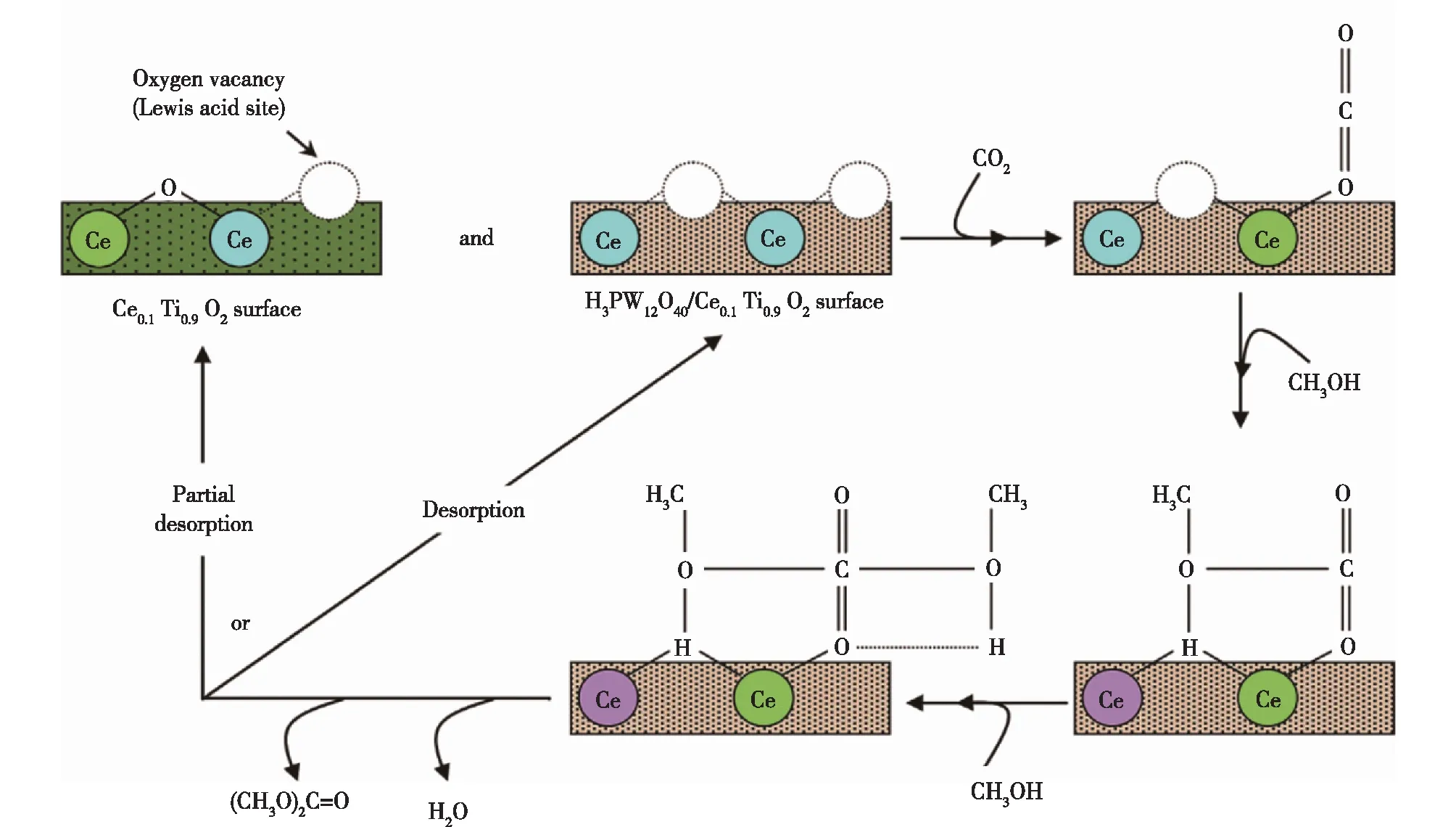
图6 H3PW12O40/Ce0.1Ti0.9O2的催化反应机制[30]
杂多酸催化剂通常由杂多酸和过渡金属氧化物组成,其中杂多酸起着促进剂的作用,它极大地改善了过渡金属氧化物的催化性能。杂多酸催化剂作为一种绿色催化剂,其表现出了令人满意的催化性能,丰富了直接法合成DMC反应的催化剂体系。
2.5 负载型催化剂
负载型催化剂易于从产物中分离,能够解决均相催化剂的分离回收及重复使用的问题,近年来成为该反应中非均相催化剂领域的研究热点。负载型催化剂的主要活性组分一般为双金属(如Cu-Ni),载体通常具有特殊的孔道结构或较高的比表面积,有利于活性组分的分散。
Zhang等[31]利用新型硫化法制备了Cu-Ni/V2O5-SiO2催化剂,并探究了反应温度、压力和金属负载量等对其催化性能的影响。研究表明,在最优反应条件下(140 ℃和1.2 MPa)、Cu-Ni(n(Cu)∶n(Ni)=2∶1)负载量为10%时,甲醇转化率为4.2%,DMC选择性为93.1%。
Bian等[32-34]以多壁碳纳米管、膨胀石墨和氧化石墨为载体,通过浸渍法制备了一系列碳载Cu-Ni催化剂。结果表明,膨胀石墨负载纳米Cu-Ni催化剂的性能最佳,在最优反应条件下(105 ℃和1.2 MPa),甲醇转化率高达9.0%,DMC选择性为88.0%。他们认为Cu、Ni和Cu-Ni合金的协同作用对CH3OH和CO2的活化发挥重要作用,Cu-Ni与载体之间的相互作用以及金属活性组分的良好分散有助于提高催化活性。
脱水能够有效地促进直接法合成DMC反应的正向进行,硅藻土[35]和3A分子筛[36]由于具有吸水性,也被作为载体或脱水剂用于该反应。Han等[35]研究表明,以3A分子筛作脱水剂,在最优反应条件(120 ℃、1.0 MPa)下,硅藻土负载Cu-Ni-K2O的催化性能最佳,其甲醇转化率为8%,DMC选择性为88%,催化剂寿命长达13 h。
另外,镁铝类水滑石由于具有丰富的酸碱活性位和脱水功能,也被用于直接法合成DMC反应。Stoian等[37]的研究表明,硅溶胶固载镁铝类水滑石是一种新型高效、可用于直接法合成DMC的多相催化剂;在130 ℃和1.0 MPa的条件下,甲醇转化率高达15.9%,DMC选择性可达99.9%。
近年来,MOFs(金属-有机框架)结构材料因其高比表面积和孔隙率以及优异的热稳定性而备受关注。Xuan等[38]发现UiO-66(锆基金属有机框架材料)可以催化CO2和CH3OH直接合成DMC,而且在UiO-66合成过程中三氟乙酸的添加量对其催化性能影响显著。研究结果表明,以UiO-66-24(24为三氟乙酸/对苯二甲酸的摩尔比)为催化剂、在120 ℃和CO2/CH3OH体积流量比为1/1的条件下反应1 h,甲醇转化率为0.084%,DMC选择性为100%。为了提高DMC收率,他们又制备了一系列锆基金属有机框架材料MOF-808-X(X为八水氧氯化锆/均苯三甲酸的摩尔比),并研究了MOF-808-X催化剂在直接法合成DMC反应中的结构-性质-性能关系[39]。研究表明,MOF-808-X的催化活性随比表面积和酸碱活性位数量的增大而增大;以MOF-808-4为催化剂、在140 ℃和CO2压力12 MPa的条件下,反应48 h,甲醇转化率最高可达21.5%,DMC选择性为100%。此外,他们借助原位红外技术提出了MOF-808-4的催化反应机制,如图7所示。1)CH3OH在MOF-808-4的Lewis酸位上吸附活化形成Zr—OCH3并释放出H原子,随后H原子立即与Zr—OH反应形成H2O;另外,CH3OH在Lewis酸位上吸附活化也可生成CH3+,CH3+吸附在Lewis碱位上形成桥接的甲氧基(Zr—(OCH3)—Zr),CH3OH解离的OH吸附在Lewis酸位上形成Zr—OH。2)CO2在Lewis碱位上吸附并插入到Zr—OCH3形成中间体Zr—OCOOCH3。3)最后,中间体Zr—OCOOCH3与Zr—(OCH3)—Zr反应生成DMC并解离出CH3+。

图7 MOF-808-4的催化反应机制[39]
近年来,研究人员在设计负载型催化剂时,通常选择兼具脱水功能的载体,因此,相较于其他类型催化剂,负载型催化剂在直接法合成DMC反应中展现了更好的催化性能。然而,负载型催化剂的活性金属组分容易流失,从而导致其催化稳定性较差,这制约了其工业应用。
3 展望
由CO2引发的温室效应严重威胁着地球环境,世界各国都积极致力于控制和减少CO2的排放。DMC广泛应用于有机合成、绿色溶剂和燃油添加剂等领域,是近年来备受市场追捧的环保型绿色化学品。以廉价丰富的CO2为原料直接合成DMC是最符合绿色化学和可持续发展的工艺路线,在碳资源利用和碳减排方面具有重要意义。通过研发人员的不断探索,近年来催化剂体系持续更新迭代,DMC的收率也在不断提高,然而,到目前为止,仍未有一种有效的催化剂体系能够满足工业化要求。笔者认为,加强催化剂的研发,实现CO2和CH3OH高效稳定地转化,大幅提高DMC的收率,仍是现阶段研究的重点任务:① 以活性高且性能稳定的金属氧化物作为催化剂的主要活性组分,值得一提的是,金属氧化物的表面应具有丰富的酸碱位点与氧空位;② 选择合适的载体,载体通常具有较大的比表面积和丰富的孔道,以促进活性组分的分散,提高催化效率;③ 探索对催化剂进行改性或添加助剂,实现催化剂性能的最大化。另外,通过对直接法合成DMC催化剂的研究进展综述可以发现,离子液体、碳酸盐类、过渡金属氧化物、杂多酸和负载型催化剂与脱水剂进行耦合后均能得到良好的催化性能,因此,开发经济的原位脱水剂或脱水工艺,进一步对催化剂的性能进行耦合增强,或许是直接法合成DMC工业化实现突破的重要途径。
