SNRIs类药物在神经病理性疼痛中的临床应用进展*
2023-06-02赵丽玲黄彦珊王利刘书豪王婧
赵丽玲,黄彦珊,王利,刘书豪,王婧
(1.上海交通大学医学院附属第六人民医院药剂科,上海 200233;2.河南省胸科医院,郑州大学附属胸科医院药学部,郑州 450000;3.广东省江门市五邑中医院药学部,江门 529000;4.济宁医学院附属医院药学部,济宁 272007;5.南昌大学第一附属医院药学部,南昌 330006)
神经病理性疼痛(neuropathic pain,NP)定义为由躯体感觉系统的损害或疾病导致的疼痛,其发病率为7%~10%[1]。NP发病机制复杂,主要包括外周敏化、中枢敏化、离子通道改变、下行疼痛抑制系统失能等。其治疗方式包括药物治疗、物理治疗、疼痛心理疗法和介入治疗(含手术干预)等,其中主要治疗药物包括5羟色胺(5-HT)和去甲肾上腺素(NE)再摄取抑制剂(serotonin and norepinephrine reuptake inhibitors,SNRIs)、阻断多种离子通道同时抑制 5-HT和NE再摄取的三环类抗抑郁药物(tricyclic antidepressants,TCAs)、调节钙离子(Ca2+)通道的抗惊厥药物、阻断钠离子(Na+)通道的抗癫痫药物、阿片类药物等。基于疼痛与抑郁的共病机制,SNRIs类抗抑郁药物在我国、加拿大、英国、欧洲等NP相关指南共识中均被推荐为一线治疗药物[2-4]。其特异性相对较高,与传统抗抑郁药TCAs比较,不作用于毒蕈碱和组胺受体等,从而减少不良反应的发生,提高患者耐受性,是NP伴情绪障碍患者的更佳选择[5]。临床常见药物有:度洛西汀、文拉法辛和米那普仑、左旋米那普仑等,前两者临床应用较为广泛,在NP治疗中发挥重要作用。
1 SNRIs类药物在NP中的作用机制
1.1NP与抑郁的共病性 NP临床表现复杂多样,含自发和诱发症状,病程一般较长(多数>3个月),大多在原发致痛因素消除后仍存留疼痛,且通常伴有情感障碍。研究显示,在糖尿病性NP患者中,焦虑或抑郁的发生率为32%~76%[6]。BAIR等[7]一项纳入56项研究的荟萃分析显示,约65%抑郁症患者伴随疼痛症状。疼痛和抑郁不仅高共存,且互相促进。糖尿病性NP,是处于长期应激反应下的慢性疼痛,通过多种途径诱导抑郁症状,如诱导中枢、外周炎症反应,激活氧化/硝化应激通路、诱导下丘脑-垂体-肾上腺(HPA)轴亢进、神经元变性、色氨酸代谢途径改变等[8]。抑郁的发生与神经内分泌、遗传、心理等因素诱发中枢5-HT、NE、多巴胺(DA)、乙酰胆碱及其他神经递质含量降低及其受体功能下调有关[9],而5-HT和NE为下行疼痛调节系统中重要物质,其功能失调使得大脑接受放大的疼痛信号,导致疼痛感知。疼痛与抑郁的共病现象提示SNRIs类药物为伴有情绪障碍的NP患者的更优选择。
1.2SNRIs类药物治疗NP的作用机制 SNRIs类药物治疗NP的作用机制有:①激活导水管周围灰质区的内啡肽和中缝核的5-HT镇痛系统。如激活5-HT1A受体,抑制5-HT神经元活性,发挥镇痛作用;或与5-HT2A受体结合,导致抑制性神经递质γ-氨基丁酸(GABA)增多,发挥镇痛作用[10]。②激活蓝斑核的NE镇痛系统。研究显示,双重抑制剂如SNRIs类和TCAs类药物镇痛效果强于选择性SSRIs等类药物,提示在镇痛方面NE系统的作用比 5-HT更为重要[11]。LI等[12]报道文拉法辛用奥沙利铂诱导的NP有较强缓解作用,其中NE对冷触痛和机械性异位痛均有调节作用,而5-HT仅参与对机械性异位痛的调节。主要通过选择性激活脊髓α2-肾上腺素能受体,而非α1-肾上腺素能受体来缓解冷触痛,并通过选择性激活α2-肾上腺素能和5-HT3受体,而非α1-肾上腺素能和5-HT1,2受体缓解机械异位痛[12]。4种常见SNRIs类药物药效强度和对5-HT及NE转运蛋白亲和力略有差异,文拉法辛、度洛西汀和米那普仑对5-HT转运蛋白结合力略优于对NE转运蛋白的结合力。比较而言,文拉法辛为相对较弱的SNRIs,与两种转运蛋白的结合差异略大[1],疗效具有明显的剂量依赖性,小剂量时主要与5-HT转运蛋白结合;度洛西汀与米那普仑药效强于文拉法辛,对二者转运蛋白亲和力相当;与其他优先抑制5-HT再摄取的SNRIs类药物有很大不同,左旋米那普仑对NE转运蛋白亲和力是对5-HT转运蛋白亲和力的2倍[13-14]。GAUTAM等[15]证明,当左旋米那普仑剂量≥40 mg时,抑制NE的再摄取率>90%,5-HT>80%,而度洛西汀、文拉法辛则需要更大剂量。③直接或间接影响内源性阿片系统等。KREMER等[16]研究表明度洛西汀长期应用时可通过激活外周阿片δ受体,而急性作用时则同时激活中枢阿片μ和δ受体发挥镇痛作用。同时急性注射阿片受体拮抗剂纳洛酮可以诱导长期用度洛西汀治疗的异常性疼痛的复发。4种药物靶点作用强度、药动学及代谢特点[1,13-16]见表1。

表1 SNRIs类药物特点
2 SNRIs类药物在NP中的临床应用
2.1SNRIs类药物在NP中的临床应用现状 2015年,国际疼痛学会进行一项囊括229项随机、双盲、对照试验的荟萃分析,该分析强烈建议SNRIs类药物、TCAs类药物等作为NP一线治疗用药。该研究共纳入SNRIs类药物研究13项,9项度洛西汀(20~120 mg·d-1,7项阳性)和4项文拉法辛(2项阳性,150~225 mg·d-1,2项阴性,但剂量较小),经评价证据质量高[3-4]。临床实践证明,SNRIs类药物治疗NP的剂量略小于抗抑郁剂量且起效较快,不良反应小,安全性较高。不同指南推荐SNRIs类药物治疗NP剂量[2,17-19]见表2。JHA等[20]研究起始剂量20~30 mg·d-1的度洛西汀,患者疼痛评分仍明显降低,提示低于抗抑郁剂量的度洛西汀仍发挥较好的镇痛作用。FARSHCHIAN等[21]研究文拉法辛用于治疗化疗诱导的周围神经病变时,维持剂量37.5 mg·d-1,持续1个月,该剂量远低于抗抑郁治疗剂量(75~225 mg·d-1),结果显示与安慰药比较,文拉法辛明显降低疼痛评分。考虑到疼痛与抑郁的共病性及影响药物疗效的外部因素,使用低于抗抑郁剂量的SNRIs类药物治疗NP仍有较好疗效,可能与临床医生和药师对患者的用药宣教和心理干预有较大关系。ENOMOTO等[22]经线性回归分析,证明度洛西汀治疗伴有疼痛的重度抑郁症患者时,起始2周对疼痛的直接改善作用大于通过改善抑郁症状所产生的间接影响,此结论与URITS等[23]认为疼痛改善独立于情绪改善的结论保持一致,再次证明SNRIs类药物具有独立于抗抑郁作用之外的镇痛作用。
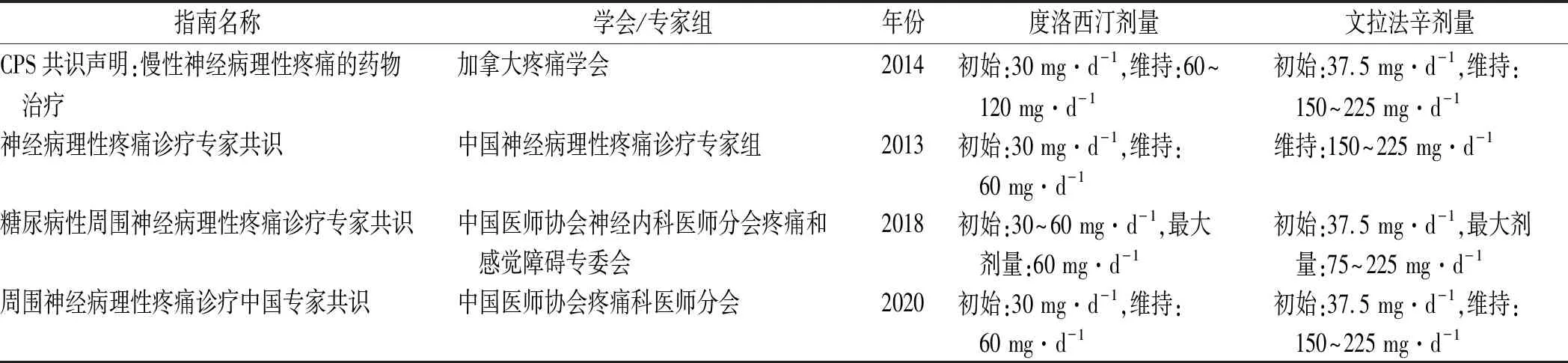
表2 不同指南推荐度洛西汀、文拉法辛治疗NP剂量
SNRIs类药物传统上通常用于抑郁症的治疗,不同SNRIs类药物在我国国家药品监督管理局(NMPA)和美国食品药品管理局(FDA)获批适应证略有差异,其中仅度洛西汀被FDA批准用于糖尿病周围神经痛治疗。4种常见SNRIs类药物获批适应证见表3。由表3可见,SNRIs类药物用于NP大多属超说明书用药。因医学研究的不断探索进展,基于循证医学证据制定的药品说明书通常滞后于临床实践研究。《中华人民共和国医师法》第二十九条指出:在尚无有效或者更好治疗手段等特殊情况下,医师取得患者明确知情同意后,可以采用药品说明书中未明确但具有循证医学证据的药品用法实施治疗[24]。因此,在临床应用时,应对患者进行充分的知情告知,规避法律风险。
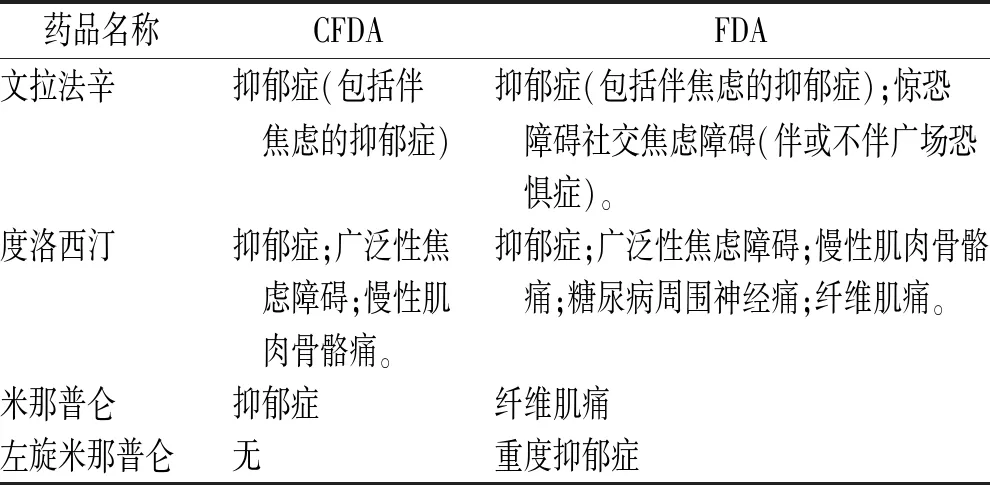
表3 SNRIs类药物在我国与FDA获批适应证
2.2SNRIs类药物在NP中的具体临床应用
2.2.1SNRIs类药物在化疗诱导的周围神经病理性疼痛(chemotherapy-induced peripheral neurotoxicity,CIPN)中的应用 化疗作为恶性肿瘤常用治疗手段,大脑和脊髓神经损伤导致的周围神经病变为其副作用之一,患者伴有瘙痒、麻木、灼痛、异常感觉等主诉[25-26]。具神经毒性的常用化疗药物有奥沙利铂、顺铂、氟尿嘧啶、长春新碱、紫杉醇、甲氨蝶呤和长春瑞滨等[27]。FARSHCHIAN等[21]研究对比度洛西汀和文拉法辛对于CIPN疗效差异,结果表明治疗第2周和第4周,度洛西汀和文拉法辛组患者运动神经、颅神经、感觉神经等病变及NP等级与治疗前比较,各神经病变级别及疼痛级别显著下降,且差异有统计学意义。SMITH等[28]发现,与紫杉醇诱导CIPN比较,奥沙利铂诱导的CIPN更可能受益于度洛西汀的使用,这也表明度洛西汀的作用机制可能与奥沙利铂诱导的CIPN特定的分子机制密切相关,具体机制有待深入研究。
目前多数指南推荐度洛西汀等作为CIPN一线用药,部分指南推荐文拉法辛为二线治疗药物[29-30],基于当时药品价格,度洛西汀明显高于文拉法辛,故研究者建议将文拉法辛作为一线用药。考虑目前度洛西汀和文拉法辛均被纳入国家药品集中采购目录,其价格不再是影响患者选择药品的限制因素。此外,如FARSHCHIAN等[21]研究表明文拉法辛在37.5 mg·d-1的小剂量下对疼痛改善不如度洛西汀30 mg·d-1,可能是此剂量下文拉法辛对5-HT转运体的亲和力较高,而对NE转运体的亲和力相对较低,这也是二者存在疗效差异潜在原因,但该结论还需进一步临床研究证实。
2.2.2SNRIs类药物在糖尿病周围神经病理性疼痛(painful diabetic neuropathy,PDN)中的应用 约1/2长期糖尿病患者会出现神经病变,约1/3患者伴有PDN,其发病机制尚不确定[31-32]。文拉法辛是疼痛治疗中研究最多的抗抑郁药物之一,研究表明其可以有效治疗PDN[33],但仅有度洛西汀和普瑞巴林被FDA批准用于PDN[34]。RAZAZIAN等[35]研究证明文拉法辛对PDN有中等镇痛疗效,在降低工作和睡眠干扰分数方面,文拉法辛疗效低于普瑞巴林,在改善情绪和生活质量方面文拉法辛优于卡马西平。HOSSAIN等[36]对比分析度洛西汀与阿米替林、普瑞巴林对PDN的疗效差异,结果显示:度洛西汀与安慰剂和普瑞巴林比较对PDN疗效明显,与阿米替林比较疼痛改善无明显差异。由于PDN多发于老年患者,TCAs药物相关的α-肾上腺素能阻滞、抗胆碱能和心脏传导效应对患者影响较大,安全性欠佳[33],SNRIs类药物由于其相对特异性,安全性略好。
2.2.3SNRIs类药物在幻肢痛(phantom limb pain,PLP)及其他NP中的应用 PLP在截肢患者中出现的概率为60%~80%。目前发现度洛西汀、文拉法辛、米那普仑用于PLP的研究多为临床个案报道,研究结果均显示较好疗效,但由于纳入人群较少,其有效性仍需考证[37-39]。SNRIs类药物除对以上几种NP有效外,对于治疗术后慢性疼痛、慢性腰痛、脊髓损伤性疼痛等亦有报道。度洛西汀对慢性腰痛有轻度缓解作用,对功能改善、情绪调节和生活质量改善具有中等效果。WENG等[40]荟萃分析表明,度洛西汀能够降低慢性腰痛患者的BPI-24 h平均疼痛评分,对疼痛的有效缓解率为50%。而以米那普仑为关键词检索到用于慢性腰痛的研究仅1项,研究纳入患者40例,结果证明米那普仑对于缓解慢性腰疼有效,但由于纳入患者局限性,无法作为有力数据支持[41]。
2.3SNRIs类药物的不良反应 尽管SNRIs类药物用于NP与抑郁症比较,起始剂量和维持剂量均较小,但其不良反应仍然不容小觑[34]。一项Ⅲ期随机试验中,文拉法辛对奥沙利铂引起的急性神经感觉毒性具有临床疗效,但其副作用不容忽视,包括乏力(39.2%)和恶心(43.1%)等,部分患者因无法耐受相关不良反应而退出研究[42],因此,文拉法辛在治疗奥沙利铂诱导的CIPN的效用尚存争议。HOSSAIN等[36]通过系统评价显示,小剂量度洛西汀(20~30 mg·d-1)治疗NP时耐受性良好且安全。但与安慰剂比较,大剂量度洛西汀(60~120 mg·d-1)组存在因无法耐受其不良反应而退出研究的现象。此外,与普瑞巴林组比较,度洛西汀组患者出现恶心、失眠、过度出汗和食欲下降的概率更高,普瑞巴林组外周水肿比度洛西汀更常见。
由于多数研究周期较短(≤4个月),因此,无法评估这些药物用于NP的长期疗效和安全性。2004年,FDA发布一项针对抗抑郁药的黑框警告,提示SNRIs类药物可能会导致儿童和青少年的自杀意念和行为。HENGARTNER等[43]报道长期(23~39个月)给予度洛西汀治疗肌肉骨骼疼痛后,部分青少年突发自杀意念和行为,以及其他严重精神不良事件,但安慰剂组未记录此类事件。与安慰剂比较,度洛西汀组突发严重精神不良事件的发生率显著高于安慰药。由此推断,即使不是用于治疗抑郁或焦虑,SNRIs类药物作为镇痛辅助治疗药物也可能使青少年面临自杀和其他严重精神障碍的风险,应尽量避免长期应用。
长期应用却突然停止或中断SNRIs类药物可能导致停药综合征,如焦虑、易激惹、失眠、震颤、休克样感觉、眩晕和注意力下降等。FAVA等[44]分析显示,停用任何SNRIs类药物,如文拉法辛、去甲文拉法辛、度洛西汀、米那普仑或左旋米那普仑,均可能出现停药综合征,停药后其发生率,文拉法辛23%~78%,去甲文拉法辛17.2%~55%,度洛西汀6%~55%,米那普仑13%~30%,左旋米那普仑9%~10%,可见在停用SNRIs类药物时停药综合征发生率较高,是其临床应用中急需攻克的难题。基于目前研究并无发现SNRIs药物成瘾性报道,因此SNRIs类药物的停药综合征也就区别于其他中枢神经系统药物如苯二氮类药物或阿片类的戒断症状。目前认为SNRIs类药物逐渐减量似乎是一种合理的临床策略,但它并不能防止停药综合征的发作,更好的解决方案亟待研究。
2.4SNRIs类药物的基因多态性 CYP同工酶介导多数精神药物的氧化代谢。一些同工酶(如CYP2C19或CYP2D6)遗传多态性导致酶活性的变化而影响药物代谢[45]。度洛西汀主要经肝药酶CYP2D6、CYP1A2代谢,与CYP2D6、CYP1A2酶相关抑制剂或代谢底物合用时均能影响度洛西汀体内药动学。CYP2D6基因呈高度多态性,已鉴定出100多种等位基因变异和亚变种。有限数据表明,CYP2D6 慢代谢者的度洛西汀浓度较高。FDA指出CYP2D6 慢代谢者如度洛西汀与氟伏沙明同时应用,度洛西汀AUC 和Cmax增加6倍。荷兰药物遗传学工作组(DPWG)目前没有给出基于CYP2D6基因型的度洛西汀使用剂量建议。文拉法辛主要经肝药酶CYP2D6和CYP2C19代谢,ZHANG等[46]研究结果显示汉族人群应用文拉法辛受CYP2C19遗传多态性影响较小,荷兰药物遗传学工作组建议对于 CYP2D6慢代谢者 和中间代谢者,选择替代药品或减少文拉法辛剂量并监测患者的血浆代谢物水平。对于 CYP2D6 超快速代谢者,建议将剂量增加至正常剂量的150% 或选择替代品。VOLON等[47]报道1例男性患者应用文拉法辛(首日75 mg·d-1,其后225 mg·d-1)1周后,因意识改变、高热转入重症监护室,其神经系统检查显示弥漫性震颤、下肢肌张力亢进、反射亢进和诱发性阵挛。此外,还伴有心动过速和多汗。根据Hunter's标准怀疑为5-HT综合征,停用文拉法辛后治疗好转。3个月后重新予文拉法辛(前2 d为37.5 mg·d-1,第3天75 mg·d-1)后再次出现震颤、肌张力亢进、反射亢进等,再次停用文拉法辛后行基因检测发现患者具有CYP2D6*41/*41等位基因,为CYP2D6中间代谢型。由此可见,应用度洛西汀、文拉法辛等受遗传基因多态性影响较大药物前予药物基因检测可以成为减少药物不良反应发生,提高患者用药安全的有效手段。
3 结束语
SNRIs类药物作用机制及NP病理机制仍在深入研究,目前SNRIs类药物在多种NP治疗中具明显优势,但其用于PLP等部分NP的疗效与安全仍有待确定。随着研究推进,SNRIs类药物正探索式应用于脊髓损伤性疼痛、慢性术后疼痛等中枢及外周神经性疼痛,有望作为其他药物治疗失败时的替代药品。SNRIs类药物作为镇痛药物治疗时长期及大剂量应用的安全性尤其是自杀风险、5-HT综合征及其与多种药物的相互作用仍为临床应用面临的严峻挑战。借助基因检测等精准用药方式,根据疼痛症状、性质、程度个体化选择SNRIs类药物是为患者提供优质药学服务的重要方向,相信在国内外学者的不断推进与探索下,SNRIs类药物在NP中的应用将会更加系统与规范。
