基于肺叶三维重建的肺结节术前无创定位的临床应用
2023-05-25董麒锋卢军杨振杰张国飞
董麒锋 卢军 杨振杰 张国飞
随着CT 检查在肺癌筛查中的广泛应用,多原发性肺癌(multiple primary lung cancer,MPLC)的检出率逐渐增加[1-2]。当主要病变被手术切除时,在不损失过多肺功能的前提下,剩余的小病灶应尽可能地切除。电视辅助胸腔镜手术(video-assisted thoracic surgery,VATS)下的亚肺叶切除包括楔形切除和肺段切除,已广泛应用于单纯性或混合性磨玻璃结节(ground-glass nodule,GGN)的手术切除[3]。然而,这些非实性肺结节因直径较小或位于胸膜表面以下较深位置而无法在胸腔镜手术中看到或触到,必须在术前进行定位。目前临床应用较多的术前肺结节定位技术是CT 引导下放置弹簧圈或Hook-wire,但是这些方法存在一定的局限性与安全问题,增加了手术的复杂性,并使患者接受更多的辐射,医疗费用也会增加[4-5]。此外,CT 引导的经皮定位方法存在“盲区”,包括纵隔附近的区域、叶间裂附近的区域和肩胛骨阴影区[6]。肺叶三维重建(three- dimensional computed tomography lung reconstruction,3D-CTLR)可以准确地判断结节在肺叶中的相对位置,在肺段或楔形切除术中,可实现对结节无创可视化定位。笔者总结了35 例MPLC 患者采用基于3D-CTLR 的肺结节术前无创可视化定位的应用经验,现报道如下。
1 对象和方法
1.1 对象 选取2019年1月至2022年7月杭州市萧山区中医院和浙江大学医学院附属第二医院收治因怀疑MPLC 并接受胸腔镜下手术切除治疗的35 例患者,其中男20 例,女15 例。纳入标准:(1)高分辨率胸部CT 检查后发现结节≥2 个;(2)3~6 个月复查发现直径增大或者密度增加,且结节最大径≤20 mm;(3)均行胸腔镜下手术切除。排除标准:(1)CT 结节最大径>20 mm,单个结节;(2)术中转开胸手术;(3)病理检查结果为转移性肺癌、鳞状细胞癌或大、小细胞肺癌者;(4)病理检查结果为腺癌,但分期超过T1bN0M0者(第8 版肺癌TNM 分期);(5)病例资料不完整者。本研究经杭州市萧山区中医院医学伦理委员会批准(2022025),所有患者均知情同意。
1.2 方法 术前常规进行1.5 mm 层厚的高分辨率胸部CT 扫描。使用三维重建软件(如3Dslicer,Mimics)处理CT 数据,将DICOM 原图导入3Dslicer 或者Mimics软件,使用图像插件进行重建,运用裁剪、旋转等工具患者创建准确的肺叶三维重建模型,同时标识肺结节,导出三维动画视频,从而显示重建的肺叶和结节的相对位置,进行准确的结节定位,包括浅表结节、固定解剖标志、在肺叶间隔附近的结节、位于肺平面边界或印迹附近的结节以及深部结节。三维重建模型在术前1 天完成。所有患者均在全麻下接受胸腔镜下手术,切除方式包括楔形切除术、肺段切除术或肺叶切除术,根据病灶的大小和位置决定。同时对切除的结节进行术中病理检查,若检查结果提示侵袭性腺癌,则根据术前肺功能结果决定是否行肺叶切除术。对于位于较深位置且不能通过楔形切除的结节行肺段切除。
1.3 观察指标 收集患者临床数据,记录本组患者肺结节大小、数量、特征和部位、手术方式(楔形切除、节段切除或肺叶切除)、结节切除数目、手术时间、术中出血量、术后住院时间、并发症和病死率等。
1.4 统计学处理 采用SPSS 24.0 统计软件。计量资料以表示,计数资料以例(%)表示。
2 结果
35 例患者CT 检查共发现96 个结节,其中单纯性磨玻璃结节39 个,混合性GGN[磨玻璃样密度灶(ground-glass opacity,GGO)≥50%]43 个,混合性GGN(GGO<50%)6个,实性结节8个。1个结节因最大径>15 mm 术前未定位,其他结节均在术前行3D-CTLR 无创定位。96 个结节中位于“盲区”21 个,位于纵隔区附近7 个,靠近叶间裂10 个,被肩胛骨遮挡4 个,均行手术切除,每例患者平均切除(2.7±1.3)个结节,结节平均最大径为(8.7±3.7)mm。所有结节均采用胸腔镜下切除,无需转为小切口或者开胸手术,其中楔形切除术22 例,肺段切除术22 例,肺叶切除术18 例,同时接受2 种或者2 种以上切除方式22 例。术中病理检查提示有1 个或多个浸润性病灶,需进一步行纵隔淋巴结清扫。病理检查结果提示良性结节4 个,不典型腺瘤样增生11 个,原位腺癌14 个,微浸润腺癌21 个和浸润性腺癌46 个。本组患者平均手术时间为(148.5±28.3)min,平均术中出血量为(40.9±22.6)ml,平均住院时间为(3.3±0.6)d。术中或术后未出现严重并发症,未发生术后30 d或住院死亡病例。典型病例见图1。
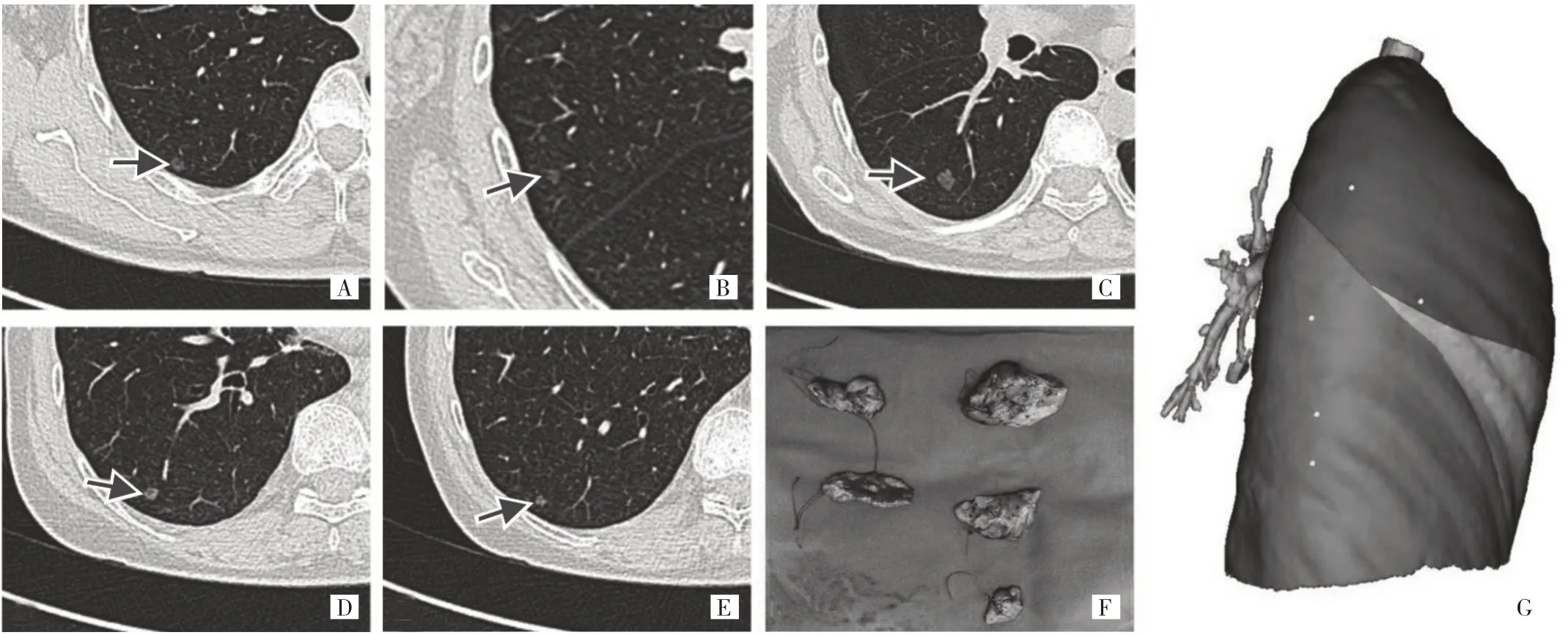
图1 51 岁男性多原发性肺癌患者影像图及标本[A、B:右上肺2 个磨玻璃结节(原位腺癌,箭头所示;C、D、E:右下肺3 个磨玻璃结节(C 为微浸润腺癌,D、E 为原位腺癌,箭头所示);F:切除的手术标本;G:右肺三维重建显示5 个磨玻璃结节的位置,白点所示]
3 讨论
随着低剂量螺旋CT 在肺癌筛查中的应用,MPLC检出率越来越高。目前胸腔镜下手术切除仍然是治疗的主要手段。然而,这些结节的术前定位仍然是一个主要挑战。本研究中,笔者评估了术前3D-CTLR 作为一种非侵入性可视化定位方法,发现这种定位方法对于MPLC 患者在亚肺叶切除术术前进行无创定位是安全可行的,而且对小病灶和周围病变效果较好,是一种安全、简便的定位方法。
对于MPLC 患者,当主要病变被切除时,常采用楔形切除术切除剩余的小病变。术中肉眼观察和手指触诊是肺结节术中最直接、最简单、最安全的定位方法。然而,<1 cm 的结节、非实性或部分实性结节以及距离胸膜表面较远的结节在胸腔镜手术中很难或不可能通过触诊定位,通常需要扩大切除,甚至肺段切除或肺叶切除。目前报道临床上常规应用的术前定位方法的成功率为68%~100%,最常用的定位技术即CT 引导下用Hook-wire 或弹簧圈进行经皮有创定位[7-8]。但是临床报道相关的并发症发生率并不低,包括辐射暴露、脱位、气胸和出血[9-10]。另外,经皮定位过程中遇到“盲区”,包括纵隔附近的区域、叶间裂附近的区域和肩胛骨阴影区,是这种有创定位技术的主要局限[11]。理想的术前定位方法应该是避免侵入性,但是目前关于无创术前定位方法的报道较少。
基于CT 的支气管和血管三维重建已广泛应用于肺段切除术的手术导航,这种术前模拟有助于手术规划,包括识别目标血管、支气管和手术边缘,任何解剖变异[12-14],但是上述方法不能完全解决结节的术前定位问题。在没有准确定位浅表肺结节的情况下,楔形切除可能不准确。本研究使用3D-CTLR 可以直观、准确地识别多个结节的位置。具体来讲,位于肺叶特定部位的结节,例如上叶尖部、下叶背段的上部以及每个叶的多个平面交汇处的连接区域,可以通过楔形切除直接切除结节。手术可以运用一些固定的解剖标志物,比如在Y 点(斜裂和水平裂的交叉点)附件的结节,在肺塌陷之前,用电刀在Y 点的内脏胸膜上做一个灼烧印记,然后用无菌尺子测量结节相对于Y 点的距离,就可以定位行楔形切除。对于靠近叶间裂的结节,尤其是深部结节,使用CT 引导下的穿刺定位存在困难和风险,但是这些结节可以在三维重建模型中进行可视化定位。另外,对于靠近一些特殊印迹的结节,如第一肋骨、上腔静脉、心脏、奇静脉和食管,也可以在三维重建模型上容易识别和切除。此外,通过肺叶三维重建对MPLC可以进行精准的定位,避免了侵入性定位方法相关的不适和并发症,适用于整个肺野的结节定位以及患者或医疗人员无需额外的辐射暴露。
综上所述,对于MPLC 患者,术前行3D-CTLR 进行肺结节无创定位是一种安全可行的定位方法,值得临床推广应用。
