CDK4/6 抑制剂治疗HR+/HER2-晚期乳腺癌的效果及安全性研究*
2023-05-25倪静怡张葆春高湘湘金聪慧
倪静怡,陈 佳,张葆春,高湘湘,金聪慧
(南通大学附属肿瘤医院,江苏省南通市肿瘤医院乳腺内科,南通 226361)
乳腺癌是全球最常见的恶性肿瘤,也是女性肿瘤死亡的第二大原因,严重威胁人类的健康[1]。其中,激素受体阳性/人表皮生长因子受体2 阴性(hormone receptor positive/human epidermal growth factor receptor 2 negative,HR+/HER2-)是乳腺癌最常见的类型,占所有乳腺癌的70%[2]。我国女性乳腺癌的发病率也逐年升高,3%~8%的患者初诊即为晚期,而接受手术及辅助治疗的早期患者中30%~40%仍会复发转移[3]。虽然早期乳腺癌的预后较好,但一旦发生转移,患者5 年生存率仅25%[4]。内分泌治疗是大部分HR+/HER2-晚期乳腺癌的主要治疗方案,但随后出现的内分泌治疗耐药和疾病进展仍是主要的临床挑战[5]。
近年来,细胞周期蛋白依赖性激酶4/6(cyclindependent kinase 4/6,CDK4/6)抑制剂的应用改变了HR+/HER2-晚期乳腺癌的治疗模式。临床研究[6-8]表明CDK4/6 抑制剂联合内分泌治疗可减轻对内分泌治疗的耐药性,延长患者无进展生存期(progressionfree survival,PFS)和总生存期。CDK4/6 抑制剂联合内分泌治疗已成为HR+/HER2-晚期乳腺癌的标准治疗[9]。在美国,2018 年一线使用CDK4/6 抑制剂联合内分泌治疗的患者已达48.7%[10],但在中国其应用相对滞后,相关的临床研究也较少。目前在中国上市的进口CDK4/6 抑制剂有哌柏西利和阿贝西利。阿贝西利于2021 年初在国内被批准用于治疗HR+/HER2-局部晚期或转移性乳腺癌及早期高危乳腺癌辅助强化治疗。目前国内对阿贝西利治疗的临床疗效及安全性数据较少,本研究对南通大学附属肿瘤医院应用阿贝西利联合内分泌治疗的HR+/HER2-晚期乳腺癌患者的临床资料进行分析,旨在为HR+/HER2-晚期乳腺癌的治疗方案提供新思路。
1 对象与方法
1.1 研究对象 回顾性分析2021 年2 月—2022 年9 月在南通大学附属肿瘤医院接受阿贝西利联合内分泌治疗的70 例HR+/HER2-晚期乳腺癌患者的临床病理资料。由于缺乏前瞻性临床试验指导,根据治疗模式分成3 组,A 组:一线使用阿贝西利18 例;B组:哌柏西利转阿贝西利18 例;C 组:未使用哌柏西利的阿贝西利二线及以上34 例。纳入标准:(1)组织病理学诊断为乳腺癌;(2)临床分期为Ⅳ期;(3)接受CDK4/6 抑制剂联合内分泌治疗(包括阿那曲唑、来曲唑、依西美坦、氟维司群);(4)具有符合实体瘤疗效评价标准的可测量病灶;(5)可获得完整临床数据。排除标准:合并第二原发恶性肿瘤或严重的心脑血管疾病。
1.2 治疗方法 阿贝西利(礼来公司)的起始剂量为150 mg,bid,后续根据患者的不良反应及耐受情况进行药物剂量调整。期间若出现严重不良反应,可暂停或延迟给药,或减低剂量或停用。
1.3 疗效与不良反应评价 患者每8 周进行1 次影像学评估,如头、胸、全腹部增强CT 或MRI。采用实体瘤疗效评价标准(response evaluation criteria in solid tumours,RECIST)1.1 版进行疗效评价。主要研究终点为PFS,即使用阿贝西利开始至疾病进展或末次随访日期之间的时间。如患者在治疗过程中多次发生不良反应,则记录最高级别的不良反应。末次随访时间为2022 年11 月30 日。
1.4 统计学方法 采用SPSS 22.0 软件及R 软件(3.6.1 版本,http://www.R-project.org/)进行统计分析,计量资料用中位数表示,分类计数资料用n(%)表示。Kaplan-Meier 法绘制生存曲线,并采用Log-rank 检验。单因素及多因素Cox 比例风险模型分析影响HR+/HER2-晚期乳腺癌PFS 的独立预后因素,并计算HR 和95%CI,P<0.05 为差异有统计学意义。
2 结果
2.1 临床特征 本研究70 例HR+/HER2-晚期乳腺癌患者中位年龄58.5 岁(34~89 岁)。接受阿贝西利联合氟维司群治疗48 例(68.6%),无单独使用阿贝西利者。3 组患者的临床病理特征及治疗情况比较见表1。
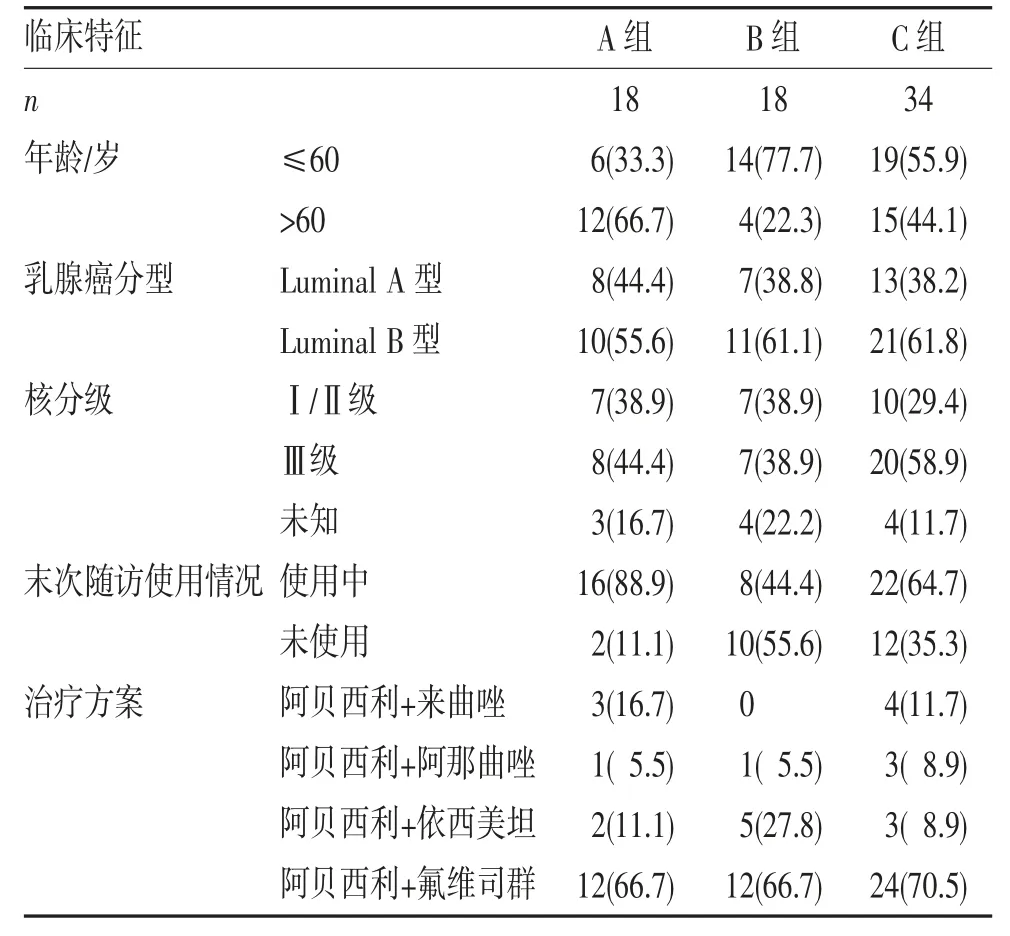
表1 各组患者临床特征的比较(n,%)
2.2 疗效评价 截至2022 年11 月30 日,因疾病进展停用阿贝西利治疗23 例(32.9%),因严重腹泻停用1 例(1.4%)。接受阿贝西利治疗后首次疗效评价即进展的患者7 例(10.0%),治疗时间>6 个月30例(42.9%),客观缓解率(objective response rate,ORR)为44.3%(31/70),疾病控制率为67.1%(47/70),中位随访时间为7 个月。3 组患者PFS 比较差异有统计学意义(P<0.01),1 年PFS 率分别为46.7%、33.5%及42.7%,其生存曲线见图1A,C 组患者的PFS 优于B组(P=0.048)(图1B)。单因素分析结果显示:年龄>60岁及哌柏西利转阿贝西利治疗是PFS 的独立影响因素,而乳腺癌的Luminal 分型、核分级及阿贝西利联合的内分泌治疗药物种类对PFS 无影响。多因素分析结果显示:年龄>60 岁对≤60 岁的PFS 的HR=0.3,95%CI:0.3~0.9,P=0.04。与阿贝西利一线治疗组相比,哌柏西利转阿贝西利组的PFS 的HR=5.4,95%CI:1.1~26.4,P=0.04。
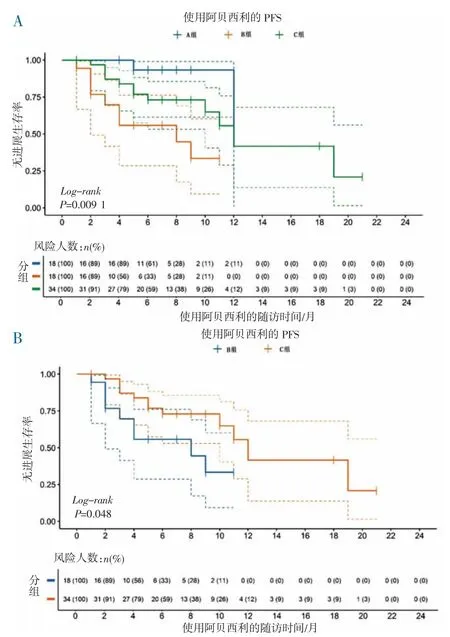
图1 HR+/HER2-晚期乳腺癌的PFS 曲线
2.3 不良反应 在治疗过程中,发生白细胞减少30 例(42.9%),中性粒细胞减少24 例(34.3%),贫血20 例(28.6%),血小板减少8 例(11.4%);腹痛腹泻7例(10.0%),其中1 例(1.4%)患者因严重腹泻终止治疗;转氨酶升高8 例(11.4%),胆红素升高3 例(4.3%);静脉血栓1 例(1.4%),见表2。通过对症治疗及减量、延迟用药后恢复,未见不良反应死亡事件。
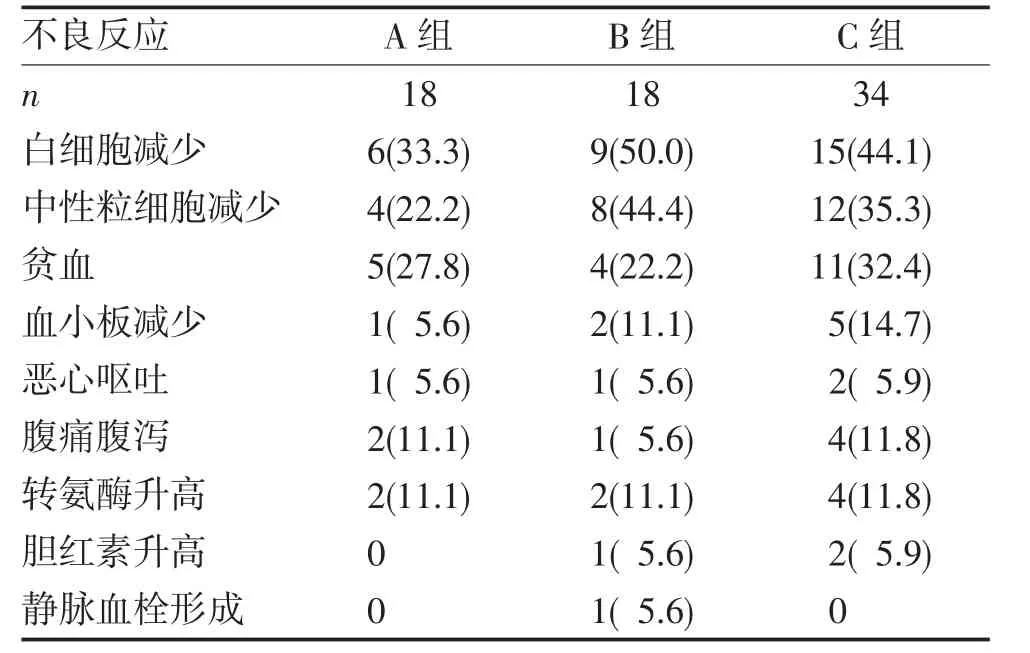
表2 3 组患者不良反应发生情况比较(n,%)
3 讨论
HR+/HER2-晚期乳腺癌的内分泌耐药是临床常见的问题,CDK4/6 抑制剂的出现改变了HR+乳腺癌的治疗模式,提供了除化疗之外的新思路,在一线和后线治疗中与内分泌治疗药物结合,可显著改善患者的生存结局[11]。基于Ⅱ期MONARCH1 临床试验的结果,阿贝西利是唯一被批准可以单药治疗经内分泌治疗或化疗后进展的HR+/HER2-晚期乳腺癌的CDK4/6 抑制剂[12]。但在MONARCH1 临床试验中,没有患者在接受阿贝西利治疗之前使用过哌柏西利,无法研究哌柏西利转阿贝西利治疗的疗效与不良反应,且国内有关阿贝西利治疗的疗效与安全性的报道也较少。本研究分析阿贝西利不同治疗模式的疗效与安全性,拟为后续临床治疗提供一定的参考。
在MONARCH2 研究中,阿贝西利联合氟维司群治疗内分泌治疗期间进展的HR+/HER2-晚期乳腺癌的ORR 为48.1%,可显著改善患者的PFS 和ORR[13]。本研究中所有接受阿贝西利治疗患者的ORR为44.3%,疾病控制率为67.1%,3 组患者的PFS 差异有统计学意义。阿贝西利一线治疗患者的PFS 更长,接受哌柏西利转阿贝西利组的疾病进展风险是一线接受阿贝西利治疗组的5.4 倍。但本研究中一线接受阿贝西利治疗患者大部分在2022 年才接受治疗,随访时间较短,且人数较少,可能会影响结果的准确性。希望后续能有更多接受阿贝西利治疗的研究提供相关的数据参考。
既往研究[14]发现,CDK4/6 抑制剂的不良反应主要表现为血液系统毒性、胃肠道反应、疲劳及转氨酶升高。其中,阿贝西利联合内分泌治疗导致的疲劳和胃肠道毒性发生率更高。阿贝西利导致的腹泻通常在早期就出现,中位发病时间为1 周,使用常规止泻药或降低剂量即可控制。与化疗导致的骨髓抑制不同,CDK4/6 抑制剂导致的血液系统毒性更易恢复,主要原因为其药理学机制是通过周期停滞导致骨髓抑制[12,15]。本研究中,哌柏西利转阿贝西利组患者白细胞减少发生率较高,肝功能不全及消化道系统毒性发生率各组类似。由于本研究纳入的病例数较少,各组不良反应类型及整体趋势相似,耐受性良好。
综上所述,在HR+/HER2-晚期乳腺癌中,一线接受阿贝西利治疗患者的PFS 更长。与阿贝西利一线治疗相比,哌柏西利转阿贝西利组的疾病进展风险更高。阿贝西利联合内分泌药物在HR+/HER2-晚期乳腺癌患者中具有良好疗效,且不良反应可控,耐受性良好。由于本研究的样本量较少,后续需通过纳入更多样本进一步验证。
