血清CA125、HE4 联合检测诊断复发性卵巢癌价值的Meta 分析
2023-05-23王露,林英
王 露,林 英
(重庆医科大学附属永川医院妇科,重庆 402160)
卵巢癌(ovarian cancer,OC)病死率居妇科恶性肿瘤之首[1]。约70%~80%的上皮性卵巢癌患者在行标准化治疗达到完全缓解后仍可能发生疾病复发[2]。复发性卵巢癌(recurrent ovarian cancer,ROC)是指经过满意的肿瘤细胞减灭术和正规、足量的化疗后达到临床完全缓解,停止治疗超过6 个月再次发现病灶的情况,主要以糖类抗原125(carbohydrate antigen 125,CA125)升高、体检发现肿块、影像学检查发现肿块、出现胸腔或腹腔积液、出现不明原因的肠梗阻等为主要临床表现。血清CA125 是目前最常用于诊断卵巢癌的肿瘤标志物,但CA125 诊断早期卵巢癌敏感度高,特异性差,其在子宫内膜异位症、妇女月经期也会升高。血清人附睾蛋白4(human epididymis protein 4,HE4)对于早期卵巢癌的诊断灵敏度(sensitivity,SE)低,特异度(specificity,SP)高。HE4 对复发性卵巢癌的诊断价值是否优于CA125 尚未有定论,本研究纳入公开发表的单独检测CA125、HE4 和(或)联合检测CA125、HE4 对于复发性卵巢癌诊断价值的数据,通过Meta 分析比较和评价它们对复发性卵巢癌的诊断价值,从而为复发性卵巢癌患者预后改善作出一定贡献。
1 资料与方法
1.1 纳入与排除标准 纳入标准:①血清CA125、HE4 并联检测与复发卵巢癌诊断价值的病例对照研究、队列研究以及随机对照试验;②研究对象:所有患者经组织病理学确诊为复发性卵巢癌;实验组为卵巢癌复发组或转移组,对照组为非复发组或转移组;③提供全部CA125 和或HE4 检测结果和正常值范围;④所有诊断复发性卵巢癌的金标准一致;⑤从文献中能获取真阳性(TP)、假阳性(FP)、真阴性(TN)、假阴性(FN)值;⑥每组样本量≥30 例;⑦所有检测标本为血清,标本检测方法为化学发光免疫法;⑧发表语种为英文和中文。排除标准:①综述、Meta 分析、系统评价、案例、指南解读、会议讲座、科技成果类;②实验组和对照组不符合;③根据文献中的数据不能获TP、FP、TN、FN 的文献;④病例金标准诊断标准不一致。
1.2 检索策略 以“CA-125”“糖链抗原125”“人附睾蛋白4”“人附睾分泌蛋白4”“人附睾上皮分泌蛋白4”“诊断”“卵巢肿瘤”“卵巢癌”主题词及其自由词为检索词检索CNKI、维普中文科技期刊全文数据库、万方医学网、CBM 等中文数据库;以“Ovarian Neoplasms”“CA-125 Antigen”“WFDC2 protein,human[Supplementary Concept]”主题词及其自由词为检索词,检索Pubmed、Embase、Cochrane 图书馆、Web of science 等英文数据库,全面收集CA125、HE4 并联检测与卵巢癌相关文献。本研究不包括尚未公开发表的文献,检索时间限定为数据库建库至2022 年2 月。
1.3 文献筛选与资料提取 初筛获得包含有中英文文献的相关文献共2773 篇。根据纳入标准和排除标准,排除相关文献(其中包含重复文献,动物实验等文献及与研究内容不符的文献,不能获得TP、FP、FN 及TN 值的文献),最终纳入本次Meta 分析的文献10 篇[3-12]。从中提取的信息包括第一作者、年份、对照来源、单独检测CA125/HE4 和或联合检测CA125+HE4 的TP、FP、FN、TN 值及SE、SP。
1.4 文献质量评价 由2 名评价人员独立根据QUADAS 2 工具对文献进行评价,条目包括:A.病例选择是否纳入了连续或随机的病例;B.病例选择是否避免了病例对照类研究设计;C.病例选择研究是否避免了不恰当的排除;D.相关纳入的病患和背景与评价问题匹配情况;E.待评价试验的结果判读是否是在不知晓金标准试验结果的情况下进行的;F.若使用了阈值,那么它是否是事先确定的;G.待评价试验的实施和解释与评价问题的匹配情况评价;H.金标准是否可以正确地区分目标疾病状态;I.金标准结果判读是否使用了盲法;J.金标准的适用性评价;K.待评价试验和金标准之间是否有恰当的时间间隔;L.所有的患者是否只接受了一个相同的金标准;M.是否所有的病例都纳入了分析;根据这13 项评价指标分别对纳入文献作出结果判断:“是”“否”“低偏倚风险”“偏倚风险不确定”“高偏倚风险”。
1.5 统计学方法 运用Meta-DiSc 软件进行Meta 分析,首先对纳入文献用I2检验进行异质性检验,当P>0.1、I2<50%则认为研究间无统计学异质性,采用固定效应模型对文献进行分析;当P≤0.1、I2≥50%则认为研究间有统计学异质性,进一步查找异质性的来源,若仍无法消除异质性,但临床又具有一致性,则采用随机效应模型对文献进行统计分析,反之则采用描述性分析[27]。将SE 对数值与(1-SP)对数值做Spearman 相关分析,检查有无阈值效应引起的异质性,合并计算SE、SP、诊断比值比(diagnostic odds ratio,DOR)及其阳性似然比(positive likelihood ratio,+LR)、阴性似然比(negative likelihood ratio,-LR)、曲线下面积(area under the curve,AUC)、Q 指数。计算综合受试者工作特征曲线和AUC、诊断试验的综合准确率Q*[Q*=(1+e-A/2)-1,表示诊断试验的准确度,反映了SROC 曲线与左上角接近的程度,数值越大表示诊断试验的准确度越高]。运用STATA 16.0 对本研究的数据进行敏感性分析以及Deeks 发表偏倚检验。通过固定效应模型和随机效应模型同时分析同一数据完成敏感性分析,采用漏斗图对文献进行发表偏倚分析。
2 结果
2.1 文献筛选结果与基本特征 初筛获得包含有中英文文献共2773 篇。根据纳入标准和排除标准,排除的文献共2733 篇(其中903 篇重复文献,1 篇动物实验,212 篇综述、Meta 分析、系统评价、案例、指南解读、会议讲座、科技成果类文献,1617 篇与研究内容不附的文献),剩余的有CA125、HE4 单独或联合检测指标的40 篇文献,从中进一步筛选,排除无对照组或对照组为铂耐药组的文献17 篇,不能获得或获得TP、FP、FN 及TN 值不可靠的文献13 篇,最终纳入本次Meta 分析的文献10 篇[3-12],全部包含有单独检测CA125、HE4 和(或)联合检测CA125、HE4的结果,文献筛选流程见图1。此10 篇文献,发表于建库以来至2022 年,其中4 篇文献[3-6]中的卵巢癌已正规治疗(手术+标准化疗)(组1)单独检测CA125的SE、SP 的取值范围分别为0.583~0.880、0.424~0.714,单独检测HE4 的SE、SP 的取值范围分别为0.609~0.780、0.450~1。其中6 篇文献[7-12]中的上皮性卵巢癌已正规治疗(手术+标准化疗)(组2)单独检测CA125 的SE、SP 的取值范围分别为0.522~0.867、0.405~0.983,单独检测HE4 的SE、SP 的取值范围分别为0.091~0.913、0.379~0.977,其中3 篇文献[9-11]中联合检测CA125+HE4 的SE、SP 的取值范围分别为0.159~0.810、0.177~0.884,纳入文献基本特征见表1。

图1 文献筛选流程图

表1 纳入文献的基本特征

表1(续)
2.2 文献质量评价结果 采用诊断准确性研究质量评价工具QUADAS 2 对纳入研究的文献进行质量评估,结果显示QUADAS 的13 条目,有10 条全部满足条件,评估表明此次Meta 分析纳入的10 篇文献质量一般,有待多样本数据的支持,可信度一般,具体结果见表2。

表2 QUADAS 2 工具质量评价结果
2.3 Meta 分析结果
2.3.1 单独检测CA125 共纳入10 项研究,其异质性检验结果I2>50%,提示存在异质性,故均选用随机效应模型合并各效应量。组1 中单独检测CA125(图2)的合并灵敏度为0.72(0.65~0.79),合并特异度为0.64(0.56~0.71),合并阳性似然比为1.80(1.19~2.73),合并阴性似然比为0.46(0.27~0.81),合并AUC 为0.6989,合并Q指数为0.6520,合并诊断比值比为3.99(1.58~10.10);组2 中单独检测CA125(图3)的合并灵敏度为0.59(0.53~0.65),合并特异度为0.59(0.54~0.64),合并阳性似然比为2.4(1.10~5.26),合并阴性似然比为0.56(0.34~0.91),合并AUC 为0.744,合并Q指数为0.6885,合并诊断比值比为5.24(1.36~20.1)。
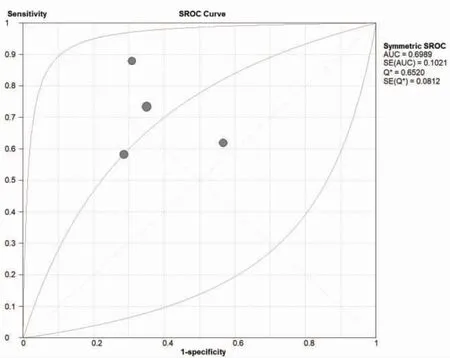
图2 组1 单独检测CA125 SROC 曲线图

图3 组2 单独检测CA125 SROC 曲线图
2.3.2 单独检测HE4 共纳入10 项研究,组1 中4 项研究其异质性检验结果I2>50%,提示存在异质性,故均选用随机效应模型合并各效应量,组2 中6 项研究异质性检验结果I2<50%,提示不存在异质性,故均选用固定效应模型合并各效应量。组1 中单独检测HE4(图4)的合并灵敏度为0.71(0.63~0.77),合并特异度为0.72(0.64~0.79),合并阳性似然比为2.45(1.88~3.19),合并阴性似然比为0.40(0.30~0.52),合并AUC 为0.7891,合并Q指数为0.7264,合并诊断比值比为6.78(4.09~11.25);组2 中单独检测HE4(图5)的合并灵敏度为0.59(0.52~0.65),合并特异度为0.63(0.58~0.68),合并阳性似然比为6.47(1.34~31.17),合并阴性似然比为0.53(0.37~0.74),合并AUC 为0.7998,合并Q指数为0.7357,合并诊断比值比为15.60(2.40~101.53)。

图4 组1 单独检测HE4 SROC 曲线图

图5 组2 单独检测HE4 SROC 曲线图
2.3.3 联合检测CA125、HE4 共纳入3 项研究,其异质性检验结果I2>50%,提示存在异质性,故均选用随机效应模型合并各效应量。组2(图6)中联合检测CA125+HE4 的合并灵敏度为0.81(0.74~0.87),合并特异度为0.30(0.25~0.36),合并阳性似然比为2.24(0.67~7.45),合并阴性似然比为0.37(0.12~1.17),合并AUC 为0.8961,合并Q指数为0.8271,合并诊断比值比为6.44(0.74~55.81)。

图6 组2 联合检测CA125+HE4 SROC 曲线图
对比单独检测CA125,组1 单独检测HE4 的合并SE 低0.01,合并SP 高0.08,合并+LR 高0.65,合并-LR 低0.06,合并AUC 高0.0902,合并Q指数高0.0744,合并诊断比值比高2.79,且差异均有统计学意义(P<0.05)。组2 中联合检测CA125+HE4 合并SE 最高,单独检测HE4 合并SP 最高,联合检测CA125+HE4 合并+LR、-LR 较高,联合检测CA125+HE4 合并AUC、Q指数较高,且差异均有统计学意义(P<0.05)。结果显示联合CA125+HE4 检测或单独检测HE4 均较单独检测CA125 判别能力强,提示HE4 在诊断复发性卵巢癌上有一定的临床价值。
3 讨论
卵巢癌是严重威胁妇女健康的恶性肿瘤之一,发病率在女性生殖系统恶性肿瘤中位居第3,病死率居妇科恶性肿瘤之首[1]。卵巢癌发病部位隐匿,症状不典型,75%的患者初治时即为晚期,虽然初次治疗的反应率颇高,但75%的晚期卵巢癌患者3 年内会出现肿瘤复发[13]。肿瘤标志物是反映肿瘤存在和生长的化学类物质,由肿瘤组织产生或肿瘤与宿主相互作用产生,可在血液、组织液、分泌液或肿瘤组织中测出[1]。本研究显示,对比单独检测CA125,组1单独检测HE4 的合并SE 低0.01,合并SP 高0.08,合并+LR 高0.65,合并-LR 低0.06,合并AUC 高0.0902,合并Q指数高0.0744,合并诊断比值比高2.79;组2 中合并SE、合并SP、合并+LR、合并-LR、合并AUC、合并Q指数、合并诊断比值比可以看出联合CA125+HE4 检测或单独检测HE4 的AUC 和诊断试验的综合准确率均比单独检测CA125 值大,提示HE4 在诊断复发性卵巢癌准确率较高。
CA125 是一种粘蛋白型糖蛋白,由MUC16 基因产生,与细胞膜相关,广泛存在于卵巢上皮性肿瘤和各种苗勒管起源的正常或病理组织上皮中。有研究表明69%~90%的卵巢癌患者血清CA125 浓度显著升高(>35 U/ml),可作为诊断、治疗监测和预后判断的指标[14],因此这种生物标记物最常用于卵巢病变。其对于早期卵巢癌以及卵巢子宫内膜样癌、透明细胞癌和卵巢黏液性癌等的诊断灵敏度较低,且对早期卵巢癌的诊断缺乏特异性。80%的卵巢上皮性癌患者CA125 水平升高,90%以上的卵巢癌患者CA125 水平与病程进展相关,其单独检测诊断卵巢癌的SE 为82.5%,SP 为57.7%,适用于早期筛查,但单独检测的SP 不高。且其在卵巢良性肿瘤、子宫内膜异位症、盆腔炎性疾病等中均有高表达,诊断特异度低。目前对于复发性卵巢癌治疗后的随访频率(受患者依从性影响)、监测内容仍未真正规范,复发的定义包括基于CA125 变化的GCIG 标准、影像学RECIST 标准(1.1 版)以及临床症状体征,这就导致每个患者诊断复发的时间点和肿瘤负荷存在巨大异质性,无进展间期无法真实的反映患者肿瘤生物学特征[13]。上皮性卵巢癌复发诊断标准妇科肿瘤协作组(GICG)的CA125 标准:治疗效果好的标准是治疗后CA125 水平下降至少50%,且保持至少28 d。当卵巢癌患者CA125 指标短时间内进行性升高至翻倍时应当警惕该患者卵巢癌生化复发,应尽早干预。又有研究认为单纯CA125 升高后立即干预(28 d 内)并不能带来生存获益[15]。少部分复发性卵巢癌患者监测CA125 水平正常,但影像学或临床已有相关的表现,因此目前对于复发性卵巢癌的治疗时机仍有很大争议。
HE4 是一种糖蛋白,属于乳清酸性四二硫核心蛋白家族,最初是在附睾中分离出来的。这种生物标记物在正常女性生殖道、乳腺、呼吸道、肾远曲小管、结肠、唾液腺中均有表达,但在卵巢肿瘤,尤其是子宫内膜样卵巢癌中过度表达[16,17]。2003 年,HE4 被FDA 批准为血清肿瘤标志物,并用于EOC 的诊断、监测治疗效果及肿瘤复发[18]。有研究显示HE4 和CA125 联合检测在卵巢癌的早期诊断中特异性更高[19-21]。Rong Y 等[22]的研究提示在一线化疗期间监测HE4 和CA125 可能有助于预测铂的敏感性和进展和复发的风险。这就提示了可以通过监测HE4 和CA125 两者水平的变化早期发现复发性卵巢癌[23],从而改善复发性卵巢癌患者的预后。因此,本研究通过Meta 分析综合评价联合检测CA125、HE4 并联诊断复发性卵巢癌的价值,为复发性卵巢癌的诊断提供循证医学证据。
综上所述,从本研究中可以看出联合CA125+HE4 检测或单独检测HE4 的AUC 和诊断试验的综合准确率均比单独检测CA125 值大,可提高复发性卵巢癌诊断的敏感性和准确性,有利于复发性卵巢癌的早期发现和诊断,为后续研究和临床决策提供参考意义。
