糖尿病视网膜病变的全科医学管理
2023-05-13刘涵方晏红综述陈健审校
刘涵,方晏红 综述,陈健 审校
(1.重庆大学附属江津医院,重庆 402260,2.重庆市江津区中医院,重庆 402260)
糖尿病是世界上各个国家各个阶层的重大健康危机,随着全球老龄化发展,糖尿病患病率正在不断增加,全球20~79岁成年人的糖尿病患病率估计为8.8%,也就是说在2017年全世界范围内有4.25亿成年人受到影响,预计到2045年,这一数字将增至6.29亿[1]。我国是世界上糖尿病患者最多的国家,2020年中国居民营养与慢性病状况报告数据显示,我国成人糖尿病患病率为11.9%,患者人数高达1.25亿[2]。糖尿病视网膜病变(diabetic Retinopathy,DR)是由糖尿病引起的一种微血管病变,是最常见的视网膜血管性疾病。2020年,DR是全球50岁及以上人群中最常见的可预防失明原因之一,也是最常见的视力中重度损害原因。基层糖尿病患者常在社区医院由全科医师治疗,由于专科化发展的趋势,全科医师常独立工作,然而在更广泛的眼科和全科团队之间协调这一复杂的糖尿病全身健康管理普及得微乎其微。当今医疗发展的快速化、多样化,所有医疗人员都需要了解糖尿病管理各个方面的发展。
1 DR的流行病学
Li等[3]依照2018年美国糖尿病学会的诊断标准在2015—2017年针对全国范围内31省区75880例≥18岁的成年人进行调查,发现糖尿病总患病率为11.2%,其中DR总患病率为34.60%,预估国人中的中老年DR患者数为1316万[4]。一项荟萃分析表明,在20~79岁的糖尿病患者中,DR的总患病率为34.6%,增殖性糖尿病视网膜病变(proliferative Diabetic Retinopathy,PDR)的总患病率为7.0%,1型糖尿病患者的DR患病率高于2型糖尿病患者(分别为77.3%和25.2%),并且在美国黑人中最高,在亚洲人中最低,预估全世界约有9300万DR患者、1700万PDR患者、2100万糖尿病性黄斑水肿(diabetic Macular Edema,DME)患者[5]。糖尿病患者无糖尿病视网膜病变(no diabetic retinopathy,NDR)的中位时间为8.7年,在初诊糖尿病的首个3年随访中,DR的发病率为14/1000人/年,在6年随访后增加到131/1000人/年的高发病率[6]。与DR发生及其进展风险相关的眼外因素包括血糖控制不良、高血压、血脂异常、糖尿病持续时间、妊娠和遗传因素[7-8]。
2 DR的疾病机制、分期、自然病程和症状
DR的发病机制复杂,主要涉及炎症、氧化应激、多元醇途径、己糖胺途径、细胞因子、肾素-血管紧张素系统(renin-angiotensin-aldosterone system,RAAS)等[9]。高血糖可促使局部多元醇旁路代谢途径分泌自由基消耗还原型烟酰胺腺嘌呤二核苷酸,使视网膜细胞内缺氧,产生血管内皮生长因子(vascular endothelial growth factor,VEGF),使血管通透性增加,导致DR和DME[10]。
DR分为非增殖期(non-proliferative diabetic retinopathy,NPDR)和增殖期(proliferative diabetic retinopathy,PDR),NPDR主要是进行性视网膜内微血管改变,PDR的特点是在视网膜或视盘上生长新形成的血管。DME是指视网膜黄斑区增厚,可能发生在NPDR或PDR中[10]。
DR的分期和DR、DME的眼底表现见表1、图1~10。
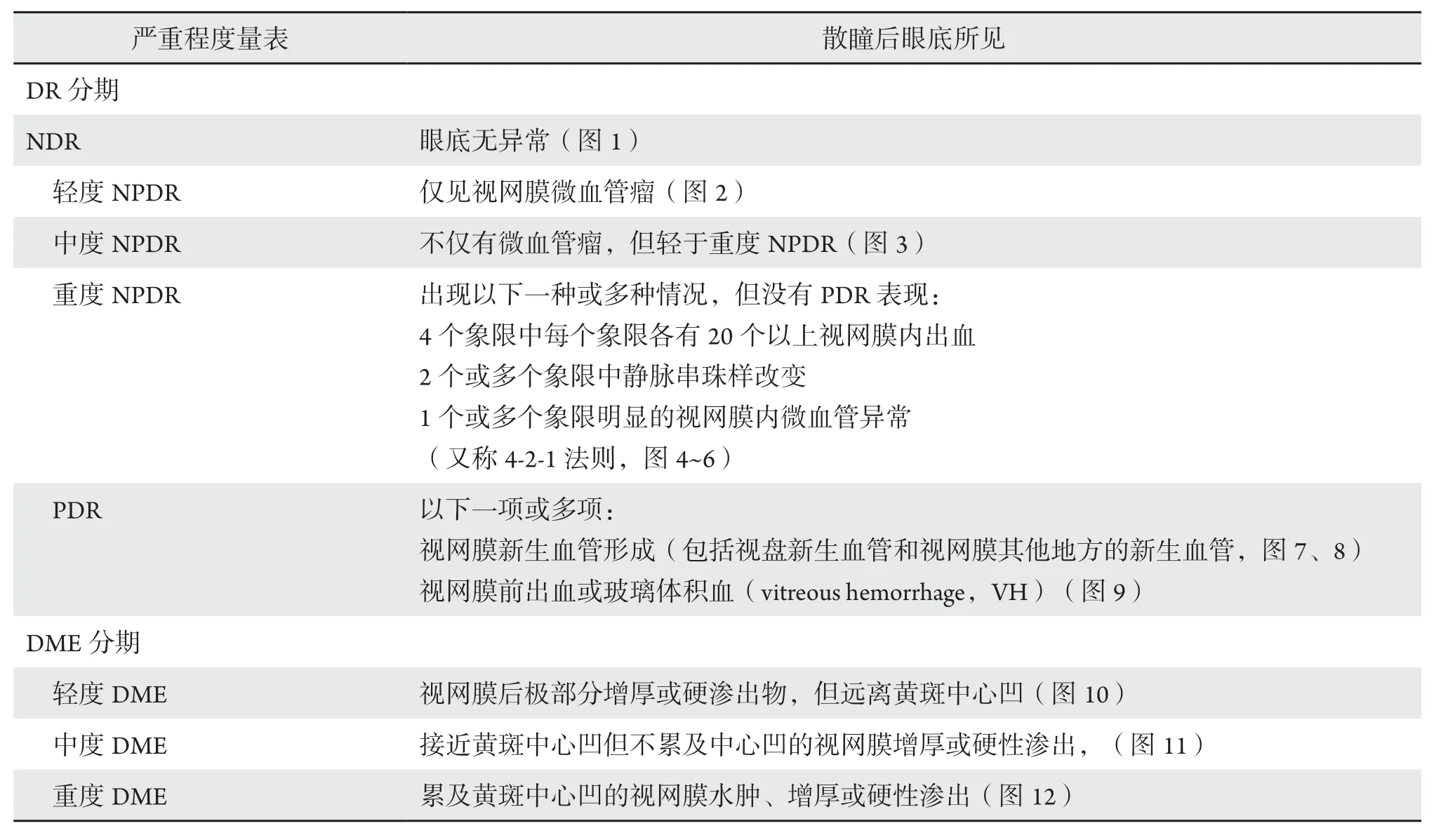
表1 DR 和DME 分期Table 1 Classification of DR &DME
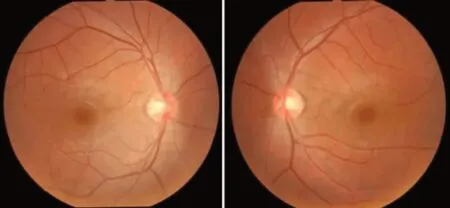
图1 正常眼底Figure 1 No abnormalities
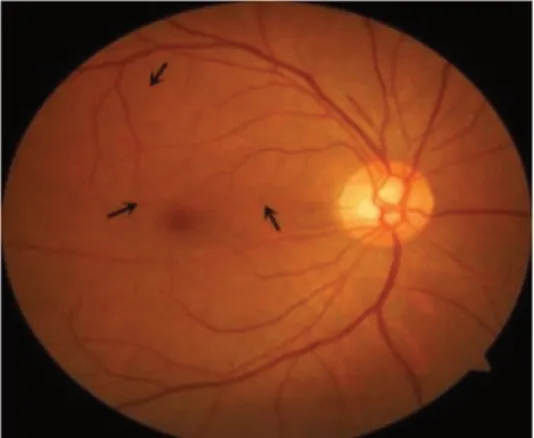
图2 轻度NPDR仅微血管瘤,见黑色箭头Figure 2 Microaneurysms only (as indicated by the black arrow)

图3 中度NPDR较轻度NPDR严重,但轻于重度NPDRFigure 3 More than just microaneurysms but less than severe NPDR
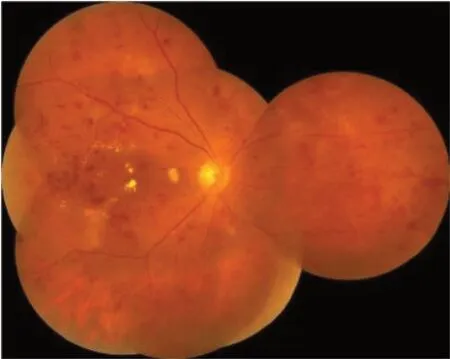
图4 重度NPDR每个象限视网膜出血均大于20个Figure 4 More than 20 intraretinal haemorrhages in each of four quadrants
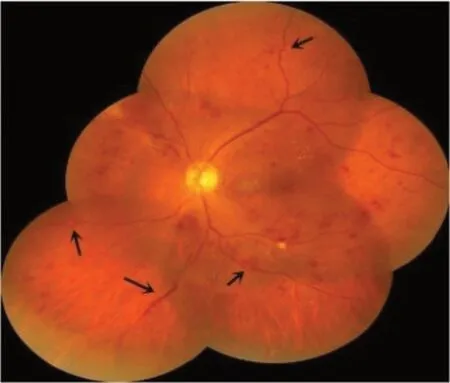
图5 2个及2个以上象限静脉串珠样改变如箭头所示Figure 5 Definite venous beading in two or more quadrants (as indicated by the black arrow)
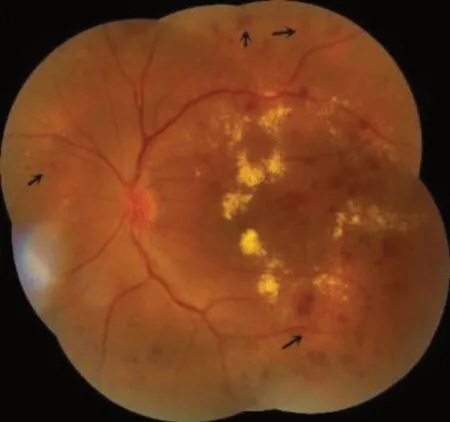
图6 一个象限及以上的视网膜微血管异常如箭头所示Figure 6 Prominent intraretinal microvascular abnormalities in one or more quadrants (as indicated by the black arrow)
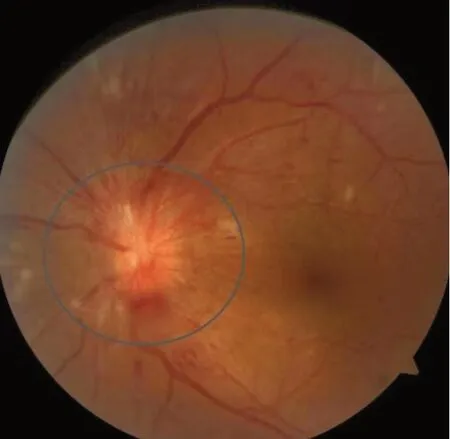
图7 视盘新生血管如蓝圈内所示Figure 7 Neovascularization at the disc (as shown in the blue circle)
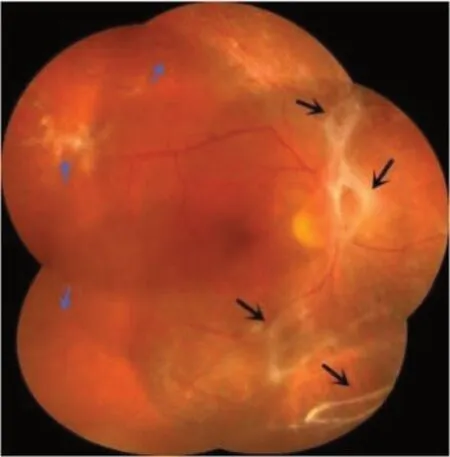
图8 视网膜新生血管和视网膜增殖膜视网膜新生血管(蓝色箭头所示)和视网膜增殖膜(黑色箭头所示)Figure 8 Neovascularization of the retina (as indicated by the blue arrow) and retinal proliferative membrane (as indicated by the black arrow)

图9 视网膜前出血和VH如黑色箭头所示Figure 9 Vitreous or preretinal haemorrhage (as indicated by the black arrow)
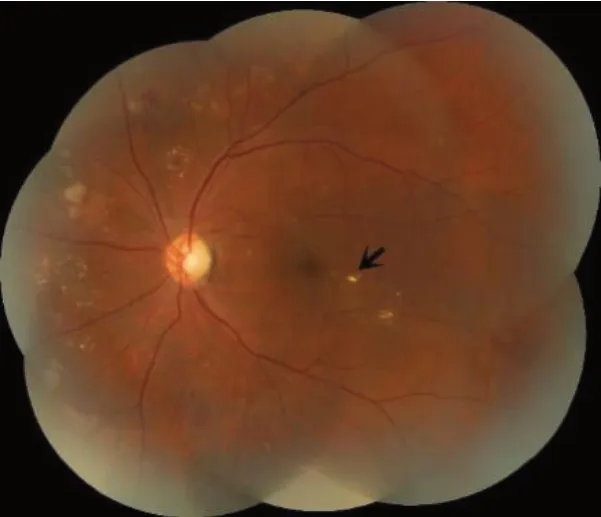
图10 后极部视网膜增厚或硬性渗出,离黄斑较远如箭头所示。Figure 10 Retinal thickening or hard exudates in posterior pole but distant from the centre of the macular (as indicated by the black arrow)
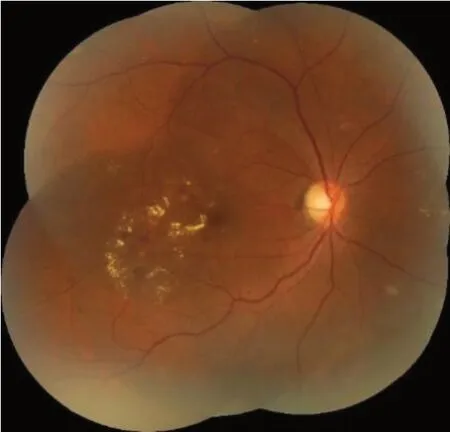
图11 视网膜增厚或硬性渗出接近黄斑中心凹但未累及黄斑中心凹Figure 11 Retinal thickening or hard exudates approaching the centre of the macular but not involving the centre
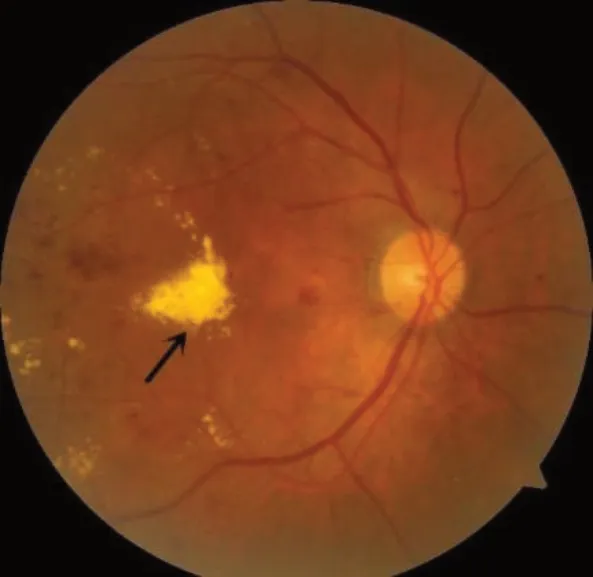
图12 累及黄斑中心凹的硬性渗出Figure 12 Retinal thickening or hard exudates involving the centre of the macular
自然病程包括轻度NPDR以血管通透性增高为特征,中度和重度NPDR以进行性视网膜毛细血管渗漏或丢失为特征,导致视网膜缺血,再到PDR以视盘和视网膜上新血管的形成为特征。这些新的血管生长通常伴随着增殖膜的形成,随后新生血管破裂或增殖膜收缩导致VH和牵拉性视网膜脱离,患者的视力水平取决于发生的关键结构损坏程度。威胁视力的DR包括重度NPDR、PDR和DME[11]。NPDR患者通常无症状,如果发生PDR,患者可能会因玻璃体积血而突然失明,或视网膜脱离而丧失视力,DME会导致视力逐渐丧失。
3 DR的全科医师检查、评估和转诊
3.1 DR患者的全面眼科检查
包括测量裸眼视力、矫正视力和眼压,通过裂隙灯显微镜评估眼前节,如在眼压升高或虹膜新生血管的时候还需要进行房角镜检查,以及眼底检查。DR的临床诊断和特征主要基于眼底检查的特异性异常,直接眼底镜检查可在无创条件下直接、快速观察视网膜结构,可在早期发现DR、DME等,从而使全科医生能够及时采取措施,同时也能观察到艾滋病、梅毒、高血压、肾病等全身疾病的眼底表现,为诸多疾病提供诊治线索,因此是眼科专科医师的必备技能,也是每个全科医生应该熟练掌握的基础技能。检查方法:患者及被检者于暗室中,采取“三右三左”的位置,即被检者查看患者右眼,需在患者右侧,用右手持检眼镜,同理左侧。无闭角型青光眼病史的患者可用复方托吡卡胺滴眼液散瞳。嘱被检者先平视前方,将检眼镜置于被检眼前约2 cm处,光带在瞳孔区,根据检查者和被检眼的屈光状态旋转检眼镜轮盘,直到看清视网膜结构,先沿血管走行方向看到视盘,再到视网膜后极部和黄斑,最后检查周边视网膜,可嘱被检者转动眼球以扩大观察范围。将所见的视盘、黄斑、视网膜血管、周边视网膜等进行描述。
3.2 眼底筛查评分和转诊要求
眼底筛查评分见表2[12]。转诊要求:1)DR眼底筛查1级病变无视力障碍(视力≥0.7),可不转诊,每年筛查1 次;2)DR眼底筛查1级病变有视力障碍(视力<0.7),或无视力障碍但评分较前次筛查增加,应转诊到有评估条件的医院;3)DR眼底筛查2级以上病变无视力障碍,可继续观察;若视力<0.7或评分较前次前次筛查增加,应转诊到有评估条件的医院;4)DR眼底筛查3级以上病变无视力障碍,可继续观察;若视力<0.7或评分较前次前次筛查增加,应转诊到有评估条件的医院;5)DR眼底筛查4级病变,应转诊有评估和治疗条件的医院;4级且评分达到20分,应尽快转诊。

表2 眼底筛查评分Table 2 Fundus screening score
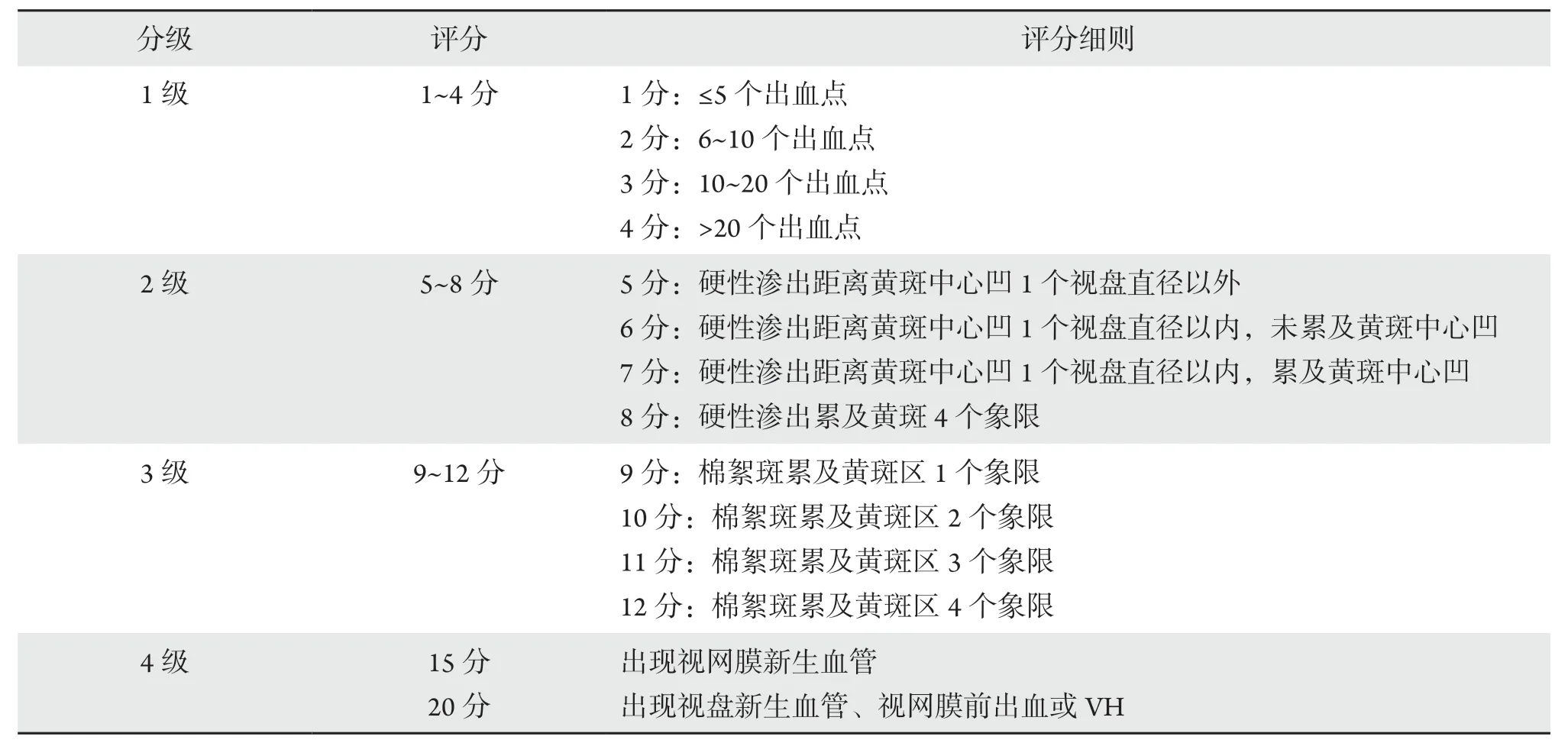
续表
4 治疗
4.1 全科预防治疗
4.1.1 控制高血糖、血糖波动和糖化血红蛋白
较高的血糖和HbA1c水平与DR的进展显著相关[13-14],较大的血糖波动也与DR发生发展有关,故纠正餐后高血糖对于预防DR也很重要[15]。严格控制高血糖和糖化血红蛋白水平可降低发生DR及其进展的风险,强化血糖控制可使DR风险降低20%[16],研究表明糖化血红蛋白宜控制在6.5%以内以避免DR发生和进展,若经最大努力降糖治疗,糖化血红蛋白仍未降至7%以下,也应该控制在7.1%~8.5%范围内[17]。高血糖对视网膜的损害还存在一个“代谢记忆”,即早期高血糖对视网膜存在持续的损害,即使后来将血糖控制在一个安全的范围内,DR还是会继续发生和发展。很早之前在动物身上进行的一项研究显示,在血糖控制不佳2.5年后,当时没有明显的DR迹象,即使在随后的2.5年间血糖控制良好,实验动物还是患上了严重的DR,和在整个5年期间血糖控制不佳的动物身上观察到的情况一致[18]。已有研究证实,视网膜是易受葡萄糖诱导的记忆效应影响的组织[19]。值得注意的是,胰岛素增敏剂有引发水肿的药物不良反应,特别是联合胰岛素使用时,有文献报道吡格列酮可能增加DME的患病风险[20],但也有学者经过4年对照研究,发现该类药物对DME发生或进展没有必然的联系[21]。基层全科医师应根据患者的具体病情制定降糖治疗方案,并指导患者使用药物,将患者的血糖水平控制在一个相对安全的水平。
4.1.2 控制高血压
很早的一项研究随机分配糖尿病合并高血压病的患者到不同的血压控制组[<150/85 mmHg(1 mmHg=0.133 kPa)组和<180/100 mmHg组],经过7.5年的随访,血压控制良好组的DR进展率下降了34%,接受视网膜激光减少了33%,而视力丧失下降了50%[22]。目前大多数研究都支持严格控制血压能降低DR进展风险[23-24],且舒张压比收缩压更能预测患者DR的恶化程度[25]。在糖尿病合并高血压的治疗中,血管紧张素转化酶抑制剂(angiotensin-converting enzyme inhibitor,ACEI)及血管紧张素Ⅱ受体阻断剂(angiotensin Ⅱ receptor blocker,ARB)这两类药都是临床上用于糖尿病合并高血压的一线降压药物,两者在降压同时不减少心、脑、肾等重要器官的血流量,还可降低肾内血压,改善肾小球滤过膜的通透性,减少蛋白尿的排出、抑制肾脏组织细胞的硬化,并可改善机体对胰岛素的敏感性,减低胰岛素抵抗,有效改善动脉内皮功能,延缓大血管与微血管损伤,且对糖、脂代谢无负面影响。有研究者发现,RAAS是VEGF控制内皮细胞屏障的效应器之一,故ACEI还可延缓DR进展[26]。长效钙通道阻滞剂(calcium channel blockers,CCB)具有可靠的降压效果和靶器官保护作用,且对糖代谢无不良影响,因而可用作不能耐受ACEI/ARB治疗的2型糖尿病合并高血压患者的首选药物,或在单用ACEI/ARB治疗血压不能达标时与之联合应用。有报道短效二氢吡啶类(如硝苯地平),大剂量使用可能有潜在的抑制胰岛素释放的作用,故不推荐使用[27-28]。β受体阻滞剂在降压的同时,可降低心血管危险因素,但此类药物可引起胰岛素抵抗、甘油三酯增高、降低高密度脂蛋白胆固醇,在降压同时对糖脂代谢具有不利影响,故此药不作为具有糖代谢异常的高血压患者降压的首选用药。长期大剂量应用利尿剂对内分泌代谢系统具有潜在的负面作用,如引起低血钾、增加胰岛素抵抗、加重糖脂代谢和嘌呤代谢紊乱等,所以利尿剂不能单独作为2型糖尿病伴高血压患者降压的用药,仅可联合用药。糖尿病合并高血压的降压药物联合使用ARB/ACEI是首选用药,再联合利尿剂或CCB等,可提高2型糖尿病合并高血压患者的降压效果[29]。降压药物选择时应综合考虑降压疗效、对重要脏器的保护、安全性和依从性以及对代谢的影响等因素。中华医学会糖尿病学分会推荐糖尿病合并高血压患者,在安全达标的前提下降压目标在130/80 mmHg以下,糖尿病伴严重冠心病或年龄在65~80岁的老年患者,可采取相对宽松的降压目标值,控制在140/90 mmHg以下,80岁以上患者或有严重慢性疾病(如需要长期护理、慢性疾病终末期)者,血压可控制在150/90 mmHg以下,对于伴有缺血性心脏病的老年高血压患者,在强调收缩压达标的同时应关注舒张压,舒张压不宜低于60 mmHg[30]。
4.1.3 控制血脂
脂代谢异常可加重DR进展,在DR病程中起重要作用[31]。一项针对200例糖尿病患者的研究中发现,与NDR患者相比,DR患者的平均总胆固醇,甘油三酯和低密度脂蛋白显著更高,且DR患者的高密度脂蛋白胆固醇非常低[32]。也有研究发现,甘油三酯-葡萄糖指数与DR显著相关[33]。内皮功能障碍在高胆固醇血症患者中比较常见,而内皮功能障碍是发生糖尿病血管并发症的重要因素,血清总胆固醇升高是DR的重要危险因素,也是视网膜硬性渗出密度的独立危险因素[34]。低密度脂蛋白与DR的危险性的增加显著相关,降低低密度脂蛋白水平能够显著降低DR危险[35]。控制血脂临床首选他汀类调脂药物,一项关于1648300多例糖尿病患者的临床试验表明,他汀类药物治疗明显降低了NPDR、PDR和玻璃体积血的发病率,并表明他汀类治疗对于威胁视力的糖尿病患者的治疗是必须的[36]。Pranata等[37]发现他汀类药物治疗可降低DR的风险,并减少了治疗性玻璃体内注射和玻璃体切割术的需要。非诺贝特对视网膜色素上皮层细胞显示出保护性抗炎和抗凋亡作用,这种机制与其调脂作用无关[38],在一项针对9795例糖尿病患者的研究表明,非诺贝特将DME的激光治疗频率降低了31%,PDR降低了30%[39]。控制低密度脂蛋白胆固醇的目标值:有明确有动脉粥样硬化性心血管疾病病史患者低密度脂蛋白胆固醇<1.8 mmol/L,无动脉粥样硬化性心血管疾病病史的糖尿病患者低密度脂蛋白胆固醇<2.6 mmol/L[30]。
4.1.4 干预生活方式
有研究者报道,吸烟、肥胖也会导致DR发生、发展[40-41],生活方式干预是控制DR的重要手段,主要包括健康教育、减少钠盐摄入、合理膳食、规律运动、不吸烟、不饮酒、控制体重、减轻精神压力、保持心理平衡等,故在全科治疗中干预生活方式,倡导健康行为也同样重要。
4.1.5 宣教
关于患者对糖尿病和DR的认识,大多数糖尿病患者都知道糖尿病管理,然而对DR的认识较少。有调查显示,66.88%的患者表示他们没有被告知DR,仅有33.11%的患者最初谈到了发生DR的风险,对DR的不了解率与较低的教育水平、女性、年轻和较短的糖尿病病程显著相关[42],故对糖尿病患者进行DR宣教非常重要。
4.1.6 早期发现
虽然DR在全世界的发病率正在上升,但发达国家的流行病学证据表明,由于糖尿病及其并发症管理的改善,通过定期筛查DR和及时激光光凝治疗,早期发现DR的发病和进展,失明率呈下降趋势[43]。结合后期的视功能严重受损导致的劳动力丧失减少收入、DR治疗开支费用综合评估,若在美国开展1型糖尿病的常规年度筛查并及时治疗以阻止疾病进展,将会在20年内节省10亿美元[44]。DR的早期筛查和病情随访是非常重要的。DR在威胁视力之前往往缺乏眼部症状,故这类患者多数没有进行眼部检查。若在严重视力丧失发生之前就及时行眼科干预,这对于降低DR所导致的视力丧失风险是最有效的。根据国际眼科学理事会和美国糖尿病协会于2018年报告的DR筛查指南,对于2型糖尿病患者,一旦确诊糖尿病,应开始第一次眼科检查,而1型糖尿病,初次筛查可延长至糖尿病诊断后5年,另一方面,最低限度的筛查包括视力检查和视网膜检查[45]。随后NDR患者至少每年进行1次复查。有DR者,则应增加检查频率:轻度NPDR患者每年1次,中度NPDR患者每3~6个月1次,重度NPDR患者每3个月1次。在英国,所有12岁及以上的糖尿病患者每年都会接受DR筛查,所有DR筛查都需要拍摄眼底照相,且眼底照片由经过培训的专业人员审查,如果有疑似的DR或图片成像不清,均会转交给眼科医师判断[46],所以在英国实施的糖尿病眼底筛查下,视力丧失明显减少,DR不再是工作人群视力损失的最常见原因。近年来,随着人工智能的兴起,已有资料显示在识别DR方面,人工智能可与眼科专科医师水平相当,甚至更好,人工智能系统还可以节约人力资源成本来改善DR筛查,并可能被纳入当前实施或常规实施的未来筛查计划[47-49]。人工智能应用程序和可穿戴设备通过允许人们实时跟踪自己的健康行为,包括饮食、运动、减肥、睡眠模式以及血糖和血压等健康指标,改善了自我保健;并通过自动化时间表、警报和提醒等功能提高药物依从性[50]。
4.2 眼科治疗
4.2.1 全视网膜激光光凝术
早在20世纪七八十年代进行的随机对照试验结果就已支持在PDR中使用全视网膜激光光凝术(panretinal photocoagulation,PRP),PRP改善DR的机制尚未完全了解,一种可能的机制是产生新生血管生长因子的缺血视网膜被PRP破坏,从而减少血管生成刺激,另一种可能的机制是PRP区域的视网膜变薄,激光瘢痕增加了从脉络膜到视网膜内部的含氧量[51-52]。PRP在未来多年内将继续在DR和DME的治疗中发挥关键作用。
4.2.2 经平坦部玻璃体切割术
目前为止,经平坦部玻璃体切割术(Pars Plana Vitrectomy,PPV)用于严重的PDR、VH、视网膜脱离的治疗,在PPV术中还可以完成PRP治疗。PPV对糖尿病并发症的结局总体上有所改善,但部分患者的术后视力和视网膜解剖结构较差,需要再次、多次手术[53]。
4.2.3 玻璃体抗VEGF药物注射术
VEGF通过破环视网膜内皮细胞间的紧密连接而影响血视网膜屏障,在DME发生、发展中起着关键作用,且DME的严重性与VEGF呈正相关[54]。目前抗VEGF治疗是DME的一线治疗,玻璃体腔直接注射抗VEGF药物这种给药途径的优势是药物经玻璃体腔注射,可使药物直达病灶,快速发挥作用,避免药效在机体内扩散过程中被削弱,还避免了全身用药的不良反应,对减少DME患者的视力损失具有明显效果。在治疗初期,患者需要进行每月1次眼内注射、3次或者5次的负荷治疗,随着病情稳定,注射间隔可能会延长。
5 小结和展望
在我国老龄化的当前和未来,糖尿病患者将越来越多,DR是最常见的致盲性视网膜血管疾病,其危险因素包括血糖控制不佳、高血压、血脂异常、糖尿病持续时间延长和遗传因素。糖尿病眼睛早期筛查可降低糖尿病患者视力下降的风险,全科医师识别和管理可改变的危险因素对于预防DR的发生和发展非常重要,根据病情和眼底评分将患者及时转诊眼科。DR的眼科治疗包括PRP、PPV和玻璃体注射抗VEGF药物,将视力受威胁的DR患者及时转诊至眼科有助于挽救其视力,降低个人、家庭、社会乃至国家的负担,期望我国DR的诊治率能逐步提升而致盲率逐步下降。
利益冲突所有作者均声明不存在利益冲突
开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。详情请访问:https://creativecommons.org/licenses/by-ncnd/4.0/。
