骨科植入材料用三维高孔隙率金属钽的制备研究
2023-04-29谷立民孙宇辰井蕊璇代丽娜马传佳李渭
谷立民 孙宇辰 井蕊璇 代丽娜 马传佳 李渭

摘 要:多孔金属钽是一种具有良好亲生物性和骨长入特性的新型骨科植入材料,采用传统制备工艺获得的产物,具有物相不纯、孔隙率较低以及制备成本高的弊端.采用多方位分段式出气化学气相沉积(MDSO-CVD)技术,以三维网络连通结构的多孔碳为基底,制备了一种新颖的三维高孔隙率金属钽材料,并深入研究了沉积温度和沉积时间对三维金属钽结构演变的影响,揭示了沿气体流场方向金属钽的沉积规律.分别利用X射线衍射仪、扫描电子显微镜和透射电子显微镜对金属钽的物相和微观结构进行分析;采用失重法测量金属钽的孔隙率.研究结果表明:当沉积温度为1 000 ℃和沉积时间为12 h时,获得纯相金属钽材料的孔隙率高于80%,该材料可作为一种压缩性能优异的骨科植入材料.因此,本文开发的高效、规模化制备三维高孔隙率金属钽的MDSO-CVD方法,可为金属钽应用于医学领域提供重要的制备技术支撑.
关键词:金属钽;三维结构;高孔隙率;可控制备;压缩性能
中图分类号:TB33
文献标志码: A
文章编号:2096-398X(2023)04-0119-07
Abstract:Porous metallic tantalum is a new type of orthopedic implant material with the characteristics of good biocompatibility and bone ingrowth.The product obtained by the traditional preparation process has the disadvantages of impurity,low porosity and high cost.In this work,a novel three-dimensional (3D) metallic tantalum with high porosity was prepared controllably by a multi-directional segmented outgassing chemical vapor deposition (MDSO-CVD) technique with 3D network connected structure porous carbon as the substrate.The effects of deposition temperature and deposition time on the structure evolution of 3D tantalum material were investigated,and the deposition law of tantalum along the direction of gas flow field was revealed.The phase and microstructure of metallic tantalum were analyzed by XRD,SEM and TEM,respectively.The porosity of tantalum was measured by weight loss method.When the deposition temperature was 1 000 ℃ and the deposition time was 12 h,the as-prepared pure metallic tantalum showed the high porosity of more than 80%,which can serve as an orthopedic implant material with good compression property.Therefore,the efficient,large-scale and controllable MDSO-CVD method of 3D high-porosity tantalum material developed in this work provides important technical support for the application of metallic tantalum in the medical field.
Key words:metallic tantalum; three-dimensional structure; high porosity; controllable preparation;compressive property
0 引言
多孔鉭骨科植入材料是通过在多孔材料表面沉积金属钽,制备具有良好亲生物性和骨长入特性的新型骨科植入材料,其高孔隙率、低弹性模量和高摩擦系数等特性,特别适用于骨替代、关节置换和人体组织填充等领域,具有广阔的应用前景[1-5].作为新兴的骨科植入材料,第一例多孔钽假体在1997年植入人体,已经有20年的历史了.多孔钽骨科植入材料创造了8~10年随访多孔钽金属臼杯翻修率为0的记录,平均10.3年(9.6~10.8年)的随访没有发现任何的骨溶解,在治疗关节疾病方面具有优异的效果[6-8].
目前,制备多孔钽材料的工艺主要有化学气相沉积法(CVD)、粉末浇筑高温烧结法、激光快速成型法、有机泡沫浸渍法、3D打印法等[9-14].由于医用多孔钽必须具备三维连通结构,如十二面体结构等,与自然骨相近,以便进行骨长入,因此需具有较高的孔隙率,一般达到70%以上[15].而采用CVD法制备多孔钽骨科植入材料,能够让反应气体充分深入孔隙内部,在多孔结构表面沉积具有极高纯度的金属钽,避免其他杂质对其生物相容性的影响[16,17],并且能够通过调整沉积工艺,对多孔钽的力学性能(比如压缩性能)进行调控,以满足不同部位骨组织的力学性能要求.然而,采用普通CVD法制备多孔钽大多为二元气相反应过程,沉积反应较为复杂,产物纯度低;而且金属钽属于难溶金属,蒸发困难,往往需要在真空环境下进行,从而导致制备成本增加,进一步限制其实际应用.
因此,为了提升多孔钽材料孔隙率的同时,并使其纯度提高且制备成本降低,本工作开发出多方位分段式出气化学气相沉积(MDSO-CVD)技术,以高孔隙率三维连通结构多孔碳为基体,制备出沉积均匀性提升、孔隙率较高的三维纯相金属钽材料.首先,将纯钽置于沉积炉前端与氯气反应生成气相氯化钽(TaCl5),随后TaCl5在沉积室不同位置与多通道通入的氢气发生还原反应,从而在多孔碳上原位沉积高纯金属钽.通过研究不同沉积温度、沉积时间和沉积位置对金属钽沉积效果的影响,探索了沿气体流场方向金属钽在多孔碳上的沉积规律.因此,该工作为制备高效、低成本、三维高孔隙率的多孔钽材料开辟了一条新途径,为多孔钽作为骨科植入材料应用于医学领域提供了技术支撑.
1 实验部分
1.1 主要原料
前驱体为三维连通结构多孔碳材料(孔隙率>96%,自制),纯钽(纯度>95%,宁夏东方钽业),氢气、氩气、氯气,氮气(AR,>99.9%).
1.2 多孔碳基底的制备
将聚氨酯泡沫在去离子水与乙醇中分别进行超声清洗,然后置于烘箱中干燥.将预处理后的泡沫放置在气氛炉中保证其受热均匀,在惰性气氛下加热至900 ℃,保温2 h后冷却至室温得到具有三维连通结构的多孔碳基底.
1.3 三维金属钽的制备
将多孔碳基底切割为5×10×120 mm的长条,置于自主研制的化学气相沉积设备反应室内,再将纯钽放置于沉积炉的前端,同时以2 mL/min的氯气流量從沉积炉的前端通入反应室内与5 mL/min的氢气流量从沉积炉不同位置通入反应室内,分别在沉积温度为700 ℃、800 ℃、900 ℃、1 000 ℃和1 100 ℃时制备了五个样品.
1.4 性能表征
(1) X射线衍射仪 (XRD)
采用日本岛津公司生产的XRD-7000S型X射线衍射仪对制备的样品进行物相分析,辐射源采用Cu Kα射线(λ=0.154 18 nm),扫描2θ范围为10°~90°,扫描速率为10° min-1.
(2) 扫描电子显微镜分析 (SEM)
采用蔡司MERLIN Compact超高分辨率场发射扫描电镜观察制备样品的形貌及孔隙分布情况.
(3) 透射电子显微镜分析 (TEM)
通过透射电子显微镜(TEM,JEM-3010)对样品进行晶相结构与元素分布分析.
(4) 孔隙率
采用失重法对多孔钽进行孔隙率计算.将质量为m0的样品吊于干净的烧杯中,将烧杯注入乙醇至样品悬浮于乙醇中质量为m1,将其完全浸入溶液中至其饱和状态取出去除表面多余溶液得到质量m2,孔隙率由式(1)确定:
式(1)中:P—材料孔隙率,%;m0—材料在自然状态下的质量,或称干重,g;m1—材料在乙醇中的悬浮质量,或称悬浮重,g; m2—材料在乙醇中浸泡至饱和状态的质量,或称湿重,g.
(5) 密度测试
密度指在规定温度下把某种物质单位体积内所含物质的质量数即同种物质质量m0和体积v0的比值,由式(2)求出:
式(2)中:ρ—材料密度,g/cm3;m0—材料在自然状态下的质量,或称干重,g;ν0—材料在自然状态下的体积,cm3.
2 结果与讨论
2.1 多孔碳基体的表征
图1为三维多孔碳基体的微观形貌表征.由图1能够明显看出,碳基体具有三维网络连通结构,且表面较为粗糙,有利于金属的沉积和生长.随后,通过对碳基体进行孔隙率测试,其结果如表1所示,制得的样品密度较均匀且具有较高的孔隙率(95%~97%),这将为制备三维高孔隙率金属钽材料提供了有效的前驱体.
2.2 氯气和氢气的流量比对金属钽沉积效果的影响
在本研究中,金属钽沉积反应依据如下反应方程式进行:
在实验中,氯气和氢气的流量比是按照化学反应公式的反应计量比1∶1确定的,还原气体氢气与氯气只要不低于1∶1,就能保证反应的顺利进行.若提高氢气的流量,由于被还原的TaCl5没有增加,对沉积效果的影响不大;若降低氢气流量,反应生产的TaCl5不能被充分还原,沉积效果会大幅度降低.
2.3 沉积温度对金属钽沉积速率与微观形貌的影响
为了探究沉积温度对金属钽的沉积速率的影响,首先将8×20×20 mm同种多孔碳试样放置于距离反应室前端30 mm的位置,在相同的工作气体流量下,分别将试样在700 ℃、800 ℃、900 ℃、1 000 ℃和1 100 ℃的反应温度下沉积12 h.图2为不同反应温度与沉积速率之间的关系图.从图2可以看出,从700 ℃上升至1 000 ℃时,金属钽的沉积速率随着温度的升高,呈现快速上升趋势(斜率大小:kba<kcb<kdc).而当温度升高至1 100 ℃,沉积速率的增加逐渐变的缓慢(ked变小),由此可知过高的温度不利于金属钽的高效沉积.
图3呈现的是不同温度下沉积的金属钽的微观形貌表征.具体表现为:试样在700 ℃和800 ℃温度下,沉积速率较低时,沉积的金属钽晶粒呈现“菜花状”;随着温度的升高,TaCl5和H2的还原反应速率急剧增加,大量金属钽沉积在多孔碳基体上,形成致密的金属钽涂层,将碳骨架完全包裹.当沉积温度为1 000 ℃时,碳基体表面样品的均匀程度和致密性较高,而当温度继续升高到1 100 ℃时,沉积生成的晶粒变得粗大,甚至开始出现少量细微裂纹,破坏了表面的致密性,可能会导致材料易脆易断裂,对其后续的应用造成很大的影响.由此可知,温度在1 000 ℃的沉积条件下所制备的金属钽样品具有最佳的形貌,在三维碳骨架的表面均匀分布且致密性良好.因而,碳基体上沉积的金属钽形貌可通过调控沉积温度进行优化.
2.4 沉积温度对金属钽压缩性能的影响
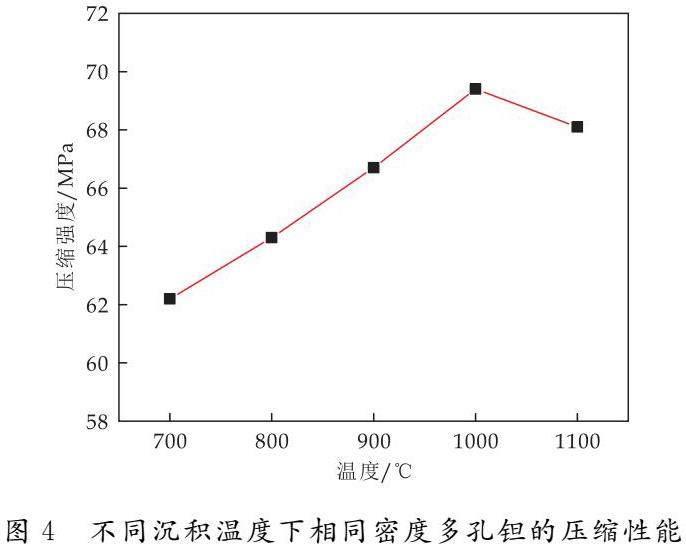
良好的骨科植入物应具备优异的力学性能.为研究沉积温度对碳载金属钽材料的压缩性能影响,在不同沉积温度下将金属钽沉积到相同的密度后,进行压缩性能测试.从图4所示的测试结果可以看出,随着沉积温度的增加,压缩强度逐渐提高,这可能由于沉积温度升高,钽的晶粒尺寸增大,致使晶型更加完整且结合得更加紧密的缘故.当沉积温度进一步升高至1 100 ℃时,由于晶粒尺寸不断生长,出现晶粒粗大,样品表面开始出现微裂纹现象(如图3(f)所示),造成压缩强度出现一定程度的降低.总的来看,不同沉积温度下相同密度碳载金属钽的力学性能出现一定的差异.综上所知,1 000 ℃为样品最佳的沉积温度.
2.5 沉积时间对制备金属钽的影响
多孔钽作为骨科植入体,其应用环境多为植入体与原生骨组织融为一体,长期留在人体,不需要二次手术取出,因此制备的多孔钽必须具有较高的纯度[18-21],以确保其具有良好的生物相容性.因此,在调控沉积温度的基础上对其进行实验条件的进一步优化,通过在1 000 ℃沉积温度条件下,分别进行了6 h、12 h和18 h沉积时间来制备出了一组样品.
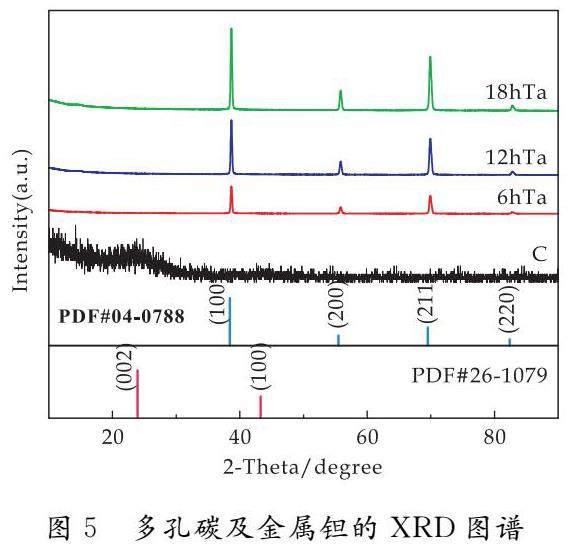
首先,对实验用的多孔碳和制备的金属钽进行X射线衍射分析.从图5所示的XRD图谱可以看出,多孔碳基体表现出明显的非晶态衍射峰,说明该多孔碳为无定型态.而金属钽在2θ为38°、55°、69°和84°处出现了明显的衍射峰,分别对应于金属Ta(PDF#04-0788)的(110)、(200)、(211)及(220)晶面,且峰型尖锐且无杂峰,这可归因于所制备的金属钽具有良好的结晶性和较高的纯度.随着沉积时间的逐渐增加,衍射峰强度逐渐增加且更为尖锐,这是由于沉积时间的增加,所制备得到金属钽的结晶性更高.
将实验用多孔碳基体剪裁成5×10×120 mm的多孔碳长条后沿沉积室长度方向放置,前端距离反应室30 mm,在设定的反应气体流量和1 000 ℃沉积温度下,沉积时间分别为6 h、12 h和18 h,制备样品的表面状态如图6所示.
实验结果表明,自主研制的多孔碳进行6 h沉积后,试样前端出现少量淡银色金属光泽,具有一定的硬度,表明金属钽已经沉积在多孔碳表面.而试样末端呈现出大部分的深黑色,为多孔碳颜色,这可能由于沉积时间太短,多孔碳末端沉积少量金属钽.沉积12 h后,试样末端颜色也变为淡银色,表明随着反应时间的延长,试样前端孔隙率变低,气流阻力增大,使得部分反应气体能够到达试样末端并沉积.沉积时间延长至18 h,试样整体银色加深,说明随着沉积时间的延长,金属钽在多孔碳上的沉积量增加.对不同沉积时间试样的末端取样进行扫描电镜分析,其结果如图7所示.
从图7所示的扫描电镜照片可以看出,进行6 h沉积后,黑色部位局部有少量的金属钽沉积,绝大部分仍为多孔碳的三维连通结构,并且由于取样过程中的挤压、碰触,部分碳结构断裂,表明碳骨架结构在沉积过程中受到Cl2和HCl气体的腐蚀影响,结构强度显著降低.当沉积12 h后,末端呈现为银色,已经有较明显的金属钽沉积,并且完全包裹了碳表面,形成具有三维连通的多孔结构.当沉积18 h后,金属钽能够形成致密的沉积层,并在局部形成了较粗大的晶粒沉积.可见,沉积时间过长,大量的金属钽会过渡堆积而形成不均匀的杂乱结构,从而影响孔结构的形成.
2.6 最优金属钽样品的分析表征
基于上述结果,以1 000 ℃的沉积温度和12 h的沉积时间制备高纯多孔金属钽能够获得最佳的微观形貌.因此,对于该实验条件下制备的样品进行了透射电子显微镜表征,图8为金属钽的透射电镜照片.
图8(a)显示了样品的微观形貌,其是由大量的金属钽颗粒互相融合,沉积的金属钽致密性良好.在图8(b)所示的高分辨透射照片中可以看出該样品呈现出多晶的特征,晶粒取向各不相同,还有丰富的晶界.其中0.23 nm和0.13 nm的晶格条纹分别对应于金属钽的(110)和(211)晶面,能够很好地与XRD结果相对应.由此可见,已成功将金属钽沉积于碳骨架基体上.图8(c)~(f)的元素mapping图表明样品含有C、Ta和O元素,C元素的mapping图颜色与碳膜颜色接近,表明样品中C的含量较低;O元素的存在可能是金属Ta表面被空气部分氧化造成的;而金属钽均匀分布在样品中,这表明了碳载金属钽材料的成功制备.
2.7 沿气体流场方向金属钽的沉积规律及改进方法研究
采用普通CVD技术,将沉积温度为1 000 ℃和沉积时间为12 h的试样沿长度方向切割成11个5×10×10 mm的试样块,编号为a1~a11,并放入沉积设备中制备样品,如图9(a)所示.然后,测量a1~a11样品的质量、密度和孔隙率,测试结果如图10所示.从图10的测试结果可以看出,试样的质量、密度和孔隙率沿长度方向基本呈现线性变化,末端试样的质量只有前端的38.03%,孔隙率则高出了13.74%.
实验结果表明,采用普通CVD技术制备的样品因沉积室位置不同而沉积效率存在明显差异,这是因为TaCl5和H2进入反应室后,反应气体的浓度较高,使得在一定温度下还原反应迅速发生,将金属钽快速沉积在多孔碳前驱体上,同时生成大量的HCl气体.随着反应气体在反应室的流动扩散和反应的持续进行,TaCl5和H2被大量消耗,反应气体浓度延流场方向显著降低.流经反应室末端时,TaCl5和H2的浓度已经变得很低,仅能进行少量的还原反应,进而造成在试样的前后端存在较大的沉积效率差异.这种情况会造成同炉产品的性能和质量存在极大的差异,不利于工业化批量生产.
图11是采用多方位分段式出气CVD技术制备的试样沿气流方向不同位置的质量、密度和孔隙率测试结果.具体方法:将H2的导气管延长100 mm,并将其出气端面封闭,在朝向试样的方向加工6个直径2 mm圆孔,将H2引入到沉积室不同长度方向,达到控制不同位置金属钽沉积效率的目的,如图9(b)所示.采用与上述相同的方法对试样进行沉积和分割,编号为b1~b11.
结果表明,末端试样的质量是前端的46.44%,整个样品的孔隙率高于80.73%,前端较末端低11.65%,差异小于普通CVD技术制备的试样(13.74%).相比图9的结果,该样品的整体沉积速率提高了4.6%,前端和末端的质量差异有所改善.因此,采用多通道进气的方式,将TaCl5和H2分别引入到反应室的不同位置,将能够有效解决沉积室内不同位置沉积效率差异的问题.
3 结论
本文以三维网络连通结构的多孔碳为基体,采用多方位分段式出气的CVD法,成功制备了一种新颖的高孔隙率金属钽材料,其具有与成骨相似的三维连通结构且金属钽纯度高.实验研究表明,沉积过程中不同沉积位置沉积速率差异较大,采用多通道进气的方式在一定程度上能够改善制品的沉积均匀性;调变沉积温度能够提高金属钽的有效沉积效率并降低生产成本.本研究为开发具有高孔隙率的多孔钽骨科植入材料提供了研究思路.
参考文献
[1] Jonitz A,Lochner K,Lindner T,et al.Oxygen consumption,acidification and migration capacity of human primary osteoblasts within a three-dimensional tantalum scaffold [J].Journal of Materials Science Materials in Medicine,2011,22(9):2 089-2 095.
[2] 李瑞端,戴传波.骨修复材料的研究进展[J].化学工程与装备,2018(9):265-266.
[3] 于晓明,谭丽丽,杨 柯.钽金属的医学应用研究进展[J].材料导报,2012,26(1):79-82.
[4] 张文毓.生物医用金属材料研究现状与应用进展[J].金属世界,2020(1):21-27.
[5] 杨 军,杨 群.多孔金属植入材料在骨科的应用[J].大连医科大学学报,2017,39(4):397-402.
[6] Balla V K,Banerjee S,Bose S,et al.Direct laser processing of a tantalum coating on titanium of bone replacement structures[J].Acta Biomater,2010,6(6):2 329-2 334.
[7] 应 明.多孔钽及在人工关节中的应用[J].生物骨科材料与临床研究,2006,3(2):1-3.
[8] 马 剑,李 乾,伊芸生.钽金属在医学领域的应用[J],实用骨科雜志,2014 20(4):329-333.
[9] 陈长军,张 超,王晓南,等.生物医用多孔钽制备工艺研究进展[J].热加工工艺,2014,43(4):5-8.
[10] Williams B E,Tuffias R H.Composite foam structure[P].US Patent:6929866,2005-08-16.
[11] 阮建明,叶 雷.医用金属植入材料多孔钽及其制备方法[P].中国专利:CN201010136854.4,2011-10-05.
[12] 党新安,汤 腾,陈巧富,等.快速原型技术制备复合材料的研究进展[J].热加工工艺,2012,41(2):108-112.
[13] 张 力,杨明让.医用多孔钽的制备方法及用途[P].中国专利:CN201110128842.1,2011-10-19.
[14] 杨 柳,王富友.医学3D打印多孔钽在骨科的应用[J].第三军医大学学报,2019,41(19):1 859-1 866.
[15] 甘洪全,刘 鑫,李琪佳.医学领域的新型骨科植入材料——多孔钽[J].中国煤炭工业医学杂志,2014,7(6):1 023-1 026.
[16] 高芮宁,熊胤泽,张 航,等.SLM制备径向梯度多孔钛/钽的力学性能及生物相容性[J].稀有金属材料与工程,2021,50(1):249-254.
[17] 张 璞,蒋 波,张 玲,等.3D打印多孔钽的生物安全性评价[J].医疗装备,2022,35(9):44-49.
[18] 蒋 波,张 玲,张 佩,等.3D打印多孔钽浸提液体外细胞毒性和遗传毒性研究[J].中国药业,2022,31(8):53-57.
[19] 郭 敏,郑玉峰.多孔钽材料制备及其骨科植入物临床应用现状[J].中国骨科临床与基础研究杂志,2013,5(1):47-55
[20] Nasser S,Poggie R A.Revision and salvage patellar arthroplasty using a porous tantalum implant[J].The Journal of Arthroplasty,2004,19(5):562-572.
[21] Kamath A F,Gee A O,Nelson C L,et al.Porous tantalum patellar components in revision total knee arthroplasty minimum 5-year follow-up[J].The Journal of Arthroplasty,2012,27(1):82-87.
【责任编辑:陈 佳】
基金项目:西安超码科技有限公司科研项目(2021)
作者简介:谷立民(1985—),男,陕西西安人,高级工程师,研究方向:功能材料
