不同方法提取活性污泥的胞外聚合物氧化还原特性分析
2023-04-29王先宝冉家荣陈甜甜张雨笛张敏婷谢怡俐侯银萍贺超张安龙
王先宝 冉家荣 陈甜甜 张雨笛 张敏婷 谢怡俐 侯银萍 贺超 张安龙
摘 要:为了探明不同方法提取活性污泥胞外聚合物(EPS)的氧化还原特性,采用四种典型的方法:加热法、超声法、EDTA法和甲醛-NaOH法分别提取活性污泥EPS,对其组分和氧化还原特性进行分析.结果表明:甲醛-NaOH法提取EPS含量最高,达到68.59 mg·g-1,其次为EDTA法(23.40 mg·g-1)、加热法(18.2 mg·g-1)和超声法(4.07 mg·g-1);化學法(甲醛-NaOH法和EDTA法)对EPS中氧化还原物质的提取效率高于物理法(加热法和超声法);不同方法提取EPS的电子接受能力和电子供给能力分别为0.07~0.30 μmole-·g-1和0.01 ~0.04 μmole-·g-1,其中EDTA法提取EPS的电子接受能力与电子供给能力最高.紫外可见光谱图和傅里叶红外光谱图均显示出EPS中存在腐殖类物质,且化学法提取的含量高于物理法;三维荧光光谱图显示出蛋白质和腐殖酸的荧光峰,加热法提取EPS的蛋白质峰荧光强度更高,而化学法提取EPS的腐殖酸峰荧光强度更高.
关键词:活性污泥;胞外聚合物;氧化还原特性;氧化还原物质
中图分类号:TB332
文献标志码: A
文章编号:2096-398X(2023)04-0008-07
Abstract:In order to investigate the redox properties of extracellular polymeric substances (EPS) in activated sludge extracted by different methods,four typical methods (heating,ultrasonication,EDTA and formaldehyde-NaOH methods) were used to extract EPS of activated sludge and analyzed its components and redox properties,respectively.The results showed that the highest EPS content was obtained by formaldehyde-NaOH method,reaching 68.59 mg·g-1,followed by EDTA method (23.40 mg·g-1),heating method (18.2 mg·g-1) and ultrasonication method (4.07 mg·g-1).The extraction efficiency of redox substances in EPS by chemical methods (formaldehyde-NaOH and EDTA methods) was higher than that by physical methods (heating and ultrasonication methods).The electron accepting capacity and electron donating capacity of EPS extracted by different methods were 0.07~0.30 μmole-·g-1 and 0.01~0.04 μmole-·g-1,respectively,among which the electron accepting capacity and electron donating capacity of EPS extracted by EDTA method were the highest.The UV-Vis and FTIR spectra showed the existence of humic substances in EPS,and the content extracted by chemical extraction was higher than that by physical method.The three-dimensional fluorescence spectra showed the fluorescence peaks of protein and humic acid,the protein peak fluorescence intensity of EPS extracted by heating method was higher,while the humic acid peak fluorescence intensity of EPS extracted by chemical method was higher.
Key words:activated sludge;extracellular polymeric substances;redox properties;redox substances
0 引言
胞外聚合物(EPS)是活性污泥絮体内处于细胞外部的聚合物,主要来源于细菌的自然分泌物、细胞裂解和水解产物.EPS是活性污泥的主要组成部分,直接影响活性污泥絮体的传质、絮凝、沉降和生物代谢活性等理化特性[1].根据EPS在细胞外分布位置的不同,可将其划分为溶解态EPS(SEPS)和结合态EPS(BEPS),BEPS具有双层结构,又可分为松散附着EPS (LB-EPS)和紧密黏附EPS (TB-EPS)[2].
EPS的成分复杂,包括蛋白质、多糖、脂类、核酸、醛酸和一些无机成分.虽然EPS组分受污泥来源及提取方法的影响,但以有机成分为主,其中蛋白质和多糖占EPS总量的70%~80%[1,3].将EPS从细胞表面剥离即提取是EPS研究的前提.目前EPS提取方法主要分为物理法、化学法及物化结合法.物理方法主要是通过施加外力将EPS从细胞表面剥离,包括超声法、高速离心法、加热法等[4].化学法主要是通过添加化学药剂破坏EPS和细胞间的相互作用,使EPS从细胞表面脱离,包括甲醛-NaOH法、阳离子树脂交换法、EDTA法、酸碱法等[4].不同方法提取的EPS在含量及组分上存在较大差异,整体而言,化学法的提取效率要高于物理法[5].
近年来研究发现,EPS中含有大量氧化还原介体,可以介导微生物胞外电子传递过程,因此EPS的电化学特性及其对微生物胞外电子传递过程的影响逐渐受到关注[6,7].Cao等[8]在希瓦氏菌HRCR-1生物膜上提取的EPS中发现了20种氧化还原蛋白,这些蛋白可能在细胞外电子转移中发挥重要作用.Xiao等[9]研究发现,EPS中存在大量电化学活性物质(如黄素和C-型细胞色素),可以作为电子转运介质.Ma等[10]發现污泥厌氧发酵过程中添加EPS可以提高系统中C-型细胞色素含量,从而加速系统电子传递速率,提高产甲烷性能.Hu等[11]将EPS作为天然氧化还原介质来改善甲[JP2]烷生成,发现EPS的加入显著改变了氧化还原活性基团的种类,有效地降低了自由电荷的迁移阻力,促进了电子转移效率.本课题组[12]前期研究发现,EPS可以作为天然氧化还原介体,通过加速电子转移和碳源代谢来提高反硝化性能.提取方法会影响活性污泥EPS含量及组分,因此可能对EPS的氧化还原特性产生影响.Yang等[13]采用EDTA法、超声法和加热法从地杆菌生物膜中提取EPS,发现超声法对氧化还原活性蛋白的提取效率更高.然而不同提取方法对活性污泥EPS氧化还原特性的影响尚不清楚,因此本研究采用四种典型方法(加热法、超声法、EDTA法和甲醛-NaOH法)提取活性污泥EPS,并对EPS组分及氧化还原特性进行分析,考察不同方法提取活性污泥EPS的氧化还原特性.
1 实验部分
1.1 污泥来源及EPS提取方法
活性污泥EPS的提取原料采用好氧池活性污泥,污泥浓度为5 200±200 mg/L.所用活性污泥取自西安市某污水处理厂,采用AAO处理工艺,其处理能力为40万m3/d.从好氧池取活性污泥后,立即运回实验室进行EPS的提取,提取步骤如下:取40 mL活性污泥在600 rpm下离心10 min,弃去上清液,剩余底泥用0.9%氯化钠溶液补充至40 mL,于80 r/min下振荡1 min;再次将悬浮后的污泥离心(5 000 g,15 min),倒掉上清液后,分别采用加热法、超声法、EDTA法和甲醛-NaOH法处理剩余底泥,具体操作[14]如下:
(1)加热法:剩余底泥用0.9%氯化钠溶液补充至40 mL,摇匀,于60 ℃下水浴加热30 min.
(2)超声法:剩余底泥用0.9%氯化钠溶液补充至40 mL,摇匀,在20 KHz下超声10 min.
(3)EDTA法:剩余底泥用0.9%氯化钠溶液补充至20 mL,加入20 mL 2%的EDTA,摇匀,于4 ℃下存放3 h.
(4)甲醛-NaOH法:剩余底泥用0.9%氯化钠溶液补充至40 mL,加入0.06 mL 36.5%的甲醛,振荡1 h (180 r/min),加入1 mol/L NaOH至pH=11,振荡3 h.
经上述四种方法处理后,所有样品在5 000 g下离心20 min,上清液通过0.45 μm滤膜过滤,滤液为EPS.
1.2 组分分析
EPS组分主要包含蛋白质(PN)、腐殖酸(HA)、多糖(PS)和DNA.PN和HA采用修正的福林酚法测定[15];PS采用苯酚-硫酸法测定[16];DNA采用二苯胺法测定[15].EPS含量用PN、HA、PS和DNA的总和表征.
1.3 电化学特性分析
采用电化学工作站(辰华660 E)进行循环伏安、计时电流和电化学阻抗谱试验.工作电极为玻碳电极,参比电极为饱和甘汞电极,Pt网为对电极.电化学试验之前,向电解液中持续通入氮气5 min,使其维持在一个近乎无氧的状态.进行循环伏安试验时,扫描速度为10 mV/s,扫描电势范围为-1.0~0.5 V.计时电流试验中,测量电子接受能力(EAC)时还原电位设置为Eh=-0.6 V,测量电子供给能力(EDC)时氧化电位设置为Eh=+0.5 V.电化学阻抗谱测试中开路电压值设为初始电压,高频为106 Hz,低频为0.1 Hz.
1.4 光谱分析
采用UV 2600 A紫外可见分光光度计对EPS水样进行紫外扫描,扫描区间为200~600 nm.
采用傅里叶红外光谱仪对EPS官能团进行分析.将EPS水样在30 ℃的烘箱中进行烘干,取烘干样和溴化钾(105 ℃烘箱中烘干)充分混合研磨,压制成片,然后进行红外光谱的测定,测定的红外光谱范围是4 000~400 cm-1,纯溴化钾作为空白对照组.
采用三维荧光光谱仪分析EPS水样的荧光特性,激发波长Ex为220~500 nm,增量为5 nm,发射波长Em为230~600 nm,增量为1 nm,响应时间为0.1 s.
2 结果与讨论
2.1 EPS组分分析
不同方法提取EPS的含量如表1所示.四种提取方法,甲醛-NaOH法提取EPS含量最高,达到68.59 mg·g-1,其次为EDTA法(23.40 mg·g-1)、加热法(18.2 mg·g-1)和超声法(4.07 mg·g-1).结果显示,化学法提取的EPS含量明显高于物理法.Comte S的研究结果同样表明化学法提取的EPS含量高于物理法:化学法提取的产量为17%~47%,物理法提取的产量仅为2%~4%[17].Liao等[18]的研究表明DNA占EPS总量的2%~15%内,可认为EPS在提取过程中细胞没有发生严重破裂.本实验各种方法提取的EPS中,DNA占比在9.4%~25.85%之间,其中甲醛-NaOH法提取EPS的DNA占比为25.85%,因此可认为甲醛-NaOH法提取EPS可能引起了部分细胞破裂.
相关研究表明,不同提取方法下,蛋白质和多糖为EPS的主要成分[19],本研究也得到了相同的结果.不同方法对EPS各组分的提取效率存在一定差异,针对某一特定组分进行分析时,可以选取适合的提取方法.目前研究表明,EPS中具有导电特性的物质主要为蛋白质而不是多糖,同时腐殖酸中含有大量醌、酚等官能团,是EPS中主要的电化学物质[20].加热法和甲醛-NaOH法提取的EPS中PN含量较高,分别为10.01 mg·g-1和15.93 mg·g-1,明显高于超声法与EDTA法.EDTA法和甲醛-NaOH法提取的EPS中HA较高,分别为6.74 mg·g-1和4.96 mg·g-1,明显高于加热法(2.77 mg·g-1)与超声法(0.73 mg·g-1).徐小惠等[21]采用不同方法提取活性污泥EPS,同样发现加热法和甲醛-NaOH法对EPS蛋白质的提取率高于其他方法.
2.2 循环伏安分析
图1为不同方法提取EPS的循环伏安图.结果显示,所有曲线在-0.7 v处均有一个还原峰,此峰为核黄素的还原峰[22].其中甲醛-NaOH法和EDTA法提取的EPS峰值电流分别为-35 μA和-34 μA,加热法和超声法提取的EPS峰值电流分别为-23 μA和-21 μA,说明甲醛-NaOH法和EDTA法对于EPS中核黄素的提取效果更好.但其对应的氧化峰并不明显,这可能是因为EPS样品中含有多种相对含量相近的氧化还原活性组分,由于电位分布广泛,其循环伏安图无法显示出明显的氧化峰[20].
EDTA法提取的EPS在0.1 V处有一个氧化峰,为细胞色素C(Cyt-c)的峰[23].研究表明Cyt-c具有优越的电子传递能力,可参与直接电子转移和种间电子转移过程[24].甲醛-NaOH法提取的EPS在0.1 v处没有显示出氧化峰,但在其附近发现一个氧化峰,推测此峰也是细胞色素C的氧化峰,由于样品中各种氧化还原组分的干扰,发生了峰的偏移.而加热法和超声法提取的EPS并没有发现细胞色素C的氧化峰,说明加热法和超声法对EPS中细胞色素C的提取效果不佳,细胞色素含量较低,无法显示出明显的氧化峰.不同方法提取细胞色素含量的差异可能与提取原理有关,具体原因有待深入研究.EDTA法提取EPS在-0.4 V处有一个还原峰,甲醛-NaOH法提取的EPS在-0.2 V处有一个还原峰.Bi等[25]的研究表明,-0.45 V左右的峰归因于黄素,-0.2 V处的峰为黄素结合的Cyt-c.根据循环伏安曲线计算出不同方法提取EPS的电容,甲醛-NaOH法和EDTA法提取EPS电容(213和174 μF)明显高于加热法和超声法(137和142 μF),电容越高,说明其容纳的电子越多,电子传递能力越强.
2.3 计时电流分析
计时电流法可检测活性污泥EPS的电子转移能力(ETC),ETC为电子供给能力(EDC)与电子接受能力(EAC)之和.图2所示结果表明,EPS具有一定的电子转移能力,EDTA法提取EPS的ETC最高,达到0.35 μmole-·g-1,其次为甲醛-NaOH法(0.20 μmole-·g-1)、加热法(0.11 μmole-·g-1)与超声法(0.09 μmole-·g-1).这可能是因为EDTA法和甲醛-NaOH法提取的电化学物质含量更多,所以电子转移能力更高.不同方法提取EPS的EAC和EDC分别为0.07~0.30 μmole-·g-1和0.01~0.04 μmole-·g-1,與Ye等[26]对活性污泥EPS的电化学特性的分析结果相近.四种方法提取的EPS的EAC明显高于EDC,可能是由于EPS中的电化学物质主要以氧化态形式存在[27].
HA是一类典型的电化学物质,对四种方法提取EPS的电子转移能力(EAC、EDC)与HA含量进行相关性分析.结果表明,EPS的EDC与HA含量的相关性并不强(R2=0.58、P=0.027<0.05),而EAC与HA含量具有较好的相关关系(R2=0.89、P=0.027<0.05),可能是因为EPS中HA主要以氧化态形式存在,在EPS参与电子转移过程中主要担任电子受体.
2.4 电化学阻抗谱分析
图3是不同方法提取EPS的电化学阻抗谱图,并对其进行等效电路拟合.等效电路主要由溶液电阻(Rs)、生物膜双电层电容(CPE1)、电荷电阻(R1)和扩散元素(W1)组成.由表2可看出,甲醛-NaOH法提取EPS的R1和Rs均为最小,表明其电荷传递阻力最小,电子传递效率最高.相反,超声法提取EPS的R1与Rs较大,说明其电子传递能力较弱,这与循环伏安及计时电流法分析结果基本一致.此外,EDTA法提取EPS的电化学阻抗试验显示出较高的电阻,电阻越高说明电子传递能力较弱,这与循环伏安和计时电流试验结果矛盾,具体原因有待进一步深入分析.
2.5 紫外可见光谱分析
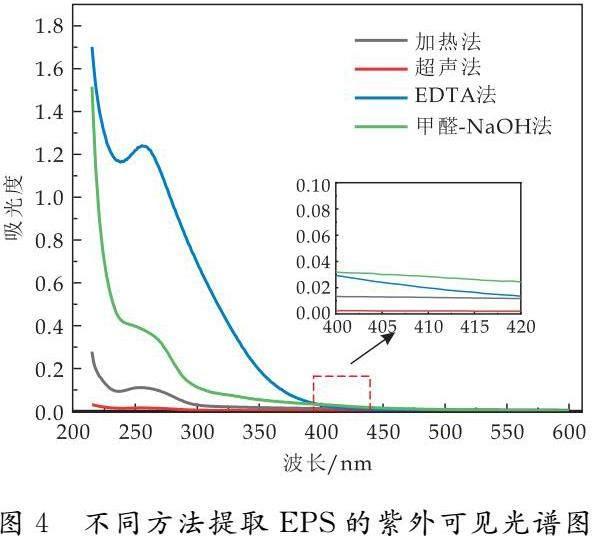
图4为不同方法提取EPS的紫外可见光谱图.由图可知,EPS的紫外可见吸光度随着波长的增加而近似呈指数级下降,在254 nm(UV254)处出现了一个明显的吸收峰.
UV254值反映水体中存在的腐殖质类有机物及含有C=C双键和C=O双键的芳香族化合物等物质的含量[28].一般来说,UV254值越大,其对应的芳香度就越大、腐殖化程度越高.不同方法提取EPS的UV254值:EDTA法>甲醛-NaOH法>加热法>超声法.说明相比于物理法,化学法更有利于EPS中腐殖质或芳香族物质的提取.有文献[29]表明EPS中还含有部分细胞色素c(UV410),在EPS的电子传递过程中起着十分重要的作用.图4结果显示,甲醛-NaOH法和EDTA法提取EPS的细胞色素c的吸光度高于加热法和超声法,再次证明化学法对活性污泥EPS电化学物质提取效率更高.
2.6 傅里叶红外光谱分析
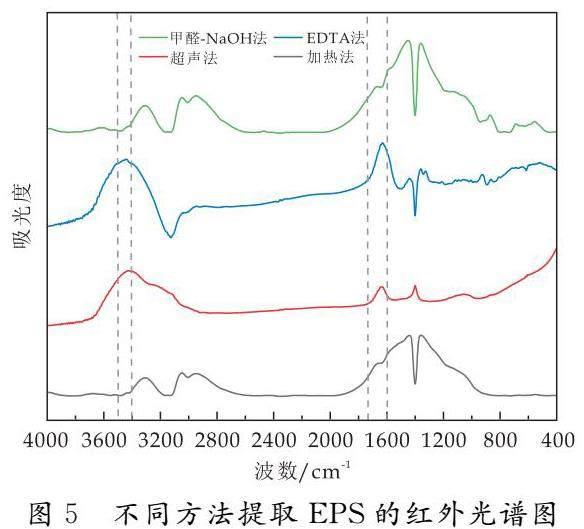
图5为不同方法提取EPS的红外光谱图.不同方法提取EPS的红外光谱峰型相似,表明这几种方法在提取EPS时,对其主要官能团种类影响不明显.各EPS的红外曲线分别在波数1 700~1 600 cm-1、3 500~3 400 cm-1之间有一个吸收峰.有研究表明,波数在1 700~1 600 cm-1的峰代表腐殖质类物质中C=C的拉伸[28].其中,EDTA法提取的EPS在波数1 700~1 600 cm-1处的吸收峰最明显,表明EDTA法更有利于EPS中腐殖质类物质的提取,这与表1的结果相吻合.波数在3 500~3 400 cm-1的峰代表-OH的伸缩振动,3 431 cm-1处的-OH也是腐殖酸的主要官能团.腐殖质已经被证实能够介导电子传递过程,相关性分析也表明电子转移能力与腐殖酸具有显著的相关关系.因此可以推测,腐殖质类物质是活性污泥EPS参与电子转移过程中的重要组成部分.
2.7 三維荧光谱分析
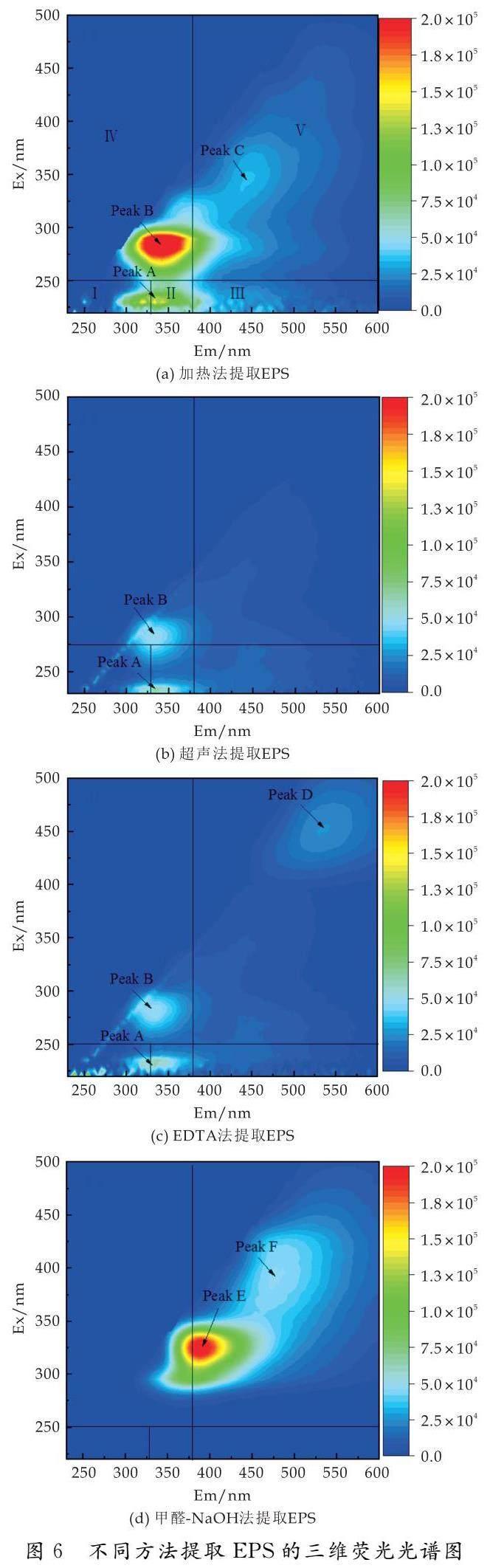
图6为不同方法提取EPS的三维荧光光谱图.根据Chen等[30]提供的荧光体积积分法,将荧光光谱图划分为五个荧光区域:区域Ⅰ(Ex<250 nm/Em<330 nm)为芳香族蛋白,区域Ⅱ(Ex<250 nm/Em:330~380 nm)为芳香族蛋白,区域Ⅲ(Ex<250 nm/Em>380 nm)代表类富里酸物质,区域Ⅳ(Ex>250 nm/Em:200~380 nm)包含络氨酸类蛋白、色氨酸类蛋白和微生物副产物物质,区域Ⅴ(Ex>250 nm/Em>380 nm)主要为类腐殖酸物质.
从图6可以看出,加热法提取的EPS得到三个明显的吸收峰,分别代表芳香族蛋白(Peak-A)、色氨酸类蛋白(Peak-B)和类腐殖酸(Peak-C).超声法提取的EPS也发现了芳香族蛋白和色氨酸类蛋白.EDTA法提取的EPS发现了芳香族蛋白、色氨酸类蛋白和类腐殖酸(Peak-D)的荧光峰.甲醛-NaOH法提取的EPS显示了两个类腐殖酸荧光峰(Peak-E和Peak-F).结果显示,加热法、超声法和EDTA法都得到了芳香族蛋白和色氨酸类蛋白的荧光峰,其中加热法提取EPS的荧光峰强度明显高于超声法和EDTA法,可能是因为加热法提取的EPS中蛋白质含量更高.
值得注意的是,表1结果显示甲醛-NaOH法提取EPS中蛋白质含量最高,但三维荧光光谱图中没有发现蛋白质的荧光峰,可能是因为甲醛-NaOH法提取的蛋白质主要为非荧光类蛋白,荧光类蛋白含量较少,无法在三维荧光光谱图中显示.三维荧光光谱分析结果表明,加热法更有利于EPS蛋白类物质的提取,而化学法对腐殖质类物质提取率更高.研究表明,腐殖酸是一类典型的具有氧化还原能力的物质,其氧化还原能力很大程度上归因于其结构中醌官能团,醌官能团是腐殖酸中重要且普遍存在的荧光团[31].因此,可以推测化学法更有助于EPS中腐殖酸等氧化还原物质的提取.
3 结论
(1)加热法、超声法、EDTA法和甲醛-NaOH法四种方法提取的EPS含量存在较大差异,化学法提取含量高于物理法,甲醛-NaOH对PN的提取效果最佳,而EDTA法对HA的提取效果最佳.
(2)循环伏安图表明EPS中存在核黄素、黄素和细胞色素C等氧化还原物质,化学法提取EPS显示出更高的电容;EPS的电子转移能力主要表现为电子供给能力,说明EPS中电化学物质主要以氧化态形式存在;化学法提取EPS的电子转移能力明显高于物理法.
(3)紫外可见光谱图和傅里叶红外光谱图均显示出EPS中存在腐殖酸物质,三维荧光光谱也显示出腐殖酸的荧光峰,推测腐殖酸是EPS电子传递过程的重要物质,而化学法对EPS中腐殖酸提取效果更佳.
参考文献
[1] Sheng G P,Yu H Q,L X Y.Extracellular polymeric substances (EPS) of microbial aggregates in biological wastewater treatment systems:A review[J].Biotechnology Advances,2010,28(6):882-894.
[2] Pellicer Nacher C,Domingo Felez C,Mutlua G,et al.Critical assessment of extracellular polymeric substances extraction methods from mixed culture biomass[J].Water Research,2013,47(15):5 564-5 574.
[3] More T T,Yadav J S S,Yan S,et al.Extracellular polymeric substances of bacteria and their potential environmental applications[J].Journal of Environmental Management,2014,144:1-25.
[4] 刘心怡,汤志业,朱晓茜,等.SBR反应器中活性污泥胞外聚合物的提取方法比较[J].中国给水排水,2021,37(17):25-31.
[5] 唐 虹,康得军,匡 帅,等.胞外聚合物提取方法的研究进展[J].市政技术,2016,34(5):162-166.
[6] Yu H Q.Molecular insights into extracellular polymeric substances in activated sludge[J].Environmental Science & Technology,2020,54(13):7 742-7 750.
[7] Sathishkumar K,Li Y,Sanganyado E.Electrochemical behavior of biochar and its effects on microbial nitrate reduction:Role of extracellular polymeric substances in extracellular electron transfer[J].Chemical Engineering Journal,2020,395:125 077.
[8] Cao B,Ahmed B,Kennedy D W,et al.Contribution of extracellular polymeric substances from Shewanella sp.HRCR-1 biofilms to U(VI) immobilization[J].Environmental Science and Technology,2011,45(13):5 483-5 490.
[9] Xiao Y,Zhang E,Zhang J,et al.Extracellular polymeric substances are transient media for microbial extracellular electron transfer[J].Science Advance,2017,3(7):1-9.
[10] Ma H,Guo C,Wu M,et al.Use of extracellular polymer substance as an additive to improve biogas yield and digestion performance[J].Energy & Fuels,2019,33(12):12 628-12 636.
[11] Hu A,Cheng X,Wang C,et al.Extracellular polymeric substances trigger an increase in redox mediators for enhanced sludge methanogenesis[J].Environmental Research,2020,191:110 197.
[12] Wang X,Chen T,Gao C,et al.Use of extracellular polymeric substances as natural redox mediators to enhance denitrification performance by accelerating electron transfer and carbon source metabolism[J].Bioresource Technology,2022,345:126 522.
[13] Yang G,Lin J,Zeng E Y,et al.Extraction and characterization of stratified extracellular polymeric substances in Geobacter biofilms[J].Bioresource Technology,2019,276:119-126.
[14] D Abzac P,Bordas F,Van Hullebusch,et al.Extraction of extracellular polymeric substances (EPS) from anaerobic granular sludges:Comparison of chemical and physical extraction protocols[J].Applied Microbiology and Biotechnology,2010,85(5):1 589-1 599.
[15] 王 晨.城镇污水处理厂剩余污泥胞外聚合物解离技术研究[D].青岛:青岛理工大学,2019.
[16] 苏高强.剩余污泥碱性发酵产酸性能与优化[D].北京:北京工业大学,2013.
[17] Comte S,Guibaud G,Baudu M.Effect of extraction method on EPS from activated sludge:An HPSEC investigation[J].Journal of Hazardous Materials,2007,140(1-2):129-137.
[18] Liao B Q,Allen D G,Droppo I G,et al.Surface properties of sludge and their role in bioflocculation and settleability[J].Water Research,2001,35(2):339-350.
[19] Chen Y P,Li C,Guo J S,et al.Extraction and characterization of extracellular polymeric substances in biofilm and sludge via completely autotrophic nitrogen removal over nitrite system[J].Applied Biochemistry and Biotechnology,2013,169(2):526-538.
[20] Lu Q,Chang M,Yu Z,et al.The effects of three commonly used extraction methods on the redox properties of extracellular polymeric substances from activated sludge[J].Environmental Technology,2015,36(22):2 884-2 891.
[21] 徐小惠,魏德洲,張兰河.胞外聚合物的提取及其吸附性能[J].东北大学学报(自然科学版),2021,42(10):1 467-1 474.
[22] Wang J,Lin W,Chen Y,et al.Prompting the FDH/Hases-based electron transfers during Pt(IV) reduction mediated by bio-Pd(0)[J].Journal of Hazardous Materials,2021,417:126 090.
[23] Huang L,Liu X,Ye Y,et al.Evidence for the coexistence of direct and riboflavin-mediated interspecies electron transfer in Geobacter co-culture[J].Environmental Microbiology,2020,22(1):243-254.
[24] Summers Z M,Fogarty H E,Leang C,et al.Direct exchange of electrons within aggregates of an evolved syntrophic coculture of anaerobic bacteria[J].Science,2010,330(6 009):1 413-1 415.
[25] Bi S,Liu H,Chen Y,et al.Promoting interspecies hydrogen/electron transfer in Bio-PdNPs-mediated denitrification with the selectivity towards N-2[J].Biotechnology Engineering Journal,2022,181:108 395.
[26] Ye J,Hu A,Ren G,et al.Enhancing sludge methanogenesis with improved redox activity of extracellular polymeric substances by hematite in red mud[J].Water Research,2018,134:54-62.
[27] Yuan Y,Tao Y,Zhou S,et al.Electron transfer capacity as a rapid and simple maturity index for compost[J].Bioresource Technology,2012,116:428-434.
[28] Weishaar J L,Aiken G R,Bergamasch B A,et al.Evaluation of specific ultraviolet absorbance as an indicator of the chemical composition and reactivity of dissolved organic carbon[J].Environmental Science & Technology,2003,37(20):4 702-4 708.
[29] Jensen P S,Chi Q,Grumsen F B,et al.Gold nanoparticle assisted assembly of a heme protein for enhancement of long-range interfacial electron transfer[J].Journal of Physical Chemistry C,2007,111(16):6 124-6 132.
[30] Chen W,Westerhoff P,Leenheer J A,et al.Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J].Environmental Science & Technology,2003,37(24):5 701-5 710.
[31] 王先寶,陈甜甜,高楚玥,等.AAO工艺中活性污泥胞外聚合物的电化学特性[J].陕西科技大学学报,2021,39(6):32-38.
【责任编辑:陈 佳】
基金项目:国家自然科学基金项目(52000126);陕西省科技厅重点研发计划项目(2022SF-234);陕西省咸阳市重点研发计划项目(L2022ZDYFSF049)
作者简介:王先宝(1986—),男,黑龙江五大连池人,副教授,博士,研究方向:污水处理理论与技术
