高中化学教学中守恒法的有效应用
2023-03-23吴超
吴 超
(福建省莆田第十一中学,福建 蒲田 351166)
高中化学中守恒法的应用主要体现在电子守恒、电荷守恒、物料守恒、质子守恒以及能量守恒上.
1 电子守恒的应用
电子守恒是氧化还原反应遵循的重要规律.高中化学教学活动中应注重电子守恒在氧化还原反应问题中的运用,使学习者体会运用电子守恒解题的便利,养成运用电子守恒分析问题的意识与习惯.
例1将7.6g铁铜合金放入到100mL某浓度的稀硝酸溶液中,合金完全溶解后,共收集到标准状况下NO气体2.24L.同时测得溶液中H+的浓度为0.5mol/L.忽略反应前后溶液体积变化,则以下说法错误的是( ).
A.上述反应中金属共失去电子0.3mol
B.合金中铜的质量为4.8g
C.原硝酸的浓度c(HNO3)=3mol/L
D.要将溶液中的金属离子沉淀完全则需加70mL 5mol/L的NaOH溶液.
稀硝酸一部分表现为酸性,一部分表现为氧化性.表现氧化性的稀硝酸从金属中夺取电子,使得N的化合价由+5价降低至+2价.n(NO)=2.24L/22.4L/mol=0.1mol,N得到的电子数为0.3mol.设合金中铁、铜物质的量分别为x、y,由电子守恒可知3x+2y=0.3mol,又有56x+64y=7.6g,解得x=0.05,y=0.075,对应铜的质量为64y=4.8g.溶液中H+的浓度为0.5mol/L,表明剩余硝酸的物质的量为0.05mol.由N守恒可得:n(HNO3)=(0.05+0.1+0.05×3+0.075×2)mol=0.45mol,则c(HNO3)=0.45mol/0.1L=4.5mol/L.金属离子完全沉淀需要先中和剩余的HNO3,并根据Cu(OH)2和Fe(OH)3进行分析.需要消耗NaOH的物质的量为(0.05+0.05×3+0.075×2)mol=0.35mol,则所需5mol/L的NaOH溶液的体积为0.35mol/5mol/L=70mL.综上分析只有C项错误.
2 电荷守恒的应用
电荷守恒指电解质溶液中阴离子和阳离子所带电荷的总数是相等的,溶液对外不显电性.

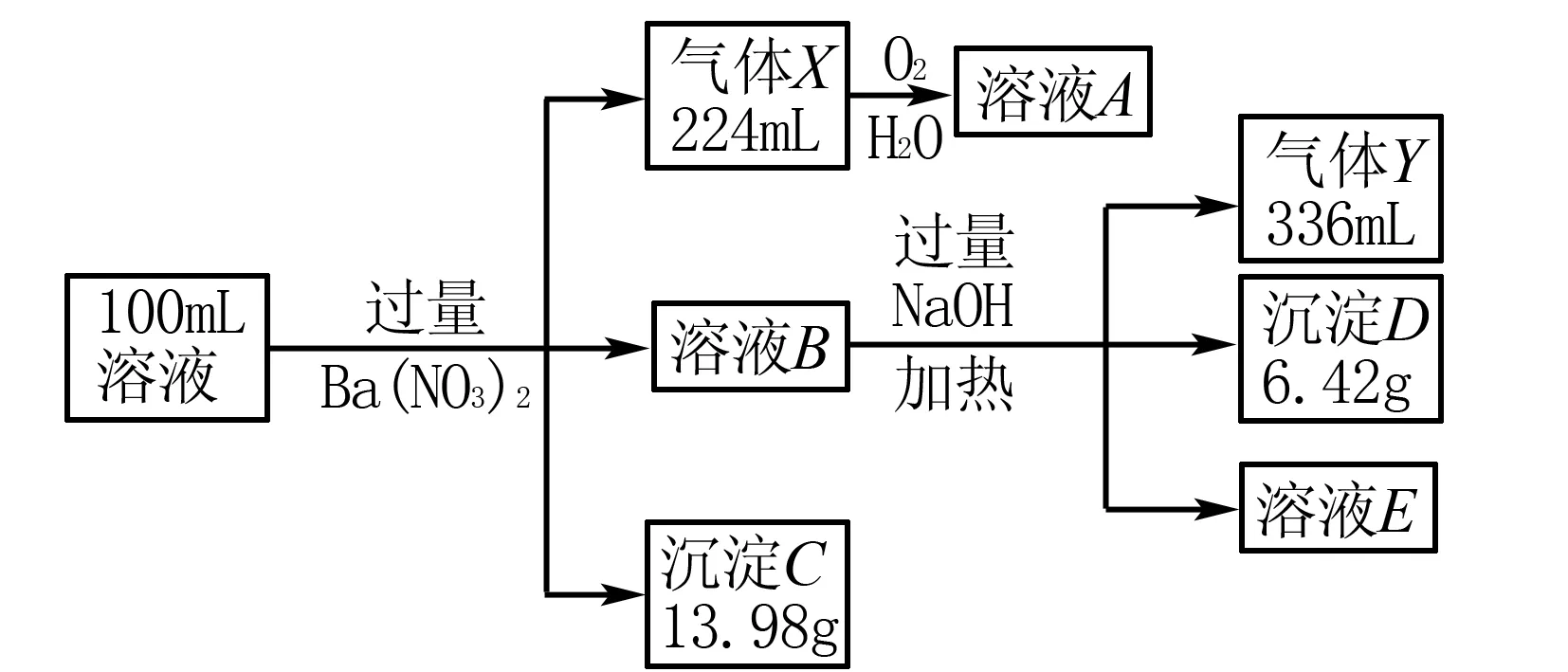
图1
B.原100mL溶液中c(Cl-)=0.9mol/L
C.原100mL溶液中c(Fe3+)=0.3mol/L
D.生成气体X的离子方程式为

3 物料守恒的应用
物料守恒实际上是质量守恒的微观体现,指某一元素的原子在化学反应前后不会发生改变.该守恒常用于化学计算以及电解质溶液中离子浓度的大小比较中,计算时可不用考虑反应的过程,只需考虑原子的来源以及去向便可构建对应的等量关系.
例3常温下,向NaOH和NaAlO2的混合溶液中滴加NaHCO3溶液,测得溶液pH和生成的Al(OH)3的物质的量和加入NaHCO3溶液的体积关系如图2所示,则以下说法错误的是( ).

图2
A.加入的NaHCO3先和NaOH反应

C.NaHCO3溶液的物质的量浓度为0.9mol/L


综上只有C项错误.
4 质子守恒的应用
质子守恒是指酸失去的质子和碱得到的质子数目相同.需要注意的是质子守恒并不需要死记硬背,而是运用电荷守恒、物料守恒进行整理便可得出质子守恒等式.
例4常温下,H2A为一种易溶于水的二元酸,将NaOH溶液滴入到等物质的量浓度的H2A溶液中,溶液中H2A、HA-、A2-的物质的量浓度随溶液pH的变化关系如图3所示,则( ).
A.常温下,H2A的一级电离平衡常数为Ka1=10-6.27
B.当V(NaOH溶液)∶V(H2A溶液)=1∶1时,c(H+)-c(OH-)=2c(A2-)-c(H2A)
C.当pH=6.27时,c(A2-)=c(HA-)>c(H+)>c(OH-)
D.当溶液呈酸性时,c(Na+)>2c(A2-)+c(HA-)

图3
由图可知c(H2A)=c(HA-)时pH=3.3,则H2A的一级电离平衡常数为10-3.3.V(NaOH溶液)∶V(H2A溶液)=1∶1时,分别由物料守恒、电荷守恒推导出质子守恒,即c(H+)-c(OH-)=c(A2-)-c(H2A);pH=6.27时,c(A2-)=c(HA-),溶液显酸性,则c(A2-)=c(HA-)>c(H+)>c(OH-).溶液显酸性时,c(H+)>c(OH-),由电荷守恒可得c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),c(Na+)<2c(A2-)+c(HA-).综上分析只有C项正确.
5 能量守恒的应用
能量守恒是自然界普遍的基本规律之一,体现在化学反应中主要指热量.在分析热量时主要运用盖斯定律.实际上盖斯定律是能量守恒的具体体现.


下列说法正确的是( ).
A.C(s)的燃烧热为110.5kJ/mol


D.将2mol H2O(g)分解成H2(g)和O2(g)至少需要提供4×463kJ的热量

