2021欧洲Graves眼病临床管理指南解读
2023-03-11廖洪斐熊超王耀华
廖洪斐 熊超 王耀华
作者单位:南昌大学附属眼科医院眼眶病眼肿瘤眼外伤科,南昌 330046
Graves眼病(Graves' orbitopathy,GO)也称为甲状腺眼病(Thyroid eye disease,TED)或甲状腺相关性眼病(Thyroid associated ophthalmopathy,TAO),是Graves病(Graves' disease,GD)的主要甲状腺外表现。目前GO的发病率为男性0.54~0.90例/10万/年,女性2.67~3.30例/10万/年[1]。GO严重影响着患者的生活质量,中重度和极重度GO是当前治疗的难题,现有的药物并不能对所有患者产生效果。自2016年欧洲甲状腺协会(ETA)/欧洲GO专家组(EUGOGO)GO管理指南[2]推出后,有关新型生物制剂治疗中重度活动期GO的随机临床试验(RCT)研究相继发表。这促使委员会致力于对GO管理指南进行更新,EUGOGO于2021 年7 月发布了新版GO临床管理指南[3]。为方便广大临床医师理解和把握最新的GO治疗建议,现将该指南解读如下。
1 病情评估
GO的治疗方案制定主要基于GO的炎症活动情况、病情严重程度以及病程时间[2],对于病程超过18个月的GO患者,抗炎或免疫抑制治疗效果明显较差。
1.1 GO的分级和分期
2021版指南继续沿用2016版指南的分级及分期原则。按照临床严重程度分级(见表1),将GO分为轻度、中重度和极重度(视力威胁型)。临床活动性分期也仍然沿用临床活动性评分(Clinical activity score,CAS)进行评估,分为活动期和非活动期。2021版指南在原CAS评分(7项指标)的基础上增加了3项来评估复诊患者的进展情况(见表2)。初检患者症状条数≥3/7或第1次就诊后总症状条数>4/10为活动期。其中第9项眼球运动指标在CAS评分中通常是指使用视野计进行评估。

表1.GO临床严重程度分级

表2.2021版指南GO临床活动性评分
1.2 转诊策略
专业的病情评估和个性化的治疗建议对患者的治疗效果和疾病预后尤为重要。因此,建议基层医师、全科医师、全科内科医师和专科医师需要将可疑GO患者以及GO高风险人群(轻度活动期GO、吸烟者、严重的或不稳定的甲状腺机能亢进、血清促甲状腺激素受体抗体水平高者)[2]转诊至可同时提供内分泌和眼科治疗的甲状腺相关性眼病中心。
1.3 治疗效果评估
2021版指南推荐采用患者自我报告(Patient reported outcome,PRO)和临床医师报告(Clinician reported outcome,CRO)相结合的方式来评估治疗效果。生活质量评分(GO-QoL问卷)是首选的PRO[4]。对于中重度活动期GO,建议使用近期修订的综合指标[5]进行CRO的评估(见表3)。如单眼的特征改善≥2个而另一只眼没有恶化表现,被认为是治疗的积极反应。恶化的定义是出现DON或修订的综合指标的4个组成部分中至少有2个出现恶化。评估时间应在最后一次治疗干预后的3个月[4],6个月后也可再次评估。

表3.中重度活动期GO综合指标
2 一般治疗及预防措施
2.1 控制危险因素
当患者怀疑有GD时,应尽力消除危险因素以防止GO的发生和进展。2021版指南在原有的2项危险因素,即甲状腺功能异常及吸烟的基础上,新增了放射性碘和高胆固醇这2项危险因素。
2.1.1 控制甲状腺功能 甲状腺功能的亢进和减退都会对GO造成负面影响。
2.1.2 吸烟 所有GD患者,不论发生GO与否均应该敦促其戒烟,并避免接触二手烟[1,6]。
2.1.3 放射性碘 放射性碘治疗会增加GO新发和进展的风险,因此需给予预防性口服糖皮质激素。预防方案:大剂量(有GO进展风险或新发生GO风险):每日口服强的松0.3~0.5 mg/kg,逐渐减量,3个月后停药[7];小剂量:每日口服强的松0.1~0.2 mg/kg,逐渐减量,6 周后停药[8]。有进展或新发风险GO患者包括吸烟者、严重或不稳定甲亢及高血清TSHR-Ab的患者。
2.1.4 高胆固醇 高胆固醇血症是GO的一个新发现的潜在危险因素[9]。高胆固醇血症与GO的发生存在关联[10]。且有证据表明他汀类药物的使用与GO风险的降低有关[11],建议GO患者通过饮食控制或者他汀类药物控制高胆固醇血症。
2.2 局部治疗
无论是否合并GO,干眼和眼表炎症普遍存在于GD患者中[12]。在局部治疗方面,新指南与2016版共识推荐内容类似:所有GO患者推荐全程使用人工泪液,夜间加用眼用凝胶或软膏,严重角膜暴露(特别是Bell征阴性)的患者可进行眼部包扎或配戴湿房镜。
3 GO的眼科治疗
3.1 轻度GO的治疗
轻度GO在局部治疗和控制危险因素的基础上,定期随访观察即可。建议轻度患者进行6个月疗程的补硒,因为在缺硒地区的轻度GO患者补充硒剂可以改善眼部症状和生活质量。生活质量明显受影响的轻度GO患者,可采取免疫抑制治疗或康复性手术进行干预。2021版指南有关轻度GO的治疗策略见表4。

表4.2021版指南关于轻度GO的治疗策略
3.2 中重度活动期GO的治疗
中重度活动期GO患者治疗的初期目标是:①缩短疾病的活动期病程;②改善患者的主观和客观眼部症状。通常GO发病后1 年内及早接受治疗的效果较好。治疗方案的选择和制定需要考虑多种因素,并与患者做充分的沟通,使其知晓不同治疗方案的目的、益处和风险,最终共同制定个性化的治疗方案。
3.2.1 中重度活动期GO的一线治疗 2021版指南对于中重度活动期GO的治疗,在使用大剂量糖皮质激素冲击治疗的基础上更改为联合口服霉酚酸钠治疗。指南推荐方案:对于大多数中重度活动期GO患者,建议将静脉滴注甲泼尼龙12周内4.5 g的中度累积剂量与口服霉酚酸钠(0.72 g/d)联合用药24周作为一线治疗。霉酚酸酯(1 g的霉酚酸酯相当于0.72 g的钠制剂)可替代肠溶霉酚酸钠。而对于中重度活动期中病情严重(包括持续性或不稳定性复视、严重软组织受累)的GO患者,建议静脉采用较高累积剂量的甲基强的松龙(12周内累积剂量7.5 g)单药治疗作为替代一线治疗方案。见图1。

图1.中重度活动期GO的一般推荐和一线治疗方法
3.2.1.1 糖皮质激素 每个周期(12周)静脉注射糖皮质激素的累积剂量不应超过8.0 g。GO禁用静脉糖皮质激素的情况包括:严重感染、近期病毒性肝炎、明显肝功能障碍、严重心血管疾病并发症、未控制的高血压、未控制的糖尿病等。口服糖皮质激素起始量1 mg/kg或60 mg/d起始,1周后逐渐减量,每周减5~10 mg,4~6个月后停药。临床医师应监测患者使用糖皮质激素治疗后的药物不良反应和不良事件,当弊端大于益处时,应考虑停药。当全身糖皮质激素绝对禁用时,可使用曲安奈德进行局部结膜下注射[13](注射1~3次,间隔3周,每次20 mg)或眼周注射[14](每周4次,每次20 mg,持续4周)。
3.2.1.2 霉酚酸钠 霉酚酸酯竞争性和可逆性地抑制肌苷单磷酸脱氢酶,导致B细胞产生的抗体减少,并对B细胞和T细胞产生双重抗增殖作用。霉酚酸酯诱导活化T细胞凋亡,抑制黏附分子表达和免疫细胞募集,还可抑制成纤维细胞增殖和功能。霉酚酸酯联合糖皮质激素与单一激素治疗相比更有效,联合治疗显示CAS评分、眼睑和泪阜肿胀、眼眶疼痛以及GO-QoL视觉功能评分有更明显的改善。此外,联合治疗在改善疼痛和眼球运动方面优于单独使用霉酚酸[15],且不增加感染和肝毒性的风险。
3.2.2 中重度活动期GO的二线治疗 对于一线治疗不敏感或复发的中重度活动期GO患者,指南推荐进行二线治疗。根据2016年ETA/EUGOGO指南[2]的推荐建议,进行仔细的眼科和生化(肝酶)评估,3~4周后可进行第2个疗程的静脉注射甲泼尼龙单药治疗(12周内累积剂量7.5 g,静脉滴注甲泼尼龙0.75 g/周/次,连续6周后,改为0.5 g/周/次),每周用法用量同替代一线治疗方案。2021 版指南新增替妥木单抗和托珠单抗为中重度活动期GO的二线治疗方案,见图2。
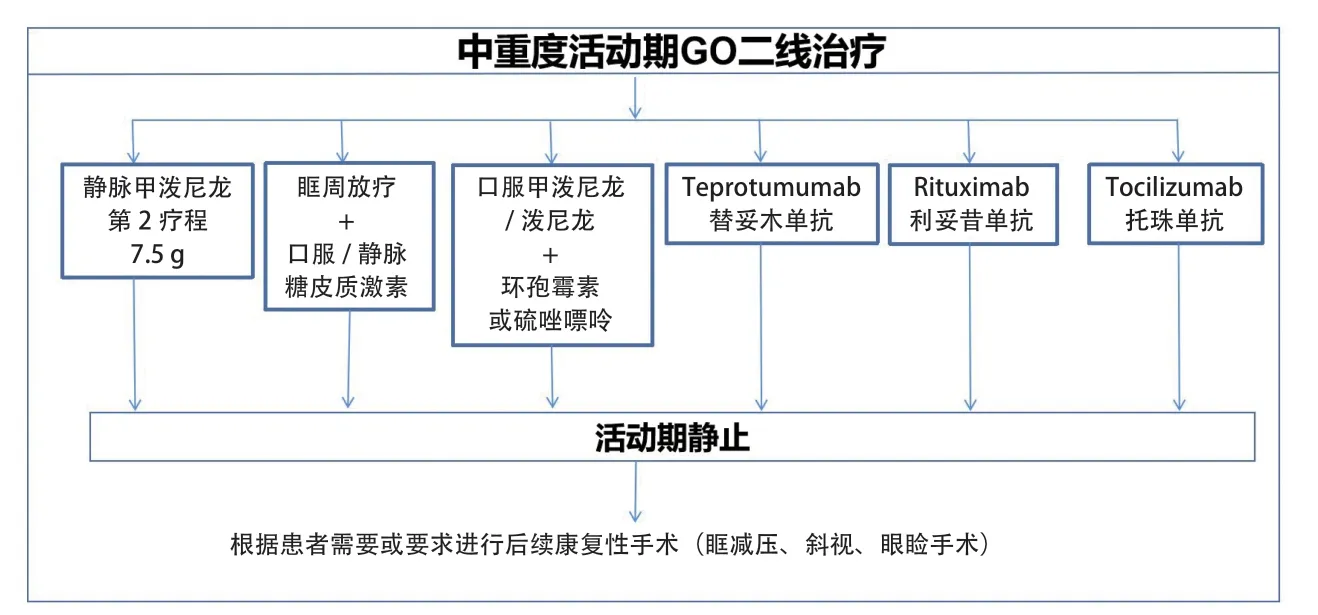
图2.中重度活动期GO的二线治疗方法
3.2.2.1 口服/静脉激素治疗+眼眶放疗 在出现眼外肌功能障碍的中重度活动期GO患者中,眼眶放疗联合静脉注射糖皮质激素为备选二线治疗。治疗方案:①20戈端(Gray,Gy)单侧眼眶累积剂量,分成10 d放疗,每日1次2 Gy,2周完成[16];②20周内每周1 Gy的治疗方案显示同样有效且耐受性更好[17]。注意事项:眼眶放疗期间可能会出现轻度和短暂的眼部症状恶化,可通过同时口服低剂量泼尼松龙进行控制。值得注意的是合并高血压、糖尿病视网膜病变及35 岁以下考虑到远期致癌风险等情况应避免进行眼眶放射治疗。
3.2.2.2 口服激素联合环孢素 环孢素是一种强效免疫抑制剂,可抑制钙调神经磷酸酶通路,减少T细胞增殖和白介素-2分泌。环孢素(初始剂量:5.0~7.5 mg/kg/d)与口服泼尼松龙联合治疗的眼科疗效优于口服泼尼松龙单药治疗[18]。根据治疗效果决定用药持续时间,在口服糖皮质激素停药后还可以继续使用环孢素。
3.2.2.3 口服激素联合硫唑嘌呤 硫唑嘌呤是一种抗增殖药,抑制参与免疫反应的细胞的增生。常用作自身免疫性疾病中的“类固醇减量剂”。将硫唑嘌呤作为二线用药用量100~200 mg/d(体质量<50 kg,口服100 mg/d;体质量50~79 kg,口服150 mg/d;体质量>80 kg,口服200 mg/d)与口服糖皮质激素联合,可减少糖皮质激素的用量,可一定程度改善复视、缓解眼球突出和眼睑退缩[19]。
3.2.2.4 注射替妥木单抗 替妥木单抗是一种完全人源化的免疫球蛋白(Ig)G1单克隆抑制抗体,该抗体可与GO眼眶成纤维细胞和淋巴细胞中过度表达的胰岛素样生长因子-1 受体结合。结合后既阻断其内源性配体的激活和信号转导,也促使胰岛素样生长因子-1的内化和降解。
目前替妥木单抗的给药方案(静脉输注每3周1次,共进行8次,首次剂量为10 mg/kg,随后7次为每次20 mg/kg)已被证明对GO有效,可明显减少眼球突出、复视和改善生活质量[20-21]。替妥木单抗是美国食品药品监督管理局批准的第1种治疗成人GO的药物,但尚未进行剂量范围(不同浓度、输注频率和持续时间)的研究,目前仅在美国上市。
3.2.2.5 注射利妥昔单抗 利妥昔单抗是一种针对B细胞上表达的CD20 表面抗原的人和小鼠嵌合单克隆抗体,通过B细胞耗竭导致免疫抑制。对于糖皮质激素不敏感的患者,排除甲状腺相关性眼病视神经病变(Dysthyroid optic neuropathy,DON),利妥昔单抗可被视为近期发病(<12个月)的中重度伴活动期GO患者的二线治疗。近期文献中的方案:①静脉注射1000 mg利妥昔单抗间隔2周再进行1次注射或仅进行500 mg单次注射[22],2种方案疗效接近;②单次静脉注射100 mg(小剂量)利妥昔单抗,也有不错的效果[23]。
3.2.2.6 注射注射托珠单抗 托珠单抗是一种针对白介素-6(lnterleukin-6,IL-6)受体的人源化单克隆抗体。IL-6 除了作为促炎细胞因子在T和B细胞活化中发挥作用外,还直接作用于眼眶前脂肪细胞,促进体积扩张。用法:每4周静脉输注托珠单抗8 mg/kg,连续注射4次[24]。目前的研究数据表明,托珠单抗可能有利于糖皮质激素治疗耐药的中重度活动期GO患者炎症体征迅速缓解[25]。
总的来说,静脉注射糖皮质激素、口服霉酚酸钠以及静脉注射托珠单抗、利妥昔单抗和环孢素可不同程度降低眼部的炎症体征,而眼眶放疗(优选与糖皮质激素联合)显著改善了眼肌运动性和复视。相比之下,替妥木单抗对突眼的改善作用最强。
3.3 极重度GO的治疗
极重度GO出现视力下降或丧失的原因可能是眶尖拥挤导致视神经受压、严重的角膜暴露、眼球半脱位(极少数),此时需紧急干预,见图3。DON的一线治疗是在第1周内连续3 d或隔日给予高剂量(单剂量500~1000 mg)静脉注射甲基强的松龙[26],根据治疗效果可再重复使用1周。2021指南中提及的DON激素治疗方案,治疗效果的评判标准以及部分有反应的患者进行紧急眶减压的手术指征在新旧指南中均提及。目前国内外专家及各共识均未对此点进行详细阐述,常规来说临床上诊断为DON,出现进行性视力下降者均应进行减压手术。查阅文献国内目前有将最佳矫正视力小于0.1的DON进行眶减压[27],将激素治疗有效[28]定义为:治疗前视力(Visual acuity,VA)<0.8时,治疗后视力提高2行以上;治疗前VA≥0.8时,视野MD值降低。

图3.极重度GO的治疗方法
当激素治疗反应差或视力(视野)继续下降时,须进行紧急眼眶减压手术。角膜暴露(溃疡)或角膜损伤,可进行睑裂修补术、睑缘缝合术、眼睑延长术和角膜覆盖或粘连术等来保护角膜。眼球半脱位则行眶减压手术。
3.4 GO的眼科手术治疗
2021 版指南对于GO的眼科手术治疗没有更新,故手术治疗原则依然参考2016版指南。在GO的活动期,对于严重的暴露性角膜炎和静脉注射糖皮质激素无反应的DON患者进行减压手术。局部治疗(睑缘缝合术、角膜覆盖或粘连术等)是保护角膜免受浅表损伤及溃疡的临时措施,以降低后续减压手术过程中自发性角膜溃疡穿孔的风险。病情稳定后的6个月可进行康复性手术,手术的类型和范围取决于目前容貌和功能损毁程度。如需行多种手术时,按眼眶减压手术、斜视矫正手术、眼睑手术的步骤进行。
4 病毒大流行期间GO的管理
新冠病毒大流行期间指南建议:轻度GO患者应继续常规的局部治疗,敦促戒烟以防止GO进展。虽然糖皮质激素等免疫抑制剂会使患者更易发生感染[29],但是除外进行过新冠病毒疫苗接种或接触过新冠病毒的人群外,所有人对新冠病毒均无免疫力。因此,目前认为增加免疫抑制治疗不会增加感染新冠病毒的风险,而且地塞米松、甲基强的松龙或托珠单抗已成为感染新冠病毒的标准治疗方法。新冠病毒期间使用的高剂量类固醇不会抑制肾上腺功能,因为在新冠肺炎感染存活的患者中观察到了正常的肾上腺功能[30],且停用静脉注射糖皮质激素与肾上腺功能衰竭无关[31]。
目前尚无关于新冠疫情期间静脉注射糖皮质激素或其他免疫抑制剂用于治疗GO的研究文献。随着人群持续接种疫苗,与免疫抑制相关的风险将逐渐降低。建议已经接受治疗的患者在严密监护下继续进行糖皮质激素或其他免疫抑制剂治疗[32],在治疗期间应严格遵守社交距离、做好隔离和卫生防疫措施。对于极重度GO,无论病毒如何流行,都应紧急就医处理。
5 总结
鉴于静脉注射甲泼尼龙和霉酚酸(钠)联合治疗的实用性,优于静脉注射甲泼尼龙单药治疗的疗效,2021版指南在中重度活动期一线治疗方案上进行变更,推荐其作为中重度活动期GO的更新治疗标准。另外,2021版指南表示生物制剂如替妥木单抗、托珠单抗和利妥昔单抗拥有广阔前景,特别对标准免疫抑制治疗不耐受或耐药的患者可能有用。
在未来的GO管理治疗中,GO患者及早接受规范治疗尤为重要,因此临床医师应积极转诊可疑患者以及GO高风险人群至甲状腺相关性眼病中心治疗。在共同决定治疗方案前需告知患者初次治疗的效果无法进行预测,疾病过程中可能需要其他药物和(或)手术治疗以恢复眼部外观和功能。由于GO疾病的漫长性和反复性,期望每一位接诊医师有足够的耐心与满怀的关心对待这类患者,只有这样才能做好GO患者的病情管理。
该指南的更新主要基于近期国外的RCT研究,值得我们学习和借鉴,但其中还存在需要探讨的细节以及人种差异所导致的评分偏差,因此,期望国内的眼科和内分泌专家共同制定出更适合于我们中国人的GO管理指南。
利益冲突申明本研究无任何利益冲突
作者贡献声明廖洪斐:参与选题、指南的深入解读;根据编辑部意见进行修改。熊超:参与指南的初步翻译;撰写论文;根据编辑部的意见进行修改。王耀华:参与指南的初步翻译;根据编辑部的意见进行修改
