加速康复外科理念在脊柱结核外科中应用的专家共识
2023-03-09中国防痨协会骨结核专业分会中国防痨杂志编辑委员会
中国防痨协会骨结核专业分会 《中国防痨杂志》编辑委员会
加速康复外科(enhanced recovery after surgery, ERAS)概念由丹麦外科医生Kehlet于1997年首次提出,是指采用一系列有循证医学证据的围手术期优化措施,阻断或减轻机体的应激反应,促进患者术后快速康复,达到缩短住院时间、降低术后并发症发生率及降低再入院风险和死亡风险的目的[1]。实施ERAS管理模式可以缩短脊柱结核患者的住院时间,降低并发症发生率和再入院率,减少医疗费用。ERAS管理模式的实施需要外科医师、麻醉医师、内科医师、康复医师、护士及营养师等多个科室成员共同配合完成[2-3],其核心是强调以患者为中心的诊疗理念。ERAS 相关路径的实施有助于提高外科患者围手术期的安全性及满意度,缩短术后住院时间,有助于降低术后并发症的发生率[4]。
目前,ERAS理念被越来越多的脊柱结核外科医师所接受,但尚未形成统一的专家共识,严重限制了其在脊柱结核外科中的应用。因此,中国防痨协会骨结核专业分会联合《中国防痨杂志》编辑委员会,在脊柱结核疾病自身特点的基础上,结合既往ERAS模式在脊柱结核治疗应用中的研究成果,组织专家撰写了《加速康复外科理念在脊柱结核外科中应用的专家共识》及具体实施表单(附表1~5),以期进一步规范及指导ERAS理念在脊柱结核外科中的应用,推动脊柱结核外科的进一步发展。
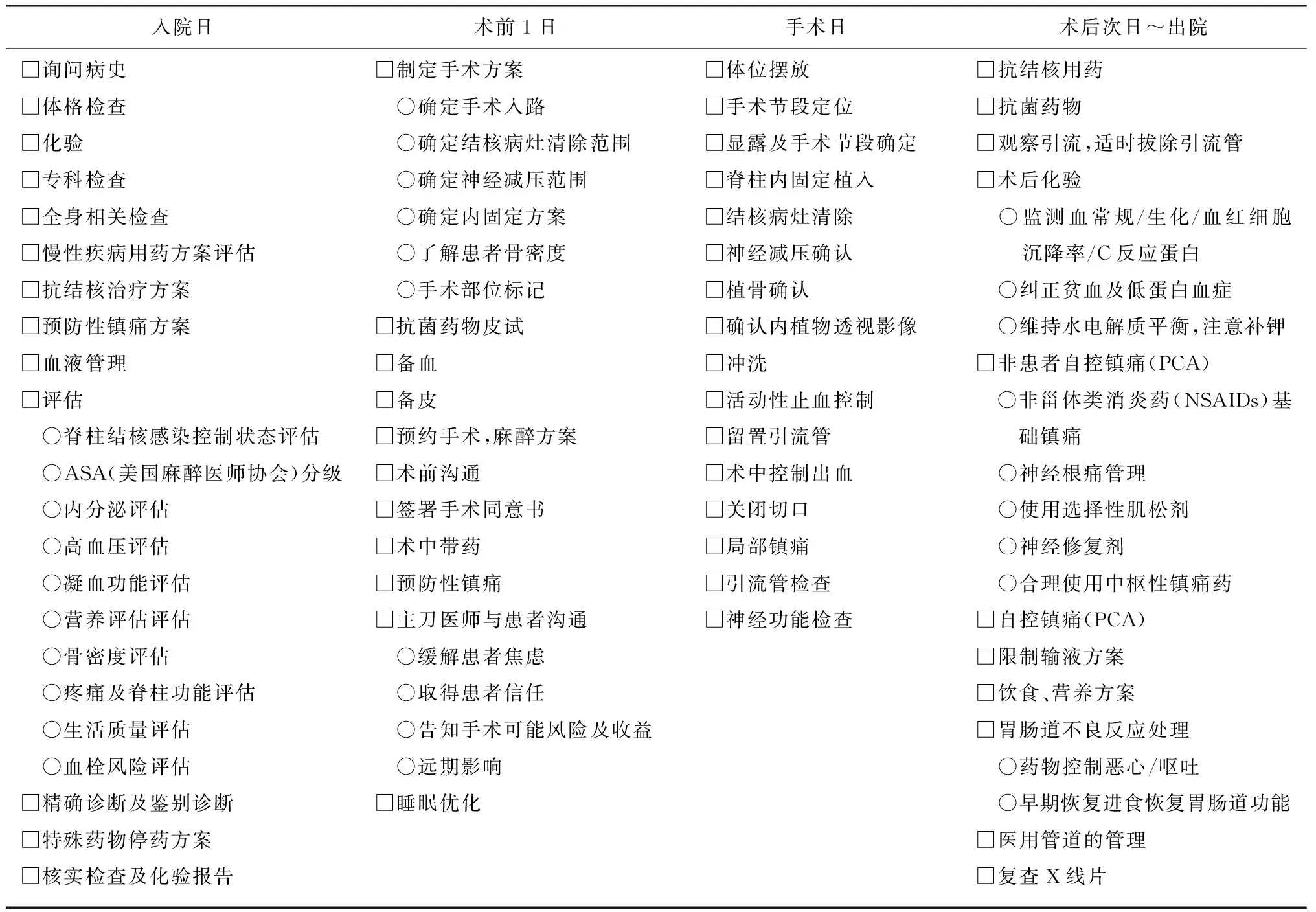
附表1 脊柱结核手术加速康复外科实施流程——外科医师表单

附表2 脊柱结核手术加速康复外科实施流程——麻醉医师表单

附表3 脊柱结核手术加速康复外科实施流程——病房护士表单
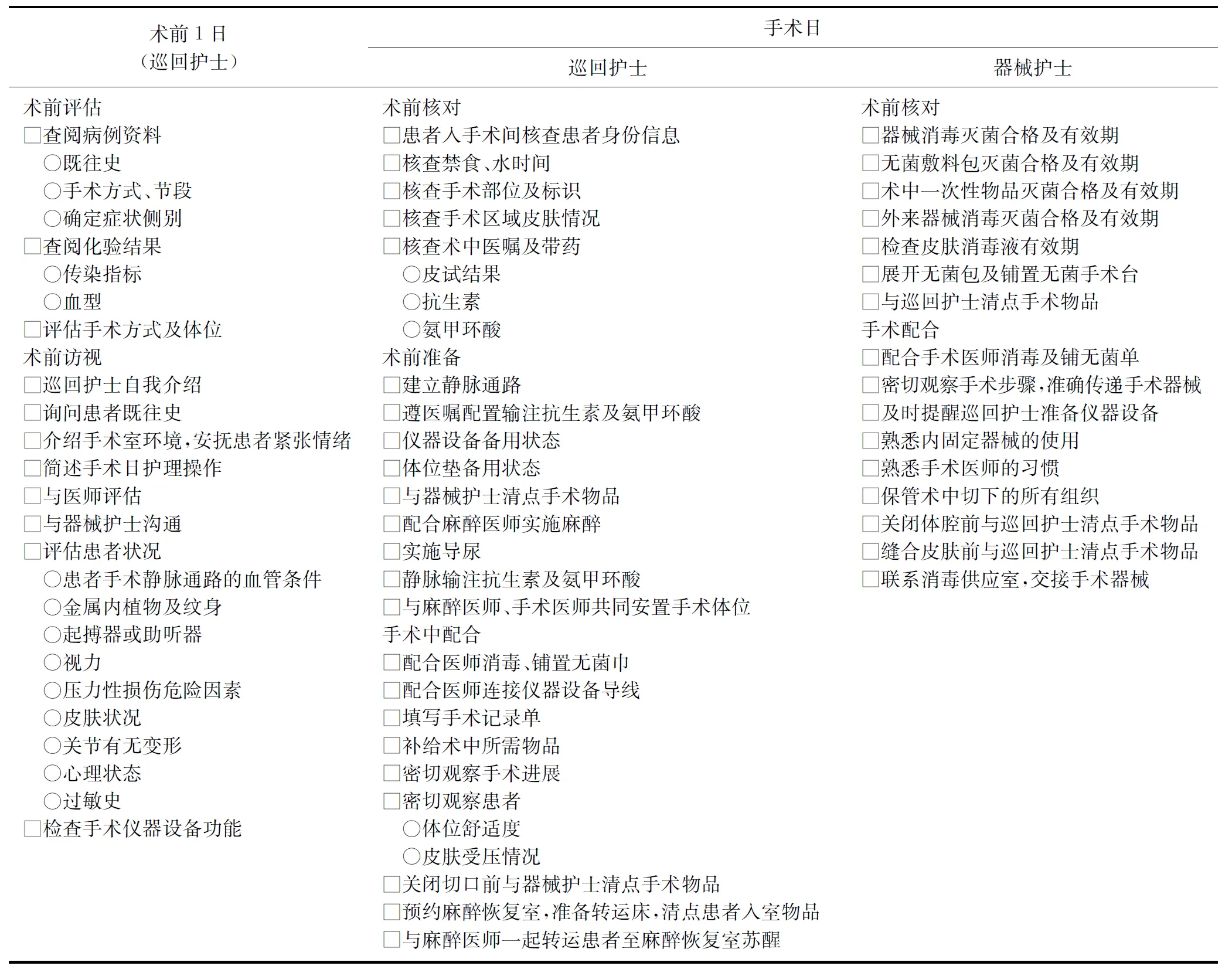
附表4 脊柱结核手术加速康复外科实施流程——手术室护士表单

附表5 脊柱结核手术加速康复外科实施流程——康复医师表单
一、脊柱结核的病变特点
脊柱结核是最常见的骨结核,约占骨结核患者的50%,其常造成骨质破坏及脓肿形成,导致患者脊柱稳定性丧失及神经功能障碍,致机体功能障碍及残疾[5]。脊柱结核患者临床发病过程中既有由感染造成的发热、厌食、消耗及脓肿等炎症反应引起的病理生理变化;也有由感染造成的骨质破坏,进而导致脊柱功能障碍、骨质疏松、神经功能障碍、血栓、压疮、疼痛等病理生理变化。同时,脊柱结核患者也存在治疗时间长和术后康复慢等问题[6]。因此,针对脊柱结核患者的治疗措施,应当以脊柱结核病变的病理生理特点为依据,进行有针对性地调整,同时,也要兼顾神经功能康复、脊柱稳定性恢复及活动功能的恢复等目的。
二、脊柱结核手术评估
1.脊柱结核感染控制状态评估:对于非耐药脊柱结核患者,术前规范抗结核药物治疗2~4周,术前要求患者全身中毒症状(低热、乏力、盗汗)缓解,体温得到有效控制。体温是反映脊柱结核感染控制状态的重要指标,手术前要求体温<37.5 ℃;疼痛缓解是脊柱结核得到有效控制的另一个重要指标;血红细胞沉降率也是反映脊柱结核感染控制状态的指标,其处于下降期或稳定期说明结核感染得到有效控制[7-8]。
2.影像学评估:进行脊柱结核手术的患者,常规需完善脊柱正侧位X线摄影检查、脊柱CT扫描及三维重建、脊柱MRI平扫或增强扫描。其中,脊柱正侧位X线摄影检查主要用于评估脊柱序列、脊柱曲度、椎间隙高度和有无畸形等;CT扫描及三维重建可清晰显示骨质破坏的范围及程度、死骨位置、椎旁脓肿的范围,以及椎间隙狭窄的情况,在评估骨骼的细微结构方面具有优势;MRI主要用于评估脊柱结核感染的范围、脊髓及神经根受压情况、脊髓水肿变性程度、椎管狭窄程度、神经受压情况,以及椎旁脓肿的边界等,MRI增强扫描主要用于鉴别诊断。影像学检查是评价脊柱结核病变程度和制定手术方案的重要依据[9-11]。
3.疼痛及脊柱功能评分:疼痛程度采用视觉模拟评分法(visual analogue score,VAS)评价;脊髓损伤情况使用美国脊髓损伤协会(American Spinal Injury Association,AISA)的伤残评分(AISA impairment scale,AIS)评价;颈椎功能评分可参考颈椎功能障碍指数(neck disability index,NDI);胸椎功能评分可参考美国脊柱创伤研究学组胸腰椎损伤分类和严重程度评分系统(Thoracolumbar injury classification and severity score,TLICS);腰椎功能评分可参考日本骨科协会评估治疗评分(Japanese Orthopaedic Association scores,JOA评分)。
4.骨密度评估:老年脊柱结核患者多存在骨质疏松,在治疗结核病的同时,应给予抗骨质疏松症的治疗,以增加抗结核治疗的效果。因此,骨质疏松症的治疗就成为ERAS管理措施中的一个重要组成部分[12]。对于绝经后妇女和65岁以上男性,需在围手术期进行骨密度测量。对于骨质疏松的治疗,具体实施方法可参考《原发性骨质疏松症诊疗指南(2017)》[13]。
5.康复评估:对于所有脊柱结核患者都应进行康复评估,以更好地制定分阶段和个体化的康复治疗方案,评估内容包括:(1)疼痛:VAS评分;(2)脊髓损伤的分级:常见的分级方法为Frankel分级和ASIA分级;(3)脊柱损伤的康复评定:包括生命体征、致病原因及机制、体格检查和辅助检查等;(4)活动和参与方面:改良Banhel指数(modified Banhel index,MBI)。
三、健康教育
ERAS模式下的脊柱结核患者围手术期的健康教育建议从患者住院前的门诊即开始实施。门诊医务工作者可为患者发放脊柱结核健康教育材料或应用相关健康教育网络信息平台等方式,使患者能及时了解脊柱结核的疾病特点、抗结核药物的服药注意事项,以及住院、手术、诊疗、康复等内容。门诊健康教育的开展有利于患者提高服用结核药物的依从性,为患者配合手术治疗做好前期准备。
ERAS模式下的脊柱结核住院患者的健康教育建议采用路径式教育模式。健康教育路径是一种规范化的健康教育模式,是根据患者健康教育计划表,指导护理人员在规定时间对患者实施可参考的健康教育计划[14]。医护、麻醉、康复、营养、药剂科等一体化的多学科协作诊疗团队,根据脊柱结核健康教育路径计划表为患者实施健康教育,使患者及其家属充分了解自己在ERAS路径中的重要作用,以更好地配合项目实施,同时,了解手术、麻醉、护理、营养和康复药品使用的相关知识及注意事项等。应用健康教育路径为脊柱结核患者进行系统的健康指导,有利于降低并发症发生率,对脊柱结核患者的快速康复具有相当重要的临床意义[15-16]。
四、围手术期血液管理
结核病为慢性消耗性疾病,脊柱结核患者常合并贫血,因此,脊柱结核围手术期血液管理目标主要为预防和治疗贫血。对于择期手术患者,术前及术后均应进行贫血筛查并及时治疗贫血。脊柱结核患者的贫血主要由营养不良及结核感染消耗造成,因此,在抗结核治疗的同时,应补充铁剂及改善营养状态。对于血红蛋白降低(男性血红蛋白<130 g/L,女性血红蛋白<120 g/L)的患者,应明确其贫血原因,针对不同病因进行相关治疗。对于术中失血≥500 ml或手术时间>2 h的患者建议使用静脉铁剂进行补铁,也可应用促红细胞生成素进行围手术期红细胞动员。术前血红蛋白<100 g/L的患者,建议备血,术中视情况进行异体输血治疗[17-18]。
五、麻醉要点
目前ERAS理念推荐采用全身麻醉联合局部麻醉,从而减轻术后疼痛、减少阿片类药物的使用、减轻患者应激反应和炎症反应[19]。术前要做好宣教,缩短禁食水时间,预镇痛,减少胰岛素的抵抗。术中麻醉医师通过对患者总体情况和并存疾病的了解,制定个体化的麻醉方案,选择适宜的麻醉药物和镇痛方法。要全面的麻醉监测、气道和呼吸道的管理、液体管理、体温监测和肌松监测。术中维持各重要器官的功能,维持循环和体温的稳定,从而减少或尽量避免术后不良反应的发生,以达到快速康复的目的。麻醉医师在术后要采用多模式镇痛及其优化镇痛,预防恶心呕吐,使患者术后早期进食水,早期活动和功能锻炼。麻醉医师对创伤和应激反应的处理直接关系到是否能够改善患者预后,以实现快速康复[2-3]。
1.麻醉监测:通过监测设备实现安全麻醉。脊柱结核手术常要求适度的肌松状态,以利于手术操作。术中进行肌松监测以指导肌松药物的使用。长效肌松药物及术中低体温可延迟神经肌肉的功能恢复。术后应严格掌握拔管时机,避免肌松残留所致的呼吸无力及低氧血症,依具体情况选择是否给予肌松拮抗药物。
2.术中体温管理:多项研究表明,手术中当人体核心温度<36 ℃时即为低体温[20]。我国手术患者术中低温发生率高达44.3%。避免低体温可降低感染率、降低出血量和缩短麻醉苏醒时间。术中应常规进行体温监测并采取必要的保温措施,维持核心体温不低于36 ℃,预防发生低体温[21-22]。
六、手术要点
脊柱结核手术的重点在于结核病灶清除、脊柱稳定性重建、神经减压,以及畸形矫正;核心在于选择正确的手术入路、适当的结核病灶清除范围、合适的融合节段、有效的内固定装置、减少出血、避免神经损伤[23]。
脊柱结核手术方式主要分为前路手术、后路手术、前后路联合手术,以及微创手术。应根据患者的病变情况,选择相应的手术方式。
1.前路手术:脊柱结核病变主要累及前、中柱,椎旁脓肿及流注脓肿也多位于椎体前方及侧方。传统观点认为前路手术具有理论和技术上的优势,切口可以直达病灶,可以直视下进行病灶清除。但前路手术也存在入路复杂、对胸腹腔脏器功能影响大、内固定稳定性不足,以及脊柱畸形矫正效果差的缺点[24-25]。
2.后路手术:近几年脊柱结核后路手术技术得到了快速发展,逐渐被临床医师接受。在疗效方面,脊柱结核后路手术与前路手术并无明显差异。后路手术入路安全、对胸腹腔脏器功能影响小、神经减压充分、内固定稳定性好,脊柱畸形矫正效果好。后路手术适用于相邻多椎体病变,对于脊柱结核继发后凸畸形的患者,后路手术的矫形效果明显优于前路手术。后路手术可以在一个切口内完成手术,创伤小,其缺点是视野受限、彻底清除病灶困难、神经及硬膜囊损伤风险增加,并且有可能将前中柱的结核病灶扩散到脊柱后方[26]。
3.前后路联合手术:前后路联合手术结合了前路和后路手术的优势,对于能耐受并需要同时解决前后路问题的患者,联合手术可以更好地进行病灶清除、植骨及增加脊柱的稳定性,但前后路联合手术对患者造成的创伤也大于单纯前路或后路手术[27]。
4.微创手术:脊柱结核微创手术具有创伤小和恢复快的优点,但由于视野狭窄,其病灶清除、植骨及内固定的操作受到限制,因此,临床上应掌握好手术指征[28]。
七、疼痛管理
疼痛是脊柱结核的最主要症状之一。脊柱结核发病隐匿且病程较长,引起的疼痛通常以炎症刺激导致的慢性疼痛为主。如果病变椎体发生病理骨折,则可能引起急性疼痛。如果合并神经损伤,则可能引起神经病理性疼痛。脊柱结核术后还会出现急性术后疼痛。骨科围手术期疼痛管理可有效降低围手术期疼痛,减少镇痛相关并发症,促进患者术后康复。
1.疼痛评估方法:患者应于入院当天、术前1 d、术后第1天、出院当天等4个时间点进行疼痛程度评估。有急性暴发性疼痛者,随时进行评估并记录。对于10岁以上且有一定文化程度者,采用数字评价量表(numerical rating scale,NRS)评估;对于10岁以下儿童、老年人、文化程度较低、语言表达困难者、意识不清及有认知功能障碍者,采用WongBaker面部表情疼痛评估法(WongBaker faces pain scale revision,FPSR)进行评估[29]。
2.疼痛的处理措施:脊柱结核患者术前多数存在慢性疼痛,均可表现为疼痛的持续存在和间断性急性发作。术前可使用环氧化酶-2(cyclooxygenase-2,COX-2)抑制剂控制疼痛,比如塞来昔布、氟比洛芬、帕瑞昔布等。有神经根放射痛的患者,可给予甘露醇减轻水肿。有神经病理性疼痛者可加用加巴喷丁或普瑞巴林。根据患者病情和疼痛程度,可在COX-2抑制剂的基础上联用不同类型的药物,如阿片类药物等。经评估合并焦虑、抑郁的患者,术前应加强对患者的关心和心理疏导,必要时加用镇静抗焦虑药物[30]。在药物不良反应监测方面,应根据镇痛效果及不良反应情况,及时调整镇痛方案[31]。
脊柱结核患者术后需要尽早开始功能锻炼,术后的疼痛特别是运动锻炼时疼痛的管理尤为重要。患者术后疼痛管理的目的是通过多模式预防性镇痛,达到静息状态下基本无痛,不影响睡眠,活动时疼痛可耐受,不影响脊柱功能恢复,避免急性疼痛转为慢性疼痛。术后镇痛药物首选口服选择性COX-2抑制剂,必要时静脉给药。中重度疼痛患者应联合阿片类药物,必要时辅以镇静催眠抗焦虑药物。镇痛药物疗程应覆盖术后康复期,根据患者康复情况逐步调整药物用量[30]。
八、围手术期营养管理
结核分枝杆菌感染可导致机体免疫调控紊乱,炎症水平提高,出现负氮平衡,影响患者的营养状况。结核病患者长期发热可导致蛋白质分解代谢增加;部分脊柱结核患者还会出现食欲减退及因被动平卧导致经口饮食不便且胃肠功能紊乱加重,导致能量、蛋白质摄入不足。脊柱结核患者术中血清白蛋白随血液流失多,术后分解代谢增强使之进一步减低,加重了低蛋白血症,影响伤口愈合。多种因素均可导致脊柱结核患者极易出现营养风险,甚至蛋白质-能量营养不良。纠正营养风险和营养不良可以改善患者的负氮平衡,增强免疫力,保证术后抗结核药物的有效杀菌浓度,还可以维持细胞、器官与组织的代谢,使之发挥正常的功能,加速组织的修复,促进患者康复[32-35]。研究表明,每餐中摄入25~35 g蛋白质可最大限度刺激肌肉蛋白的合成[36]。脊柱结核患者在围手术期术前应保持每餐≥25 g的蛋白质摄入,以达到每天蛋白质需要量[37]。因此,无营养风险的患者给予高蛋白饮食即可,建议每餐摄入蛋白质≥25 g;存在营养风险但无营养不良的患者进行营养宣教,建议每餐摄入蛋白质≥25 g;存在营养不良的患者首选肠内营养治疗,只要患者能经口进食、胃肠道结构及功能基本完整者,应给予口服营养补充(oral nutritional supplements,ONS),建议ONS每日3次,每次150~200 kcal,全日ONS的热量至少400~600 kcal;当ONS不能满足60%的能量需求3~5 d时,可依次选择肠内营养治疗、部分肠外营养联合肠内营养治疗或肠外营养治疗;严重营养不良患者应先进行营养治疗1~2周再手术,部分患者可延长至4周,以改善患者营养状况。营养不良的改善有利于减少手术风险。
九、术后液体管理
脊柱结核患者术后切口引流量多,低热造成体液蒸发。液体治疗的原则:(1)每日评估和管理患者的液体及电解质需要量,在术后早期不能经口或胃肠道补充液体的患者应提供静脉液体治疗;一旦可以经口进食,应尽可能早地减少补液量;(2)制订24 h 输液计划,包括液体种类、输液量和速度等,并随时调整;尤其是针对老年患者及有心肺并发症的患者,要减少补液总量及减慢补液速度;(3)兼顾其他途径如经胃肠道补充的水分与电解质,还应考虑静脉途径药物、营养和输血对液体及电解质补充的影响[38]。
十、医用管路管理
脊柱结核术后常规留置病灶引流管以引流病灶渗出液。脊柱结核术后病灶引流管在确保安全的前提下,应尽早拔除,以减少发生术后经引流管继发感染的风险。患者在24 h病灶引流量少于50 ml,引流液清亮的前提下即可拔管;术中留置的尿管和深静脉通道也应在患者恢复进食和恢复自主排尿的前提下尽早拔除。留置尿管者,女性患者麻醉清醒后拔管,男性患者术后第2天清晨拔除导尿管;对于具有尿潴留高危因素的患者(男性、高龄、麻醉时间>200 min),可适当延长拔管时间[39-40]。
十一、抗生素管理
脊柱结核患者围手术期在抗结核治疗的同时,术中及术后建议常规应用第二代头孢菌素预防性抗感染治疗,头孢菌素过敏者建议使用克林霉素。应在切开皮肤前30~60 min输注完毕抗生素,手术时间超过3 h或超过使用药物半衰期2倍以上,或成人术中出血量超过1500 ml,术中应追加1次。多数指南推荐术后预防性抗生素使用不建议超过24 h,但是应当具体结合患者情况合理预防性使用抗生素。若出现呼吸系统感染、泌尿系感染等其他系统感染则建议常规留取标本培养,培养结果出来之前请相关科室医师会诊共同决定抗生素的使用,培养结果出来后针对性合理使用抗生素。抗生素的使用应和抗结核药物相适应[41-42]。
十二、围手术期抗结核治疗方案
抗结核治疗是脊柱结核治疗的基础,也是治疗成败的关键。对于需要手术的脊柱结核患者,围手术期抗结核治疗的目的:(1)术前有效的抗结核治疗,快速杀灭骨病灶中的结核分枝杆菌,控制结核感染;(2)术后继续巩固抗结核治疗,预防术后结核病复燃[7-8]。
对于脊柱结核患者围手术期的抗结核治疗方案,应根据患者的脊柱结核病情、合并症及其对抗结核药物的反应和耐受情况而定。应选择合理的抗结核药物,保证足够的药物数量组成,制定个体化抗结核治疗方案,保证抗结核治疗方案的有效性及安全性。对于非耐药脊柱结核,抗结核药物治疗推荐H-R-E-Z(H:异烟肼;R:利福平;E:乙胺丁醇;Z:吡嗪酰胺)四联方案,不建议过多使用抗结核药物,以避免仅增加药物相关不良反应,而不增加临床疗效。术前推荐抗结核治疗2~4周,术后抗结核治疗9~18个月。而对于耐药脊柱结核,则推荐依据药物敏感性试验结果及世界卫生组织耐药结核病治疗指南选择治疗方案[43-44]。
十三、围手术期血栓预防方案
脊柱结核接受手术患者手术创伤大,围手术期长期卧床,是静脉血栓栓塞症(venous thromboembolism,VTE)发生的高危因素。脊柱脊髓损伤患者术后深静脉血栓发生率高达40%~80%,故应在无禁忌证的前提下尽早积极预防[45-46]。
骨科手术VTE预防指南推荐应用Caprini血栓风险因素评估表对手术患者进行VTE风险评估,其中,0~2分为VTE低度风险,建议在基本预防的基础上应用物理预防;3~4分为VTE中度风险,建议在基本预防的基础上应用药物预防或物理预防;≥5分为VTE高度风险,推荐在基本预防的基础上应用药物预防,或建议药物预防联合物理预防[47-48]。基本预防即早期活动,协助患者勤翻身,早期进行床上踝泵运动,直腿抬高训练等主动、被动训练。物理预防一般使用足底静脉泵、间歇充气加压装置及梯度压力弹力袜等促使下肢静脉血流加速,减少血液瘀滞,降低下肢深静脉血栓形成风险。药物预防包括低分子肝素、抗血小板药物、维生素K拮抗剂、华法令和利伐沙班等。目前,脊柱疾病术后预防性应用抗凝药物具有争议,在VTE高危患者无出血风险情况下可尝试联合应用抗凝药物,低分子肝素钙是使用最多的药物。临床实际情况各异,需根据患者的实际情况,个性化选择是否抗凝、抗凝时机、抗凝方式及抗凝疗程等,充分权衡患者的血栓风险和出血风险利弊,合理选择抗凝药[49]。
十四、围手术期的康复锻炼
ERAS理念指导下的康复锻炼,应遵照个体化、循序渐进和全面性原则,整个康复过程包含术前和术后全周期。
1.术前康复:脊柱结核患者避免绝对卧床,可以在床上适当进行训练,如轴向翻身、四肢及躯干肌群的肌力锻炼,适当范围的关节活动度训练,可以根据患者的反应进行相应的调节,尽量使患者以一个相对好的状态面对手术。同时,呼吸肌群训练、排痰训练和咳嗽训练有助于提高患者呼吸功能状态,减少和延缓卧床期并发症的发生[50-51]。
2.术后卧床期康复:术后卧床期,即术后3周内,依据患者情况并遵从医嘱确定卧床期的缩短或延长。建议术后患者麻醉清醒后即可开始进行康复训练,术后1~2 d进行呼吸训练,上肢主动训练,下肢肌肉等长收缩训练(臀肌、股四头肌、腘绳肌、小腿肌肉等),踝关节的趾背屈运动;术后2~4 d开始肢体的活动度训练及抗阻训练,包括双手握球、对拉弹力带、交替直腿抬高、交替双下肢蹬踏等[52]。颈椎结核患者训练时需佩戴颈托。
3.术后离床期康复:即在术后的4~8周。术后第4周行CT检查,若骨性愈合较好,患者可在躯干支具保护下进行床边坐起、站立及行走训练。指导患者保持上身直立、不要扭曲身体,保持躯体的整体性、协调性。详细指导转移、站立、行走、入厕等注意事项,避免二次损伤。对椎体破坏严重、脓腔大、稳定性差者,遵医嘱适当延长卧床期。
十五、随访评估
术后随访对于判断脊柱结核预后和抗结核化疗结束时间具有重要临床意义。建议患者术后每个月至少复查1次,建议第1、3、6、9、12、15、18个月时门诊进行脊柱CT扫描或MRI复查,以了解患者病变转归情况,并每月进行血常规、肝肾功能、血红细胞沉降率等检查,以了解患者的一般状况及避免抗结核药物治疗带来的不良反应。术后疗效及安全性评价指标包括:(1)患者结核中毒症状和脊柱疼痛的改善情况;(2)血红细胞沉降率和C反应蛋白等实验室指标的动态变化,以及患者营养状况改善情况;(3)神经受损症状是否得到改善;(4)术后残腔积液或切口窦道等并发症是否好转;(5)影像学检查脊柱畸形矫正与病椎植骨融合情况,脓肿消失或钙化、死骨吸收或替代、移植骨或钛笼植骨与植骨床骨性融合状况,脊柱矫形后有无明显丢失,内固定有无松动;(6)临床观察脊髓运动功能和括约肌功能的恢复情况;(7)综合评估脊柱结核病灶的治疗情况[53-54]。
执笔者李元
编写组成员(排名不分先后) 秦世炳、李元、雷国华、刘伟、王倩、唐恺、马皎洁、张岩(首都医科大学附属北京胸科医院);何盛伟、梁秀清(大连医科大学附属第二医院);蒲育、何敏(成都市公共卫生临床医疗中心);张强(首都医科大学附属北京地坛医院);王文胜(内蒙古自治区第四医院);刘丰胜、贾晨光(河北省胸科医院);张文龙、唐亮(天津市海河医院);石仕元(杭州市第九人民医院);陈其亮(陕西省结核病防治院)
利益冲突所有作者均声明不存在利益冲突
作者贡献李元:酝酿和设计实验、采集数据、起草文章、对文章的知识性内容作批评性审阅;秦世炳:酝酿和设计实验、实施研究、对文章的知识性内容作批评性审阅;雷国华、王倩、马皎洁:酝酿和设计实验、起草文章、对文章的知识性内容作批评性审阅;刘伟和张岩:起草文章、对文章的知识性内容作批评性审阅;唐恺:起草文章、对文章的知识性内容作批评性审阅、统计分析
