心室主动电极体外临时持续起搏的安全性及有效性
2023-03-09郑文成昃峰李学斌李鼎周旭段江波王龙苑翠珍
郑文成,昃峰,李学斌,李鼎,周旭,段江波,王龙,苑翠珍
近年来,随着心脏起搏装置植入的增加,植入装置发生感染的概率也在增加[1],包括单纯囊袋感染、菌血症以及感染性心内膜炎。按照指南要求,发生上述感染,建议将起搏系统完全移除,待感染完全控制后再植入新的起搏装置[2]。对于起搏器依赖患者,在等待感染控制期间需要植入临时起搏器进行过渡[3]。传统的使用球囊漂浮导管以及经股静脉临时起搏的方式可保留的时间较短且并发症发生率很高,尤其是电极脱位率更高[4]。既往研究曾证实心室主动电极体外临时起搏较为安全[5-6]。这种临时起搏方式,于右心室植入主动固定电极,然后连接体表的脉冲发生器,并将脉冲发生器程控为仅双极模式作为临时起搏的桥接。本研究选择起搏器感染且起搏器依赖的患者,以评价心室主动电极体外临时起搏在中国患者中应用的安全性及有效性。
1 资料与方法
研究对象:回顾性分析2014 年1 月至2022 年1 月于北京大学人民医院心内科住院治疗的因起搏器感染行电极拔除术且起搏器依赖患者共415 例,均使用心室主动电极体外桥接临时持续起搏。入选标准:(1)囊袋感染包括破溃及囊袋脓肿,菌血症及感染性心内膜炎;(2)接受经静脉起搏器电极拔除治疗;(3)患者为起搏器依赖,再植入新的起搏器之前需要临时起搏器桥接。本研究获北京大学人民医院医学伦理委员会批准(批件号:2016PH130-01),所有患者均签署书面知情同意书。
心室临时主动电极植入方法:感染装置拔除之前,所有患者会接受起搏器程控以确定患者是否存在起搏器依赖,起搏器依赖的标准:(1)病态窦房结综合征伴有明显的症状性心动过缓;(2)高度或完全性房室阻滞或自主心率<40 次/min;(3)慢心率相关的获得性长QT 综合征[7]。对于起搏器依赖的患者术中及术后均需要临时起搏支持。术前在X 线指引下首先经股静脉植入心室四极导管到达右心室心尖部做临时起搏备用,完善双侧肘静脉造影确定双侧锁骨下静脉或腋静脉是否通畅,穿刺前完成囊袋的清创及消毒,并拔除起搏系统,以感染侧的锁骨下或腋静脉为穿刺入路(对侧作为新的永久起搏器植入部位),穿刺点避开感染区域且尽量远离感染切口,同时经穿刺针进导引钢丝的时候确保钢丝不通过囊袋空腔,如果肘静脉造影发现感染侧锁骨下或腋静脉严重狭窄或闭塞,则选择右侧颈内静脉作为穿刺入路,穿刺成功后沿钢丝置入7 F 可撕开鞘,将永久起搏器使用的心室主动固定电极(ST 1888TC 或2088TC,58 cm,美国圣犹达医疗公司)固定在右心室间隔部。测试心室电极的阻抗、振幅及阈值,均符合要求后电极导线尾端在体外与再利用的永久起搏器脉冲发生器相连,起搏模式为单腔起搏,双极起搏、双极感知,将脉冲发生器固定在患者颈部或者肩部尽量远离囊袋感染的部位,撤出股静脉入路的四极心室电极。如果患者因单腔起搏模式而出现低血压、头晕等表现需要房室顺序起搏时,则需要植入一根心房电极至右心耳,体外连接起搏器为双腔起搏模式。
观察指标:所有患者入院后均记录一般临床资料,完善超声心动图及X 线检查,证实有无心腔内赘生物的形成,术前行双侧血培养,电极拔除术后再次抽血培养。单纯囊袋感染患者血培养阴性>48 h后,可在感染对侧胸壁植入新的永久起搏器。感染性心内膜炎患者需要起搏器拔除后>14 d,且血培养阴性>72 h 后再次植入新的永久起搏器。新的永久起搏器在感染对侧植入成功后拔除临时心室主动电极。观察临时起搏器相关并发症:(1)电极穿孔,患者往往会突然出现明显的胸痛,程控时发现双极不能起搏或起搏阈值明显升高,心室双极感知不良,超声心动图可见心包积液,胸部CT 可见穿出心室肌的电极头端;(2)电极脱位,患者起搏阈值明显升高或不能起搏,感知<2 mV 或无感知,需立即行电极复位;(3)临时起搏电极体表穿刺点周围局部感染;(4)临时起搏相关的发热,临时起搏器桥接过程中新出现的发热。
随访:所有患者出院后会进行每月1 次门诊随访,偏远地区患者可以通过电话或者视频连线方式进行每月1 次随访。
统计学方法:所有数据采用SPSS 19.0 统计软件进行分析。正态分布的计量资料用均数±标准差表示,偏态分布的计量资料采用中位数(P25,P75)表示,计数资料以例(%)表示。
2 结果
2.1 415 例患者的临床特征
415 例患者平均年龄(63.8±11.7)岁,男性315 例(75.9%)。局部囊袋感染310 例(74.7%,图1A),菌血症75 例(18.1%),感染性心内膜炎30 例(7.2%)。合并症包括高血压150 例(36.1%)、糖尿病78 例(18.8%)、慢性肾功能衰竭38 例(9.2%)、贫血26 例(6.3%)、心肌病96 例(23.1%)。左心室射血分数(61.1±12.3)%。
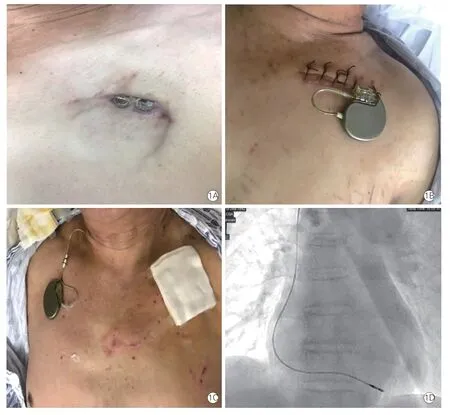
图1 囊袋感染及桥接起搏器
2.2 415 例患者感染装置的特征(表1)

表1 415 例患者感染装置的特征[例(%)]
在感染装置中,单腔起搏器105 例(25.3%),双腔起搏器225 例(54.2%),单腔植入型心脏转复除颤器65 例(15.7%),双腔植入型心脏转复除颤器20 例(4.8%)。在临时起搏适应证中病态窦房结综合征185 例(44.6%),高度或完全性房室阻滞230 例(55.4%)。临时起搏电极入路为同侧锁骨下或腋静脉315 例(75.9%,图1B),右侧颈内静脉入路100例(24.1%,图1C)。仅需要植入右心室间隔部临时起搏电极405 例(97.6%,图1D),采用右心耳+右心室间隔部双腔体外临时起搏模式10 例(2.4%)。
2.3 415 例患者临时起搏参数及相关并发症(表2)
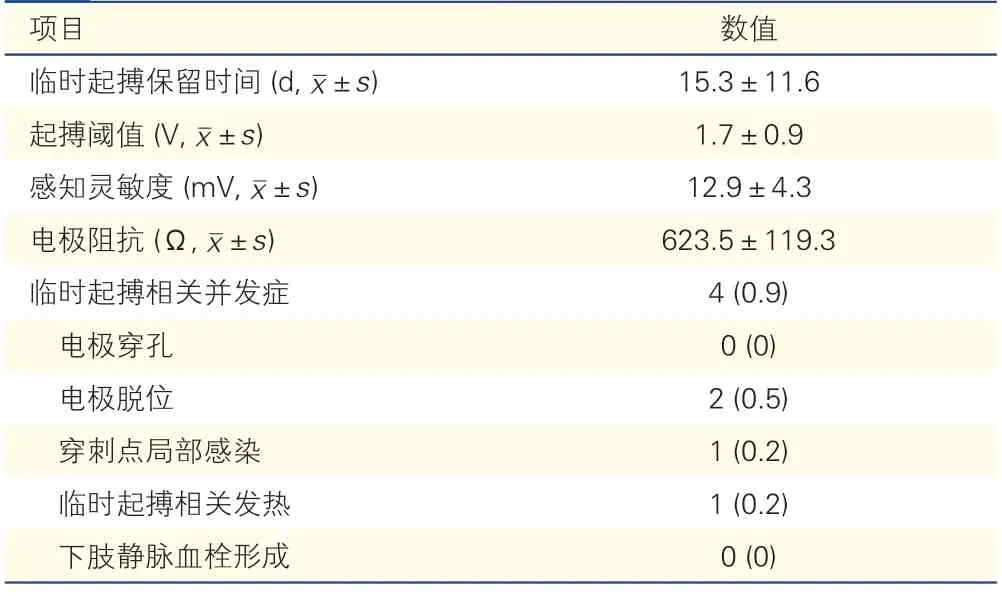
表2 415 例患者临时起搏电极参数及相关并发症[例(%)]
临时起搏电极保留时间为(15.3±11.6)d,新的起搏器植入后,临时起搏电极被移除,临时起搏器起搏阈值、感知灵敏度及电极阻抗均在正常范围内。有4 例(0.9%)患者出现了临时起搏相关并发症,其中2 例(0.5%)出现电极脱位,予以立即复位;1 例(0.2%)出现穿刺同侧腋静脉入路的部位局部红肿伴脓性渗出,改穿刺右侧颈内静脉后红肿逐渐消退;1例(0.2%)同侧锁骨下静脉入路临时起搏桥接过程中新出现发热、血培养阳性,拔除临时起搏电极改右侧颈内静脉入路后24 h 内体温恢复到正常,血培养转阴。
2.4 随访结果
415 例患者中,385 例(92.8%)规律接受随访,中位随访时间为24.5(7.8,51.3)个月,其中310 例(80.5%)随访超过了1 年,只有1 例(0.3%)在起搏器拔除及再植入4 年后出现再植入部位囊袋感染,于是再次拔除感染的起搏系统,择期再次植入,前后两次感染所培养出的细菌完全不同。随访过程中未发生与起搏器感染相关的死亡病例。
3 讨论
本研究报道了心室主动电极临时起搏桥接的安全性、可靠性以及非常低的并发症发生率。该研究也是目前入选病例较多的一个关于心室主动电极体外桥接起搏的研究,传统的临时起搏器电极脱位率可高达14.3%[4,8],而本研究仅为0.5%。对于起搏器依赖的患者而言,起搏电极的脱位会引起很大风险,轻者出现症状性心动过缓,重者可出现心脏停跳甚至引发恶性心律失常危及生命。心室主动固定电极导线头端为螺旋电极,体外连接永久起搏器,保证了临时起搏系统的稳定性,极大地降低了电极脱位的风险。同时由于患者下肢无需制动,可自由活动,也就大大降低了下肢静脉血栓形成的风险,本研究中无一例下肢静脉血栓形成。
对于起搏器感染的患者,指南建议拔除所有的电极导线[2],对于这些患者起搏系统拔除后需要抗生素治疗,直到血培养阴性后方可考虑在对侧植入新的起搏器。在这一等待的过程中,需要长时间的临时起搏,有研究显示起搏器依赖的感染性心内膜炎患者最长临时起搏时间高达1 个月[5],而本研究临时起搏停留时间为(15.3±11.6)d。
Pecha 等[5]报道临时起搏电极在感染侧桥接起搏,无临时起搏器相关性感染发生。在本中心为了保证感染对侧作为新的起搏器植入部位,通常在充分清除感染侧伤口后,将桥接的心室电极穿刺入路选在感染侧的锁骨下或腋静脉,必要时选择右侧颈内静脉作为穿刺入路,为了最大限度地降低临时起搏相关的感染风险,穿刺时尽量远离感染的囊袋并且保证了导引钢丝不在感染的囊袋中穿过。本研究中仅有2 例(0.5%)患者出现了感染,1 例为局部穿刺点红肿伴脓性分泌物,1 例发生与临时起搏电极植入相关的发热,均通过改为右侧颈内静脉入路重新植入临时起搏电极后好转。有报道起搏器植入后同侧锁骨下静脉或腋静脉发生严重狭窄或闭塞率较高,甚至大于30%[9-10]。因此在桥接起搏器之前,所有患者均先完善双侧肘静脉造影,以评估感染侧锁骨下或腋静脉情况,如发现感染侧穿刺静脉严重狭窄或闭塞,则选择右侧颈内静脉作为桥接临时起搏电极入路。Cipriano 等[10]报道右侧颈内静脉是最适合体外桥接临时起搏器的入路,且未发现临时起搏相关的感染病例。
在本中心,每年有上百台感染装置被拔除[11],大多数患者的起搏器功能和电量均处于较好的状态,对于这些起搏器会在充分的消毒灭菌后再利用,待血培养阴性后择期将其植入到患者对侧。2014 年本中心曾报道了99 例患者再植入经过充分消毒的原起搏器,113 例患者植入新的起搏器,两组患者在长达3.52 年的随访过程中,再感染的发生率差异无统计学意义(P>0.05)[12]。
本研究在中位随访24.5(7.8,51.3)个月的过程中,只有1 例患者在拔除感染装置再植入4 年后再次感染,但是前后两次感染所培养出的细菌完全不同,这表明第二次感染可能独立于第一次感染,属于孤立性事件。
主动固定电极临时起搏虽然可行且显著降低电极脱位等相关并发症,但是其基本操作相对复杂且费用偏高,因此,认为其主要适用于起搏器完全依赖且需要长时间起搏的患者,但是长时间右心室起搏可引起心室内失同步[13],对于短时间的临时起搏,比如介入手术中或外科手术中临时起搏保驾以及紧急临时起搏的时候,传统的临时起搏方式仍为首选。本研究仍有一定的局限性,为单中心、回顾性研究,另外数据分析可能有偏差,没有进行对照研究。
综上所述,心室主动电极临时体外持续起搏在起搏器感染且依赖的患者中的应用是安全且可行的,在选择性的患者中值得临床推广应用。
利益冲突:所有作者均声明不存在利益冲突
