外界因素对茶黄素(TF)水溶液稳定性的影响研究
2023-03-08俞晨秀孙益民秦亚东
俞晨秀,孙 莉,孙益民,秦亚东,高 焕
((1.安徽中医药高等专科学校药学系,安徽 芜湖 241000;2.芜湖市食品药品检验中心,安徽 芜湖 241000;3.安徽师范大学化学与材料科学学院,安徽 芜湖 241000)
近年来,茶黄素功效的报道日益增多,其研究也备受关注。茶黄素因其在乙酸乙酯中呈现黄色而得名[1],它是Roberts在1957年从红茶中分离并鉴定获得,是茶叶中多酚类物质氧化聚合而成的一类多酚羟基具苯骈卓酚酮结构的物质[2],是形成红茶茶汤“黄金圈”的物质,对红茶茶汤鲜爽度和强度等滋味起着重要作用[3]。茶黄素具有良好的抗氧化性[4]、抗炎症[5-6]、抗尿酸[7]、抗病毒[8]、抗菌[9]、抗肿瘤等作用[10-12]。到目前为止,各类茶黄素有28种之多[13],其中最主要的单体有4种化合物,即茶黄素(Theaflavins,TF)、茶黄素-3-单没食子酸酯(Theaflavin-3-gallate,TF-3-G)、茶黄素-3'-单没食子酸酯(Theaflavin-3'-gallate,TF-3'-G)、茶黄素-3,3'-双没食子酸酯(Theaflavin-3,3-digallate,TFDG)。
茶黄素结构式见图1。

图1 茶黄素结构式
在这4种单体中及总的28种中,茶黄素是具有最基础结构的单体,其稳定性与其他单体的稳定性密切相关。因此,研究茶黄素的稳定性能较好反映其他单体的稳定性。在茶黄素中有多个酚羟基、多个环和大共轭体系,这种结构有着怎样的稳定性无疑是茶黄素提取、分离和应用中需要考虑的,而这方面系统的专题研究却未见报道。研究了TF在多种环境下的稳定性,以期为茶黄素的开发应用和深入研究中提供一定的参考依据。
1 材料与方法
1.1 材料
茶黄素(TF),纯度99.636%,成都瑞芬思生物科技有限公司提供;乙酸、EDTA-2Na、抗坏血酸、三氯化铁、硝酸银、盐酸均为分析纯,国药集团化学试剂有限公司提供;甲醇、乙腈均为色谱纯,德国默克公司提供;水(娃哈哈纯净水)。
1.2 仪器与设备
Agilent HPLC-1260型高效液相色谱仪、DAD检测器,美国安捷伦科技有限公司产品;DV215CD型精密电子天平,上海民桥精密科学仪器有限公司产品;RA24型电热恒温水浴锅,北京市永光明医疗仪器有限公司产品;FYL-YS-310L型冰箱,北京福意电器有限公司产品;PHS-25型pH计,上海今迈仪器仪表有限公司产品;JK-250DB型数控超声波清洗器,合肥金尼克机械制造有限公司产品;20 W家用日光灯,PAK/三雄极光产品。
1.3 试验方法
1.3.1 茶黄素水溶液的配制
精密称取一定量的茶黄素(TF)(万分之一天平称取),用40℃水溶解,配成约40μg/mL的溶液。
1.3.2 茶黄素不同pH值溶液的配制
pH值约为4的茶黄素溶液(茶黄素水溶液:pH值为3的盐酸=9∶1),pH值约为5的茶黄素溶液(茶黄素水溶液:pH值为4的盐酸=9∶1),pH值约为7的茶黄素溶液(1.3.1中所配茶黄素水溶液),pH值约为8的茶黄素溶液(茶黄素水溶液:pH值为9的氢氧化钠=9∶1),pH值约为9的茶黄素溶液(茶黄素水溶液:pH值为10的氢氧化钠=9∶1),溶液均过0.45μm膜。
1.3.3 不同浓度Fe3+的茶黄素溶液的配制
分别取1 mmol/L的三氯化铁溶液0.1,0.2,0.3,0.4 mL于4支5 mL容量瓶中,用茶黄素水溶液(见1.3.1)稀释至刻度,配成含不同浓度Fe3+的茶黄素溶液,摇匀后过0.45μm膜。
1.3.4 稳定溶液的配制
依据GB/T 31740.3—2015[7]配制稳定溶液,分别将EDTA-2Na溶液25 mL,抗坏血酸溶液25 mL,乙腈50 mL加入500 mL容量瓶中,用水定容至刻度,摇匀。
(1)EDTA-2Na溶液。10 mg/mL(现配)。精密称取EDTA-2Na 1.0 g,用水稀释至100 mL。
(2)抗坏血酸溶液。10 mg/mL(现配)。精密称取抗坏血酸1.0 g,用水稀释至100 mL。
1.3.5 茶黄素的稳定液溶液
称取一定量的茶黄素(TF),用稳定溶液稀释至刻度,摇匀后过0.45μm膜。
1.3.6 茶黄素溶液的含量变化测试
茶黄素含量测定采用高效液相色谱法,依据GB/T 31740.3—2015[7]测定中的色谱条件和梯度条件,以常温下同批次标准品水溶液的吸收峰面积为100%含量,比较不同环境下样品的峰面积变化值,来确定含量的变化。
2 结果与分析
2.1 茶黄素(TF)标准物的测试
茶黄素(TF)标准品纯度高,测试其HPLC色谱图中峰数单一,峰形尖锐;基线平直,零点吻合,因此可以作为试验中参比的标准。
HPLC色谱图见图2。

图2 HPLC色谱图
2.2 加热温度的影响
试验结果显示,茶黄素水溶液在40℃以下较稳定,50℃以上加热30 min分解明显,吸收峰面积(响应值)只有空白样的49.76%,80℃以上加热30 min吸收峰面积为0,表明此时已经全部分解完全,可见温度对茶黄素水溶液的稳定性影响非常大,温度越高影响越大。
温度对茶黄素水溶液稳定性的影响曲线见图3。
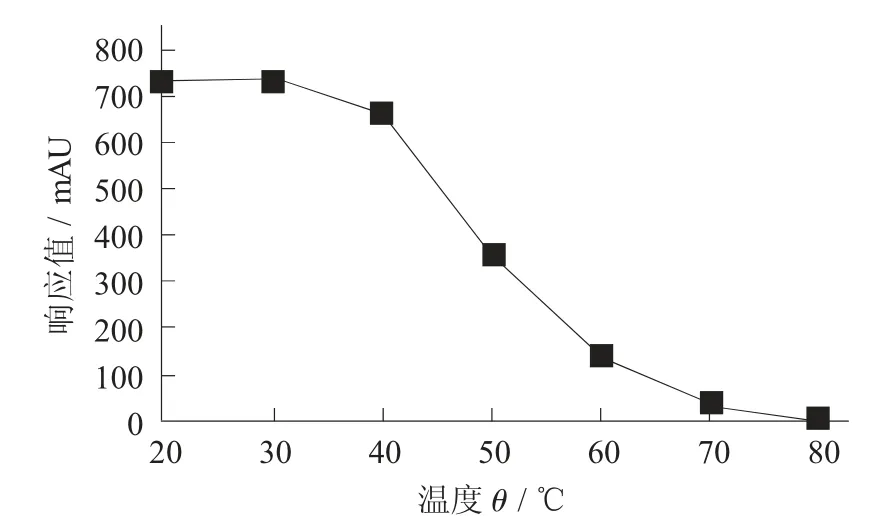
图3 温度对茶黄素水溶性稳定性的影响曲线
2.3 酸碱度的影响
试验结果显示,茶黄素水溶液在pH值为4~7,酸性和中性条件下比较稳定,在pH值〉8的碱性条件下不稳定,pH值=8时吸收峰面积(响应值)只有空白样的26.74%,这与酚类化合物自身是弱酸性物质,在酸性和中性条件下较稳定的推测一致。
pH值对茶黄素水溶性稳定性的影响曲线见图4。

图4 p H值对茶黄素水溶性稳定性的影响曲线
2.4 Fe3+的影响
试验结果显示,Fe3+极易与茶黄素反应,当Fe3+的浓度为0.02 mmol/L的极低浓度时,茶黄素仍然与Fe3+有明显的反应。
不同浓度Fe3+存在下的吸收峰面积见图5。
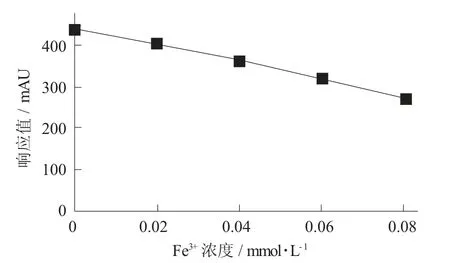
图5 不同浓度Fe3+存在下的吸收峰面积
2.5 室温、低功率照射、稳定液中放置时间的影响
试验结果显示,茶黄素水溶液在冬天10~20℃下放置有缓慢的分解,8 d后茶黄素的吸收峰面积是空白样的87.55%;在低功率照射下(20 W日光灯),茶黄素的吸收峰面积变化曲线与室温下面积变化曲线基本一致,照射8 d后茶黄素的吸收峰面积是空白样的89.91%,与87.55%接近,说明低功率照射对茶黄素水溶液的稳定性基本无影响;稳定液中的茶黄素在10~20℃下放置8 d几乎不分解,8 d后吸收峰面积是空白样的101.58%,没有降低,说明有稳定液存在对茶黄素的稳定性起到了一定的保护作用。
3种条件下的吸收峰面积变化曲线见图6。

图6 3种条件下的吸收峰面积变化曲线
3 讨论
茶黄素(TF)由中间的苯与七员双烯环酮并合结构,另2个苯与四氢吡喃并合结构共3个部分构成。中间的并合结构是大共轭体系,七员双烯环酮上有一个烯醇式结构;另2个并合结构通过单键与中间并合结构相连,在2个并合结构与单键连接的两旁都有氧吸电子基,这些因素使得单键上电子云向两端转移而容易断裂,当温度升高有可能发生断键的分解作用。从温度增加吸收峰面积降低,HPLC法测定中的吸收峰数目增多,说明了分解反应的发生。
在茶黄素中有多个酚羟基而显示弱酸性[14],因此茶黄素在酸性和中性中稳定,而在碱性中试验结果是吸收峰面积下降明显,吸收峰数目明显增多,可能是茶黄素发生了开环和断键反应,具体原因还不清楚。
酚能与三氯化铁发生显色反应[15],茶黄素中有多个酚羟基,所以茶黄素极易与Fe3+发生反应,反应属于配位反应[16],从反应的现象由淡黄色变为淡紫色都说明了该反应的特点。
酚具有易氧化的性质[15],烯醇式结构不稳定,茶黄素的多酚结构和烯醇式结构使得茶黄素的水溶液容易被氧化,在实验室常温密闭放置下也会缓慢被氧化;加入了由抗氧化剂(VC)和金属离子配合物(EDTA)组成的稳定液,因稳定液能参与氧化,结合大部分金属离子,因此它们能提高茶黄素的稳定性;低功率照射则因照射能力低而几乎没有影响。
4 结论
茶黄素(TF)是由3个并合结构通过单键连接的多酚物质,易发生分解和氧化及与Fe3+的配位反应,在加热、碱性和Fe3+存在下不稳定,因此,茶黄素在使用时要尽量选择低温、酸性和无Fe3+影响的条件下,避免加热、碱性和Fe3+的影响,普通日光灯照射基本不影响,稳定液对茶黄素水溶液的稳定性有一定的保护作用。
