吉西他滨联合曲妥珠单抗治疗人表皮生长因子受体 2阳性晚期乳腺癌的疗效
2023-03-05郝凯峰张明芳仲广生
郝凯峰,张明芳,仲广生
平煤神马医疗集团总医院乳腺科,河南 平顶山 467000
乳腺癌是女性常见恶性肿瘤之一,属于一种全身性疾病,尤其是人表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)阳性乳腺癌,更易出现早期转移及浸润[1]。研究指出,HER2在细胞生长、分化过程中具有重要作用,15%~20%的乳腺癌患者中存在HER2基因扩增[2]。蒽环类、紫杉类药物是目前临床辅助化疗的常用药物,应用较为广泛,但患者对蒽环类、紫杉类药物的耐药性也随之增加[3-4]。如何对蒽环类、紫杉类药物耐药的晚期乳腺癌患者进行解救治疗是目前临床需解决的重要难题之一。鉴于此,本研究通过收集HER2阳性晚期乳腺癌患者的临床资料,对比吉西他滨联合曲妥珠单抗(GH)方案与吉西他滨联合顺铂(GP)方案治疗HER2阳性晚期乳腺癌的疗效,旨在为临床治疗提供可靠依据,现报道如下。
1 资料与方法
1.1 一般资料
收集2016年8月至2020年8月平煤神马医疗集团总医院收治的HER2阳性晚期乳腺癌患者的病历资料。纳入标准:①符合晚期乳腺癌的诊断标准[5];②具有化疗适应证;③相关资料齐全;④未合并其他脏器肿瘤;⑤既往未行针对晚期疾病的化疗和靶向治疗。排除标准:①对化疗过敏;②心、肺、肝、肾等脏器功能障碍;③合并造血系统、免疫系统疾病;④精神疾病、妊娠期女性等特殊人群。根据纳入、排除标准,共纳入127例HER2阳性晚期乳腺癌患者,按化疗方案的不同分为GH组66例和GP组61例。GH组患者,年龄34~71岁,平均(55.98±11.06)岁;病理类型:导管癌43例,小叶癌23例。GP组患者,年龄34~72岁,平均(56.12±12.85)岁;病理类型:导管癌44例,小叶癌17例。两组患者年龄、病理类型比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会批准通过,所有患者均知情同意。
1.2 治疗方法
GH组采用GH方案治疗:吉西他滨1250 mg/m2,第1天及第8天静脉滴注,21天为一个周期;曲妥珠单抗首次8 mg/kg静脉滴注,随后剂量为每次6 mg/kg,每天1次,连续使用21天。GP组采用GP方案治疗:吉西他滨用法用量同GH组,顺铂25 mg/m2静脉滴注,每天1次。于两个周期治疗结束1个月后评价疗效。
1.3 观察指标
①比较两组患者临床疗效。根据实体瘤疗效评价标准[6]评估近期疗效,根据病灶变化情况分为完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD)。CR:疾病完全被控制,所有靶病灶消失,无新病灶出现;PR:疾病部分控制,靶病灶最大径之和减少≥30%;SD:病情稳定,基本已控制,介于PR和PD之间;PD:靶病灶最大径之和增加≥20%,或出现新病灶。总有效率=(CR+PR)例数/总例数×100%。②比较两组患者恶心呕吐、血小板下降等不良反应发生情况。③比较两组患者总生存率、无进展生存率。对患者进行1年电话随访(随访截至2021年8月),根据随访资料,计算总生存期(从确诊至患者死亡或者末次随访时间)和无进展生存期(一线治疗开始至疾病进展或者患者死亡的时间)。
1.4 统计学方法
采用SPSS 22.0软件进行数据分析,计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料以例数及率(%)表示,组间比较采用χ2检验;以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效的比较
GH组患者的总有效率为72.73%(48/66),明显高于GP组的52.46%(32/61),差异有统计学意义(χ2=10.466,P<0.01)。(表1)
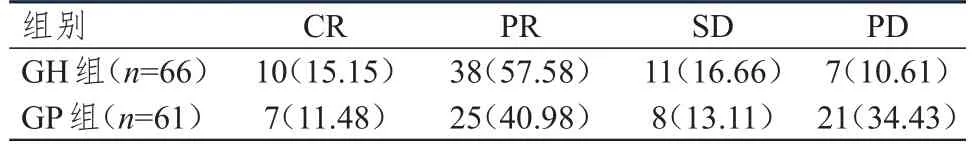
表1 两组患者的临床疗效[ n(%)]
2.2 不良反应发生情况的比较
GP组患者治疗期间白细胞减少、血小板下降发生率均高于GH组,差异均有统计学意义(P<0.05);两组患者脱发、恶心呕吐发生率比较,差异均无统计学意义(P>0.05)(表2)。两组患者均给予5羟色胺3受体拮抗剂、造血生长因子、白细胞介素-11等对症处理,处理后症状有所缓解或恢复。
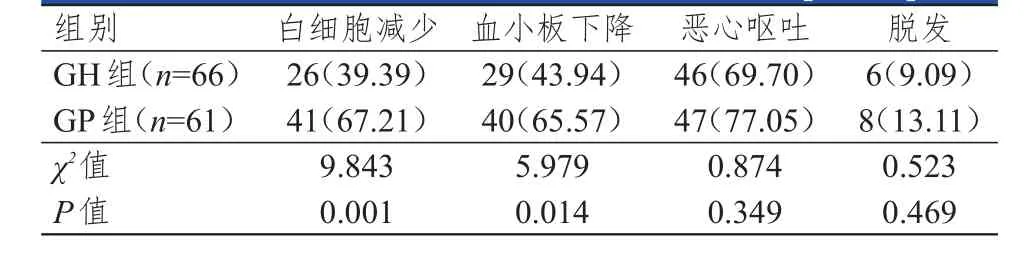
表2 两组患者不良反应发生情况的比较[ n(%)]
2.3 预后的比较
GH组患者总生存率明显高于GP组,差异有统计学意义(P<0.01);两组患者无进展生存率比较,差异无统计学意义(P>0.05)。(表3)
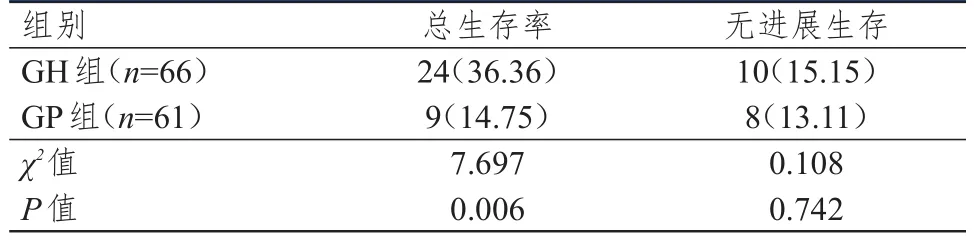
表3 两组患者预后的比较[ n(%)]
3 讨论
乳腺癌是恶性程度较高的一种妇科肿瘤,特别是HER2阳性乳腺癌患者,病情进展迅速、化疗缓解率低[7]。近年来,随着化疗方案的不断改进,乳腺癌患者的5年生存率有所提升,尤其是化疗药物联合应用使乳腺癌整体疗效大大提高,但患者5年内复发转移现象仍无法避免。报道指出,与单药化疗相比,联合靶向药物治疗效果更佳,可减少不良反应、非细胞毒性,且不需最大耐受药物剂量便可获得较好的临床效果,对提高肿瘤控制率、患者长期生存率具有重要作用[8]。本研究特别针对临床HER2阳性晚期乳腺癌患者,对GH、GP方案的疗效进行对比研究。
吉西他滨属于一种新型脱氧胞苷类药物,可有效抑制核糖核苷还原酶形成掩蔽链,又可使DNA双链合成终止断裂,导致细胞凋亡[9]。吉西他滨与紫杉类、蒽环类药物无交叉耐药,可作为紫杉类、蒽环类均耐药的晚期乳腺癌患者的基本治疗药物。既往报道认为,对于紫杉类、蒽环类耐药的晚期乳腺癌患者,使用吉西他滨单药治疗的总有效率低于20%[10]。对于基本情况较好,且可耐受联合化疗的患者来说,选择合适的药物与吉西他滨联合,可能获得更好的治疗效果。铂类与吉西他滨联合应用是最为常见的组合,亦有学者采用吉西他滨联合曲妥珠单抗。本研究发现,经GH方案治疗的GH组患者临床总有效率、总生存率均明显高于经GP方案治疗的GP组患者。说明与GP方案相比,GH方案治疗疗效更佳。但韩逸群等[11]发现,GH、GP方案治疗乳腺癌患者,两组患者无进展生存率差异显著,与本研究报道不符。推测其原因可能与样本量较少、随访时间不同等因素有关。国内较多报道支持曲妥珠单抗良好的疗效及药物耐受性,使得以曲妥珠单抗为基础的联合治疗方案可改善HER2阳性晚期乳腺癌患者的预后[12-13]。黄文发等[14]通过Ⅱ期和Ⅲ期临床试验证实,曲妥珠单抗联合铂类、吉西他滨等化疗药物的治疗方案具有一定的安全性和有效性,这与本研究结果一致。
化疗不良反应亦是临床值得密切关注的问题,因为不良反应可能对患者的整个化疗疗程造成一定影响。李雨琴和黄剑[15]报道指出,曲妥珠单抗联合其他化疗药物的联合化疗方案在晚期乳腺癌中具有效果好、不良反应轻的优势。本研究通过观察两组不良反应发现,GH组的主要不良反应为骨髓抑制、消化道不良反应,其中骨髓抑制以白细胞数减少、血小板下降为主,但上述不良反应发生率均低于GP组;胃肠道反应主要表现为恶心呕吐,但本研究中两组患者恶心呕吐发生率比较无显著差异,与上述报道相符,说明GH方案治疗HER2阳性晚期乳腺癌安全可靠。综上所述,GH方案治疗HER2阳性晚期乳腺癌较GP方案疗效更佳,可有效减少患者不良反应,提高总生存率。
