沙利度胺联合CHOP方案在非霍奇金淋巴瘤中的应用效果△
2023-03-05马东升徐玉秀王萍钟亚平高红秀王萌任晓艳吴胜胜
马东升,徐玉秀,王萍,钟亚平,高红秀,王萌,任晓艳,吴胜胜
驻马店市中心医院血液内科,河南 驻马店 463000
非霍奇金淋巴瘤是一种常见的淋巴细胞肿瘤,其发病机制与环境、遗传等因素有关。非霍奇金淋巴瘤好发于老年人群,且发病率和病死率较高,严重威胁患者的生活质量及生命安全[1-2]。非霍奇金淋巴瘤主要发生在淋巴结、胸腺和脾等器官,也可发生在淋巴结外淋巴组织,严重威胁人类生命健康。早期非霍奇金淋巴瘤主要表现为淋巴结肿大,无痛感,其次是腋窝下和腹股沟淋巴结肿大,且随着肿块发生纤维化,肿块开始变硬[3-4]。目前,临床常见的治疗方法为化疗,标准化疗方案为环磷酰胺+表柔比星+长春新碱+泼尼松(CHOP)方案,虽然能够延缓肿瘤进展,但治疗效果有限,不能有效提高患者的生存率,且肿瘤复发率较高,因此,寻找一种有效治疗非霍奇金淋巴瘤的方案成为临床亟待解决的医学难题之一[5]。沙利度胺是一种新型抗肿瘤药物,能够有效延缓肿瘤进展,改善生活质量[6-7]。对于非霍奇金淋巴瘤患者,延缓病情进展是治疗肿瘤的关键。本研究探讨沙利度胺联合CHOP方案在非霍奇金淋巴瘤患者中的应用效果,现报道如下。
1 资料与方法
1.1 一般资料
选取2016年1月至2021年1月驻马店市中心医院收治的非霍奇金淋巴瘤患者。纳入标准:①符合非霍奇金淋巴瘤的诊断标准[8],患者伴有发热、出汗、体重减少、无痛淋巴结肿大症状;②年龄>18岁;③无化疗禁忌证;④生存时间>1年;⑤病历资料完整。排除标准:①合并严重心、肝、肾功能障碍;②合并其他恶性肿瘤;③对化疗药物过敏;④精神状态较差,甚至伴有精神障碍。依据纳入和排除标准,本研究共纳入120例非霍奇金淋巴瘤患者,依据治疗方案的不同分为对照组(n=60)和观察组(n=60),对照组患者给予CHOP方案化疗,观察组患者给予沙利度胺联合CHOP方案化疗。对照组中,男31例,女29例;年龄30~62岁,平均(48.23±3.23)岁;临床分期:Ⅱ期15例,Ⅲ期25例,Ⅳ期20例。观察组中,男33例,女27例;年龄32~61岁,平均(47.64±3.46)岁;临床分期:Ⅱ期19例,Ⅲ期16例,Ⅳ期25例。两组患者性别、年龄、临床分期比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会批准通过,所有患者均知情同意。
1.2 治疗方法
对照组患者给予CHOP方案化疗,第1天,环磷酰胺750 mg/m2+表柔比星70 mg/m2+长春新碱1.4 mg/m(2最大剂量2.0 mg)静脉注射,第1~5天,泼尼松60 mg/m2口服,每天1次,3周为1个疗程,共治疗4个疗程。
观察组患者给予沙利度胺联合CHOP方案治疗,CHOP方案与对照组相同,沙利度胺100 mg,每天1次,口服21天,停药7天,第2个疗程开始时治疗剂量增加至200 mg,4周为1个疗程,治疗4个疗程。
1.3 观察指标和评价标准
1.3.1 临床疗效 参照实体瘤疗效评价标准评估两组患者的临床疗效:完全缓解(complete response,CR),肿瘤病灶完全消失;部分缓解(partial response,PR),肿瘤体积缩小≥50%;疾病稳定(stable disease,SD),肿瘤体积缩小<50%或增大<25%;疾病进展(progressive disease,PD),肿瘤体积增大≥25%或出现新病灶。总有效率=(PR+CR)例数/总例数×100%。
1.3.2 炎性因子 治疗前后,抽取两组患者静脉血4 ml置入抗凝管中,采用酶联免疫吸附测定检测两组患者炎性因子水平,包括白细胞介素-6(interleukin-6,IL-6)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)。
1.3.3 免疫功能 治疗前后24 h内,抽取两组患者静脉血,分别加入对应荧光标记的单克隆抗体,依次加入乙二胺四乙酸抗凝的全血中孵育20 min,再加入红细胞裂解液,用磷酸盐缓冲液(phosphate buffered solution,PBS)反复洗涤3次,采用流式细胞仪检测CD4+、免疫球蛋白A(immunoglobulin A,IgA)、免疫球蛋白G(immunoglobulin G,IgG)水平。
1.3.4 肿瘤标志物 治疗前后,抽取两组患者清晨空腹静脉血5 ml,采用酶联免疫吸附测定检测两组患者血清血管内皮生长因子(vascular endothelial growth factor,VEGF)、诱生型一氧化氮合酶(inducible nitric oxide synthase,iNOS)和乳酸脱氢酶(lactate dehydrogenase,LDH)水平。
1.3.5 不良反应 比较两组患者的不良反应发生情况,包括恶心呕吐、肝脏损害、便秘和外周神经毒性等。
1.4 统计学方法
采用SPSS 22.0软件对所有数据进行统计学分析,计量资料以均数±标准差(±s)表示,组间比较采用两独立样本t检验,组内比较采用配对t检验;计数资料以例数和率(%)表示,组间比较采用χ2检验;以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效的比较
观察组患者的治疗总有效率为83.33%(50/60),明显高于对照组患者的61.67%(37/60),差异有统计学意义(χ2=7.064,P<0.01)。(表1)
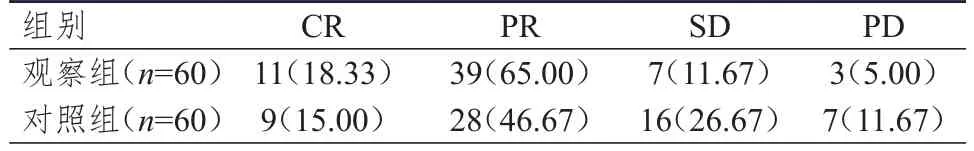
表1 两组患者的临床疗效[ n(%)]*
2.2 炎性因子水平的比较
治疗前,两组患者IL-6、TNF-α水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者IL-6、TNF-α水平均低于本组治疗前,且观察组患者IL-6、TNF-α水平均低于对照组,差异均有统计学意义(P<0.05)。(表2)
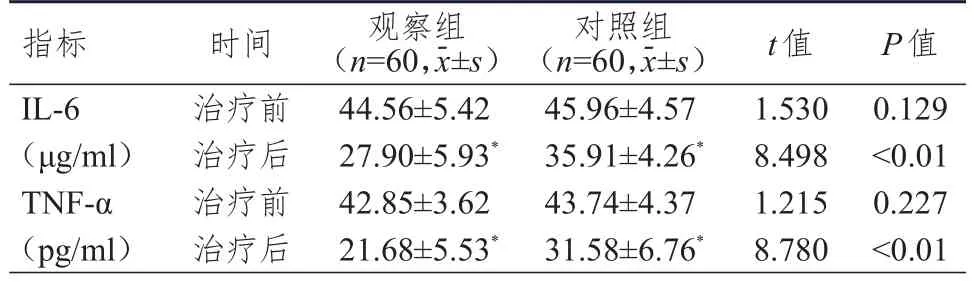
表2 治疗前后两组患者炎性因子水平的比较
2.3 免疫功能指标的比较
治疗前,两组患者CD4+、IgA、IgG水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者IgA、IgG水平均低于本组治疗前,CD4+水平均高于本组治疗前,且观察组患者IgA、IgG水平均低于对照组,CD4+水平高于对照组,差异均有统计学意义(P<0.05)。(表3)
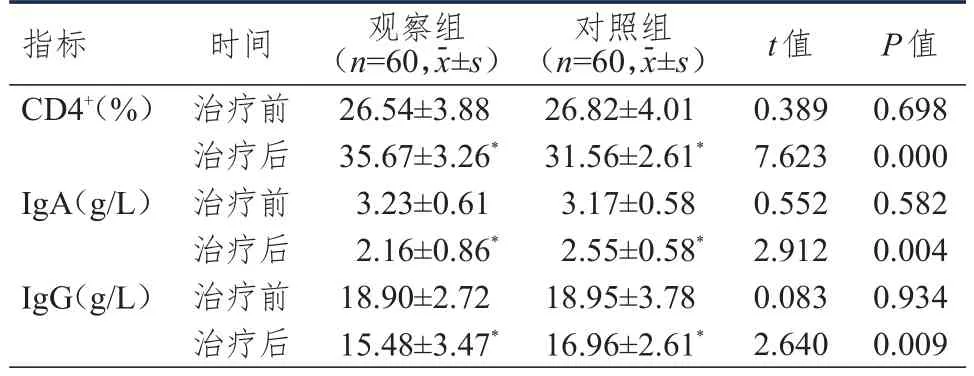
表3 治疗前后两组患者免疫功能指标的比较
2.4 肿瘤标志物水平的比较
治疗前,两组患者VEGF、iNOS、LDH水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者VEGF、iNOS、LDH水平均低于本组治疗前,且观察组患者VEGF、iNOS、LDH水平均低于对照组,差异均有统计学意义(P<0.05)。(表4)

表4 治疗前后两组患者肿瘤标志物水平的比较
2.5 不良反应发生情况的比较
观察组患者不良反应总发生率为6.67%(4/60),低于对照组患者的18.33%(11/60),差异有统计学意义(χ2=5.445,P<0.05)。(表5)

表5 两组患者的不良反应发生情况[ n(%)]
3 讨论
非霍奇金淋巴瘤是一种临床常见的恶性肿瘤,主要发生在动物淋巴结和淋巴细胞中,是一组发生在淋巴系统的恶性肿瘤[9-10]。非霍奇金淋巴瘤是由多种因素引发的淋巴结恶性肿瘤,其发病机制可能与感染化学物质或其他因素有关[11]。非霍奇金淋巴瘤进展速度较快,且病死率较高,严重威胁人类生命健康。非霍奇金淋巴瘤患者颈部和锁骨处没有痛感、淋巴结肿大,伴有发热、出汗及消瘦等症状[12]。目前,临床非霍奇金淋巴瘤常用的化疗方案为CHOP方案,方案中的环磷酰胺注射液、长春新碱、表柔比星、泼尼松治疗早期非霍奇金淋巴瘤疗效显著,能缓解肿瘤进展,减轻患者的身体痛苦;但常规化疗的效果有限,且不良反应明显,短期内肿瘤复发率高[13]。CHOP方案与其他药物联用能增强疗效。沙利度胺是一种抗肿瘤药物,对血管和免疫功能具有调节作用,对多种肿瘤的治疗效果较好,其通过调节相关的白细胞介素-7、白细胞介素-1及转录因子,抑制成纤维细胞生长因子和VEGF的表达,抑制新生血管生成;沙利度胺能够刺激T淋巴细胞增殖,增强其细胞诱导过程,促进白细胞介素-2和干扰素的分泌,从而减轻肿瘤细胞对机体的损伤,增强自然杀伤细胞活性,有效加强机体对肿瘤细胞的抵抗能力,抗肿瘤治疗效果较好[14-15]。
沙利度胺能促进机体IL-6和肿瘤坏死因子的表达,从而增强机体淋巴细胞功能,抑制新生血管生成,有效抑制肿瘤细胞的分化[16]。本研究结果显示,观察组患者治疗总有效率高于对照组,不良反应总发生率低于对照组,表明沙利度胺联合CHOP方案可有效改善临床疗效,降低不良反应发生率。苏永红和焦宁超[17]研究沙利度胺联合CHOP方案对B细胞淋巴瘤的疗效,结果发现,观察组患者的临床效果明显高于对照组,且不良反应事件的发生率降低;沙利度胺联合CHOP方案用于非霍奇金淋巴瘤,治疗效果明显优于单独CHOP方案治疗。
IL-6和TNF-α是由细胞所产生的促炎因子,主要参与机体免疫应答、抗体反应和造血过程[18]。本研究结果显示,治疗后,两组患者IL-6、TNF-α水平均低于本组治疗前,且观察组患者IL-6、TNF-α水平均低于对照组,提示沙利度胺联合CHOP方案可减轻非霍奇金淋巴瘤患者的炎性反应,治疗效果更显著。CD4+可辅助T细胞识别抗原信号,IgA和IgG是反映机体免疫功能的重要指标[19]。本研究结果显示,治疗后,两组患者IgA、IgG水平均低于本组治疗前,CD4+水平均高于本组治疗前,且观察组患者IgA、IgG水平均低于对照组,CD4+水平高于对照组,提示沙利度胺联合CHOP方案能明显改善非霍奇金淋巴瘤患者的免疫功能,且二者联用的效果更佳,这可能与沙利度胺能够改善患者的炎性因子水平有关。
LDH是一种糖降解酶,是衡量患者肿瘤细胞增殖能力的重要指标;VEGF能够衡量肿瘤细胞的侵袭能力及肿瘤进展[20]。本研究结果显示,治疗后,两组患者VEGF、iNOS、LDH水平均低于本组治疗前,且观察组患者VEGF、iNOS、LDH水平均低于对照组,提示沙利度胺联合CHOP方案可改善非霍奇金淋巴瘤患者的VEGF、iNOS、LDH水平,明显抑制肿瘤细胞增殖能力和血管生成能力,降低肿瘤的增殖速度,延长患者生存时间。综上所述,沙利度胺联合CHOP方案治疗非霍奇金淋巴瘤的效果较好,能够明显改善患者炎性因子水平,增强免疫功能,安全性较好。但本研究纳入的样本量较小,且为单中心研究,后续需开展大样本多中心研究进一步验证。
