微波热疗联合化疗治疗晚期消化道肿瘤的疗效观察
2023-03-04赵智晨东港市中心医院肿瘤内科辽宁丹东118300
赵智晨 东港市中心医院肿瘤内科 (辽宁 丹东 118300)
内容提要: 目的:分析晚期消化道肿瘤疾病特点、治疗需求,评价微波热疗联合化疗治疗的优势。方法:选择2019年1月~2020年4月本院诊治的80例晚期消化道肿瘤疾病患者,进行随机法分组治疗,伦理委员会批准。对照组患者采取常规化疗治疗,观察组患者采取微波热疗联合化疗治疗。比较2组晚期消化道肿瘤患者的治疗情况,包括疾病近期疗效、生活质量以及骨髓抑制、胃肠道反应、血象异常不良反应发生情况。结果:近期疗效方面,观察组晚期消化道肿瘤患者的总有效率90.00%明显高于对照组的65.00%(P<0.05);不良反应发生情况比较,观察组晚期消化道肿瘤患者的骨髓抑制(12.50%)、胃肠道反应(5.00%)、血象异常(2.50%)不良反应发生率均低于对照组(P<0.05);生活质量方面,观察组晚期消化道肿瘤患者的生活质量评分(88.80±6.60)分高于对照组(P<0.05)。结论:与单纯化疗治疗比较,联合微波热疗治疗晚期消化道肿瘤提升了疾病近期治疗效果、患者安全性,提升了患者的生活质量,是有效的治疗方案。
消化道肿瘤是肿瘤内科常见恶性占位病变之一,据统计其发病率在所有肿瘤发病率中排前三,临床常见的消化系统肿瘤包括胃癌、直肠癌、结肠癌、胰腺癌等[1]。疾病多发与患者生活习惯、生活环境、遗传等因素有关,晚期消化道肿瘤患者具有较高的致死风险,需积极诊断、治疗。消化系统肿瘤早期症状多较隐匿,多数患者甚至没有明显临床不适,疾病发展到一定时期后患者可伴有腹痛、腹泻等不适临床症状,但此时完善检查多发现已经发展到较为严重的程度。这也是消化系统肿瘤一经发现多需临床手术干预治疗的一个原因。随着治疗经验的积累,发现早期消化系统肿瘤多建议手术治疗,疗效确切,但中晚期肿瘤患者随着癌细胞不断在体内扩散,手术治疗已经很难获得满意的临床疗效;对于患者病情进展迅速,扩张程度较高的患者,已经不适宜应用手术治疗,此时多采用化疗,化疗对于不能耐受手术治疗或手术治疗效果不佳患者进行姑息疗法,具有明显的效果,可以有效改善患者临床症状,提高患者生存期。然而化疗存在的副作用也比较明显,常见的包括骨髓抑制、胃肠道反应、血象异常等。所以,为了提升患者治疗效果,需不断优化治疗方案。热疗治病的原理是利用肿瘤细胞与正常细胞对热敏感程度有较大差异,进而通过热疗增加化疗的治疗效果。张婕等应用辅助微波热疗治疗乳腺癌患者,发现微波热疗联合化疗能够显著增强化疗效果,使化疗药物全部覆盖肿瘤病灶,从而提高疾病的治疗结果[2]。本文就本院2019年1月~2020年4月80例晚期消化道肿瘤患者为例,进行常规化疗治疗、化疗辅助微波热疗治疗对比研究。
1.资料与方法
1.1 临床资料
研究对象均为晚期消化道肿瘤患者,时间选自2019年1月~2020年4月,总计80例,研究治疗方案伦理委员会批准。将晚期消化道肿瘤患者分为对照组、观察组进行治疗,各40例。对照组:男23例,女17例;年龄42~72岁,平均(50.50±8.50)岁;疾病类型:胃癌患者20例,直肠癌患者10例,其他患者10例。观察组:男25例,女15例;年龄43~73岁,平均(51.20±7.20)岁;疾病类型:胃癌患者18例,直肠癌患者13例,其他患者9例。分组治疗后的2组晚期消化道肿瘤患者资料完整,对比均衡,P>0.05。
纳入标准:①化疗等治疗方案患者、家属知情签署同意书;②患者身体治疗耐受;③患者预计生存期>6个月;④病历资料完整;⑤伦理委员会审核批准。排除标准:①依从性较差患者;②退出治疗患者;③治疗不耐受情况患者;④合并其他重大疾病患者[3]。
1.2 方法
对照组:予以患者化疗治疗。胃癌患者予以紫杉类、铂类等药物联合化疗,肠癌患者予以铂类、氟尿嘧啶类联合化疗,采用FOLFOX XELOX方案。
观察组:在对照组化疗治疗基础上配合热疗治疗。晚期消化道肿瘤患者放入治疗舱内,温度43.5°C,时间1h,2次/周,1周=1个周期,持续治疗2~3周期。
另外,予以80例患者5-HT3受体拮抗剂、止吐等药物,并进行静脉营养处理。
1.3 观察指标
统计2组晚期消化道肿瘤患者治疗后近期疗效、不良反应发生情况以及生活质量状况。
1.4 效果评价标准
显效:治疗后患者症状消退、腹水量大量减少;有效:治疗后患者症状改善、腹水量减少;无效:治疗后患者症状以及腹水量情况基本无变化[4]。治疗总有效率=(显效+有效)例数/总例数×100.00%。
1.5 生活质量评价
采用欧洲癌症研究与治疗组织生活质量测定量表(european organzation for research and treatment of cancer quality of life-C30,EORTC QLQ-C30)评价晚期消化道肿瘤患者治疗前后的生活质量,包含躯体功能、角色功能、认知功能以及情绪功能、社会功能5项,满分百分制。评分越高,晚期消化道肿瘤患者的生活质量越好[5]。
1.6 统计学分析
数据导入SPSS19.0进行计算机处理。计数型指标以n、%的形式描述,组间指标差异采用χ2检验;计量型指标以±s的形式描述,组间指标差异采用t检验。P<0.05为具有统计学意义。
2.结果
2.1 治疗效果比较
治疗后,观察组、对照组晚期消化道肿瘤患者的近期总有效率分别为90.00%、65.00%,经统计学计算,与对照组比较,观察组治疗效果更为理想P<0.05,具有统计学意义,见表1。
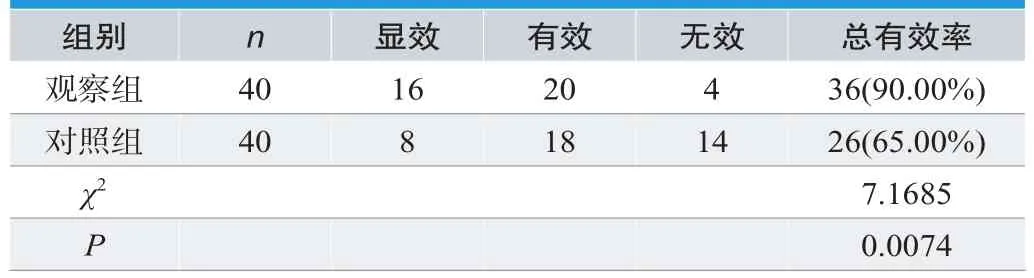
表1. 晚期消化道肿瘤患者组间临床疗效分析
2.2 不良反应情况比较
治疗后,观察组、对照组晚期消化道肿瘤患者的骨髓抑制、胃肠道反应、血象异常不良反应发生情况见表2。经统计学计算,与对照组比较,观察组不良反应发生率更低,P<0.05,具有统计学意义。

表2. 晚期消化道肿瘤患者组间不良反应情况分析
2.3 生活质量评分比较
治疗后,观察组、对照组晚期消化道肿瘤患者的生活质量评分情况见表3。经统计学计算,与对照组比较,观察组评分更高,P<0.05,具有统计学意义。
表3. 晚期消化道肿瘤患者组间生活质量评分对比(±s,分)
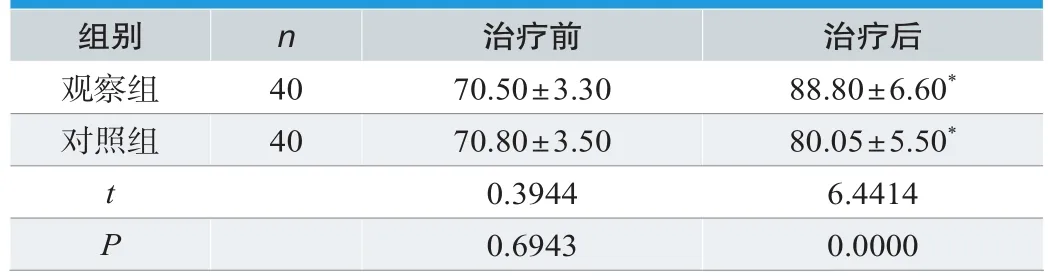
表3. 晚期消化道肿瘤患者组间生活质量评分对比(±s,分)
注:*比较治疗前生活质量评分,P<0.05
组别 n 治疗前 治疗后观察组 40 70.50±3.30 88.80±6.60*对照组 40 70.80±3.50 80.05±5.50*t 0.3944 6.4414 P 0.6943 0.0000
3.讨论
消化道肿瘤即发生于消化道位置的良性瘤、恶性肿瘤,其中,晚期消化道肿瘤患者合并腹膜炎情况明显,增加了疾病的治疗难度[6]。关于食管癌、胃癌、大肠癌等晚期消化道肿瘤疾病主要采取化疗治疗手段,但是化疗后近期疗效并未达到预期要求,且患者不良反应发生情况明显,影响患者化疗治疗的耐受性和配合程度[7]。当前,热疗凭借理想治疗效果、良好耐受性等特点,开始常用于化疗辅助治疗中,发现对于提升晚期消化道肿瘤患者近期效果与安全性方面效果理想[8]。热疗原理是将化疗药物温度进行一定范围提升,进而增加肿瘤细胞及组织的温度,因肿瘤细胞及正常细胞对温度的耐受程度有差异,因此能够提高化疗效果加快肿瘤细胞死亡速度,达到在杀灭肿瘤细胞同时保护正常组织不受损害的治疗目的。热疗依据治疗范围可分为全身热疗和局部热疗两种方式,前者因操作繁杂,且容易引发严重的周身反应,副作用也高,因此临床应用较少。而局部热疗则被广泛应用。热疗能帮助药物快速进入细胞组织,促进药物吸收、预防细胞损伤、抑制肿瘤细胞生长,且能够加快血液流动总量、扩大药物范围、有效发挥药效、促进肿瘤死亡[9,10]。另外,热疗能缩短肿瘤细胞、抗癌药物距离,联合化疗治疗在抑制DNA复制的基础上增强化疗效果。常用的热源包括微波、红外线、热水浴、热浴、超声波等,本研究主要采用微波热疗。张则才等[11]研究指出,晚期消化道肿瘤患者行微波深部热疗联合化疗治疗可以促进患者临床症状进改善,进而提高患者的生存质量。分析热疗能够提高化疗对抗肿瘤细胞的作用机制为以下几点:①高热可以直接杀死肿瘤,能够抑制DNA、RNA及蛋白质的合成。②正常组织受热后能够依靠有效的血液循环进行散热,而肿瘤不具备血液循环降热能力,局部温度会比正常组织高5%以上,当温度上升至45℃作用时,正常组织一般不会受到损伤。③高温状态下,肿瘤细胞膜流动性增强,膜结构功能可能受到损伤,会妨碍膜转运蛋白及细胞膜受体的正常运转。并且高温可以诱导肿瘤细胞内蛋白外溢、染色质变性,进而加速肿瘤细胞死亡。④高温还可以抑制肿瘤细胞蛋白合成,抑制其增殖速度,进而诱发细胞死亡。
本文结果显示,观察组与对照组晚期消化道肿瘤患者治疗效果、不良反应、生活质量评分差异显著,P<0.05,具有统计学意义。由此说明,采取热疗联合化疗作用突出,满足晚期消化道肿瘤患者治疗需求。本文结果与李小虎等[12]研究结果有一致性,研究组疾病好转率86.7%高于对照组,毒副作用率6.7%低于对照组,P<0.05,有统计学意义。
综上所述,对比单纯化疗治疗比较,晚期消化道肿瘤患者采取热疗联合化疗作用明显,促进患者症状改善,预防毒副作用,提升了患者的生活质量。
