超临界CO2萃取竹叶花椒挥发油的成分和分子光谱分析
2023-03-03李潮俊周孟焦张玉陈凯康明梁晓峰
李潮俊 ,周孟焦,张玉,陈凯,康明,梁晓峰 *
1. 四川中医药高等专科学校川西北中药材资源研究与开发利用实验室,绵阳市中药资源开发利用重点实验室(绵阳 621010);2. 西南科技大学材料与化学学院(绵阳 621010)
竹叶花椒(Zanthoxylum armatumDC.)为芸香科花椒属植物,主要分布在我国秦岭以南的广大西南地区[1],其根、茎、叶、果实、种子均可入药,同时也是一种广受欢迎的调味料,在食品、农业、医药、保健等领域具有巨大发展潜力[2]。近年来,对竹叶花椒挥发油的研究取得积极进展。竹叶花椒挥发油是其香气的主要来源,是鉴定竹叶花椒品质的重要依据,同时在抗炎镇痛、杀虫抑菌等方面有着重要应用[3-7]。对竹叶花椒挥发油的组成成分及其指纹图谱研究,是深入认识竹叶花椒的基础,也是拓展其综合应用领域的关键。
超临界CO2萃取集萃取、分离技术为一体,有着绿色、无毒害、产率高等优点,较低的萃取温度、无溶剂污染及无氧环境能最大程度地保护天然活性成分,因此常被用在天然活性成分的提取上[8-9],因其绿色环保、工艺简单、自动化程度高,被广泛应用于工业生产。
为建立竹叶花椒挥发油的成分和指纹图谱,进一步发挥竹叶花椒价值,提高竹叶花椒挥发油利用率,以竹叶花椒果皮为原材料,采用超临界CO2萃取法从竹叶花椒果皮中提取挥发油样品,利用GC-MS、红外光谱、拉曼光谱等技术对其进行分析和探讨。
1 材料与方法
1.1 材料与仪器
1.1.1 主要材料与试剂
干燥的竹叶花椒果皮(幺麻子食品股份有限公司,产地为四川省眉山市洪雅县);CO2气体(纯度99.99%,食品级,昌俊气体有限公司);无水乙醇(分析纯,成都市科隆化学品有限公司)。
1.1.2 主要仪器与设备
HA120-50-05型超临界萃取装置(南通市华安超临界萃取有限公司);FT-IR5700红外光谱仪(美国热电仪器有限公司);QP2020气相色谱-质谱联用仪(日本Shimadu公司);In Via型激光拉曼光谱仪(英国雷尼绍公司)。
1.2 方法
1.2.1 超临界CO2萃取法提取竹叶花椒挥发油
HA120-50-05型超临界萃取装置自带两级分离系统及分离釜Ⅰ、分离釜Ⅱ,在不调节分离系统温度、压力的情况下会从分离釜Ⅰ中得到挥发油,此时分离釜Ⅱ中无产物。通过调节分离釜Ⅰ的温度、压力,影响超临界流体的溶质能力,可在分离釜Ⅰ将挥发油中的杂质分离出来,挥发油随超临界流体通向分离釜Ⅱ中进行分离。通过调整工艺参数,获得2种工艺条件的挥发油。其一是使用超临界萃取装置,在萃取时间80 min、萃取温度25.5 ℃、萃取压力25.5 MPa条件下,从分离釜Ⅰ中得到的挥发油,编号C1。其二是在同样萃取条件下进行萃取,通过调节分离釜Ⅰ中的温度、压力,在萃取的同时对挥发油进行分离纯化,从分离釜Ⅱ中得到的纯化后的挥发油,编号C2。
1.2.2 GC-MS分析
用移液枪取0.1 mL挥发油样品,用乙醇定容至10 mL备用。
气相色谱条件:非极性SH-RXi-5Sil MS毛细管柱(30 m×0.25 mm×0.25 μm),柱温60 ℃,保持1 min,以4 ℃/min升至120 ℃,以5 ℃/min升至200 ℃,保持1 min;载气为高纯氦气,柱流量1.0 mL/min,进样口温度230 ℃,不分流进样,接口温度240℃,溶剂延迟时间3.0 min。
质谱条件为:EI电子源,电离能70 eV,离子源温度230 ℃,扫描范围(m/z)35~450 amu。
1.2.3 红外光谱分析
采用液膜法,先压制空白溴化钾片,在测试时用微型移液枪取少量待测样品涂抹在空白溴化钾片上,红外扫描波长范围400~4 000 cm-1,分辨率0.4 cm-1。
1.2.4 拉曼光谱分析
拉曼测试条件:激光波长785 nm,物镜放大倍数50 倍,采谱范围400~3 000 cm-1,分辨率1~2 cm-1。
2 结果与分析
2.1 GC-MS结果分析
通过计算机检索,利用NIST-17数据库匹配进行定性分析(选择匹配度>80%),将各组分相对含量按照峰面积归一法计算,结果见表1。
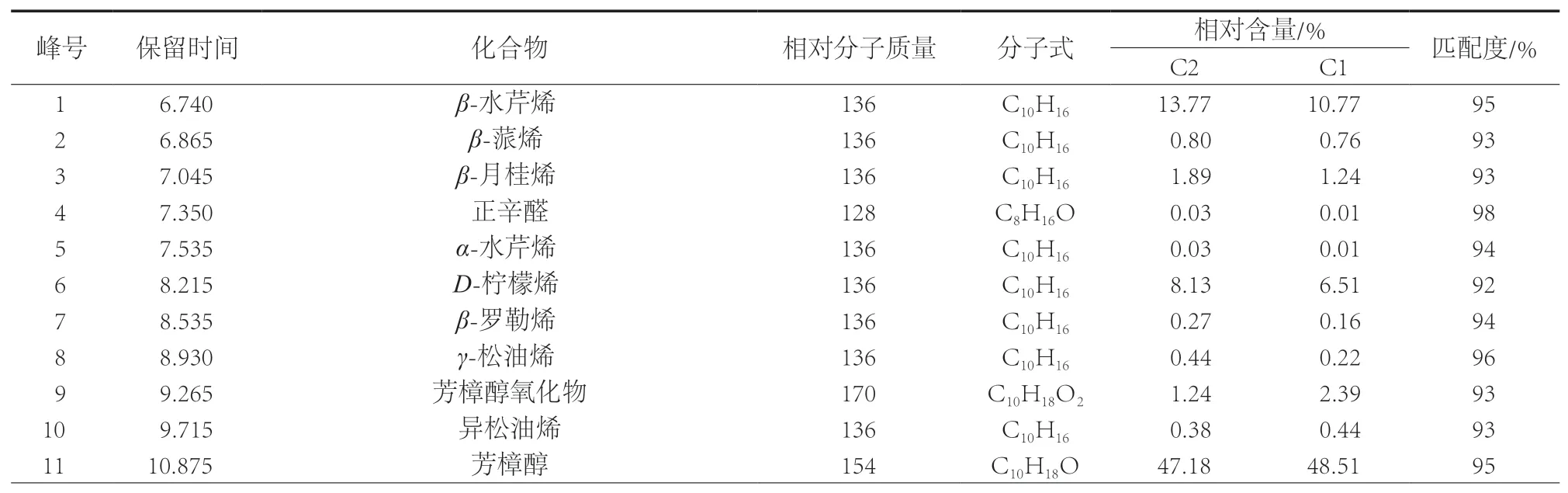
表1 GC-MS检测结果

接表1
由表1给出的数据可知,从C2和C1中共鉴定出62种化合物,分别占挥发油总量的91.85%和88.64%。以芳樟醇为主的醇类化合物占挥发油总量的52.83%和55.18%,β-水芹烯和D-柠檬烯为主的烯烃类占32.16%和25.98%,还有一些烷烃类、醛酮类、酯类物质。两者挥发性成分相同,仅在相对含量上有所区别,C2中β-水芹烯、D-柠檬烯、β-月桂烯等烯烃类成分的相对含量有所增加。
2.2 红外光谱分析
挥发油C2和C1的红外光谱图如图1和图2所示。C2在3 404,2 970,2 925,2 858和919 cm-1附近出现5个强红外吸收峰,在1 672,1 640,1 451,1 411,1 375,1 236,1 172,1 114和995 cm-1附近出现9个中等强度的红外吸收峰,在3 086,2 731,1 728,1 546,835,736和689 cm-1附近出现7个强度弱的红外吸收峰。C1在3 391,3 086,3 012,2 970,2 923,2 855,2 732,1 738,1 670,1 632,1 551,1 450,1 376,1 239,1 177,1 116,994,920,838,737和690 cm-1附近出现红外吸收峰。两者的红外吸收峰的数量和峰强基本一致,说明2种条件下获得的挥发油的成分基本相同。

图1 挥发油C1的红外光谱图

图2 挥发油C2的红外光谱图
样品红外光谱反映化合物的分子振动情况,对于每一种分子的官能团,都具特定振动频率。2 970 cm-1和2 925 cm-1两处的强峰为CH3和CH2的反对称伸缩振动,1 451 cm-1和1 375 cm-1附近的峰归属于CH3的不对称变角振动和对称变角振动。3 404 cm-1强且宽的单峰为O—H伸缩振动,1 411 cm-1处的峰可归属于C—OH面内弯曲振动,1 114 cm-1可归属为醇类C—OH伸缩振动,这应该是芳樟醇等醇类物质的特征振动。3 086 cm-1处强度较弱的吸收峰属于烯烃类化合物==CH2反对称伸缩振动,1 640 cm-1处可归属于C==C伸缩振动,同时995 cm-1和919 cm-1处的强吸收峰为烯烃类CH2的扭曲振动和面外摇摆,这应该是烯烃类化合物的特征振动。2 731 cm-1处弱而尖锐的峰为醛基上C—H的伸缩振动峰,1 728 cm-1处的红外吸收峰属于C==O振动吸收峰区域,1 236和1 172 cm-1处的吸收峰为脂肪酸酯的C—O—C伸缩振动,这应该是挥发油含有的酮醛及酯类化合物的特征振动[10]。C1和C2同为超临界CO2萃取物,从红外光谱图比较,C2的红外吸收峰更加清晰,这是由于超临界装置的工艺设置,使通过分离釜Ⅱ收集的样品C2去除一些非挥发性的物质,这与GC-MS分析的结果一致。
2.3 拉曼光谱分析
拉曼光谱技术是一种原位测试技术,反映物质的分子振动规律,其测试结果与红外光谱具有互补性。从拉曼光谱图中,可以看出C1光谱中,具有CH3、CH2、C==C、C—O—C、C==O等基团的特征光谱,在1 635,1 449,1 380,1 297,1 257,1 175和1 156 cm-1处出现散射峰,C2中具有CH3、CH2、C==C基团的特征光谱,在1 675,1 637,1 455,1 380和1 290 cm-1处出现散射峰。
其中,1 675和1 637 cm-1来自于C==C伸缩振动(环己烯的拉伸和乙烯基的拉伸),1 455 cm-1来自于CH2的弯曲振动。1 290 cm-1来自于(CH2)2的面外弯曲振动,1 380 cm-1来自于CH3的弯曲振动[11-15]。依据表1数据,C2中主要成分有芳樟醇(47.18%)、β-水芹烯(13.77%)、D-柠檬烯(8.13%)、月桂烯(1.89%)、松油烯-4-醇(1.66%)、石竹烯(1.48%)、α-松油醇(1.11%)、β-蒎烯(0.8%)等。其中,芳樟醇含量最高,而在1 675,1 637,1 380和1 290 cm-1处的峰能与其特征峰位很好地对应。C1样品的拉曼光谱图中1 257,1 175和1 156 cm-1处出现3个散射峰主要是来自于C—O—C、C==O及一些含氮基团的振动,可能是受到物质纯度或者荧光的影响,在C1样品的拉曼图中没有观察到这3个散射峰。
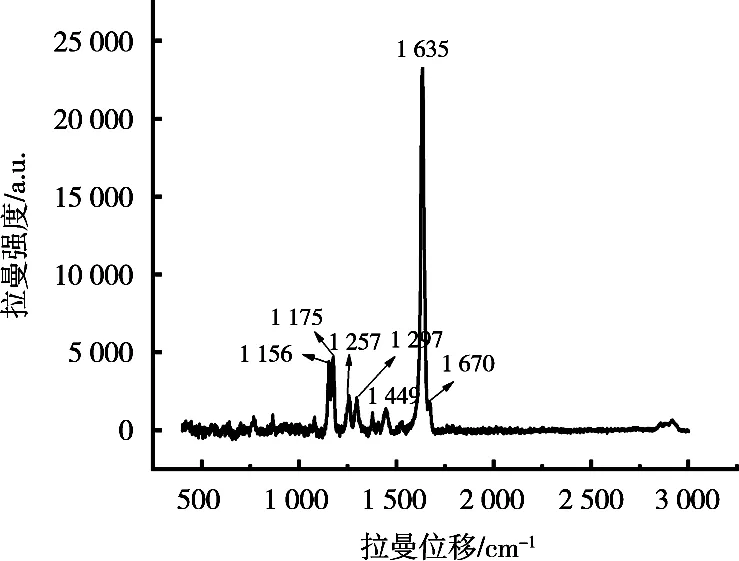
图3 挥发油C1的拉曼光谱图
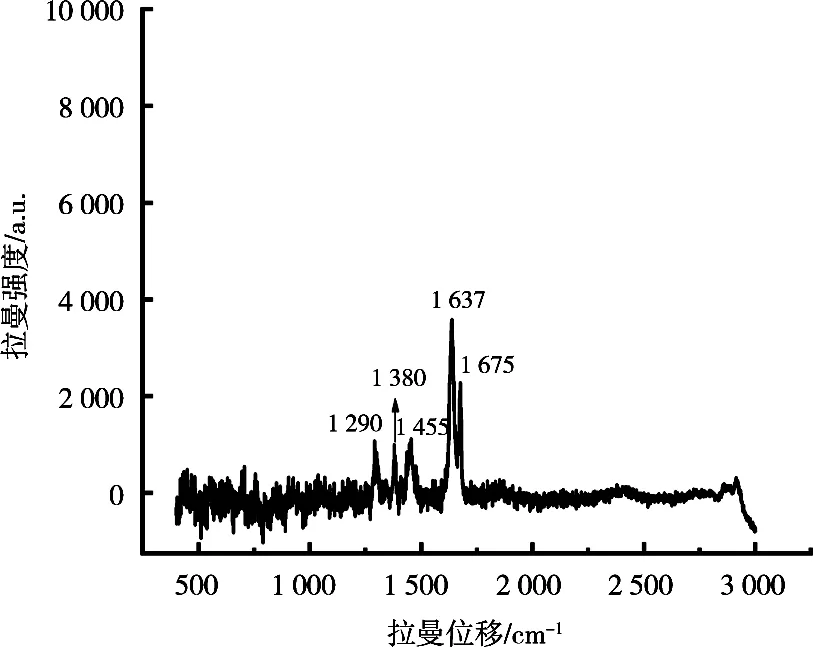
图4 挥发油C2的拉曼光谱图

表2 挥发油拉曼谱带及其归属[16, 18-19]
3 结论
超临界CO2萃取竹叶花椒挥发油中主要含有醇类、烯烃类物质,还有少量酮醛类、酯类等物质,其中含量较多的成分有芳樟醇(47.18%和48.51%)、β-水芹烯(13.77%和10.77%)、D-柠檬烯(8.13%和6.51%)等。GC-MS从2种超临界挥发油种共鉴定出62种化合物,分别占挥发油总量的91.85%和88.64%,2种超临界条件下,挥发油成分相同,但相对含量发生变化。红外光谱和拉曼光谱分析显示挥发油的主要官能团,为挥发油成分研究提供参考。
