WO3/BiOCl0.7I0.3光催化剂的制备及其光催化降解机理
2023-03-01刘海成孟无霜黄哲尤雨花瑞琪曹梦茹
刘海成,孟无霜,黄哲,尤雨,花瑞琪,曹梦茹
(苏州科技大学环境科学与工程学院,江苏 苏州 215009)
抗生素自发现以来,因其优越的抗菌性能被广泛用于制药、医疗和畜牧业等领域,其中四环素类抗生素(tetracyclines)是抗生素中应用最为广泛的一类[1−2]。抗生素具有持久性,且难以被生物体完全代谢,通过各种途径进入水体在水环境中富集,会导致微生物产生抗药基因[3−4]。抗生素耐药性引发的细菌感染将严重威胁人类的生存安全[5],水体中抗生素的去除问题亟待解决。
传统水处理技术(生物处理、吸附去除等)在面对抗生素类废水的处理时,处理能力表现出不足。相较于此,光催化技术因环保绿色、成本低廉和高效降解有机污染物等优势,成为研究热点[6−7]。WO3是一种能够可见光响应的光催化剂,禁带宽度为2.4~2.8eV,因独特的晶格结构,具有良好的电子传输能力,性质稳定且易于制备,既可用作主催化剂,也可用作助催化剂[8]。但WO3的导带电位比电子还原氧的电位低,无法将吸附在其表面的氧还原为超氧自由基,电子无法及时清除,导致了较高的电子空穴复合率,大幅降低了光催化性能。有研究证实,可以通过复合半导体构建异质结构的方式来解决这一问题[9]。
异质结构可以优化电子转移路径,促进光生电子(e−)和空穴(h+)的分离,从而提高材料光催化性能。Bi等[10]采用水热法和电沉积法成功制备了在可见光激发下具有优异光催化活性的BiOI/WO3异质结构光催化剂。BiOI禁带宽度(1.8eV)较窄,对可见光有较好的吸收性能,BiOCl 独特的层状结构形成的内部静电场可以促进电子空穴对的分离,两者结构相似,且结合在一起可以形成光催化性能更优异的固溶体BiOClxI1−x。如Deng等[11]通过溶剂热法制备了BiOCl0.7I0.3固溶体,且具有良好的光催化活性。Ma 等[12]采用沉淀法合成了新型BiOCl0.9I0.1/β−Bi2O3复合材料,有效促进了光催化反应中的电荷分离,提高了光催化性能。
因此,可通过简单的水浴加热和原位沉淀法将BiOCl0.7I0.3和WO3结合,制备复合光催化剂,并应用于盐酸四环素的降解研究。复合材料形成异质结构,可以抑制电子空穴对复合速率,拓宽可见光吸收范围,从而提高对盐酸四环素的光降解性能。通过自由基捕获试验和电子顺磁共振检测(ESR)明确光催化反应的活性物质,并分析推测出WO3/BiOCl0.7I0.3复合光催化材料的光催化作用机制。
1 材料与方法
1.1 试剂与仪器
1.1.1 试剂
钨酸铵[(NH4)10H2W12O42]、五水硝酸铋[Bi(NO3)3•5H2O]、乙二胺四乙酸二钠(EDTA−2Na),上海麦克林生化科技有限公司;乙二醇(C2H6O2)、异丙醇(IPA),无锡市晶科化工有限公司;碘化钾(KI)、氯化钾(KCl)、对苯醌(BQ),上海阿拉丁生化科技有限公司。以上试剂均为分析纯。盐酸四环素,纯度级别为USP,上海麦克林生化科技有限公司。试验用水为娃哈哈纯净水。
1.1.2 仪器
扫描电子显微镜,Quanta FEG 250 型,美国FEI公司;X射线衍射仪,D8advance型,德国布鲁克;紫外可见分光光度计,TU−1900型,北京普析通用仪器有限责任公司;傅里叶红外光谱仪,Thermo Nicolet Is5型,美国Thermo公司;X射线光电子能谱仪,Escalab 250xi 型,美国Thermo 公司;紫外可见漫反射光谱仪,UV3600 型,日本岛津;电子顺磁共振光谱仪,Bruker A3000 型,德国布鲁克。
1.2 光催化材料的制备
1.2.1 WO3的制备
称取5g 钨酸铵固体置于陶制坩埚内,转移至气氛炉中以10℃/min 的升温速度升至520℃,于520℃下煅烧2h,继续以10℃/min 的升温速度升温至540℃煅烧2h。冷却至室温后,取出研磨得到淡黄色粉末状WO3。
1.2.2 WO3/BiOCl0.7I0.3复合材料及BiOCl0.7I0.3的制备
采用水浴加热和原位沉淀法制备BiOCl0.7I0.3和WO3/BiOCl0.7I0.3。称取0.01mol 的五水合硝酸铋加入10mL 的乙二醇中,在90℃水浴条件下搅拌溶解至透明,记为A 溶液。称取不同物质的量的WO3(0.5mmoL、0.67mmoL、1.0mmoL、2.0mmoL)置于烧杯中,加入10mL 去离子水搅拌后超声形成分散液,记为B 溶液。称取7mmoL 氯化钾和3mmoL 碘化钾置于烧杯中,加入40mL 去离子水,搅拌至完全溶解,记为C溶液。在90℃水浴条件下,将C液滴加入A 液中,并持续搅拌30min。随后,在持续搅拌的条件下,将B液滴加入上述溶液中,并于滴加完成后继续搅拌60min。冷却至室温后抽滤,于60℃下真空干燥12h,得到不同摩尔比的BW(20∶1、15∶1、10∶1、5∶1)复合材料,记为BW−x(其中x为BW 复合材料中BiOCl0.7I0.3的含量)。在相同条件下,不添加WO3制备得到BiOCl0.7I0.3单体。
1.3 光催化材料的表征
利用X 射线衍射(X−ray diffraction,XRD)对材料的晶型、物相组成进行分析,扫描区段10°~80°;通过傅里叶变换红外光谱(Fourier transform infrared spectrometer,FTIR) 分析材料的化学组成、化学键;扫描电子显微镜(scanning electron microscope,SEM)用于观察样品的微观形貌;X射线 能 谱(X−ray photoelectron spectroscopy,XPS)可以表征样品的元素组成和价态;紫外可见漫反射光谱(UV−Vis diffuse reflection spectrum,UV−Vis DRS)可以研究样品的光学吸收性能,并将其与XPS结合,从而对材料禁带宽度进行分析;电子自旋共振(electron spin−resonance,ESR)用于测定样品在光催化降解过程中产生的自由基种类。
1.4 光催化降解试验
以氙灯(300W)模拟可见光源,同时加载420nm 滤光片,以100mL 的盐酸四环素溶液(20mg/L)为目标污染物,进行光催化降解试验。将磁性转子和0.1g光催化材料投加进盐酸四环素溶液,并转移到光催化反应装置中,在黑暗状态下持续搅拌30min以达吸附平衡。然后打开模拟光源进行光催化反应,在反应期间每隔10min用注射器取3mL 反应样,随后经0.22μm 的尼龙滤膜过滤,并将滤液转移到离心管中待测。采用紫外分光光度法(λ=357nm)对盐酸四环素溶液样品进行测定。
1.5 自由基捕获试验
以乙二胺四乙酸二钠(EDTA−2Na)、异丙醇(IPA)、对苯醌(BQ)分别作为空穴(h+)、羟基自由基(•OH)、超氧自由基(•O2−)的捕获剂[13],在光催化降解盐酸四环素试验中,投加催化剂后再分别加入1mmol 的EDTA−2Na、IPA、BQ,其他条件不变,测定在加入不同捕获剂后溶液中盐酸四环素浓度随时间的变化情况。
2 结果与讨论
2.1 光催化材料的表征
2.1.1 XRD分析
采用XRD 对材料的晶型和物相结构进行分析(图1)。在2θ为10°~80°范围内,制备的WO3样品在23.143°、23.623°、24.403°、33.285°、34.205°、41.666°、49.967°、55.868°处出现了明显的衍射峰,分别对应于纯WO3的(002)、(020)、(200)、(022)、(202)、(222)、(140)、(420)晶面,这与单斜相WO3(JCPDS No.43−1035)标准卡片基本吻合[14]。将制备的BiOCl0.7I0.3光催化材料的XRD 衍射图谱与BiOCl (JCPDS No.06−0249) 以 及BiOI (JCPDS No.10−0445) 标准卡片进行对照[15],可以看出BiOCl0.7I0.3样品在11.417°、25.821°、32.610°、33.259°、40.934°、46.837°、54.216°、58.526°和68.266°处出现了明显的衍射峰,分别对应(001)、(101)、(110)、(102)、(112)、(200)、(211)、(212)和(220)晶面,说明了BiOCl0.7I0.3固溶体的合成[16]。在BW−15样品材料的XRD 图谱中,可以较为明显地观察到BiOCl0.7I0.3的衍射峰,且在2θ为23.119°、23.596°、24.373°处可以观察到WO3的三个优势衍射峰,分别对应于WO3的(002)、(020)、(200)晶面,但其中WO3的特征衍射峰的强度较弱,推测可能是由于复合材料中WO3的含量较低所致。与此同时,BW−15 图谱中基本未观察到杂质峰,表明制备的样品具有较高的纯度。

图1 WO3、BiOCl0.7I0.3及BW−15光催化剂的XRD图谱
2.1.2 FTIR分析
对所制备的BiOCl0.7I0.3、WO3和BW−15 光催化材料进行傅里叶红外光谱分析(图2)。在波长1382cm−1处明显观察到一个强特征峰,这是由Bi—Cl的不对称伸缩振动产生的[17]。535cm−1处的特征峰由Bi—O伸缩振动产生[18],而位于838cm−1处的特征峰是I—O 伸缩振动产生的[19]。在波数为837cm−1处有一个强特征峰,这是由WO3晶体中O—W—O 键的伸缩振动导致的[20],但由于复合材料中WO3的含量较低,因此在BW−15 的谱图上这个特征峰较为不明显。以1616cm−1为中心的特征峰是H—O—H键的弯曲振动产生的,而以3428cm−1为中心的宽透射带是由O—H基团的伸缩振动所致,这两种特征峰由材料的吸附水所产生[21]。以上分析可与XRD 的分析结果相互印证。
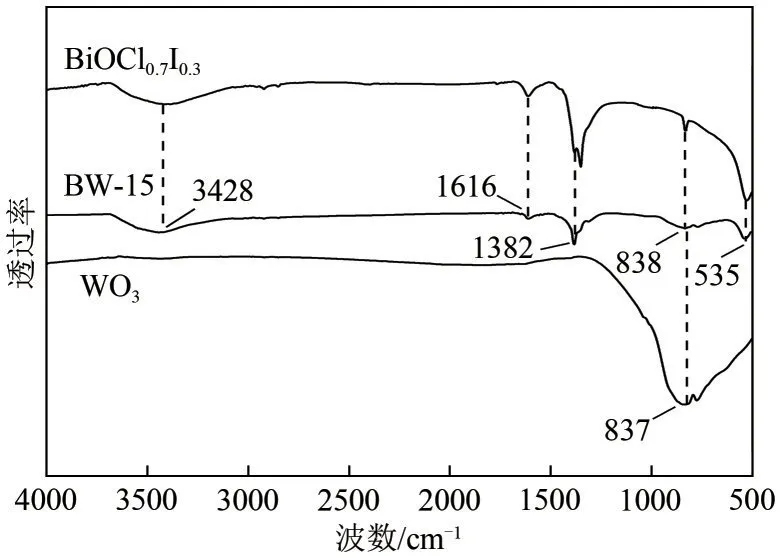
图2 WO3、BiOCl0.7I0.3及BW−15光催化剂的FTIR图谱
2.1.3 扫描电子显微镜分析
借助扫描电镜观察BiOCl0.7I0.3和WO3/BiOCl0.7I0.3复合材料的表面微观形貌。BiOCl0.7I0.3固溶体在不同放大倍数下呈现出由大量纳米薄片组成的花状[图3(a)~(c)],尺寸为1~2μm,同时也可以看出沉淀法制备的BiOCl0.7I0.3存在团聚现象,分散性较差。在WO3/BiOCl0.7I0.3复合材料的电镜图[图3(d)]中未观察到较为明显的WO3,但观察到BiOCl0.7I0.3团聚呈大小不一的块状分布。由于扫描电镜只能观测到材料的表观形态,而无法观测到材料的内部形态,且由XRD 和FTIR 的分析结果已经证实了材料中WO3的存在,因此推测可能是因为BiOCl0.7I0.3密集附着生长在了WO3的表面,且复合材料中WO3的含量较少,被BiOCl0.7I0.3掩盖在了内部所致。

图3 不同光催化剂的SEM图谱
2.1.4 X射线能谱分析
通过对BW−15 的全范围XPS 扫描谱图[图4(a)]进行分析,研究了制备的复合光催化材料BW−15的元素组成和化学状态。由图中可以清晰地看到Bi、Cl、I、O、W 五种元素均存在于BW−15 复合材料中,这与XRD以及FTIR光谱的显示结果可以互为佐证。
通过对XPS精细谱进行分析,可以研究光催化材料的各元素价态和成键情况。图4(b)是Bi 4f光谱图,从图中可以看出Bi 4f5/2和Bi 4f7/2轨道可以拟合两个峰,两个主峰分别对应的结合能为164.90eV和159.60eV,表明材料中的Bi 是以Bi3+的形式存在[22]。图4(c)是Cl 2p高分辨率光谱,以198.30eV和199.90eV 的结合能为中心的峰分别属于Cl 2p3/2和Cl 2p1/2自旋轨道能级,表明元素Cl 是以Cl−形式呈现[23]。
O 1s的精细谱如图4(d)所示,可知O 1s谱图中有三个拟合峰,分别在532.50eV、531.15eV 和530.25eV结合能处,分别对应于W—O键、吸附在样品表面的—OH和[Bi2O2]2+晶格中的Bi—O键[24−25]。
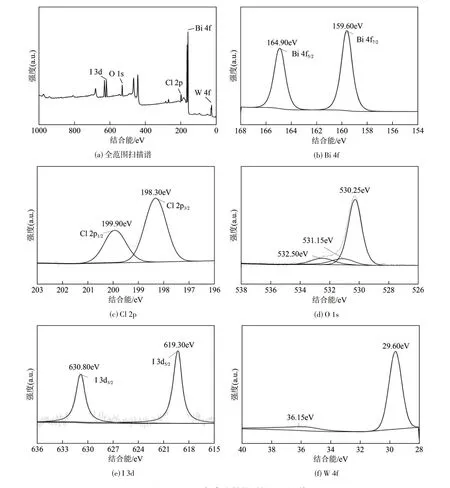
图4 BW−15复合光催化剂的XPS图谱
在I 3d的XPS光谱图[图4(e)]中可以清晰地观察到两个拟合峰,分别位于630.80eV 和619.30eV,这两个峰是独立的峰,分别归属于I 3d3/2和I 3d5/2自旋轨道,其中630.80eV 对应I3−,619.30eV 对 应I−[25]。W 4f的高分辨率光谱如图4(f)所示,结合能峰位于29.60eV和36.15eV,结合能峰分别对应W 4f7/2和W 4f5/2自旋轨道[26],表明W元素以W6+形态呈现。
2.1.5 紫外可见漫反射吸收光谱分析
光催化材料的光吸收范围是评价光催化性能的重要指标。图5(a)所示为UV−Vis DRS光谱图,WO3单体最大的吸收波长为483nm,BiOCl0.7I0.3单体的最大的吸收波长为508nm,表明两者均能吸收可见光。BW−15 复合材料相较于两种单体材料最大吸收边更宽一些,为558nm。说明BiOCl0.7I0.3和WO3两种材料的复合拓宽了光催化剂的可见光吸收范围,增强了可见光响应能力,能够产生更多的活性物质,具有更高的光催化活性[27]。
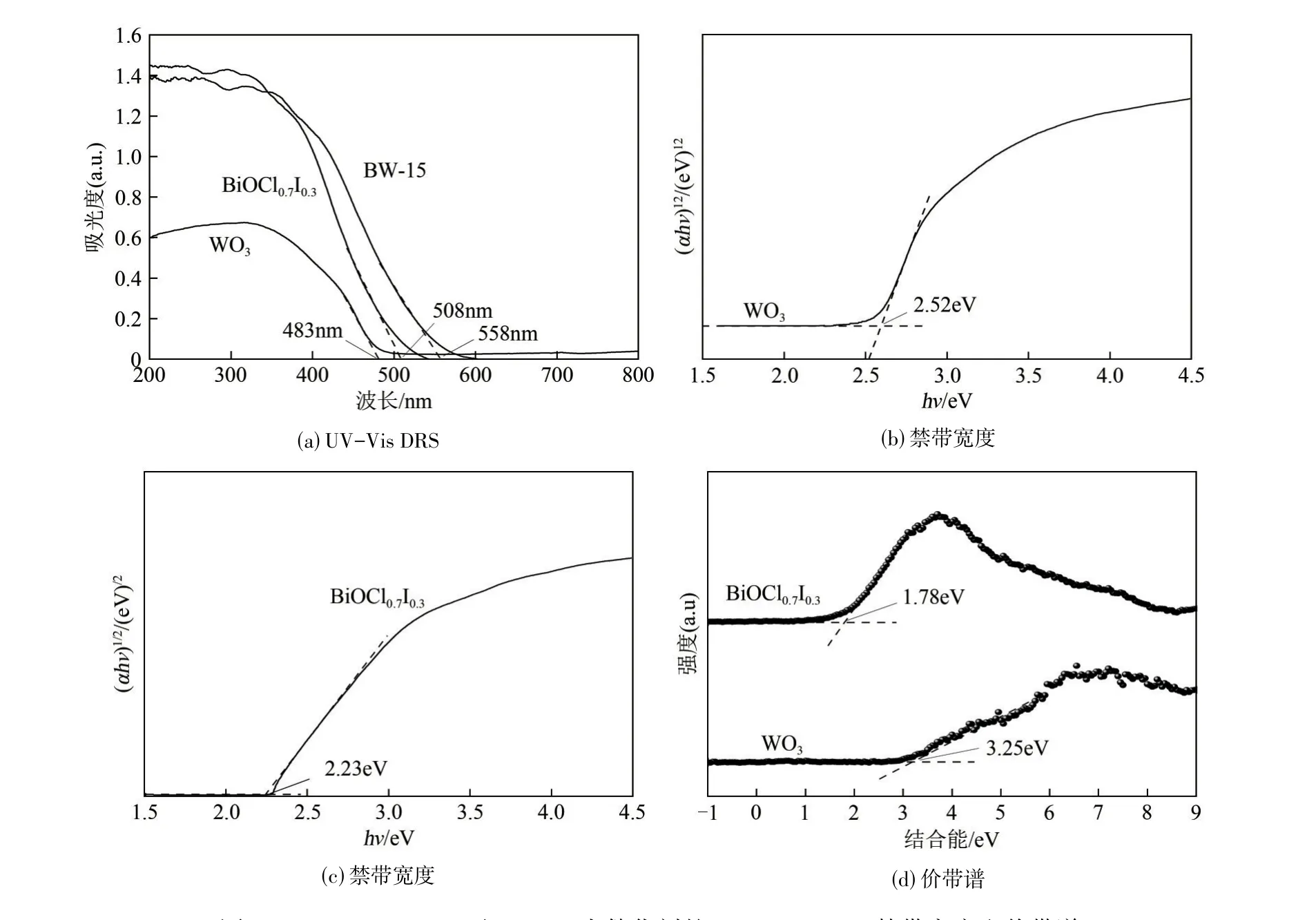
图5 WO3、BiOCl0.7I0.3及BW−15光催化剂的UV−Vis DRS、禁带宽度和价带谱
BiOCl0.7I0.3和WO3均为间接带隙半导体[27−28],其禁带宽度(Eg)可通过式(1)计算。
式中,α、h、ν、A、Eg分别代表吸收系数、普朗克常量、光频率、常数和禁带宽度。
半导体的跃迁特性分为两种,即直接跃迁和间接跃迁。其中前者n=1,后者n=4。由于BiOCl0.7I0.3和WO3均为间接跃迁的半导体,因此指数n均取4。以(αhν)1/2为纵坐标(Y)、hν为横坐标(X)作图,曲线的切线在X轴上的截距即为禁带宽度,如图5(b)、(c)所示。图中清晰地显示了WO3和BiOCl0.7I0.3的禁带宽度分别为2.52eV和2.23eV。
BiOCl0.7I0.3和WO3的XPS 价带谱如图5(d)所示。利用XPS 价带谱确定了BiOCl0.7I0.3的EVB=1.78eV,WO3的EVB=3.25eV。WO3和BiOCl0.7I0.3的ECB的位置可利用式(2)计算。
式中,ECB、Eg、EVB分别表示导带电位、禁带宽度、价带电位。
由计算可以得出,BiOCl0.7I0.3和WO3的ECB分别为−0.45eV和+0.73eV。
2.2 光催化剂活性及稳定性
2.2.1 WO3/BiOCl0.7I0.3对盐酸四环素的光催化降解
以盐酸四环素为目标污染物,以不投加任何光催化剂的100mL 盐酸四环素溶液(20mg/L)作为空白组对照,来测定所制备的WO3、BiOCl0.7I0.3以及不同配比BW−x复合光催化材料的性能。由图6(a)可以看出,空白组的盐酸四环素溶液浓度一直保持在比较恒定的状态,表明盐酸四环素具有一定的稳定性。其余几组在经过30min的暗吸附阶段后,均对盐酸四环素有一定程度的吸附去除效果,其中BW−x复合材料的吸附能力均高于单一的WO3和BiOCl0.7I0.3,可能是因为BW−x复合材料较单体材料的比表面积有所增大,更有利于吸附污染物。在光降解阶段,图6(a)中能清晰地看到BW−x复合光催化材料对盐酸四环素的降解能力均高于单一的WO3(34.37%)和BiOCl0.7I0.3(69.83%),其中BW−15 对盐酸四环素的降解率最高,达到93.84%。
光催化降解盐酸四环素符合一级反应动力学,可以利用式(3)对试验数据进行拟合[29]。
式中,C0为目标污染物盐酸四环素的初始浓度,mg/L;t为光照时间,min;Ct为t时刻溶液中盐酸四环素的浓度,mg/L;k为反应速率常数。
不同光催化剂降解盐酸四环素的伪一级动力学模型如图6(b)所示。BW−15 的反应速率常数为0.02391min−1,远远大于单一的BiOCl0.7I0.3(0.00963min−1)和WO3(0.00216min−1),是BiOCl0.7I0.3的2.47 倍、WO3的11 倍。图中清晰地显示了BW−5、BW−10、BW−20 的k值分别为0.01205min−1、0.02164min−1、0.01998min−1,均低于BW−15,由此可以看出复合材料BW−15的光催化性能最好。
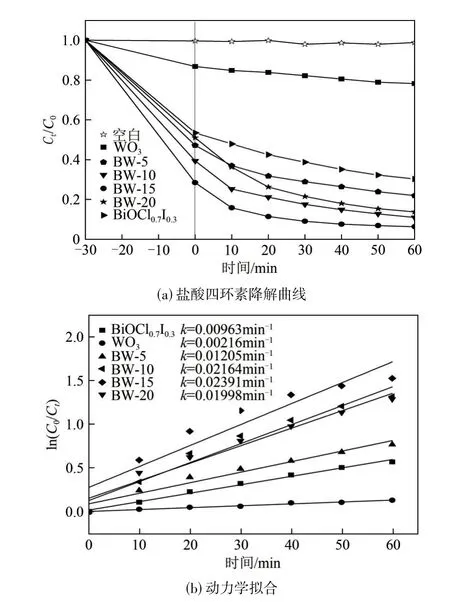
图6 不同光催化剂对盐酸四环素的降解及动力学拟合
由以上分析可以看出,将适量WO3与BiOCl0.7I0.3复合后能够显著提高光催化能力,且复合材料中组成相的比例会影响复合材料的光催化性能,WO3的含量过少会影响材料的电子转移能力,含量过多会产生屏蔽效应[30]。
2.2.2 矿化试验
为进一步评估所制备催化剂的光降解性能,在进行光催化降解盐酸四环素试验的同时进行了矿化试验,矿化试验采用TOC分析仪进行测定[30]。光降解1h 后,BW−15 复合材料对盐酸四环素的矿化率为83.27%,略低于光催化降解率,如图7所示。这是由于光降解盐酸四环素后,溶液中部分中间产物没有完全矿化,但相较于WO3(18.92%)和BiOCl0.7I0.3(55.64%)的矿化率依旧有显著提高。

图7 WO3、BiOCl0.7I0.3及BW−15光催化剂的矿化试验
2.2.3 循环试验
为了探究制备光催化剂的稳定性和可重复性,对BW−15 进行多次循环试验。如图8 所示,在进行了4次光降解盐酸四环素的试验后,BW−15的光降解率下降了13.85%,这可能是由于每次试验后回收样品均会有部分损耗所致。但尽管如此,4次循环试验后,其对盐酸四环素的去除率仍能达到79.99%,这表明BW−15 复合材料具有良好的稳定性。
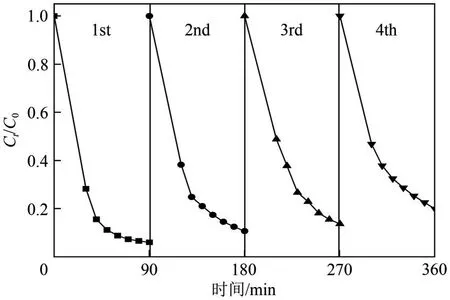
图8 BW−15复合光催化剂的循环试验
2.3 自由基捕获试验
采用EDTA−2Na、IPA、BQ分别作为h+、•OH、•的捕获剂[13],进行自由基捕获试验,以明确光催化过程中主要活性物质的种类,探究光催化剂降解盐酸四环素的作用机制。以不添加光催化剂、其余条件均相同的盐酸四环素溶液作为空白组;以加入BW−15 但不添加任何自由基捕获剂的盐酸四环素溶液作为对照组;以在盐酸四环素溶液中分别加入EDTA−2Na、IPA、BQ三种自由基捕获剂作为试验组,进行光催化剂对盐酸四环素的光催化降解试验,光催化时间为60min。如图9 所示,在目标污染物的溶液中分别加入三种不同的自由基捕获剂后,光催化剂对盐酸四环素的降解率均有不同程度的下降。在加入EDTA−2Na 后,降解率由93.84%降至24.50%,下降了约3.8 倍;加入BQ 后,盐酸四环素的降解率降至56.30%,比对照组降低了37.54%;在加入IPA 后,降解率降至80.7%。因此,光催化降解过程中活性基团的影响程度为:h+>•O2−>•OH。其中h+和•O2−为该光催化反应中的主要活性物质。
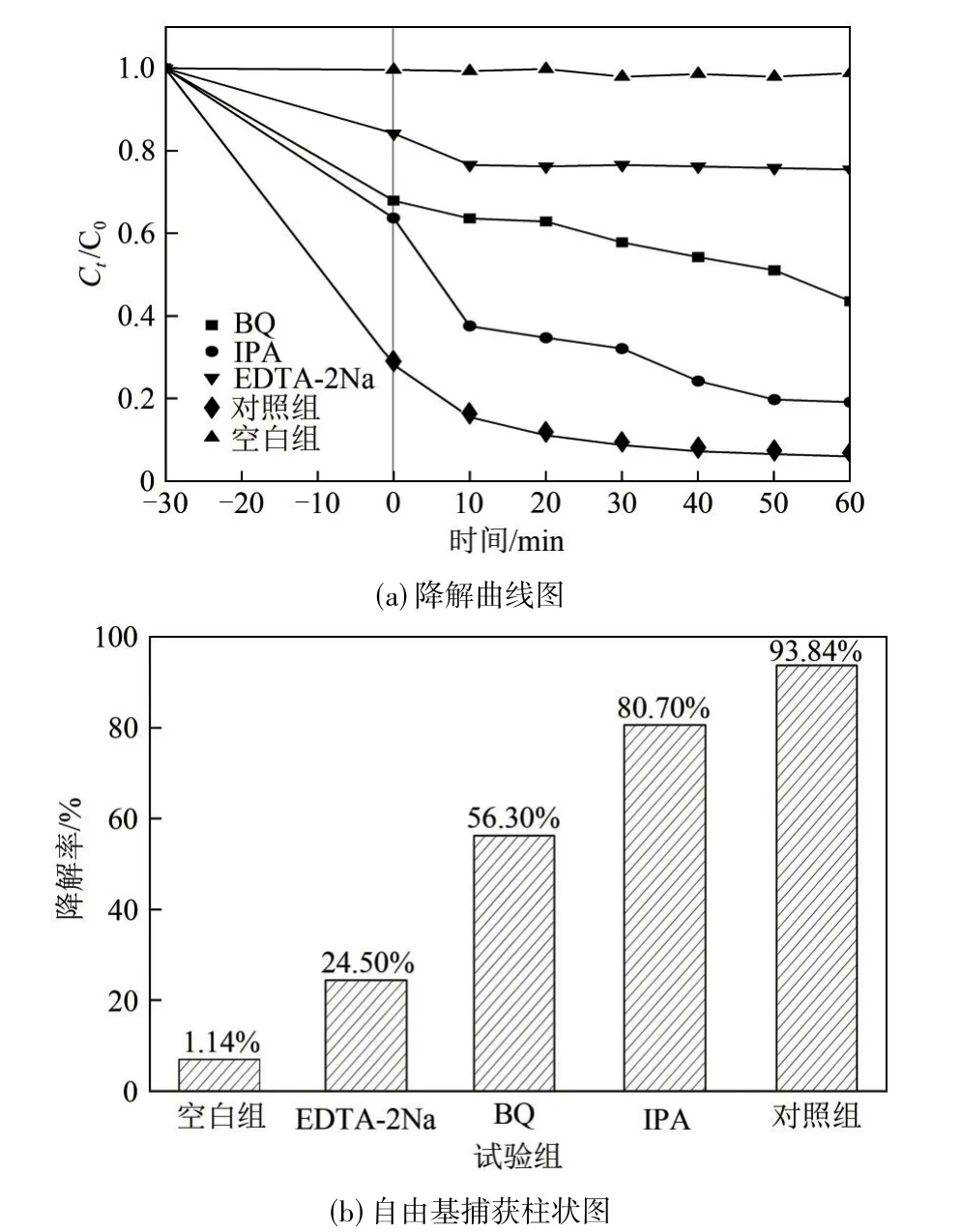
图9 加入EDTA−2Na、IPA及BQ不同自由基捕获剂后盐酸四环素的降解
2.4 电子自旋共振光谱分析
光催化过程中,光照激发产生光生电子,光生电子与空穴完全分离时称为光生载流子,参与电子转移的氧化还原反应,•OH或•O2−是光催化氧化反应过程中的重要活性物质,光生载流子参与•OH或•的生成过程,载流子的存在与否以及浓度大小可由ESR 信号的强弱判断[31]。•O2−的ESR 的特征强度比为1∶1∶1∶1,如图10(a)所示;•OH 的ESR 特征强度比为1∶2∶2∶1,如图10(b)所示。由ESR图谱可以看出,在黑暗条件下•OH和•O2−均未产生明显的ESR 信号,可见光照射3min 后,两者均产生了较为明显的特征峰信号。•O2−的信号强度较•OH 明显更强,说明BW−15 复合材料光激发所产生的•O2−浓度高于•OH。这一结果与自由基捕获试验相符合。
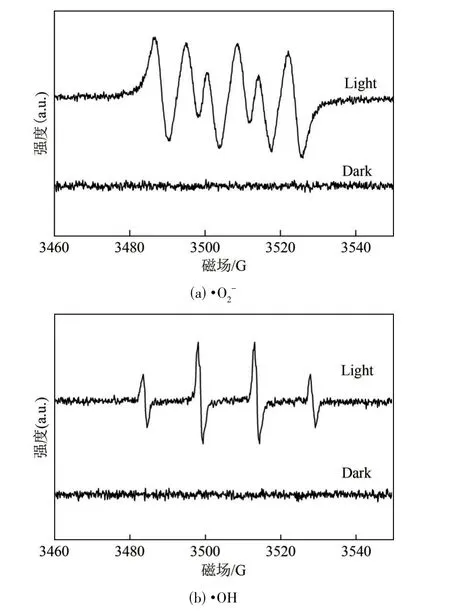
图10 BW−15复合光催化剂的ESR光谱
2.5 光催化机理分析
由UV−Vis DRS 以及XPS 价带谱分析计算,可以得出制备的BiOCl0.7I0.3和WO3的导带和价带电位,其中BiOCl0.7I0.3的价带电位EVB为1.78eV,导带电位ECB为−0.45eV,导带电位相较于O2/•O2−(−0.33eVvs. NHE)的更负,因此BiOCl0.7I0.3导带上的光生电子可以将吸附在材料表面的O2还原为•O2−[32]。WO3的价带电位EVB为3.25eV,导带电位ECB为0.73eV。对于WO3来说,其价带电位比•OH/H2O(2.4eVvs.NHE)的更正,因此WO3价带上的空穴可以将H2O氧化为•OH[33]。
基于以上分析,WO3/BiOCl0.7I0.3复合材料可能的光催化机制如图11 所示,WO3和BiOCl0.7I0.3构成了Z型光催化结构。可见光下,BiOCl0.7I0.3和WO3价带上的电子受到光照激发跃迁至导带,形成光生电子空穴对,在内部电场作用下,WO3导带上的电子转移至BiOCl0.7I0.3价带上,同其上的光生电子一样跃迁至BiOCl0.7I0.3的导带上,并在其上累积。反应式见式(4)~式(6)。

图11 WO3/BiOCl0.7I0.3复合光催化材料的光催化机制
此时,由于BiOCl0.7I0.3和WO3产生的光生电子都累积在BiOCl0.7I0.3的导带上,有效地分离了电子空穴对,因而提高了材料的光催化活性。BiOCl0.7I0.3导带电位为−0.45eV,比O2/•O2−(−0.33eVvs. NHE)的更负,可以将材料表面吸附的O2还原为•O2−并参与盐酸四环素的降解,这也让电子可以快速清除,使得光催化剂可以产生更多的活性基团。与此同时,WO3的价带电位EVB为3.25eV,比•OH/H2O(2.4eVvs. NHE)的更正,因此WO3价带上由于电子跃迁形成的空穴一部分直接参与光催化反应,另一部分将H2O 氧化为•OH 再参与反应,而BiOCl0.7I0.3价带上的空穴将直接参与光催化降解反应。这与2.3 节中自由基捕获试验结果相符合。反应式见式(7)、式(8)。

h+/•O2−/•OH + 盐酸四环素→降解产物(CO2+ H2O)(9)
3 结论
(1)采用煅烧法、水浴加热和原位沉淀法成功制备了WO3/BiOCl0.7I0.3复合光催化材料。通过XRD、SEM、FTIR、XPS 和UV−Vis DRS 等表征手段对材料进行表征分析,验证了复合材料的成功合成。
(2) WO3/BiOCl0.7I0.3最 佳 掺 杂 比 例 为WO3∶BiOCl0.7I0.3=1∶15(摩尔比),对盐酸四环素的光催化降解效果最优。
(3)通过光降解试验以及循环试验,证明WO3/BiOCl0.7I0.3对盐酸四环素具有良好的光降解能力和稳定性,循环4 次后仍具有较高的光催化性能,表明了该材料具有可循环性。
(4)通过自由基捕获试验和ESR 图谱分析,得出h+和•O2−是光催化过程中主要的活性物质,结合材料禁带宽度和价带谱,分析出WO3/BiOCl0.7I0.3光催化材料Z型异质结构的光催化作用机理。
