基于网络药理学结合动物实验探究芪玄抑甲宁治疗格雷夫斯病的作用机制
2023-02-24高长久柳长凤于栋华刘树民
高长久 丁 崧 卢 芳 柳长凤 于栋华 刘树民
1.黑龙江中医药大学研究生院,黑龙江哈尔滨 150040;2.黑龙江中医药大学中医药研究院,黑龙江哈尔滨 150040
格雷夫斯病(Graves disease,GD)又称毒性弥漫性甲状腺肿,是一种甲状腺器官特异性自身免疫性疾病,其特征是促甲状腺激素受体抗体的产生,导致甲状腺功能亢进[1]。当前,治疗GD 主要有抗甲状腺药物、手术和放射性碘3 种治疗方式[2-3],但存在着复发率高、易伴发甲状腺功能减退等问题[4]。GD 属于中医“瘿病”范畴,甲状腺肿大为中医之“痰凝”。本病初期多为气机郁滞,继而津凝痰聚,痰气搏结颈前。日久引起血脉瘀阻,气、痰、瘀三者常协同为患。随着病情的进展,本病常发生病机转化。如肝气郁结日久可化火,火热内盛,耗气伤阴,导致气阴两虚之候[5]。验方芪玄抑甲宁补气滋阴、清肝降火、化痰散结,广泛应用于临床,并取得良好疗效,其由黄芪、玄参、浙贝母、夏枯草和牡蛎5 味中药组成,前期药效学研究已证实其对GD 有显著改善作用[6-8],但其具体作用机制尚未明确。因此,本研究通过网络药理学预测芪玄抑甲宁治疗GD 的作用机制,并对筛选的部分预测结果进行动物实验验证,以期初步探讨芪玄抑甲宁治疗GD 的作用机制,为其进一步研究奠定基础,为中药防治GD 提供依据。
1 材料与方法
1.1 材料与仪器
1.1.1 实验动物6 周龄SPF 级雌性BALB/c 小鼠,体重(20±2)g,购自北京维通利华实验动物技术有限公司,许可证号SCXK(京)2021-0006。动物于温度20~26℃、湿度40%~60%条件下适应性饲养7 d,自由进食饮水。动物实验在黑龙江中医药大学中医药研究院完成,动物使用许可证号:SYXK(黑)2018-007。动物实验经黑龙江中医药大学伦理委员会批准(2021 061101)。
1.1.2 药品与试剂 芪玄抑甲宁的组方配伍如下,黄芪∶玄参∶牡蛎∶浙贝母∶夏枯草=3∶2∶2∶2∶1(以上饮片均由黑龙江修生堂药业有限公司提供,批号分别为20190401、20190401、20200601、20191101、20190701),按最优工艺提取药物[9],制备成冻干粉备用;甲巯咪唑片(Merck KGaA,批号:C10002097);重组腺病毒Ad-TSHR-289(赛业生物科技有限公司,滴度:3.13×1011PFU/ml);小鼠血管内皮生长因子(vascular endothelial growth factor,VEGF)试剂盒(上海酶联生物科技有限公司,批号:202109);血小板内皮细胞黏附分子-1(plateletendothelial cell adhesion molecule-1,PECAM-1)小鼠单克隆抗体(武汉赛维尔生物科技有限公司,货号:GB12063)。
1.1.3 主要仪器 酶标仪(奥地利安图斯公司,型号:Anthos2010);高速冷冻离心机(安徽科大创新股份有限公司中佳分公司,型号:KDC-160HR);脱水机(DIAPATH,型号:Donatello);包埋机(武汉俊杰电子有限公司,型号:JB-P5);病理切片机(上海徕卡仪器有限公司,型号:RM2016)。
1.2 研究方法
1.2.1 芪玄抑甲宁活性成分及其靶点的获取 运用中药系统药理学数据库与分析平台和化学专业数据库收集芪玄抑甲宁中5 味中药黄芪、玄参、夏枯草、浙贝母和牡蛎的化学成分,通过口服生物利用度≥30%,类药性≥0.18 筛选活性成分及其靶点[10]。
1.2.2 GD 相关靶点的获取 运用GeneCards、在线人类孟德尔遗传数据库、DisGeNET、靶点数据库和DrugBank检索“Graves’disease”,合并去重得到GD 相关靶点。
1.2.3 蛋白质-蛋白质相互作用(protein-protein interaction,PPI)网络的构建与核心靶点的筛选将芪玄抑甲宁相关靶点与GD 相关靶点取交集并绘制维恩图,将共有靶点导入STRING 平台构建PPI 网络,选择度值>2 倍中位数的靶点作为核心靶点。
1.2.4 芪玄抑甲宁-活性成分-靶点网络的构建及核心成分的筛选 将药物、活性成分、靶点导入Cytoscape得到“芪玄抑甲宁-活性成分-靶点”网络图,选择度值>2 倍中位数的活性成分作为核心成分。
1.2.5 GO 富集分析和KEGG 通路富集分析 将核心靶点导入Metascape 平台,进行GO 和KEGG 富集分析。
1.2.6 芪玄抑甲宁对GD 小鼠甲状腺血管新生的影响前期实验结果表明,芪玄抑甲宁对GD 模型小鼠的外观行为、甲状腺组织病理形态具有改善作用,并对血清中甲状腺素、促甲状腺激素受体抗体有回调作用,且高剂量组最显著。本研究以前期实验的高剂量组作为给药组,选取网络药理学所预测抑制血管新生方面的机制进行验证[8]。
1.2.7 动物分组与给药 选取6 周龄SPF 级体重(20±2)g的雌性BALB/c 小鼠40 只,其中10 只设为正常对照组,其余30 只应用重组腺病毒Ad-TSHR-289 于小鼠胫前肌注射免疫构建GD 模型,免疫剂量为1.878×109PFU/60 μl,于1、4、7 周共免疫3 次[11-12]。第10 周采用随机数字表法将造模成功的小鼠分为GD 模型组、甲巯咪唑组、芪玄抑甲宁组,每组8 只。芪玄抑甲宁组灌胃芪玄抑甲宁50 g/kg,甲巯咪唑组灌胃甲巯咪唑片3.75 mg/kg,正常对照组、GD 模型组灌胃同体积的饮用水,1 次/d,连续4 周。
1.2.8 芪玄抑甲宁对四组血清VEGF 的影响 给药4 周后,将四组以0.3%戊巴比妥钠(40 mg/kg)进行麻醉,于各组颌下静脉丛采取静脉血,取上清后采用酶联免疫吸附试验检测四组血清中VEGF 含量,具体操作按照试剂盒说明书进行,并经酶标仪检测450 nm 波长时的光密度值。
1.2.9 芪玄抑甲宁对GD 小鼠甲状腺组织PECAM-1 的影响 对四组甲状腺组织采用免疫组织化学法检测PECAM-1 水平,PECAM-1 水平可反映微血管密度。按照石蜡切片免疫组化法将四组甲状腺组织制成中性树胶封片,显微镜下观察染色情况,依照Weidner 标准,每张随机选取5 个不重叠、不相邻的视野,400 倍镜下观察,计算每个视野的PECAM-1 水平[13]。
1.3 统计学方法
采用GraphPad Prism 7 对所得数据进行统计学分析。计量资料采用均数±标准差()表示,比较采用t 检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 芪玄抑甲宁活性成分及其靶点
共获得芪玄抑甲宁的活性成分63 种,靶点281 个。见图1。

图1 芪玄抑甲宁活性成分相关信息
2.2 GD 相关靶点及PPI 网络与核心靶点
共获得GD 相关靶点1 489 个,芪玄抑甲宁与GD共有靶点为124 个,见图2。PPI 获得111 个潜在靶点,其中核心靶点有信号转导和转录激活因子3、丝氨酸/苏氨酸蛋白激酶1、VEGFA 等21 个,见图3。

图2 芪玄抑甲宁相关靶点与格雷夫斯病相关靶点维恩图

图3 芪玄抑甲宁与格雷夫斯病共有靶点的蛋白质-蛋白质相互作用网络
2.3 芪玄抑甲宁-活性成分-靶点网络及核心成分
筛选与潜在靶点对应的活性成分,将其与5 味中药及靶点导入Cytoscape 软件得到“芪玄抑甲宁-活性成分-靶点”网络图,经筛选得到槲皮素、山柰酚、木犀草素、熊果酸、β-谷甾醇等18 种核心成分。见图4。
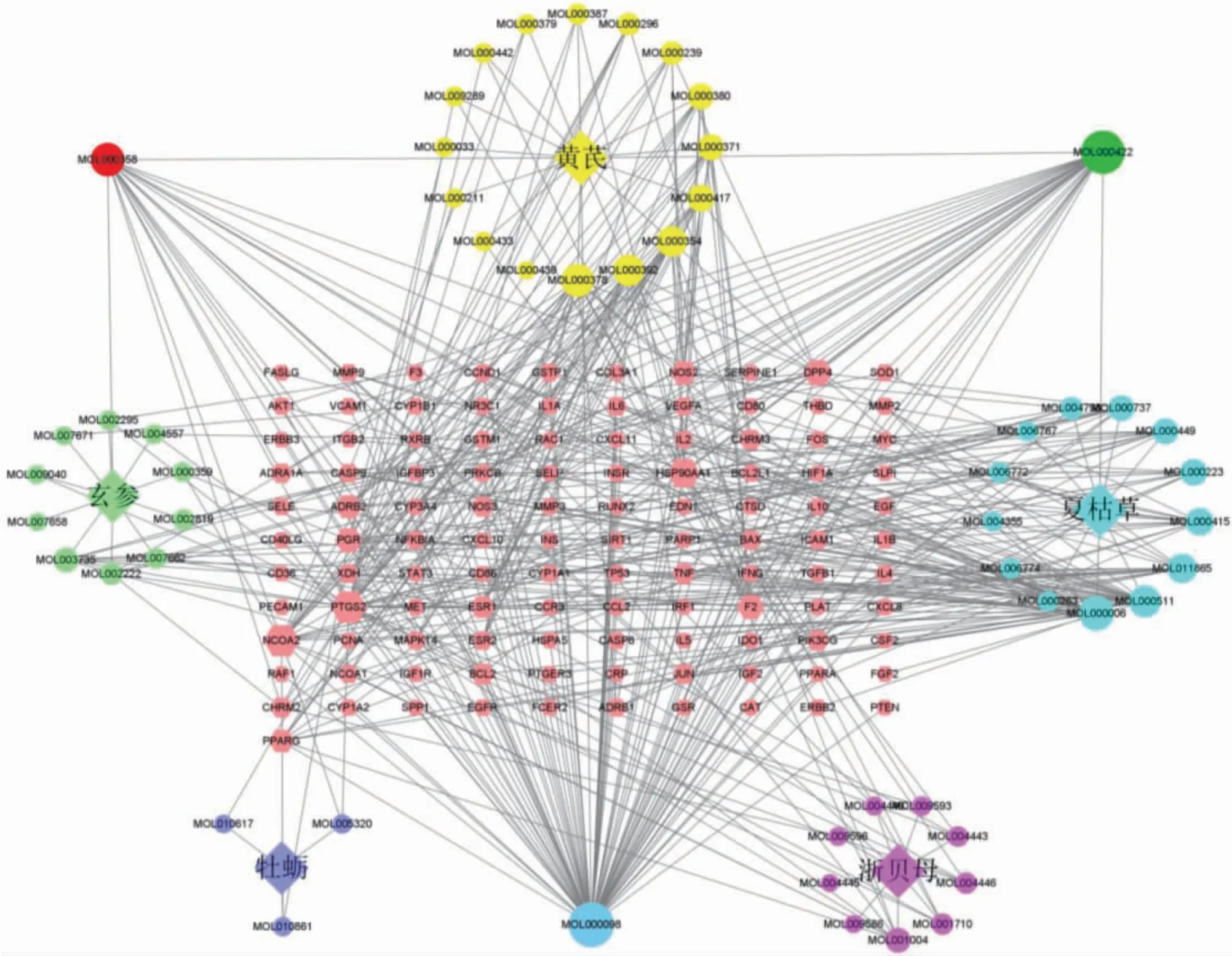
图4 芪玄抑甲宁-活性成分-靶点网络
2.4 GO 富集分析和KEGG 通路富集分析
GO 富集分析获得炎症反应、血管新生、血管形态发生、一氧化氮合酶调节活性等954 项,见图5。KEGG富集分析获得MAPK、PI3K/Akt、IL-17、VEGF 等92 条信号通路,见图6。

图5 芪玄抑甲宁治疗格雷夫斯病核心靶点的GO 富集分析

图6 芪玄抑甲宁治疗格雷夫斯病核心靶点的KEGG富集分析
2.5 四组血清VEGF 水平比较
GD 模型组血清VEGF 水平高于正常对照组,且芪玄抑甲宁组VEGF 水平低于GD 模型组,差异有高度统计学意义(P<0.01)。见图7。

图7 四组血清VEGF 水平比较
2.6 四组甲状腺组织的PECAM-1 水平比较
GD 模型组血清PECAM-1 水平高于正常对照组,且芪玄抑甲宁组PECAM-1 水平低于GD 模型组,差异有高度统计学意义(P<0.01)。见图8。

图8 四组甲状腺组织的PECAM-1 水平比较
3 讨论
网络药理学从多维角度预测中药及复方与疾病之间的相互作用关系,从而预测药物治疗疾病的作用机制,现广泛应用于中医药前中期研究工作中[14-15]。本研究通过网络药理学构建了PPI 网络、“芪玄抑甲宁-活性成分-靶点”网络、GO 和KEGG 富集分析,将核心成分、核心靶点、功能和信号通路相关联整合,揭示了芪玄抑甲宁治疗GD 的作用机制主要集中在以下两个方面。
血管新生方面,抑制甲状腺血管新生可以缩小GD 甲状腺体积、降低甲状腺激素水平[16]。核心成分山柰酚能抑制血管新生,用于包括癌症在内的许多严重疾病[17],其通过靶向VEGF 受体2 调控VEGF 刺激的人脐静脉内皮细胞中的MAPK 和PI3K/AKT 信号通路来抑制血管新生[18-19]。同时,核心成分槲皮素、熊果酸也具有抑制血管新生的作用[20]。提示芪玄抑甲宁可能通过山柰酚、槲皮素、熊果酸等成分调控VEGF受体2、MAPK 和PI3K/AKT 信号通路抑制甲状腺的血管新生。本研究通过检测VEGF、PECAM-1 的表达情况,提示芪玄抑甲宁可能通过降低GD 小鼠的VEGF水平,抑制甲状腺血管翳的新生来治疗GD。
甲状腺功能方面,GD 以甲状腺弥漫性肿大和分泌功能亢进为主要特征[21]。其核心成分槲皮素能显著降低高脂膳食小鼠血清甲状腺素水平,通过MAPK、甲状腺激素合成通路预防和逆转甲状腺激素代谢紊乱[22-23];山柰酚作为竞争性甲状腺过氧化物酶抑制剂[24],可抑制甲状腺激素的合成。有研究显示,富含山柰酚和槲皮素的海藻石莼提取物可显著降低甲亢大鼠血清T3、T4和促炎性细胞因子的水平[25]。提示芪玄抑甲宁可能通过山柰酚和槲皮素等成分调控MAPK信号通路或抑制甲状腺激素的合成,从而减轻甲状腺功能亢进的症状。
综上所述,本研究所得核心成分、靶点及信号通路与GD 的治疗密切相关,发现了槲皮素、山柰酚、熊果酸等潜在活性成分,以及信号转导和转录激活因子3、丝氨酸/苏氨酸蛋白激酶1、VEGFA 等核心靶点,提示芪玄抑甲宁可能通过调控MAPK、PI3K/AKT 和VEGF等信号通路产生抑制血管新生等作用治疗GD。然而芪玄抑甲宁治疗GD 的作用机制仍需大量的体内外实验进行阐明,本研究结果可为进一步深入探讨其作用机制奠定基础。
