普洱茶-硒掺杂碳量子点和单质硒的同时制备及其在Fe3+检测中的应用
2023-02-20胡伟英叶锡光陈忠正张媛媛姚向荣林晓蓉
胡伟英,叶锡光,陈忠正,张媛媛,姚向荣,林晓蓉,李 斌
(华南农业大学食品学院,广东广州 510642)
碳量子点(CQDs)是一类粒径小于激子波尔粒径的新型碳基荧光材料[1],具有材料来源广,毒性低,水溶性和生物相容性好,荧光强度和光催化活性高等优良特性,广泛应用于半导体、生物医学和分析检测等领域[2−5]。
纳米硒是粒径为1~100 nm 的无定型红色零价单质硒,比无机硒和有机硒具有更高的抗氧化、抗癌活性和更低的毒性[6−8];但受热不稳定,易转变为热力学稳定的灰黑色三方晶系t-Se 而失去活性[9]。
CQDs 的合成方法目前主要有化学氧化法、微波法和水热法等[10−12],其中,水热法因操作简单,成本低,成为CQDs 合成的主要方法。已有研究发现,单纯碳源合成的CQDs,荧光强度和表面活性低,而通过杂原子掺杂或表面钝化等表面修饰[13],不仅可调控CQDs 的光致发光特性,更能提供CQDs 与其他物质相互作用的活性位点,促进传感和催化过程[14]。目前已有铜[15]、氮[16]、磷[17]、硫[18]、硒[19]等元素掺杂成功制备出CQDs 的报道。硒原子作为杂原子掺杂CQDs,不仅可调控其荧光性能,提高其荧光量子产率,还可强化或赋予CQDs 功能活性[20−21]。
本团队前期采用软模板法,以绿茶、普洱茶等六大茶类水提取物和纳米聚集体、茶多糖、茶褐素等为软模板,成功制备出稳定性高、抗氧化和抗癌活性强的茶-纳米硒,其中以普洱茶稳定效果最佳[22−24]。在普洱茶-纳米硒制备过程中,生成的普洱茶-硒原子具备作为杂原子、对CQDs 进行表面修饰的巨大潜质;同时,升高水浴反应温度,可促使无定型红色纳米硒转变为晶态的灰黑色三方晶系t-Se[25]。为此,本研究探讨在普洱茶-纳米硒制备的基础上,以过量的维生素C(VC)作为还原剂和碳源,以普洱茶稳定的纳米硒作为硒源,通过改变水浴加热的温度和时间,同时制备PT-Se-CQDs 和单质硒。以PT-Se-CQDs 为荧光探针,构建荧光传感器检测Fe3+,应用于纯净水和矿泉水样品中Fe3+含量测定,以建立一种高选择性和灵敏度的快速检测方法,应用于环境中Fe3+等的快速监测。
1 材料与方法
1.1 材料与仪器
普洱茶 广东省茶叶进出口公司提供,按GB/T 8303-2013《茶-磨碎试样的制备及其干物质含量测定》磨碎干茶,筛分过20~30 目,备用;亚硒酸钠(Na2SeO3) Sigma-Aldrich 公司;抗坏血酸(VC)北京普博欣生物科技有限责任公司;硫酸奎宁 上海阿拉丁生化科技有限公司;氯化钠(NaCl)、氯化镁(MgCl2)、硝酸铅(Pb(NO3)2)、硫酸亚铁(FeSO4)广东广试试剂科技有限公司;氯化钙(CaCl2)、氯化镉(CdCl2)、氯化钡(BaCl2) 天津市科密欧化学试剂有限公司;氯化镍(NiCl2)、氯化钴(CoCl2)、氯化锶(SrCl2)、氯化锌(ZnCl2)、氯化铁(FeCl3)、硝酸铬(CrNO3) 天津大茂化学试剂厂;硫酸锰(MnSO4)广东台山粤侨试剂塑料有限公司;上述使用的化学试剂均为分析纯等级以上;农夫山泉矿泉水、纯悦纯净水 超市购入。
Milli-Q Integral 3 纯水机 德国Merck-Millipore公司;AL204 电子分析天平 梅特勒托利多仪器有限公司;HWS-24 电热恒温水浴锅 上海一恒科学仪器有限公司;Centrifuge 5804R 冷冻高速离心机 德国Eppendorf 公司;Alpha 1-2 LD plus 冷冻干燥机德国Martin Christ 公司;CRT970 荧光分光光度计上海仪电分析仪器公司;UV-2102C 紫外-可见分光光度计 上海尤尼科有限公司;HITACHIU-2900 双光束紫外分光光度计 日立高新技术公司;JEM 2100F 场发射透射电镜 日本JEOL 公司;Thermo Scientific Escalab 250Xi X 射线光电子能谱 美国赛默飞世尔公司;Ulitma IV X 射线衍射仪 日本Rigaku 公司。
1.2 实验方法
1.2.1 普洱茶-硒掺杂碳量子点和单质硒的制备
1.2.1.1 普洱茶水提取物的制备 参照叶锡光[22]的方法:称取4.5 g 普洱茶样品,按茶水比1:50 g/mL加入100 ℃超纯水,沸水浸提30 min,每隔10 min振摇一次,浸提结束后趁热抽滤,滤液转移至250 mL容量瓶中,冷却至室温,定容,经冷冻干燥获得普洱茶水提取物冻干粉,于 −20 ℃保存。
1.2.1.2 普洱茶-硒掺杂碳量子点和单质硒的制备参照叶锡光[22]的方法稍作修改:将普洱茶水提取物冻干粉用超纯水配制成浓度为2.5 g/L 的普洱茶水提取物溶液,吸取此溶液5 mL,加入7 mL 超纯水和500 mmol/L 的VC溶液8 mL,800 r/min 磁力搅拌5 min,静置反应15 min,再加入100 mmol/L 的Na2SeO3溶液5 mL,800 r/min 磁力搅拌5 min,随后将混合液置于一定水浴温度中反应一定时间,反应结束后,冰浴冷却10 min,于4 ℃、6000 r/min 离心10 min,分别收集上清和沉淀,上清液过0.22 μm 聚醚枫(PES)滤膜后,经截留分子量为100~500 Da 纤维素透析袋搅拌透析60 h(每4 h 更换透析水一次),得到PT-Se-CQDs 溶液,25 ℃储存备用。
按照上述实验步骤优化反应参数,制备荧光强度高的PT-Se-CQDs。
a. 固定加热温度为100 ℃,探究0、2、4、6、8、10、12 h 不同加热时间对PT-Se-CQDs 荧光强度的影响;
b. 固定加热时间为10 h,探究40、60、80、100 ℃不同加热温度对PT-Se-CQDs 荧光强度的影响。
1.2.2 普洱茶-硒掺杂碳量子点基本特性的表征
1.2.2.1 普洱茶-硒掺杂碳量子点的颗粒大小和形态形貌观测 PT-Se-CQDs 溶液经超声分散30 min,取8 μL 于超薄碳网上,干燥器干燥后,采用场发射透射电镜(Transmission electron microscope,TEM),于200 kV 工作电压下观测其颗粒大小及形态形貌[26]。
1.2.2.2 普洱茶-硒掺杂碳量子点的元素组成及化学键分析 取适量PT-Se-CQDs 溶液于铝箔纸上,干燥器干燥后,采用X 射线光电子能谱(X-ray photoelectron spectroscopy,XPS)测定其元素组成,同时测定C1s 高分辨图谱,分析PT-Se-CQDs 的化学键。设置X 射线光源为Al 靶,测试功率150 W,宽谱步长1 eV,停留时间50 ms,通能为100 eV,扫描区域500×500 μm。
1.2.2.3 普洱茶-硒掺杂碳量子点和单质硒的结构特性分析 取适量PT-Se-CQDs 溶液于石英样品槽中,干燥器干燥后,采用X 射线衍射仪(X-ray diffraction,XRD)测定其晶型结构。设置工作电压40 kV,工作电流40 mA,扫描范围10~80°,连续式步进扫描,步长为0.0131303,扫描速度12°/min[26]。
1.2.3 普洱茶-硒掺杂碳量子点的光学特性表征
1.2.3.1 普洱茶-硒掺杂碳量子点的紫外-可见吸收特性分析 将PT-Se-CQDs 溶液稀释500 倍,采用HITACHIU-2900 双光束分光光度计测定其紫外-可见吸收光谱。设置扫描速度400 nm/min,扫描范围200~800 nm。
1.2.3.2 普洱茶-硒掺杂碳量子点的荧光特性分析将PT-Se-CQDs 溶液稀释25 倍,采用CRT970 荧光分光光度计测定其荧光激发光谱和荧光发射光谱。设置扫描速度为高速,灵敏度为LM2~8(当样品荧光强度响应值达到峰值时,则降低灵敏度进行测定,LM 越小,荧光强度越大),狭缝宽度为10 nm,发射光谱扫描范围为350~550 nm。
1.2.4 普洱茶-硒掺杂碳量子点的荧光量子产率测定
称取一定量硫酸奎宁粉末溶解于0.1 mol/L 硫酸中,作为标准参照物(Φs=54.0%,365 nm)。调节硫酸奎宁溶液和PT-Se-CQDs 溶液的浓度,使硫酸奎宁溶液在360 nm 波长处和PT-Se-CQDs 溶液在380 nm波长处的吸光值小于0.1。采用荧光分光光度计测定该浓度下硫酸奎宁溶液和PT-Se-CQDs 溶液分别在激发波长为360 和380 nm 处的荧光发射光谱,以荧光光谱计算荧光发射峰面积,根据公式(1)计算荧光量子产率[27]。

式中:Φ:荧光量子产率,%;Ι:荧光发射峰积分面积;A:激发波长处溶液的吸光度;η:溶剂的折射率;s:硫酸奎宁标准物;x:PT-Se-CQDs 溶液。
1.2.5 普洱茶-硒掺杂碳量子点荧光探针检测金属离子
1.2.5.1 普洱茶-硒掺杂碳量子点对金属离子的选择性实验 吸取15 份稀释倍数为12.5 倍的PT-Se-CQDs 溶液2 mL,分别加入2 mL 的NaCl、CaCl2、Mg Cl2、NiCl2、BaCl2、CoCl2、CdCl2、SrCl2、ZnCl2、Fe Cl3、FeSO4、MnSO4、CrNO3、Pb(NO3)2等14 种金属离子溶液(2 mmol/L),以超纯水为对照,测定其荧光发射光谱。
1.2.5.2 金属离子对普洱茶-硒掺杂碳量子点检测Fe3+的干扰性实验 吸取14 份稀释倍数为12.5 倍的PT-Se-CQDs 溶液2 mL,分别加入1 mL 的FeCl3溶液(0.2 mmol/L)和NaCl、CaCl2、MgCl2、NiCl2、BaCl2、CoCl2、CdCl2、SrCl2、ZnCl2、FeSO4、MnSO4、CrNO3、Pb(NO3)2共13 种金属离子溶液(2 mmol/L),以超纯水为对照,测定其荧光发射光谱。
1.2.6 普洱茶-硒掺杂碳量子点荧光探针检测Fe3+的灵敏度测定 吸取11 份稀释倍数为12.5 倍的PTSe-CQDs 溶液2 mL,分别加入2 mL 不同浓度FeCl3溶液,使其终浓度为0、10、20、30、40、50、100、150、200、250、300 μmol/L,静置反应2 min 后,测定其荧光发射光谱。
1.2.7 普洱茶-硒掺杂碳量子点荧光探针检测Fe3+的荧光猝灭机制 吸取18 份稀释倍数为12.5 倍的PTSe-CQDs 溶液2 mL,加入2 mL 不同浓度FeCl3溶液,使其终浓度为0、50、100、150、200 μmol/L,充分混匀后,将混合溶液分别于21、31、41 ℃恒温水浴静置0.5 h,测定其荧光发射光谱。根据斯特恩-沃尔默(Stern-Volmer)简化方程(式2)计算猝灭常数,分析其荧光猝灭机理。

式中:F0是不存在猝灭剂时的稳态荧光强度;F 是存在猝灭剂时的稳态荧光强度;Ksv是斯特恩-沃尔默猝灭常数,L/mol;[Q]是猝灭剂的浓度,μmol/L。
1.2.8 矿泉水和纯净水中Fe3+测定 按1.2.6 方法,测定矿泉水和纯净水中Fe3+含量。同时,在矿泉水和纯净水中加标10、100 μmol/L 的FeCl3溶液,相同条件下测定其荧光强度并计算加标回收率。
1.3 数据处理
所有实验含3 次平行,2 次重复,数据结果以平均值±标准偏差表示,图表采用Origin Pro 9.0 64 软件绘制。
2 结果与分析
2.1 水浴加热温度和时间对普洱茶-硒掺杂碳量子点荧光强度的影响
本研究在普洱茶-纳米硒制备的基础上,通过改变水浴加热的温度和时间,以过量VC为还原剂和碳源,普洱茶-硒原子为杂原子,同时制备出PT-Se-CQDs(上清)和单质硒(沉淀)。为确定PT-Se-CQDs制备的最适水浴加热温度和时间,采用荧光分光光度计测定了40~100 ℃水浴加热温度、0~12 h 加热时间下制备的PT-Se-CQDs 的荧光强度,结果如图1和图2 所示。
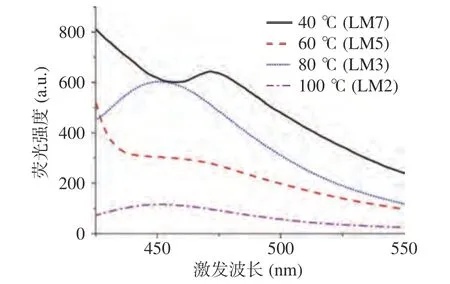
图1 不同加热温度下普洱茶-硒掺杂碳量子点的荧光光谱Fig.1 Fluorescence spectra of Pu-erh tea nano-selenium doped carbon quantum dots at different reaction temperatures
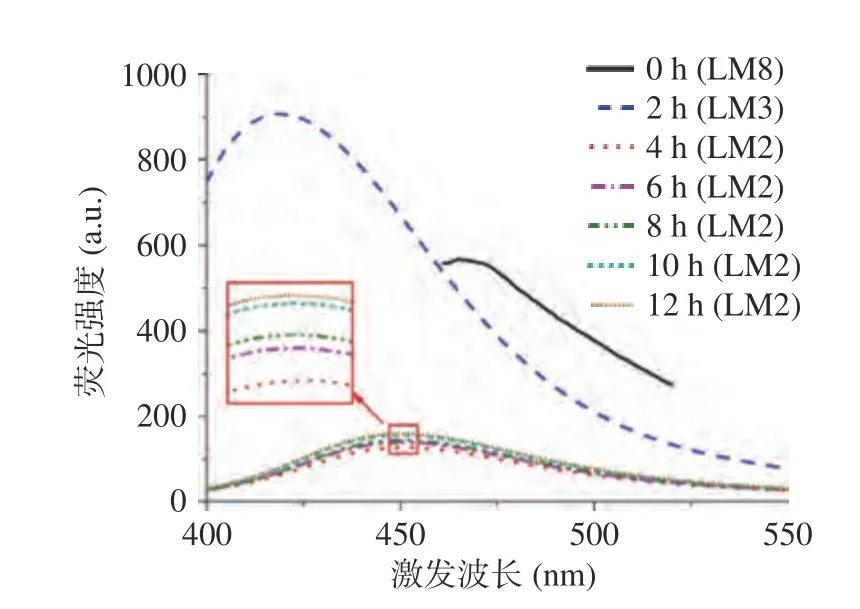
图2 不同加热时间下普洱茶-硒掺杂碳量子点的荧光光谱Fig.2 Fluorescence spectra of Pu-erh tea nano-selenium doped carbon quantum dots at different reaction time
图1 结果表明,在40~100 ℃温度范围内,随着加热温度的升高,PT-Se-CQDs 的荧光强度逐渐增大(灵敏度由7 降低至2),说明温度升高有利于VC碳化、裂解,单位时间内CQDs 产率高,荧光强度增强[28]。固定加热温度为100 ℃,加热时间由0 h 延长至4 h 时,PT-Se-CQDs 的荧光强度随之增大(灵敏度由8 降低至2);进一步延长加热时间至8~10 h,PT-Se-CQDs 荧光强度增大;当反应时间延长至12 h,PT-Se-CQDs 荧光强度变化不明显。此结果说明,当碳源(VC)含量固定时,适当延长反应时间,有利于其碳化、裂解,提高CQDs 产率,提高其荧光强度。但加热时间过长,碳源消耗接近完全,其荧光强度不再增强[28]。综上结果,在普洱茶-纳米硒制备时,设置水浴加热温度100 ℃、加热时间10 h,经4 ℃、6000 r/min离心10 min,可制备得到荧光强度高的PT-Se-CQDs(上清),同时还可制备得到单质硒(沉淀)。
2.2 普洱茶-硒掺杂碳量子点和单质硒的表征
在同时制备了PT-Se-CQDs 和单质硒的基础上,本研究进而采用TEM、XPS 表征PT-Se-CQDs形态形貌、表面元素组成和价态等基本特性;采用UV-Vis 吸收光谱和荧光光谱等表征其光学特性;采用XRD 表征单质硒的晶型结构。
2.2.1 普洱茶-硒掺杂碳量子点和单质硒的基本特性
PT-Se-CQDs 的形貌结构如图3 所示。通过TEM观察,其为类球形纳米颗粒,平均直径为3.1 nm,表明本方法制备得到了具有量子尺寸的PT-Se-CQDs。经XPS 测试可知(图4),PT-Se-CQDs 的全谱扫描中出现O1s、C1s 和Se3d 的XPS 特征峰(图4a),表明其含有O、C、Se 元素。根据图4b 的C1s 分峰拟合图谱可知,在288.2、286.7、285.3 及283.8 eV 处分别出现C=O、C-O、C-Se 及C-C/C=C 键的特征峰[29],表明普洱茶-硒原子成功掺杂CQDs。图5 的PT-Se-CQDs 和单质硒的XRD 图谱表明,PT-Se-CQDs 在约25°处显示一个范围较宽的衍射峰(图5a),这主要归因于存在的石墨(002)晶面,表明此条件下合成的PT-Se-CQDs 由无序碳排列组成[30]。对比三方晶系t-Se 的JCPDS:06-0362 卡片可知,制备得到的单质硒为三方晶系t-Se[31]。
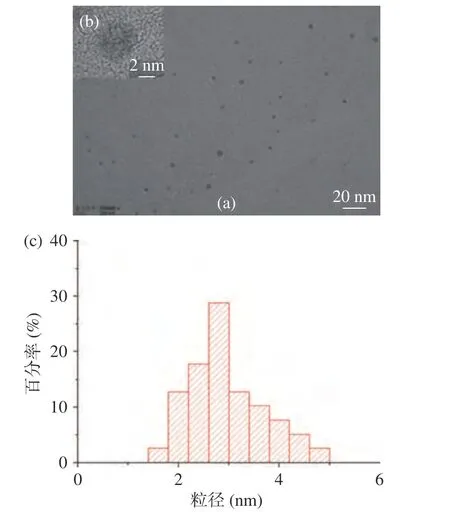
图3 PT-Se-CQDs 透射电镜扫描图Fig.3 TEM image of PT-Se-CQDs
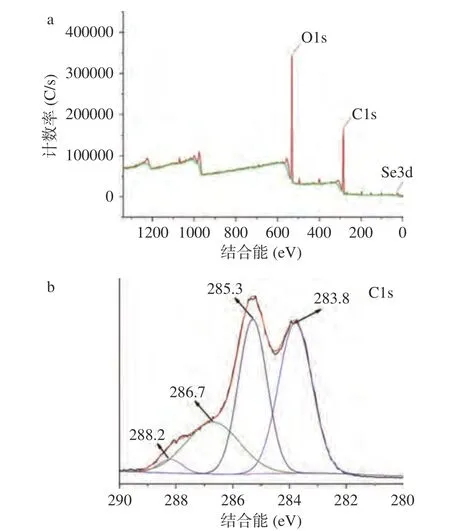
图4 PT-Se-CQDs 的XPS 全谱图(a)和C1s 高分辨图(b)Fig.4 XPS full-spectrum (a) and C1s high-resolution spectrum(b) of PT-Se-CQDs
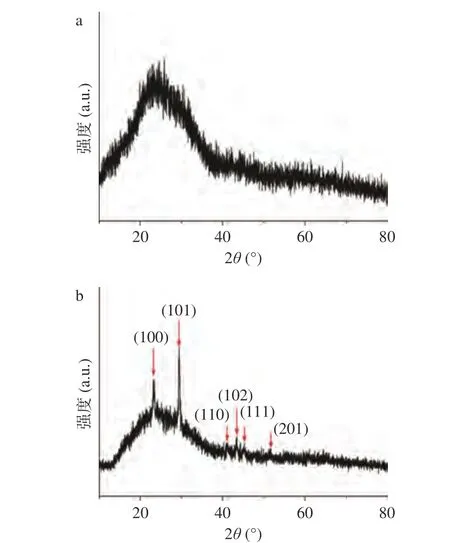
图5 PT-Se-CQDs(a)及单质硒(b)的XRD 图Fig.5 XRD spectrum of PT-Se-CQDs (a) and elemental selenium (b)
2.2.2 普洱茶-硒掺杂碳量子点的光学特性 采用UV-Vis 吸收光谱和荧光光谱分析PT-Se-CQDs 的光学特性。如图6a 所示,PT-Se-CQDs 的吸收光谱主要集中在紫外光区域,在263 nm 波长处具有特征吸收峰,主要归因为碳核里C=C 的π-π*跃迁[32]。图6b荧光光谱图表明,PT-Se-CQDs 的最大激发波长为380 nm,最大发射波长为450 nm,在365 nm 紫外光照射下发蓝色荧光(图6c 内嵌图)。以硫酸奎宁作为参比,根据公式(1)计算可知,PT-Se-CQDs 的量子产率为3.41%。对比相同反应条件下未掺杂CQDs 的荧光光谱的LM 和荧光强度值可知,普洱茶-硒原子掺杂CQDs 的LM 降低、荧光强度值增大(图7),表明普洱茶-硒原子的掺杂提高了CQDs 的荧光强度。

图6 PT-Se-CQDs 紫外-可见吸收光谱图(a)、荧光光谱图(b)和荧光发光图(c)Fig.6 Ultraviolet-visible spectra (a), fluorescence spectrum (b) and 365 nm illumination under violet light (c)of PT-Se-CQDs

图7 CQDs 和PT-Se-CQDs 的荧光光谱图Fig.7 Fluorescence spectrum of CQDs and PT-Se-CQDs
2.3 普洱茶-硒掺杂碳量子点检测金属离子
为研究PT-Se-CQDs 作为荧光探针,应用于检测金属离子的可行性,本研究探究了Na+、Ca2+、Mg2+、Ni2+、Ba2+、Co2+、Cd2+、Sr2+、Zn2+、Fe2+、Mn2+、Pb2+、Fe3+、Cr3+等14 种金属离子对PT-Se-CQDs 荧光强度的影响,结果如图8 所示。在这14 种金属离子中,仅Fe3+明显猝灭PT-Se-CQDs 的荧光,分析其可能是由于Fe3+与CQDs 表面官能团发生螯合作用,导致其荧光发生淬灭[33]。
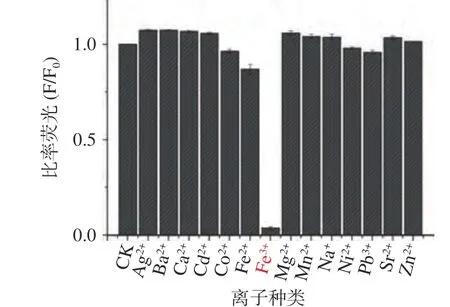
图8 添加不同种类金属离子后PT-Se-CQDs的比率荧光Fig.8 Ratio of fluorescence of PT-Se-CQDs with or without the addition of metal ions
根据上述实验结果,进一步分析Na+、Ca2+、Mg2+、Ni2+、Ba2+、Co2+、Cd2+、Sr2+、Zn2+、Fe2+、Mn2+、Pb2+、Cr3+等13 种金属离子(0.5 mmol/L)对Fe3+(0.05 mmol/L)淬灭PT-Se-CQDs 荧光强度的影响,结果如图9 所示。在高于Fe3+浓度10 倍的13 种金属离子分别存在下,Fe3+作用于PT-Se-CQDs 后,除Fe2+的比率荧光降低到0.6(F/F0)外,其余金属离子的荧光强度无显著变化,推测其可能是由于水体系中的Fe2+不稳定,可被部分氧化成Fe3+,从而猝灭PT-Se-CQDs 的荧光所致[34]。此结果说明PT-Se-CQDs 对Fe3+具有较强的离子选择性。
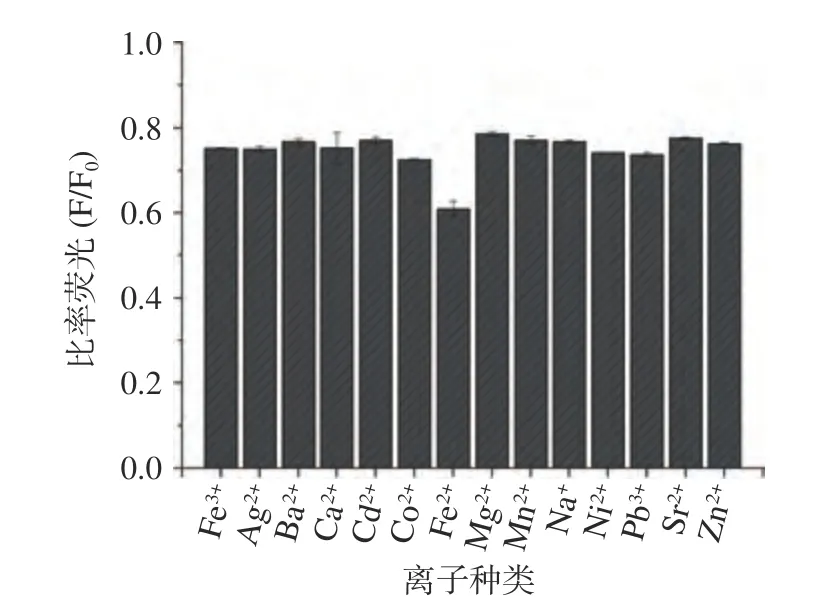
图9 不同金属离子与Fe3+作用于PT-Se-CQDs 后的比率荧光Fig.9 Ratio fluorescence of PT-Se-CQDs treated by Fe3+ in the presence of different metal ions
2.4 普洱茶-硒掺杂碳量子点对Fe3+的检测
在上述实验基础上,为实现Fe3+的定量检测,建立Fe3+快速检测方法,本研究测定了0~300 μmol/L浓度范围内,Fe3+作用PT-Se-CQDs 荧光探针2 min后,其荧光光谱及荧光强度值,结果如图10 所示。Fe3+浓度在0~300 μmol/L 范围内,PT-Se-CQDs 荧光强度随Fe3+浓度的增加而降低(图10a),其比率荧光与Fe3+浓度呈现良好的线性相关,0~50 μmol/L的线性方程为y=−0.0026x+1.0011,R2=0.9965;50~300 μmol/L 的线性方程为y=−0.0029x+1.0151,R2=0.9958。根据线性拟合方程y=−0.0029x+1.0151(R2=0.9958)计算得到检出限为0.2621 μmol/L,均达到现行有效的GB 5749-2006 及2023.4.1 即将实施的GB 5749-2022 生活饮用水卫生标准中规定的Fe3+水平限值0.3 mg/L (5.36 μmol/L)的检测要求[35]。
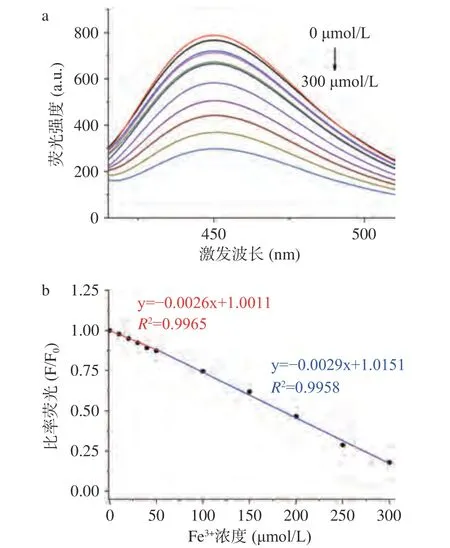
图10 PT-Se-CQDs 荧光强度随Fe3+浓度变化的荧光光谱图(a)及线性关系图(b)Fig.10 Fluorescence spectrogram (a) of PT-Se-CQDs and the linear relationship diagram (b) between the fluorescence intensity of PT-Se-CQDs and the Fe3+ concentration
从表1 可见,PT-Se-CQDs 荧光探针与未进行掺杂的鞣花酸探针相比,虽检出限较高,但检测范围却比其宽广;与SiCDs 及CuNCs 相比,检出限和检测范围均优于这两类探针;与N-CQDs 相比,PT-Se-CQDs 荧光探针检测Fe3+的范围虽略窄,但检出限更低。

表1 不同荧光探针对Fe3+的检测性能比较Table 1 Comparison of detection performance of Fe3+ by different fluorescence probes
2.5 普洱茶-硒掺杂碳量子点对Fe3+荧光检测的作用机制
PT-Se-CQDs 荧光探针检测Fe3+具有高选择性和高灵敏度。为深入分析PT-Se-CQDs 对Fe3+荧光检测的作用机制,本研究测定了0~200 μmol/L 的Fe3+在21、31、41 ℃下猝灭PT-Se-CQDs 的荧光强度,根据斯特恩-沃尔默方程计算猝灭常数,分析其荧光猝灭类型,结果如图11 所示。在21、31、41 ℃反应温度下,不同浓度Fe3+与PT-Se-CQDs 的荧光强度遵循斯特恩-沃尔默方程,经计算发现,随反应温度升高,荧光猝灭常数Ksv 减小,呈反比变化(表2)。王靖蕊等[40]以半乳甘露聚糖与人血清白蛋白的研究证明,其内源性荧光猝灭常数随温度的升高而减小,呈反比变化,即为荧光静态淬灭。综合这些研究结果可知,本研究的Fe3+与PT-Se-CQDs 的荧光猝灭类型亦为静态猝灭。

图11 不同温度下Fe3+和PT-Se-CQDs 相互作用的斯特恩-沃尔默图Fig.11 Stern-Volmer plots for the quenching of Fe3+ by PT-Se-CQDs at different temperatures

表2 Fe3+与PT-Se-CQDs 在不同温度下相互作用的猝灭常数KsvTable 2 Quenching constants Ksv for the interaction of Fe3+ by PT-Se-CQDs at different temperatures
2.6 矿泉水和纯净水样品中Fe3+的检测
为进一步评估该检测方法的准确性和实用性,本研究以PT-Se-CQDs 为荧光探针,检测纯净水及矿泉水样品中Fe3+含量,通过加标10、100 μmol/L 的Fe3+,测定其回收率,结果如表3 所示,结合Fe3+添加值为0时,PT-Se-CQDs 的荧光强度计算得出,纯净水中Fe3+浓度为0,加标回收率范围为90.93%~104.56%,RSD小于8.15%。矿泉水中Fe3+浓度为4.24±2.66 μmol/L,加标回收率为84.53%~113.90%,RSD 小于4.00%,表明该检测方法满足分析要求,可实现对实际样品中Fe3+的定量、快速检测。

表3 PT-Se-CQDs 对实际样品中Fe3+的检测能力Table 3 The detection ability of PT-Se-CQDs in the detection of Fe3+ in real samples
3 结论
本研究基于普洱茶-纳米硒制备的前期研究基础得出如下结论:以普洱茶水提取物稳定分散的普洱茶-硒原子为掺杂原子,以过量的维生素C(VC)作为还原剂和碳源,在水浴加热温度为100 ℃、加热时间为10 h 条件下,同时制备得到PT-Se-CQDs 和三方晶系t-Se;PT-Se-CQDs 和单质硒的基本特性和光学特性表征确定,所制备的PT-Se-CQDs 呈类球形结构、平均直径为3.1 nm、荧光量子产率为3.41%,普洱茶-硒掺杂提高了CQDs 的荧光强度;基于Fe3+显著猝灭PT-Se-CQDs 荧光的特性,成功构建了高选择性和灵敏度的Fe3+检测荧光传感器,建立了Fe3+快速检测方法,检测范围为0~300 μmol/L,检出限为0.2621 μmol/L,其猝灭机理符合静态结合猝灭;以此方法检测纯净水和矿泉水等实际样品中的Fe3+,回收率高达90.93%~104.56%和84.53%~113.90%,RSD小于8.15%和4.00%,该方法达到生活饮用水Fe3+卫生检测要求,具有积极的应用前景。
