罕见的低级别子宫内膜间质肉瘤乳腺转移病例报告和文献回顾
2023-02-19李佳佳吴昀枫吴秀平吴作辉通信作者
王 瑶,严 洁,李佳佳,吴昀枫,吴秀平,吴作辉(通信作者)
(遵义医科大学附属医院超声科 贵州 遵义 563000)
子宫内膜间质肉瘤(endometrial stromal sarcomas,ESS)是一种罕见的生殖肿瘤,仅占所有子宫恶性肿瘤的0.2%,占子宫肉瘤的7%~25%[1]。高级别子宫内膜间质肉瘤(high-grade endometrial stromal sarcomas,HGESS)侵袭性强、预后差、复发率高,与HG-ESS相比,低级别子宫内膜间质肉瘤(low-grade endometrial stromal sarcomas,LG-ESS)预后更好,复发转移风险仅为10%~20%,超过10~30年后的晚期复发转移是该病的特征[2-3]。LG-ESS的常见转移部位是腹部、盆腔和肺,骨转移较少见。ESS转移到乳腺的病例罕有报道。本文报道了一例低级别子宫内膜间质肉瘤术后仅1年出现的乳腺转移,描述了其乳腺X线摄影及超声的表现并回顾分析相关文献,提高对该病的诊断水平。
1 病例资料
患者女性,33岁,因“发现左侧乳腺4+月”入院。无乳腺癌家族史,患者1年前因LG-ESS行子宫全切术。体格检查:左侧乳腺扪及大小约3 cm×1 cm的肿块,质韧,活动度良好,表面光滑无压痛,与周围组织边界清,与胸壁无粘连,挤压乳头无明显溢液及溢血,腋窝未扪及肿大淋巴结。实验室检查:糖类抗原125升高,余检查均为阴性。常规超声:左侧乳腺4点钟方位距乳头30 mm处探及大小约30 mm×18 mm囊实性结节,以囊性为主,边缘清,形态规则,后方回声增强,彩色多普勒血流成像(CDFI)检测结节内未见明显血流信号(见图1),诊断:左侧乳腺囊实性结节:乳腺影像报告和数据系统(BI-RADS) 3级。

图1 常规超声
超声造影:左乳结节注射造影剂后自4 s开始强化,13 s达高峰,16 s开始消退,动脉期实质部分呈高增强,静脉期呈低增强,开始灌注早于正常组织,消退基本同步于正常组织,造影后边缘欠清,形态欠规则(见图2),诊断:左侧乳腺结节:BI-RADS 4c级,结合病史考虑转移性乳腺癌。

图2 ROI曲线
乳腺X线摄影:左乳外下象限见大小约38 mm类圆形稍高密度肿块,边缘清楚,形态规则,诊断:根据放射学特征考虑为良性结节:BI-RADS 3级(见图3)。

图3 乳腺X线摄影图像
手术与病理:左乳腺体4点至6点方向见大小约4 cm×3 cm肿块,包膜完整,质韧,边缘欠清,活动可。术中冰冻结果:左侧乳腺肿瘤,以梭形细胞为主,倾向于交界性。石蜡结果:左侧乳腺转移性子宫梭形细胞恶性肿瘤(考虑子宫内膜间质肉瘤)(见图4)。免疫组化结果:Vimentin(++)、cydinD1(+)、CD10(+++)、Ki-67(约40%+)(见图5)。

图4 HE染色
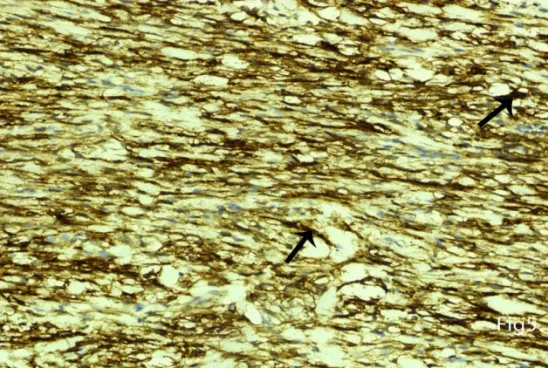
图5 免疫组化
2 讨论
ESS通常发生在绝经前和围绝经期妇女中,平均年龄为46岁(18~83岁),其临床表现因地域而异,但患者通常有子宫不规则增大、腹痛和病理性阴道流血,还可出现血尿及恶心、呕吐等消化道症状[1]。LG-ESS起源于子宫内膜间质,病程缓慢,有激素依赖性,LGESS的主要治疗方法是全子宫切除术并双侧输卵管卵巢切除,绝经前患者保留卵巢后复发率增高,但是据文献报道复发转移通常在很多年以后[4-5]。本病例中,患者保留了卵巢仅行子宫全切术,一年内即出现转移。LG-ESS的常见转移部位是腹部、盆腔和肺,还有少数转移至骨骼[6],转移至乳腺也是非常罕见的。
转移性乳腺癌仅占乳腺恶性肿瘤的0.2%~1.3%,常见转移性原发肿瘤为血液系统恶性肿瘤、黑色素瘤、卵巢癌和肺癌,此外,还可能来自于胃肠道癌、胆管细胞癌、甲状腺癌、头颈部癌和泌尿生殖道癌(包括女性宫颈癌和男性前列腺癌)[7-9],来源于子宫内膜的病例罕有报道。
转移性乳腺癌通常为外上象限单个或多个边缘清楚的圆形或椭圆形低回声结节,无毛刺、钙化或继发性皮肤或乳头改变等恶性征象,据文献报道,仅卵巢癌、肝细胞癌和胃肠道癌乳房转移灶可有微钙化,因此无微钙化也是转移性乳腺癌的典型特征,这些特征提高了其与良性肿瘤的鉴别难度[10-11],常规X线及常规超声可能在鉴别诊断时会出现误诊。在本病例中,常规超声图像上结节边缘清楚,后方回声增强,与文献报道相符。但本病例结节位于外下象限,常规超声为囊实性(以囊性为主),乳腺转移结节囊性变除大腿滑膜肉瘤、肝细胞癌和甲状腺岛状癌,来源于其他部位的目前还未见报道。
乳腺肿瘤是血管依赖性病变,肿瘤细胞表达血管内皮生长因子受体,产生大量新生小血管,这些血管弯曲扩张、形状不规则,血管壁薄,缺乏肌层,同时病变的血管被修复并随机分布,呈现出不规则的形状、厚度,易形成动静脉瘘或血栓的血管盲囊[12-14],这些病理改变均可影响病灶开始灌注时间、达峰强度及消退时间,因此本病例中造影结节开始灌注早于正常组织,动脉期呈高增强。然而小血管分布稀疏部位血供可能无法供应快速生长的肿瘤细胞,最终导致肿瘤内部坏死,超声上表现为囊实混合性。造影后观察到的血流灌注面积大于常规超声,是由于病变向周围正常组织和脂肪组织侵犯,新生毛细血管延伸至周围组织所致,这也进一步提示本病例中结节为恶性的可能性大。因此超声造影能有效鉴别乳腺肿块的良恶性,弥补常规超声的不足。
据文献报道乳腺恶性结节开始灌注时(ITP)和达峰时间(TTP)早于良性病变,峰值强度(PI)也高于良性病变。有研究表明TTP每增加10 s,诊断为恶性肿瘤的概率降低35%。中等强化病变的恶性率是血流灌注差或血供缺乏病变的5倍,高强化病变的恶性率是低血流灌注病变的13倍[15-16]。良性病变的TTP值相对相同,恶性病变的TTP值和病灶内部不同区域的灌注方式确有显著差异。恶性结节周边区域的PI、ITP和总灌注量均高于中心区,表现为高回声增强、快进慢出。肿瘤周边区域新生血管增多,血管壁薄,缺乏肌层,容易导致动静脉瘘[17],因此造影剂是从外向内灌注的,这也是周边区域的ITP早于中央区域的原因,同时造影剂滞留在周围血管床也导致周围区域总灌注量的增加。然而,静脉和外周淋巴管内癌栓的形成加剧间质水肿,导致阻力增加,因此周围区域的造影剂消退慢于中心区域。肿瘤中心区域主要为质地坚硬的结缔组织和纤维组织,导致血管生成不良、坏死和钙化,因此PI低于外围区域[18-19]。然而,周围PI高于中央区域却不能作为是恶性结节的特异性表现,因为有研究发现肉芽肿性乳腺炎也可有此表现[20-22]。但是放射状强化对乳腺恶性结节的特异度高达97.7%,其原因可能是肿瘤周围炎症促进肿瘤血管生成、生长和侵袭,结节中的血管是弯曲且不规则的,大量的分支和放射状血管从边缘渗入肿瘤,因此表现为造影剂沿血管进入呈放射状强化。但极少的良性结节中也可见放射状血管如放射状血管炎性病变[23]。总体来说,乳腺恶性结节多为不均匀高增强,呈向心性,也可见灌注缺损区及放射状强化,造影后灌注区域较常规超声扩大,时间强度特征为快进慢出;良性结节多为低增强或无增强,可为散在点状强化、树枝状强化及整体均匀强化,造影后灌注面积与常规超声一致,时间强度特征为快进快出或慢进快出。
综上所述,有已知的癌症病史,即使常规超声及X线均表现为良性征象,也不能排除转移可能,超声造影能提高乳腺良恶性结节的诊断效能,但明确诊断仍依靠病理学。
