1.5T磁共振成像在临床胃癌术前诊断和分期中的应用价值研究
2023-02-19马晓刚郑历明
马晓刚,郑历明
(北京南郊肿瘤医院放射科 北京 100076)
胃癌作为世界范围内第四大发生率较高的癌症疾病,同时也是导致癌症有关死亡的主要原因之一,其五年生存率未超过30%;且伴随着年龄的不断增大,胃癌疾病的发生率也呈明显的上升趋势,患者主要患病年龄在50~70岁之间[1-2]。此疾病的发生可能和人们日常生活饮食习惯,受到幽门螺杆菌感染,恶性贫血以及家庭遗传等因素存在密切关联性。肿瘤局部浸润深度(T)、区域淋巴结侵入(N)的临床评估结果,对于改善疾病预后效果、制定科学的治疗方案等方面均存在积极意义[3-4]。对于胃癌术前分期所采取的诊断方式具备多样化特点,如计算机断层扫描与病理组织活检等方式,但是不同成像方式其优点、缺点存在一定差异。近年来临床医疗技术的不断完善,磁共振成像(magnetic resonance imaging,MRI)具备较高的分辨率、对人体损伤程度较低、对人体不会带来明显的电离辐射等诊断优势,被广泛使用在胃癌疾病临床诊断中[5]。有相关研究表明,MRI扫描进展期胃癌肿瘤局部浸润深度分期的诊断结果和病理诊断结果准确度存在高度一致性[6]。由此可见,MRI在临床诊断胃癌分期方面具备较为明显的潜力。
1 资料与方法
1.1 一般资料
选取2020年10月—2022年10月北京南郊肿瘤医院治疗的胃癌患者90例,均对其进行1.5T MRI平扫、动态增强扫描检查。90例患者中男性48例,女性42例;年龄57~88岁,均龄(66.31±6.26)岁。通过临床病理组织诊断均进一步确定患者疾病均属于进展期胃癌。肿瘤病变位置:贲门、胃体、胃窦患者例数依次为27例、24例、39例;病理组织分型:高/中分化腺癌、低分化腺癌、印戒细胞癌、鳞状细胞癌例数分别为21例、63例、3例、3例。
纳入指标:①经临床病理学结果被诊断为胃癌进展期者;②对于MRI检查耐受程度较高者;③患者以及患者家属对本研究所有内容(检查方式、检查操作等)均表示了解与知情,主动签署声明同意书。排除指标:① 同时患有其他癌症疾病者;②对本研究所需使用的造影剂存在过敏反应或者禁忌证者;③合并存在重要脏器(如心脏)功能异常者;④合并患有精神疾病或者情绪异常者;⑤处于妊娠阶段或者哺乳阶段的女性群体。
1.2 方法
仪器采用Philips Ingenia 1.5T磁共振超导扫描仪。检查试剂:钆喷酸葡胺注射液(北京北陆药业股份有限公司,国药准字H10 960045;规格为20 mL:9.38 g)、盐酸消旋山莨菪碱注射液(江苏大红鹰恒顺药业有限公司,国药准字H32 025979;规格为1 mL:10 mg)。在扫描之前,嘱患者禁食10~12 h,在扫描前10 min,对患者使用盐酸消旋山莨菪碱注射液(剂量控制在20 mg)进行肌肉注射,以此来抑制胃部蠕动运动、收缩运动;在扫描前5 min,患者饮用温开水600~1 000 mL,促使胃腔处于充盈扩张状态,同时正确指导患者进行呼吸训练,以此来有效避免呼吸运动伪影的出现。此外,在患者即将进入MRI造影室时,应该叮嘱患者完全摘除金属物品。
MRI扫描:应用于Philips Ingenia 1.5T磁共振超导扫描仪器对患者进行MR扫描,采取8通道Torsopa腹部表面相控阵线圈,对患者实施腹部常规T1加权像(T1weighted imaging,T1WI)、T2加权像(T2weighted imaging,T2WI)平扫、动态增强THRIVE扫描。叮嘱患者保持仰卧位姿势,双臂高举并抱住头部,扫描范围应该由胸骨柄中点到脐部位置。在平扫过程中,使用T2WI TSE[脉冲序列重复时间(repetition time,TR)设置为3 000 ms,回波时间(echo delay time,TE)设置为805 ms,视场角(field of view,FOV)设置为38 cm×38 cm~40 cm×40 cm,矩阵设置为320×320,层厚控制在5 mm]+脂肪抑制技术;T1WI TFE(TR设置为3 000 ms,TE设置为805 ms,FOV设置为38 cm×38 cm~40 cm×40 cm,矩阵设置为320×320,层厚控制在5 mm),进行横轴位、冠状位扫描检查,在情况允许下需增加进行矢状位扫描。
动态增强扫描:使用THRIVE技术,其中TR设置为3.6 ms,TE设置为1.5 ms,FOV设置为38 cm×38 cm~40 cm×40 cm,矩阵控制在260×224,层厚设置为3 mm。采取手推法经手背静脉合理使用钆喷酸葡胺注射液(注射速度控制在2.0 mL/s,剂量控制为0.2 mmol/kg),在注射完成后15 s方可对患者进行扫描检查,依次为动脉期(25~50 s)、静脉期(80~120 s)、平衡器(3 min),对横轴位、冠状位、矢状位进行扫描检查。
1.3 评价标准
使用Function软件对本研究所取得的扫描图像进行分析与观察,安排两位专业且临床扫描经验丰富的影像科医生共同阅片,根据图像对肿瘤进行T分期,并且较之临床病理检查结果,对进展期胃癌敏感度、特异度进行评估[7]。其中就胃癌T分期MRI诊断指标而言,采取美国癌症联合会(American Joint Committee on Cancer,AJCC)对于胃癌临床TNM分期评估指标,①T1期:胃壁没有明显增厚,能够观察出存在异常强化胃壁内存,且强化组织没有超过中间层;②T2期:胃壁存在异常增厚情况,然而浆膜面比较整齐且光滑,或者胃壁外层结构完整度较高;③T3期:胃壁全层均限制被浸润,并且胃壁外界或者胃脂均出现侵犯情况,同时存在不规则网格状或者异常中断低信号情况;④T4期:胃壁附近脏器结果存在侵犯情况,信号出现异常变化[8]。
1.4 统计学方法
采用SPSS 25.0统计软件分析数据,符合正态分布的计量资料以均数±标准差(x-± s)表示,行t检验;计数资料以频数(n)、百分率(%)表示,行χ2检验。P<0.05则差异存在统计学意义。
2 结果
2.1 影像学检查结果评估
对90例患者均实施MRI平扫、弥散加权成像(diffusion weighted imaging,DWI)、动态增强扫描。在MRI平扫时,患者病灶区胃壁均呈现出不均匀的增厚情况,厚度大约在7.33~31.73 mm之间,一些病灶区胃壁呈现出“三明治”结构分布,且呈“高信号-低信号-高信号”。病灶区域正常的黏膜形态均完全消失或者受到不同程度的破坏(见图1、图2)。见表1。

表1 影像学检查结果
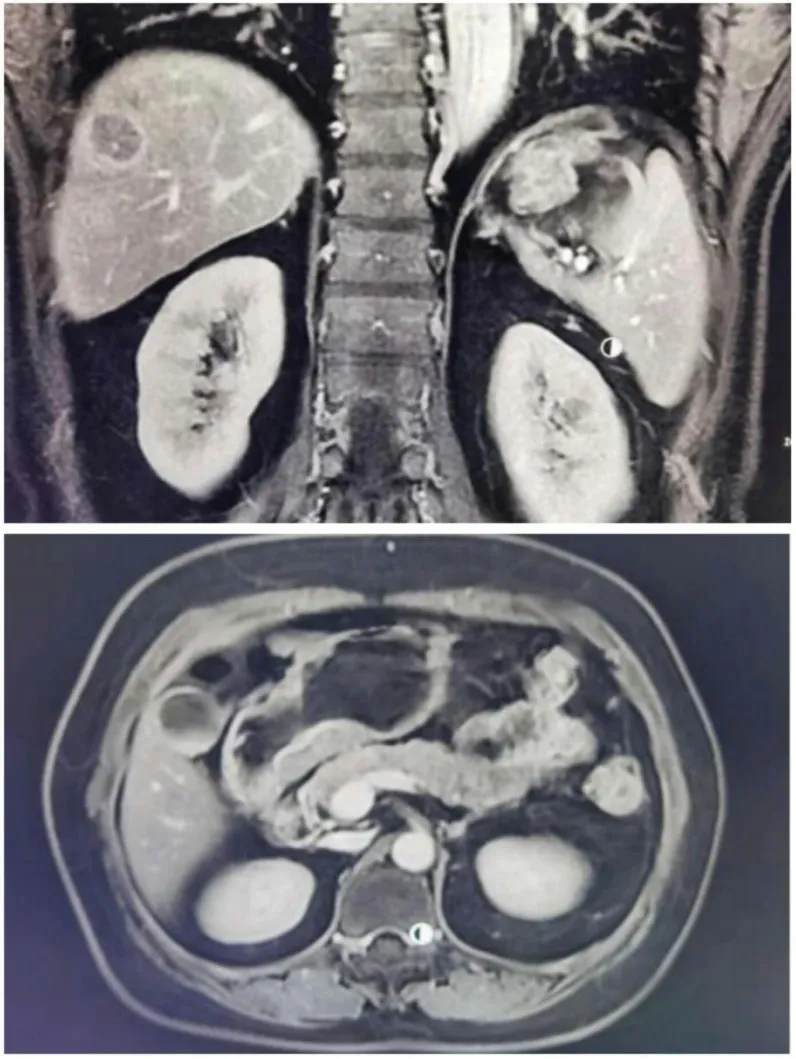
图1 同一患者,增强后病变显示明显,三层结构及浆膜层显示清晰

图2 同一患者,T2WI胃壁增厚伴溃疡,三层结构及浆膜层显示不佳
2.2 MRI T分期诊断效能
MRI T分期和临床病理学诊断准确率分别为80.00%(T2期)、90.00%(T3期)及90.00%(T4期),见表2。
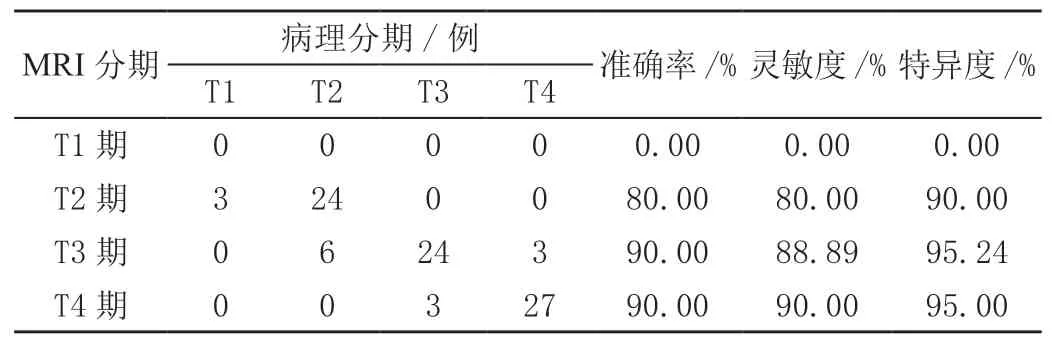
表2 MRI T分期诊断效能
3 讨论
临床研究表明,胃癌术前分期CT准确率大约在42%~69%,内窥镜分期准确率则在81%~92%左右[9]。就临床解剖学而言,胃倾斜区域和肝左叶相互接触,因为其一些体积效应,会对CT明确肝脏侵入检出率带来一定程度的干扰影响。局限的空间分辨率通常会忽略一些细微的疾病转移情况。为此,有学者建议[10]可使用磁共振成像扫描检查方式来提升胃癌术前分期诊断的精准性。内窥镜属于侵入性检查方式之一,其性能的体现离不开医生熟练的检测技巧;然而针对中晚期胃癌来讲,内窥镜顺利进入难度较大。但是MRI不需要提前做好特殊检测准备工作。通过服用温水能够促使人体胃壁处于扩张状态,能够有效地清洗黏附在胃壁组织上的胃液成分,进而促使癌壁区不会出现扩张,所以能够明显降低临床诊断的误差性。对于浆膜外侵入程度较低,则难以通过CT对其进行仔细观察,然而其可能会造成MRI上脂肪层比较模糊不清,为此识别难度较大。由此可见,浆膜对于胃癌分期具有积极意义,且术前MRI和胃癌病理分期存在较为紧密的关联性。
通过对90例胃癌患者进行MRI平扫检查。其病灶区胃壁组织均呈现出不均匀增厚情况,并且厚度大约分布在7.33~31.73 mm,一般情况下局部病灶胃壁增厚超过6.00 mm便会被视为不正常。加之,长时间的慢性炎性也会导致胃壁有所增厚,倘若存在胃溃疡症状时,胃壁会呈现出不同程度的增厚情况[11]。由此可见,胃壁增厚评估指标的诊断能力存在一定局限性。此外,病灶部位所包含的纤维结缔组织或者黏液会对信号带来一定影响,如当结缔组织相对较多时,T1WI序列会呈现出低信号;反之,黏液比较多时,T2WI序列呈高信号。对于进展期胃癌各个分期在T2WI表现均不太显著,例如T2期胃肠通常呈现出胃壁局部增厚,然而肌层外缘显影比较模糊不清。T3期、胃癌和临床标准分期偶尔会存在一定差异,例如T2WI反映肌层外缘比较光滑,对于胃部周围的脂肪组织侵犯不太限制,但是一些T3期肿瘤胃壁外缘和附近身体脏器紧密连接,针对此种情况,判读的难度较大。但是动态增强扫描能够有效体现出胃壁三层结构分布情况,能够对胃癌分期提供良好的参考依据。
综上所述,在临床胃癌术前诊断以及疾病分期过程中使用1.5T磁共振成像检查方式具备较高的临床应用价值,不仅扫描成像速度相对较快,同时还能够清楚地反映出胃壁分层情况、病灶侵犯深度,从而对疾病分期提供良好的参考依据。
