孕妇产前组织型绒毛膜羊膜炎与新生儿缺氧缺血性脑病相关性分析
2023-02-17杨金英王倩菲
杨金英,王倩菲
(西安市人民医院 西安市第四医院新生儿科,陕西 西安 710004)
胎膜早破在我国发病率为6%~16%,是导致孕产妇难产、新生儿感染的主要原因之一,胎膜早破使胎膜的屏障功能减弱,阴道病原菌可沿生殖道上行,侵犯羊膜,诱发羊膜腔感染,其中以组织型绒毛膜羊膜炎(Histological chorioamnionitis,HCA)多见[1]。HCA虽然症状隐匿,但挪威的一项最新研究调查指出[2],HCA与新生儿不良结局密切相关。HCA可影响子宫收缩,造成胎儿宫内窘迫,可诱发新生儿缺氧缺血性脑病(Hypoxic-ischemic encephalopathy,HIE)等新生儿脑损伤疾病[3]。近年研究[4]发现,多种炎症因子与HCA的发生机制有关,并参与新生儿不良结局的发生,监测相应的炎症因子变化,对预测HCA及其不良结局有利。基于此,本研究就HCA与HIE的关系及可能的发生机制展开分析,为我国母婴保健工作开拓思路,现报告如下。
1 对象与方法
1.1 研究对象 收集2020年1月至2021年12月西安市人民医院收治的86例HCA孕产妇的临床资料,并纳入同期入院的86例未发生HCA孕产妇作为对照组。病例纳入标准:符合中华医学会妇产科学分会产科学组2015年制定的胎膜早破诊断标准[5],且破膜孕周为28~36+6周;HCA经胎盘组织病理学检查确诊,且符合《妇产科学(第9版)》[6]诊断标准;孕产妇年龄>20岁;单胎妊娠;病理检查等资料完整。排除标准:胎膜早破入院前1周有抗生素或皮质类固醇药物使用史;入院后急产;胎位异常、胎儿结构或染色体异常、死胎;存在急慢性感染性疾病或不明原因发热;合并糖尿病、高血压、子宫畸形等早产高危因素。本研究标本及病例资料的收集等均获得患者知情同意,且得到西安市人民医院医学伦理委员会核查及审批。
1.2 研究方法 所有孕产妇在胎盘娩出后取胎膜破口处胎膜组织2 cm×2 cm,0.9%氯化钠溶液冲洗干净后保存于-80 ℃冰箱内;取冰冻胎膜组织研磨均匀,使用Trizol试剂盒提取总核糖核酸(RNA),经逆转录试剂盒逆转录,采用实时荧光免疫聚合酶链式反应检测胎膜组织Toll样受体4(TLR-4)、核因子-κB(NF-κB)表达情况,引物由上海生工生物工程股份有限公司设计、合成及提纯,引物序列如下:TLR-4正向引物5’-GAGGCAGCTCTTGGTGGAAGTTG-3’,反向引物5’-CAAGCACACAGGACCGACAC-3’,长度138 bp;NF-κB正向引物5’-GATGTGGCATTGGCTATGGGTAT-3’,反向引物5’-GTCACTCTGCCTGGAACCTGTC-3’,长度185 bp;内参GAPDH正向引物5’-TCGTGGAAGGACTCATGACC-3’,反向引物5’-AGGGATGATGTTCTGGAGAG-3’,长度226 bp;扩增条件:94 ℃预变性2 min,94 ℃变性20 s,65 ℃退火30 s,40个循环,最后72 ℃延伸10 min;扩增产物行2%琼脂凝胶电泳,并使用紫外光凝胶成像系统摄像观察,采用2-△△Ct法,以目的基因TLR-4、NF-κB与内参GAPDH的比值作为其mRNA相对表达量。HIE的诊断及临床分度参考《新生儿缺氧缺血性脑病诊断标准》[7],临床分度有Ⅰ度(激惹兴奋,发病1 d内症状明显,2~3 d可消失,伴自发动作增多)、Ⅱ度(嗜睡或迟钝,上肢肌张力下降,原始反射减弱,伴或不伴惊厥)、Ⅲ度(昏迷,肢体肌张力及原始反射消失,惊厥发作频繁,常伴颅内压增高);根据是否发生HIE,将HCA组分为HCA-HIE组与HCA-非HIE组2个亚组。
2 结 果
2.1 两组孕产妇一般资料比较 两组孕产妇年龄、产次及早产史比较差异无统计学意义(均P>0.05),HCA组破膜孕周低于对照组、新生儿出生体重高于对照组(均P<0.05),见表1。
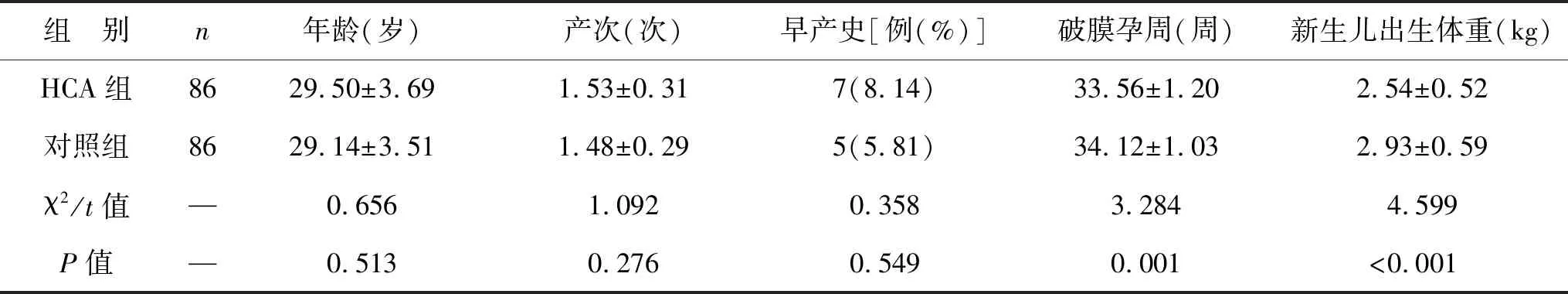
表1 两组孕产妇一般资料比较
2.2 HCA组与对照组HIE发生情况比较 HCA组发生19例HIE,其中Ⅰ度7例,Ⅱ度8例,Ⅲ度4例,对照组发生1例Ⅰ度HIE,HCA组HIE发生率明显高于对照组(χ2=18.332,P<0.001)。
2.3 HCA-HIE组、HCA-非HIE组与对照组胎膜组织TLR-4、NF-κB mRNA相对表达量比较 HCA-HIE组胎膜组织TLR-4、NF-κB mRNA相对表达量明显高于HCA-非HIE组及对照组(均P<0.05),HCA-非HIE组高于对照组(P<0.05),见表2。
表2 三组孕产妇胎膜组织TLR-4、NF-κB mRNA相对表达量比较
2.4 HCA孕产妇HIE临床分度与胎膜组织TLR-4、NF-κB表达水平的相关性 HCA孕产妇HIEⅠ度者胎膜组织TLR-4、NF-κB mRNA相对表达量明显低于Ⅱ度及Ⅲ度者(均P<0.05),Ⅱ度者低于Ⅲ度者(P<0.05),见表3。Spearman相关分析显示,HCA孕产妇HIE临床分度与胎膜组织TLR-4、NF-κB mRNA相对表达量呈显著正相关(r=0.379、0.394,均P<0.05)。
表3 HCA孕产妇不同HIE临床分度者胎膜组织TLR-4、NF-κB mRNA相对表达量比较
3 讨 论
虽然HCA与胎儿窘迫、新生儿败血症、新生儿神经系统发育异常等多种新生儿不良结局有关,但HCA产前无明显临床症状,产前诊断困难,主要由产后胎盘病理诊断,HCA诊疗仍是产科难题[8]。有报道[9]表明,阴道内微环境随着妊娠的进程逐渐趋于稳定,上行感染风险逐渐降低,故胎膜早破孕周越小越易发生宫内感染及不良结局。本研究中,HCA组破膜孕周低于对照组,新生儿出生体重高于对照组,与上述报道一致,提示对于较小孕周的胎膜早破,应警惕HCA,并注意与宫内感染相关的不良结局。
分析HCA与新生儿不良结局的关联性及其作用机制,是近年研究的热点[10]。据文献[11]报道,HCA引起胎盘功能异常,胎盘血流量减少,造成胎儿缺血缺氧,诱发脑损伤,且感染刺激子宫收缩,增加产时窒息发生风险,也易造成HIE。也有研究[12]表明,围产期的宫内感染也能引起胎儿神经元敏感性增加,缺氧缺血时更易发生神经元凋亡,导致HIE。本研究发现,HCA组HIE发生率明显高于对照组,提示HCA可能增加HIE发生风险,与上述研究结果一致。HCA可能通过促进胎盘功能异常及刺激子宫收缩等多种方式,增加HIE等新生儿不良结局发生风险。
另据文献[13]报道,多种细胞因子参与感染引起HIE的发生机制,感染引起促炎因子增多,抑炎因子减少,细胞因子平衡被打破,刺激一氧化氮等损伤介质合成及释放,诱导神经元凋亡。不仅如此,感染及炎症可激活血管内皮细胞,影响凝血-纤溶系统,造成血管内细胞黏附、血栓形成,诱导多重级联反应,引起缺氧缺血等一系列病理改变,损伤越重,患儿智力越低下,预后越差[14-15]。郭孝君等[16]研究指出,HCA症状隐匿,监测淋巴细胞比例、中性粒细胞计数、血小板淋巴细胞比值等系统性炎症参数可尽早识别HCA,指导临床诊疗,以减少HCA引起的新生儿不良结局。因此,分析与HCA发生、发展有关的炎症参数,对控制新生儿不良结局有积极意义。TLR-4/NF-κB是机体重要信号通路,可介导炎性反应与氧化损伤,参与缺血再灌注损伤等多种生理病理过程[17]。近年研究还发现[18],TLR-4/NF-κB信号通路可参与绒毛膜羊膜炎的发生。本研究结果显示,HCA-HIE组胎膜组织TLR-4、NF-κB mRNA相对表达量明显高于HCA-非HIE组及对照组,HCA-非HIE组高于对照组,提示TLR-4/NF-κB信号通路可能参与HCA的发生,还可能与HCA诱发HIE的发生机制有关。分析其原因可能为:病原菌入侵活化TLR-4,触发含白细胞介素-1受体结构域,激活NF-κB,引起下游大量促炎因子产生,促进细胞基底膜破坏,加剧胎膜屏障损伤,诱发HCA及不良结局[19-20]。不仅如此,HCA孕产妇HIE临床分度与胎膜组织TLR-4、NF-κB mRNA相对表达量呈显著正相关,提示TLR-4/NF-κB信号通路与HCA诱发HIE的病情进展密切相关。考虑与TLR-4/NF-κB信号通路的激活可诱导血管内皮细胞损伤,胎膜组织TLR-4、NF-κB 的大幅度上调提示胎盘功能受损,胎盘血流量严重下降,促进胎儿缺血缺氧性损伤,使HIE进展加快有关[21-22]。然而,HCA诱发HIE与TLR-4/NF-κB信号通路的关联性未见相关报道,本研究可为后续临床研究提供新思路,但本文结果还需后续研究的论证。
综上所述,HCA孕产妇发生HIE风险更高,TLR-4/NF-κB信号通路可能参与了HCA诱发HIE的发生与发展。
