小儿常用药ADR的发生规律、特点及给予用药指导的作用分析
2023-02-14张芳芳
张 娜 张芳芳
郑州大学附属儿童医院、河南省儿童医院、郑州儿童医院静脉用药调配中心 (河南 郑州 450000)
药品不良反应(ADR)是临床用药期间面临的主要问题,因小儿各器官、系统功能尚未发育完全,给药期间若出现一丁点错误、不合理情况,极易诱发ADR[1]。随着各类小儿用药应用日益广泛,ADR发生率逐渐升高,其危害性越来越引起临床的高度重视。由于小儿正处于生长发育阶段,各器官、系统尚未发育完善,药物治疗时稍有不慎就容易发生ADR。据522例抗菌药物不良反应报告,≤10岁患者占30.46%[2];1103份儿童药物不良反应报告,1岁以下儿童不良反应占35.54%[3]。因此评估用药合理性、准确性,减少药物用法、用量的错误,避免出现药品不良反应,提高临床用药安全性,显得极其重要。因此,本研究就总结小儿常用药ADR发生特点及规律,旨为合理用药提供指导,报道如下。
1 资料与方法
1.1 资料来源
收集河南省儿童医院2019年1月至2020年10月期间出现的150例小儿常用药ADR报告表,病历资料完整;可统计分析ADR给药途径、结果、预后等具体资料;该研究的开展,无伦理纠纷,符合医学伦理委员会审批标准。
1.2 方法
分析150例ADR报告具体资料,统计其性别、年龄、用药途径、表现等具体资料,对药物转归进行分析。按照相关评定标准评价药物因果关系:肯定,极大可能,可能,可能性低、未评价及无法做出评价。强度分级:重、中、轻度。转归:治愈、好转,后遗症及死亡。ADR对原患疾病的影响:无明显影响,延长治疗时间、疾病加重,出现后遗症。
1.3 统计学方法
2 结 果
2.1 ADR因果关系评定
150例ADR报告表明,因果关系:肯定12例,占8.0%;极大可能105例,占70.0%;可能有关系15例,占10.0%;可能性低12例,占8.0%;无法做出评价6例,占4.0%;差异有统计学意义(χ2=121.185,P=0.000)。
2.2 严重程度及对原患疾病的影响以及患儿治疗预后分析
150例ADR报告表明,轻度68例,占45.33%;中度61例,占40.67%;重度21例,占14.0%。轻度、中度ADR发生率均高于重度,差异有统计学意义(χ2=35.289,26.852;P=0.000,0.000)。
原患疾病的影响:无明显影响81例,占54.0%;延长治疗时间62例,占41.33%;疾病加重7例,占4.67%;无明显影响、延长治疗时间占比率均高于疾病加重率,差异有统计学意义(χ2=73.835,56.936;P=0.000,0.000)。
治疗情况:治愈74例,占49.33%;好转69例,占46.0%;出现后遗症7例,占4.67%。
2.3 年龄与性别分布
性别分布:男78例,占52.0%;女72例,占48.0%;两者之间比较,差异无统计学意义(χ2=0.480;P=0.488)。
年龄分布:1~3岁占35.33%,>3~6岁占27.33%,>6~9岁占23.33%,>9岁占14.0%,差异有统计学意义(P<0.05),见表1。
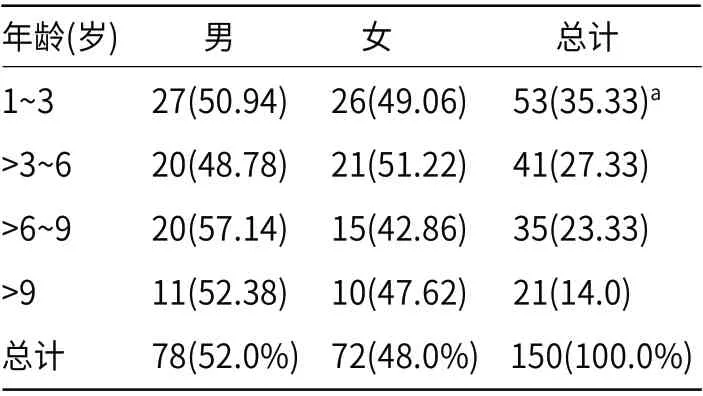
表1 150例ADR年龄与性别分布[n(%)]
2.4 药物种类
抗生素类药物75例,占50.0%;中药制剂41例,占27.33%;维生素类18例,占12.0%;呼吸系统用药6例,占4.0%;循环系统用药6例,占4.0%;解热镇痛药物4例,占2.67%;其中抗生素药物种类均高于其它药物种类,差异有统计学意义(χ2=16.248,50.531,80.518,86.620;P=0.000,0.000,0.000,0.000)。
2.5 给药剂型及给药途径
给药剂型:注射剂128例,占85.33%;颗粒12例,占8.0%;片剂8例,占5.33%;滴剂2例,占1.33%。注射剂占比率均高于其它给药剂型,差异有统计学意义(χ2=180.214,193.687,215.511;P=0.000,0.000,0.000)。
给药途径:静脉滴注125例,占83.33%;肌肉注射3例,占2.0%;口服10例,占6.67%。静脉滴注占比率均高于其它给药途径,差异有统计学意义(χ2=202.816,178.114;P=0.000,0.000)。
2.6 ADR累及的系统器官及不良反应表现
150例ADR报告表明,皮肤及其附件占59.33%;全身性损害占12.0%;五官系统占8.67%;消化系统占6.67%;神经系统占5.33%;呼吸系统占4.0%;循环系统占2.67%;肌肉及骨骼系统占0.67%,泌尿系统占0.67%,其中皮肤及其附件不良反应占比率最高,其次是全身性损害,差异有统计学意义(P<0.05),见表2。

表2 ADR累及的系统器官及不良反应表现
3 讨 论
3.1 小儿常用药ADR的发生规律、特点
随着医疗水平进展,医疗药品市场不断扩展,各种药物种类明显增加,为各种疾病治疗及临床用药提供多种选择,但随之而来的是药物不良反应增加。由于小儿正处于生长发育过程,组织器官发育不够完善,生理功能不够健全、机体耐受性差等,药物代谢能力存在差异,使药物不良反应发生风险明显增加[4]。同时小儿正处于生长发育的关键时期,新陈代谢旺盛,循环时间短,肝肾功能未发育成熟,对药物排泄率较快,且对药物存在特殊反应,此时因小儿因药物导致的不良反应严重性明显高于成人,给患儿、家庭及社会带来严重的不良后果,此时重视小儿ADR,加强用药控制,对确保小儿身心健康有重要意义。
本研究,男性占比高于女性女性,同周莉等[5]调查108例儿童ADR研究结果相似;年龄分布1~3岁占比最高,同黄贝茹等[6]调查结果相似,婴幼儿安全用药形势极其严峻。结果表明性别差异对药品不良反应的影响较轻,主要是婴幼儿为主。由于儿童年龄越小,肝肾器官尚处于发育阶段,对药物敏感性高,肝肾对药物排泄、代谢功能较低,药物蓄积性高,血药浓度增加等,极易引起ADR[7]。
研究显示,抗生素类药物占50.0%,中药制剂占27.33%,药物注射剂占85.33%,静脉滴注占83.33%,其不良反应累及组织器官主要是皮肤及其附件、全身性损害、五官系统等。结果表明抗生素主要是影响小儿安全的主要药物,可能是抗生素滥用、联合用药、超指征用药等问题,耐药菌株的产生,使药物不良反应增多;同时,我国医疗单位应用大量的抗菌药物,随着抗生素不合理应用日益严重,使多数致病菌产生明显的耐药性,也增加了ADR发生风险。同时静脉给药不经过肝脏首过效应,药物直接进入循环系统,会增加血药浓度,并作用于靶器官,使药物不良反应增多[8]。抗生素药物应用时,其不良反应主要涉及过敏反应及泌尿系统反应,变态反应主要为皮疹,可能是药物及其降解聚合物存在的半抗原与血清蛋白结合并形成抗原,故而产生与药物有关的变态反应。同时中药制剂引起的ADR也不容忽视,可能是因中药制剂的成分非常复杂,中药提取不易、工艺条件不一、而且中药制剂注射满足不了质量要求,此时引起的ADR临床表现也较为复杂[9];另一方面多数临床医师认为中药制剂安全性高、属无毒反应,造成中药制剂应用普遍,并未按照中医诊断辨证论治,盲目滥用;或在使用期间与西药注射剂配伍、溶媒使用措施、药剂浓度过高等原因,进而更容易诱发ADR[10]。
3.2 小儿常用药的用药指导
因此,根据儿童常用药ADR发生规律及特点,总结出安全用药指征:(1)抗生素是引发ADR发生的主要药物,因此在应用抗生素时,需要严格按照抗菌药物指导原则,掌握各药物使用的禁忌症、适应症,做药敏试验,掌握特殊用药使用特点以及药物使用的药效学、药动学规律,制定合理、准确的用药方案,提高用药安全性[11];(2)中药制剂成分复杂,稳定性差,容易诱发药物变态反应,因此建议临床医师在使用中药制剂时,尽量避免与西药注射剂配伍;并严格按照药物说明书的用法、用量进行给药,合理、规范的配制中药制剂的浓度,不得随意增加药物剂量,严格遵循《中药注射剂临床使用指导原则》进行给药,以此提高临床用药安全性[12];(3)静脉给药时,需要掌握输液适应证,不得随意增加输液范围,能口服给药者,不可输液;同时做好患儿家长的健康教育,教育公众能安全合理用药,注意患儿静脉滴注情况,不可擅自调整输液速度,减少因静脉给药导致的ADR;因此在选择给药途径时,在不影响临床治疗时,优先考虑口服用药,其次是肌内注射,将静脉注射作为小儿用药途径的最末选项[13];(4)用药前,明确疾病诊断,详细了解患儿既往用药史、过敏史,使治疗方案更加简化,避免药物滥用性;并严格控制给药剂量,根据个体化差异,选择合理的用药剂量;同时临床医师要熟知小儿的肾脏解剖特点及生理特点,认识药物肾毒性,严格掌握用药指征,避免药物滥用,尽量控制肾毒性药物的使用[14];(5)强化对医务人员、患儿家长的健康宣教,提倡抗生素准确、合理用药的宣传教育,强化安全用药的监督管理,使其掌握临床用药监测知识、用药方法,强化医务人员急救知识的专业培训,树立准确用药的责任意识,广泛普及ADR知识,以此提高临床用药的安全性,实现经济、安全用药的目的[15];(6)临床用药时,需要有目的联合用药,用最少种类的药物达到治疗目的,在联合用药时,需要尽量排除药物之间相互作用引起的不良反应,若患儿服用多种药物出现不良反应,需要准确分辨是哪种药物引起的不良反应,以此提高临床用药的安全性及有效性[16]。
综上所述,小儿常用药存在不良反应,以1~3岁小儿为主,抗生素、中药类制剂以及静脉注射是引起不良反应的主要情况,因此临床需要加强用药监测,强化抗生素、中药制剂的安全管理,教育公众能安全合理用药,以此减少小儿ADR的发生,为临床合理、安全用药提供参考。
