一种新型冠状病毒抗原检测试剂性能分析和临床评价
2023-02-12姜晓路杜明秋羊兰翠范晨霞郑明
【作 者】 姜晓路,杜明秋,羊兰翠 ,范晨霞 ,郑明
1 浙江省医疗器械检验研究院,杭州市,310018
2 杭州协合医疗用品有限公司,杭州市,310018
0 引言
2019年末,由严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome corona virus 2,SARS-CoV-2)导致引发的新型冠状病毒感染(corona virus disease 2019,COVID-19)疫情席卷全球,根据世界卫生组织(World Health Organization,WHO)报道,截至2022年8月3日,全球已有575887049确诊病例,其中6398412例死亡[1]。SARS-CoV-2是一种单链正义、有包膜、颗粒呈圆形或椭圆形、直径为60~140 nm的线性RNA病毒[2]。测序显示其全基因组长度约为30 kb(GenBank,MN908947.3),能编码4种结构蛋白,包括刺突蛋白S、包膜蛋白E、基质蛋白M和核衣壳蛋白N[3-4]。N-蛋白在冠状病毒中含量丰富,是一种高度免疫原性蛋白,参与基因组复制和细胞信号通路调节,具有高特异性等特点。作为SARS-CoV-2的核心蛋白,N-蛋白对新冠病毒的诊断和排查具有重要价值,也是其最重要的标志[5-6]。
目前商业使用的COVID-19诊断方法主要分为两大类:一类为基于聚合酶链式反应(polymerase chain reaction,PCR)的分子诊断技术;另一类是检测患者感染新冠病毒后体内产生的抗原或抗体的免疫诊断技术[7]。分子诊断技术是新冠病毒检测的 金标准”,具有早期诊断、灵敏度高和特异性强等特点,但其操作复杂、检测时间长,需要专业人士进行。免疫层析技术由于操作简单、检测时间短等优点而广泛应用。目前已有多种不同形式的免疫层析试纸被用于不同新冠感染相关标志物的检测,包括抗体、蛋白等,并有一些免疫层析试纸已经获批上市[8-11]。
虽然COVID-19 IgM抗体可反映近期感染,但病毒感染后COVID-19 IgM抗体的产生有滞后性(一般认为须在感染后7 d产生)[12]。新冠抗原检测兼具方便、快速和低价这3项优势,而相较抗体检测,抗原检测可对刚出现感染症状的患者及时检测,可对疑似人群早期分流和快速管理,同时也可以满足大规模人群筛查和欠发达地区应用的需求[13]。本研究对基于胶体金免疫层析法研制的新冠检测试剂盒进行系统性的验证,以评估试剂盒在快速诊断COVID-19的价值,以便能提供准确的检测结果,为及时防控疫情提供依据。
1 材料和方法
1.1 研究设计与样本采集
根据《新型冠状病毒肺炎诊疗方案(试行第九版)》[14],该研究感染后出现症状的时间分布于多个时期(0~3 d(40%)、4~7 d(40%)、>7 d(20%)),共采集阳性样本209份,在病毒核酸RT-PCR检测中的Ct值分布为10≤Ct<20有61例,20≤Ct<25有40例,25≤Ct<30有56例,30≤Ct<38有52例;另采集健康对照人群的401份阴性样本。
1.2 主要材料和试剂
评估试剂新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)为杭州协合医疗用品有限公司自制;对照试剂新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法)购于华大生物科技(武汉)有限公司和深圳华大基因股份有限公司;复核试剂新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)购于南京诺唯赞医疗科技有限公司;新冠灭活病毒培养物外购于常州欧吉生物科技有限公司,初始浓度为7.8h 107TCID50/mL(TCID50即50%组织培养感染剂量,median tissue culture infective dose)。
1.3 抗原检测试剂的制备
分别将鸡IgY、新冠抗体N-M1205与胶体金颗粒偶联在一起,用金标稀释液稀释胶体金-新冠抗体N-M1205和胶体金-鸡IgY,体积占比分别为50%和25%,用喷金机按2.0 μL/cm将溶液点在载体上,45 ℃烘干;将NC膜粘在PVC底板上,用划膜稀释液将新冠抗体N-M1204和羊抗鸡IgY分别配制成一定浓度的溶液,后用划膜仪将溶液均匀地喷在粘好的硝酸纤维素膜(NC膜)上,45 ℃烘干12~24 h;用样品垫处理液涂布处理玻璃纤维,37 ℃烘干12~24 h;将制备好的片材、金标垫、样品垫及吸水滤纸组装,用切条机切割成相应的宽度,装入检测卡,铝箔袋密封包装。
测试时将鼻拭子样本或鼻咽拭子插入装有抗原提取缓冲液的抗原提取管中,拭子头应在抗原提取缓冲液中旋转并混匀至少30 s,同时用手隔着管外壁挤压拭子头,将拭子头液体挤干,取出弃去拭子,加入3滴样本提取物至加样孔中,结果应在15~20 min。具体操作,如图1所示。
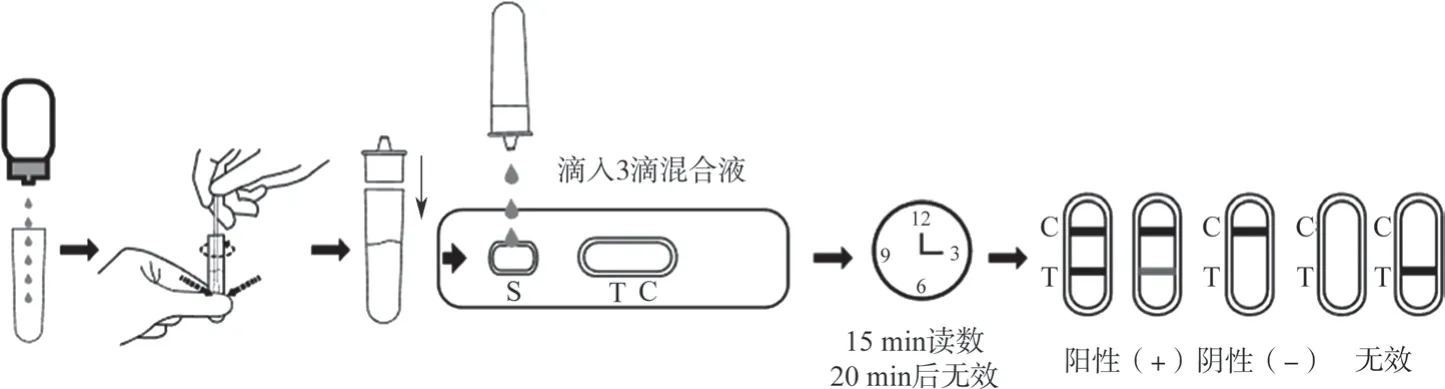
图1 抗原检测试剂操作示意Fig.1 Procedure for COVID-19 antigen test kit assay
1.4 检测试剂分析性能评估
根据LI等[15]和TAKEUCHI等[16]的研究,对检测试剂的分析灵敏度、分析特异性、精密度和钩状效应进行评估。
1.4.1 分析灵敏度(最低检测限)评价
将滴度为7.8h 107TCID50/mL的灭活病毒培养液依次稀释2万倍(3.90h 103TCID50/mL),4万倍(1.95h 103TCID50/mL)、8万倍(9.75h 102TCID50/mL)、16万倍(4.875h 102TCID50/mL)和32万倍(2.438h 102TCID50/mL)进行最低检出限检测,每种稀释度重复检测20次。
1.4.2 精密度评价
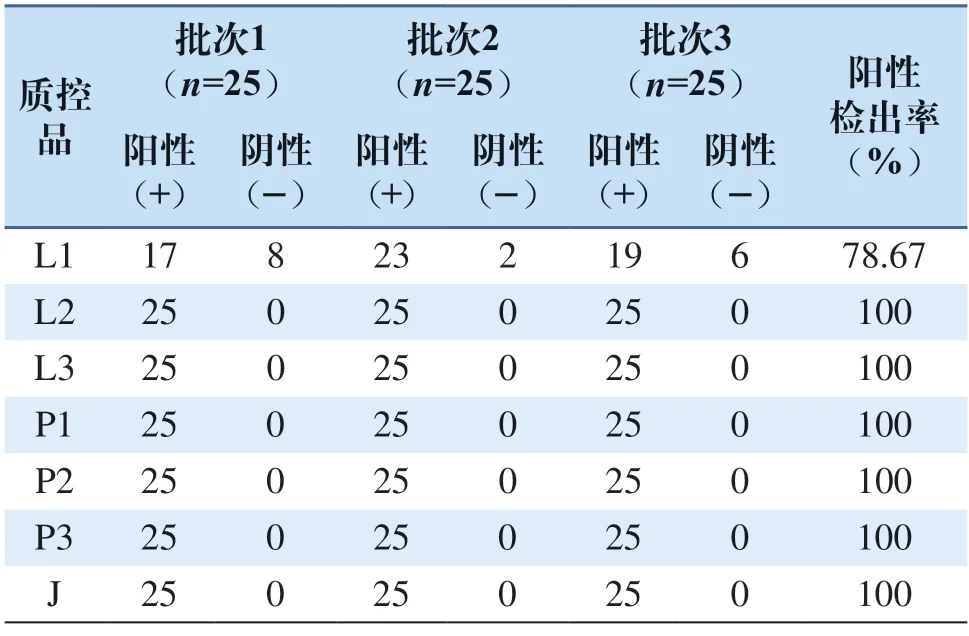
使用企业质控品测定3批产品,每个浓度质控品重复检测5次,连续检测5 d,共得到25个结果,计算25次检测结果的阴/阳性检出率。
企业质控品组成:企业阳性质控品(将一级企业标准品(COVID-19重组抗原)原液稀释为100万倍、20万倍、1000倍,作为企业阳性质控品P1~P3);企业检测限质控品L1~L3(将一级企业标准品原液稀释为2000万倍、200万倍、100万倍);企业重复性质控品(一级企业标准品原液稀释100万倍,作为企业重复性质控品J)。
1.4.3 分析特异性评价
将不同干扰物质用健康人鼻咽拭子洗脱液为阴性基质稀释相应质控品,得到3种不同干扰样本:①阴性质控加入不同干扰物质;②阳性质控P3加入不同干扰物质;③检测限质控L3加入不同的干扰物质,检测干扰物质对检测结果是否有影响。
对临床上能引起相同或相似症状的常见交叉反应病原微生物,在其医学相关水平进行交叉反应验证,通过在COVID-19灭活病毒培养液(9.75h 102TCID50/mL)中加入病原微生物制成阳性干扰,阴性样本加入病原微生物制成阴性干扰,对常见呼吸道病原体高浓度毒株进行测试,确认常见的病原微生物是否存在交叉反应。
1.4.4 钩状效应评价
将原始滴度为7.8h 107TCID50/mL的灭活病毒培养液,依次稀释400倍、4000倍、20万倍、200万倍,根据检测结果判断是否存在钩状效应。
1.4.5 稳定性评价
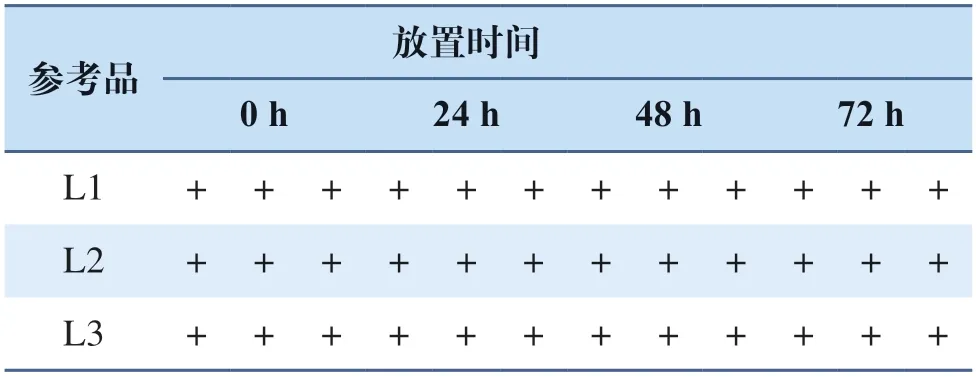
将试剂打开,取出其中的抗原提取缓冲液,打开盖子放置于室温下,用该缓冲液将P3配制成L1~L3浓度的标准品,分别放置0 h、24 h、48 h和72 h后检测。在每个时间点,使用3批产品进行检测,将每个结果与0 h进行比较。
1.5 临床性能评价
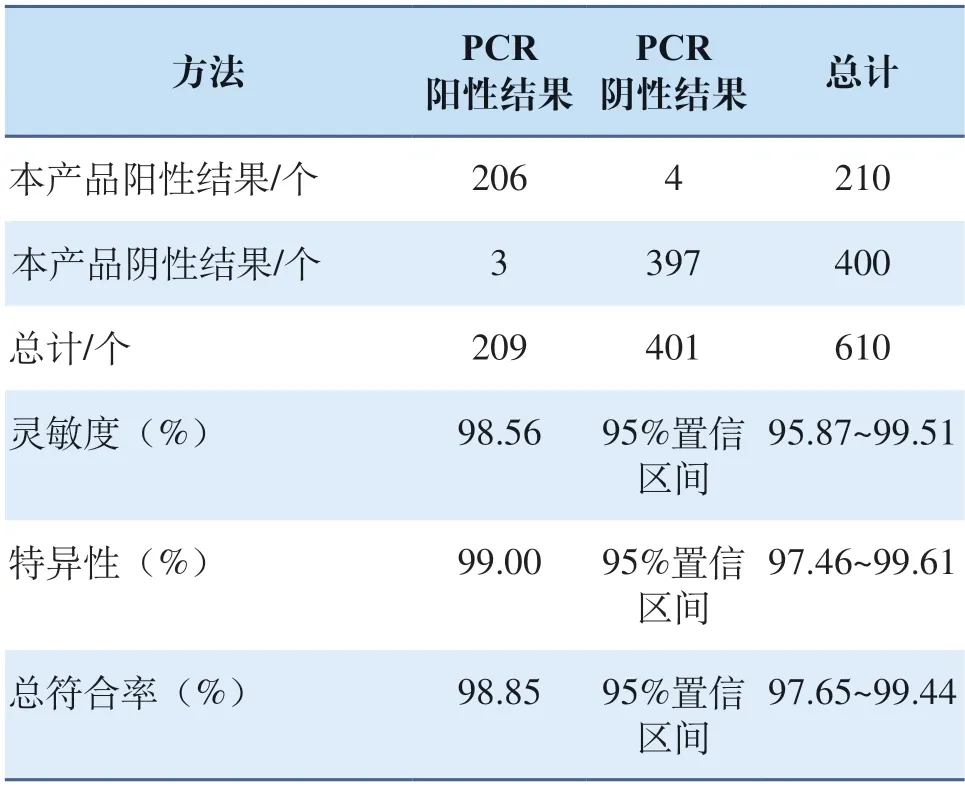
用iPonatic快速核酸检测系统及杭州协合医疗用品有限公司制备的抗原检测试剂盒同时取鼻咽拭子样本进行临床比对测试;按说明书用检验试剂检验标本,将检验结果记录在表中。将结果与RT-PCR检测比较,分析试剂临床检测的性能,包括灵敏度(包括不同Ct值的阳性样本的灵敏度)、特异性以及与RT-PCR的总符合率。
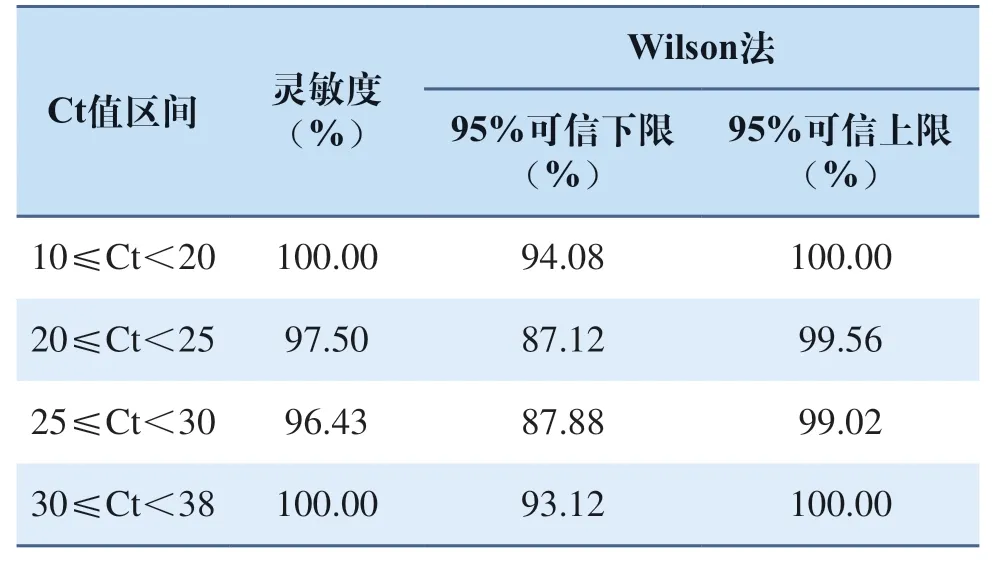
采用SPSS V23.0和Excel 2010对试剂盒的临床检测性能进行分析,计算Kappa (K)值,K≥0.75,具有高度的一致性;0.40 2.1.1 分析灵敏度(最低检测限) 热灭活的病毒培养液稀释到滴度为9.75h 102T C I D50/m L 时,所有检测结果均为阳性;再稀释至4.875h 102TCID50/mL时,仅有7次阳性结果,计算出阳性检出率为35%,病毒培养液稀释至滴度为2.438h 102TCID50/mL时,所有结果均为阴性(见表1)。根据检测结果判定试剂最低检测限为9.75h 102TCID50/mL。 表1 分析灵敏度测试结果Tab.1 Results of analysis sensitivity test 2.1.2 精密度 表2显示L1浓度时有部分检测结果为阴性,数量不大于测试总数的1/3,其余为阳性;检出限参考品L2~L3、重复性质控品J和阳性参考品P1~P3的阳性检出率均为100%,且条带结果显色均一,表明抗原检测试剂的精密度良好。 表2 精密度测试结果Tab.2 Results of precision test 2.1.3 药物和血液中若干物质的干扰试验结果 根据检测结果,2 mg/mL的血红蛋白和黏蛋白、5 mg/L人抗鼠抗体(HAMA)、10 mg/mL生物素、500 μg/mL黏液、120 μg/mL色甘酸钠、60 μg/mL盐酸羟甲唑啉、200 μg/mL的盐酸去氧肾上腺素和N-乙酰对氨基苯酚、3 μg/mL的庆大霉素、阿司匹林、布洛芬、吗啉盐酸盐、头孢氨苄、卡那霉素、四环素、氯霉素、红霉素、万古霉素、萘啶酸、氢化可的松、人胰岛素,以及30 μg/mL的β-丙内酯均不会影响本品的检测结果。 2.1.4 呼吸道疾病病原体干扰试验结果(分析特异性) COVID-19是一种由冠状病毒引起的呼吸道疾病,它的症状类似其他类型的呼吸道疾病和流感。为了确认产品特异性,使用29种常见交叉反应病原微生物进行检测。结果显示对下述的病原微生物无交叉反应(见表3),证明试剂特异性较好。 表3 常见病原微生物的干扰Tab.3 Interference from common pathogenic microorganisms 2.1.5 试剂稳定性 表4显示,抗原提取缓冲液室温放置24 h、48 h和72 h后三个浓度的参考品检测结果均为阳性,与0 h相比无明显差异。 表4 试剂稳定性验证结果Tab.4 Results of reagent stability verification 2.1.6 钩状效应 当病毒培养液滴度达到7.8h 107TCID50/mL时,未观察到高剂量钩状效应。相比初始浓度,原液稀释20万倍后条带颜色变弱;直至原液浓度稀释200万倍,试纸条带十分微弱,甚至无明显条带显现。高剂量钩状效应验证如图2所示。 图2 高剂量钩状效应验证Fig.2 High-dose hook effect validation 2.2.1 试剂盒的临床检测灵敏度、特异性及与RT-PCR结果的总符合率 本研究试剂盒临床检测的灵敏度和特异性样本总数为610个,其中209个为阳性,401个为阴性。与RT-PCR检测结果相比,本抗原检测有3例漏检样本和4例假阳性测试结果,临床统计结果如表5所示,该产品的灵敏度为98.56%(置信区间为95.87%~99.51%),特异性为99.00 %(置信区间为97.46%~99.61%),与RT-PCR结果的总符合率为98.85%(置信区间为97.65%~99.44%)。K值为0.9745,大于0.75,试验结果显示,本产品与新型冠状病毒核酸检测结果具有良好的一致性。基于胶体金法建立的新冠抗原检测试剂盒与核酸检测结果基本一致,临床评价良好,达到了预期的研究目的。 表5 临床检测性能评价Tab.5 Results of clinical performance evaluation 2.2.2 不同Ct值阳性标本的检测灵敏度 对不同C t 值阳性样本进行分层分析,显示10≤Ct<20有61例,占全部阳性样本的29.19%,试剂检测结果均为阳性,检测灵敏度为100.00%;20≤Ct<25有40例,占总阳性样本的19.14%,其中1例结果为阴性,检测灵敏度为97.50%;25≤Ct<30有56例,占总阳性样本的26.79%,其中2例结果为阴性,检测灵敏度为96.43%;30≤Ct<38有52例,占总阳性样本的24.88%,结果均为阳性,检测灵敏度为100%,结果表明该抗原检测试剂性能优越(见表6)。对抗原检测结果与核酸检测结果不一致的病例,用已上市的抗原试剂进行复核,结果与本公司试剂的检测结果一致。 表6 不同Ct值阳性标本的检测灵敏度Tab.6 Results of detection sensitivity of positive specimens with different Ct values 免疫层析法能够快速检测人体是否含有抗原或抗体,是现有核酸检测法良好的补充手段,该方法对临床实验室的操作要求更低,在基层实验室即可完成,而且对检验人员的要求也没有核酸检测那么高,简单培训即可操作[17-18]。由于低病毒载量可能导致假阴性,因此抗原检测试剂的分析性能评估是十分重要的步骤,试剂的精确度、灵敏度和特异性是基础[19]。本研究的目的是评估生产的抗原检测试剂盒诊断SARS-CoV-2感染(包括变异株)的分析敏感性和特异性。数据显示该抗原检测试剂的检测结果与PCR检测结果基本一致,临床评价良好。 分析特异性是指试剂盒对样品中的非特异性物质产生假阳性反应的可能性,有时也指与应该反应的物质不发生反应的可能性,即假阴性。同时,要识别可能引起类似临床症状的其他病毒的交叉干扰[20-21]。试验结果证明研究建立的抗原检测试剂性能良好,与29种常见呼吸道病原微生物均无交叉反应,分析敏感性和特异性表现优异。经验证,本抗原检测试剂提取液在开封三天内使用无差异,但考虑到使用时所处环境可能更加恶劣,特别是在室温高于30 ℃或高度潮湿的环境中,应尽快使用。总体来看,新型冠状病毒(2019-nCoV)检测试剂盒(胶体金法)与核酸检测结果一致性较高,按照Ct值分层,灵敏度相对较高;有一部分核酸检测结果为阳性,而抗原检测结果为阴性,分析其可能原因是用抗原检测试剂检测时,在检出限范围内检测结果呈阴性,是因为核酸比蛋白降解快,或者是核酸转录到一半时细胞破裂,此时蛋白组装未完成,其含量未达到检测试剂的检出限要求,因此核酸检测试剂能检测到,而抗原检测试剂无法准确检测。我们同时用已上市的抗原检测试剂检测样本,复检结果仍为阳性,也能说明其原因。 根据评估其检测结果具有指导意义[22],总体上能满足临床需求。抗原检测的主要优点是快速、易于解释、可居家自行操作。但本试剂也存在一些缺陷,只能进行定性检测且结果存在一定误差,有待今后进一步完善。 通过分析性能评估,本试剂的最低检出限为9.75h 102TCID50/mL;测试29种常见呼吸道病原体均无交叉反应。临床鼻咽拭子样本及健康人群鼻拭子样本测试,分析灵敏度为98.56%(置信区间95.87%~99.51%),分析特异性为99.00%(置信区间97.46%~99.61%),准确度为98.85%(置信区间97.65%~99.44%);一致性检验K值为0.9745。对不同Ct值阳性样本进行分层分析,各个层级内检测灵敏度优良。结果表明COVID-19抗原检测试剂检测灵敏度和特异性高,检测速度快,操作便携,可作为现有核酸检测法的补充手段,用于新型冠状病毒感染的早期筛查。2 结果
2.1 检测试剂的分析性能评估结果



2.2 临床检测性能评价
3 讨论
4 结论
