基于Logistic回归和人工神经网络构建老年脑卒中患者衰弱预测模型
2023-02-11张鑫宇张磊隋汝波
张鑫宇,张磊,隋汝波
(1.锦州医科大学 护理学院,辽宁 锦州 121001;2.锦州医科大学附属第一医院 神经内科,辽宁 锦州 121001)
衰弱是指老年人的生理储备功能降低或各种功能异常导致身体脆弱性增加、抗压能力下降的一种非特异性状态,容易造成跌倒、残疾、再入院等不良后果甚至可以导致死亡[1]。衰弱普遍存在于老年脑卒中患者中,发生率高达74.4%[2]。因此,早期发现衰弱并进行针对性干预,有助于减少并且延缓其发生和发展,避免相关不良结局。我国对老年脑卒中患者衰弱的研究仅限于现状调查,尚未针对其构建可靠的衰弱风险识别工具。然而,在精准医疗时代,预测模型可以利用临床收集的各种信息,直观地展示某种疾病发生的概率,并对疾病进行预测。Logistic 回归模型普遍用于筛查疾病的风险因素,并且通过绘制列线图使模型更加直观实用。神经网络模型处理不确定信息的能力很强,针对临床数据缺失患者的预测具有独特优势。故本研究通过对老年脑卒中患者衰弱影响因素的探讨,采用Logistic回归和人工神经网络的方法建立风险预测模型,为早期识别并预防老年脑卒中患者衰弱的发生提供依据。
1 对象与方法
1.1 研究对象 2021年3月至2022年5月,采用便利抽样方法选取锦州市某医院收治的脑卒中患者为研究对象。纳入标准:(1)符合全国第4届脑血管病诊断标准[3]并经颅脑CT或核磁共振成像确诊为脑卒中;(2)年龄≥60 岁;(3)意识清醒。排除标准:(1)既往患有精神病;(2)有器官衰竭、癌症等重大疾病;(3)沟通困难,不能配合完成调查者。采用 Logistics自变量事件数(events per variable,EPV)法计算样本量,即纳入最终模型的每个预测因子需至少10例阳性数[4]。本研究的 Logistic模型最终纳入了6个预测因子,则至少需要存在衰弱的脑卒中患者60人,根据老年脑卒中患者衰弱发生率为74.40%,样本量最小为81例,最终纳入532例。按7∶3比例,建模组372例,验证组160例。
1.2 方法
1.2.1 调查工具 通过查阅国内外相关文献并咨询临床专家后,设计本研究的一般资料调查问卷,并确定本研究使用的量表。
1.2.1.1 一般资料调查问卷 包括性别、年龄、民族、婚姻状况、居住情况等。
1.2.1.2 老年人衰弱评估量表(elderly frailty assessment scale,EFAS) 该量表由Gobbens等[5]于2010年编制,李菲等[6]进行汉化,用于评估老年人的衰弱状况,包括生理、心理、社会、认知、环境5个维度,共有26个条目。采用二分类计分方法,选择“是/能”得1分,选择“否”不得分,总分0~26分,≥9 分表示存在衰弱。该量表Cronbach’s α系数为0.846。
1.2.1.3 工具性日常生活能力量表(instrumental activities of daily living scale,IADL) 该量表由 Lawton等[7]于1969年编制,用于测量个体独立生活能力,包括使用电话、购物、备餐、整理家务、洗衣、乘坐交通工具、服药及理财8个条目,总分0~8分,≤7分为功能受损,该量表的Cronbach’s α系数为0.838。
1.2.1.4 匹兹堡睡眠质量指数量表匹兹堡睡眠质量指数(Pittsburgh sleep quality index,PSQI) 由Buysse等[8]于1989年编制,用于评估个体的睡眠情况,包括睡眠质量、入睡时间、睡眠时间、睡眠效率、睡眠障碍、催眠药物、日间功能障碍7个部分,采用Likert 4级评分法,评分>7分表示存在睡眠障碍,该量表Cronbach’s α系数为0.726。
1.2.2 资料收集 本研究已通过医院伦理委员会批准(202228),在神经内科管理者的同意和配合下,向患者及其家属说明了本研究的目的、意义,并征得他们的知情同意,现场发放问卷收集资料,由研究者及其家属协助不能独立完成的患者进行填写。共发放550份问卷,回收问卷550份,其中有效问卷532份,问卷的有效回收率为96.7%。
1.2.3 统计学处理 采用SPSS 26.0统计软件,计数资料以例数和百分比表示,采用χ2检验和多因素Logistic回归分析筛选出影响患者衰弱的独立危险因素,用R 4.1.3软件绘制列线图将Logistic回归模型进行可视化,借助神经网络中的多层感知器构建神经网络预测模型,采用受试者工作曲线(receiver operating characteristic curve,ROC)评价模型的预测能力,并进行模型内部和外部验证。以P<0.05或P<0.01为差异有统计学意义。
2 结果
2.1 研究对象一般资料 532名老年脑卒中患者中,男307名、女225名;年龄60~69岁183名、70~79岁203名、≥80岁146名;汉族208名;未婚/离异/丧偶者220名;独居者281名。203名(38.16%)患者处于脑卒中急性期,190(35.71%)患者为首发脑卒中;其中249名患者(46.80%)发生衰弱,建模组176名(47.31%),验证组73名(45.63%),两组衰弱检出率差异无统计学意义。
2.2 建模组老年脑卒中患者衰弱的单因素分析 单因素分析显示,老年脑卒中患者在年龄、独居、吸烟、体育锻炼、高血压、糖尿病、首发脑卒中、睡眠障碍、跌倒史、工具性日常生活能力上的差异均有统计学意义(均P<0.05),详细情况见表1。
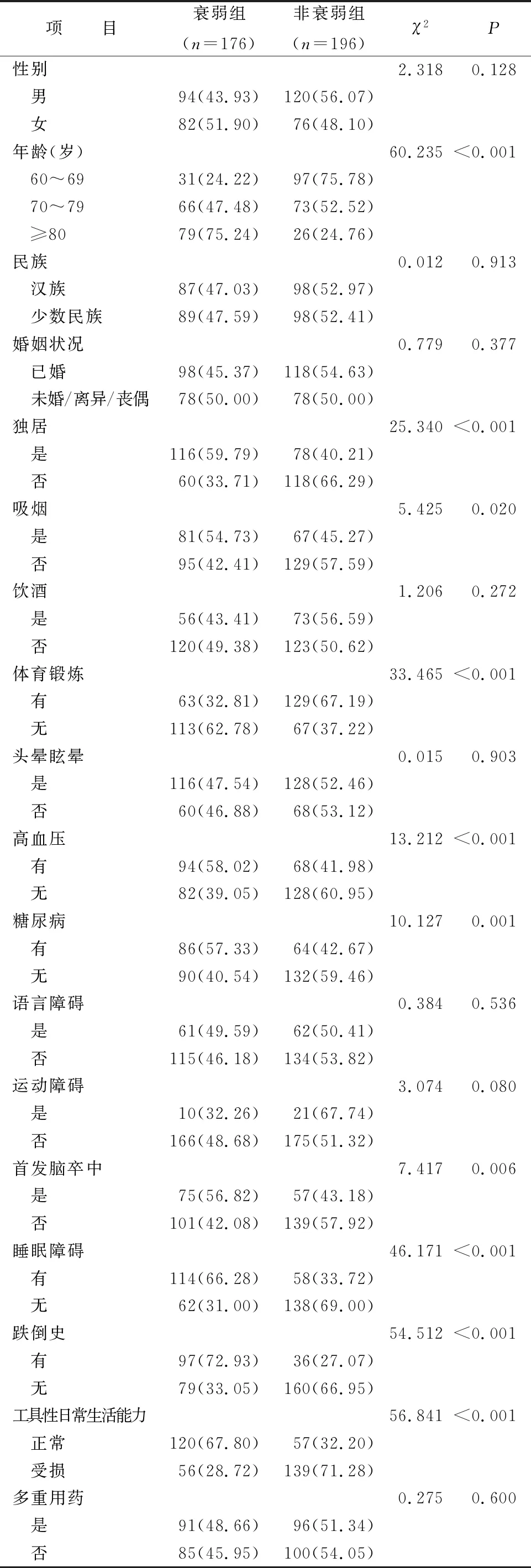
表1 建模组老年脑卒中患者衰弱的单因素分析结果[N=372,n(%)]
2.3 建模组老年脑卒中患者衰弱的多因素分析 以老年脑卒中患者是否发生衰弱为自变量,单因素分析中有统计学意义的项目为因变量进行多因素 Logistic 回归分析。多因素分析结果显示,年龄≥80岁(OR=8.407)、睡眠障碍(OR=5.244)、工具性日常生活能力受损(OR=5.166)、跌倒史(OR=5.067)、独居(OR=4.928)为老年脑卒中患者发生衰弱的独立风险因素,体育锻炼为保护因素(OR=0.338),见表2。
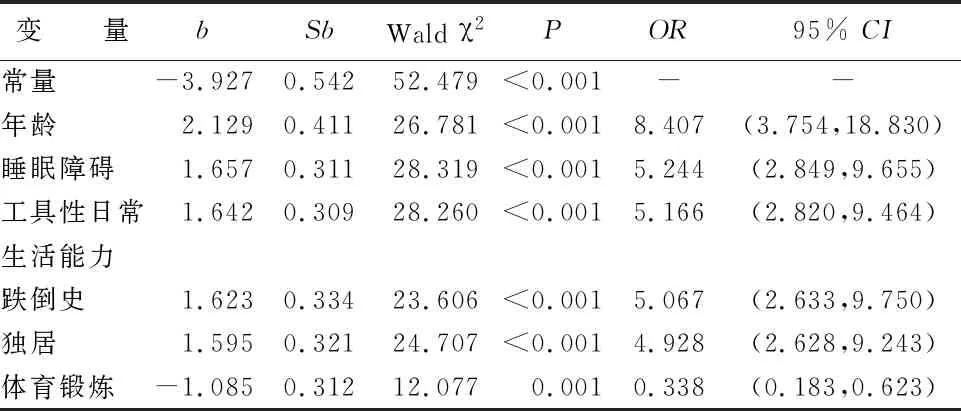
表2 老年脑卒中患者衰弱的多因素分析(n=372)
2.4 老年脑卒中患者衰弱风险预测模型的构建
2.4.1 老年脑卒中患者衰弱风险预测的列线图模型 基于Logistic回归模型:Z=-3.927+2.129×年龄≥80岁+1.657×睡眠障碍(有)+1.642×工具性日常生活能力(受损)+1.623×跌倒史(有)+1.595×独居(是)-1.085×体育锻炼(有),利用R软件构建列线图将其可视化,见图 1。

图1 老年脑卒中患者衰弱风险预测的列线图模型
列线图中每一个危险因素的具体情况对应相应的分值,将模型中6项指标的分值相加后得到总分,然后在所得总分的位置向下画垂直线,垂直线与“衰弱发生概率”坐标交点的位置所对应的数值即为老年脑卒中患者衰弱风险。
2.4.2 神经网络模型 对多因素Logistic回归分析筛选出的年龄、睡眠障碍、工具性日常生活能力、跌倒史、独居、体育锻炼6个研究变量进行赋值,借助神经网络多层感知器模块依次输入作为模型的输入神经元,隐藏层的神经元个数由系统自行设计,将老年脑卒中患者是否发生衰弱作为输出神经元,最终得到结构为:输入层( 13个神经元) ,1 层隐藏层(7个神经元) ,输出层(2个神经元) 的神经网络模型,见图2。

图2 神经网络模型
模型得出各因变量正态化重要性排序如下:年龄>睡眠障碍>工具性日常生活能力>跌倒史>独居>体育锻炼。
2.5 老年脑卒中患者衰弱风险预测模型的验证 根据模型所得的预测变量作为测试变量,将老年脑卒中患者发生衰弱作为状态变量进行ROC曲线绘制。建模组列线图模型、神经网络模型的ROC曲线的AUC值分别为0.908、0.904,敏感度、特异度分别为82.02%、83.04%、84.54%、83.08%,见图3、图4。验证组两模型ROC曲线的AUC值分别为0.923、0.916,敏感度、特异度分别为88.24%、81.01%、85.87%、88.89%,表明两模型预测效能较好。
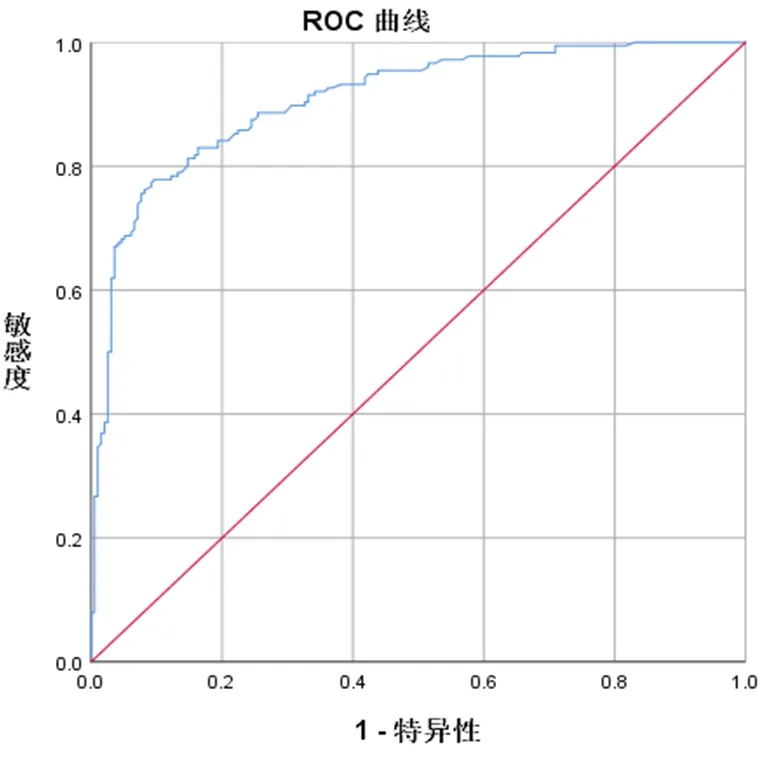
图3 列线图模型ROC曲线
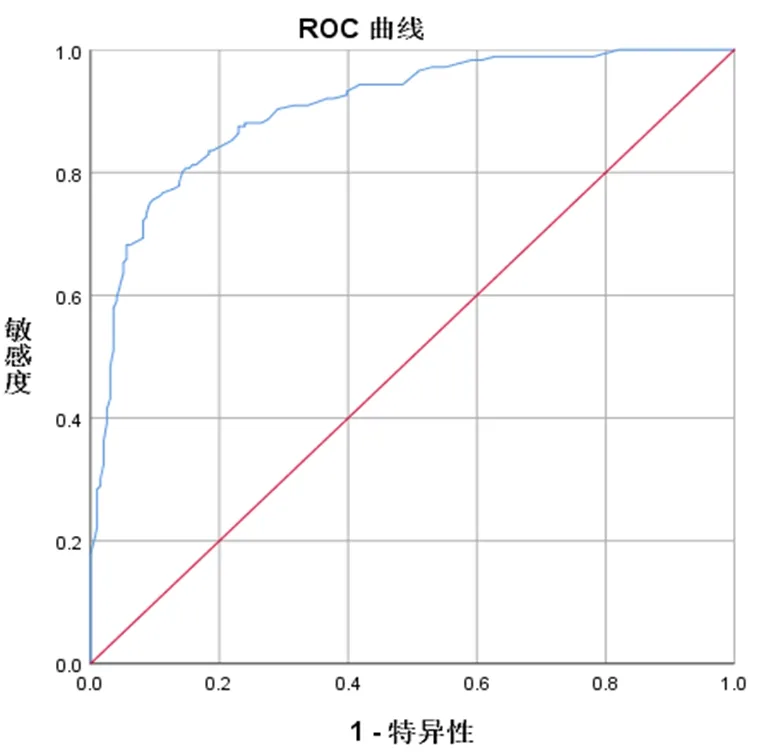
图4 神经网络模型ROC曲线
3 讨论
3.1 老年脑卒中患者衰弱现状 老年脑卒中患者由于多种慢性疾病和机体退行性变化引起易损性增加进而发展为衰弱,其核心是生理功能下降,微弱的外界刺激即可导致不良的临床事件。相关报道显示,超过65岁的老年人衰弱发生率在10%左右,而80岁的老年人衰弱发生率已达30%以上[9]。本研究老年脑卒中患者衰弱发生率为47.3%,高于前两项研究结果,并且纳入本研究的研究对象年龄均在60岁以上,这就表明患脑卒中的老年人更易出现衰弱。赵佳琪[2]在老年脑卒中患者衰弱与抑郁的两者相关性的研究中得出老年脑卒中患者衰弱发生率为74.4%,明显高于本研究结果,可能与其研究中老年人平均年龄较大有关。因此,定期运用准确可靠的工具对老年脑卒中患者进行衰弱筛查至关重要,医护人员应在积极治疗脑卒中的同时,对存在衰弱的脑卒中患者给予一定的宣教与干预,提高其生活质量。
3.2 影响衰弱的独立危险因素分析
3.2.1 年龄 本研究发现,≥80岁的脑卒中患者发生衰弱的风险是对照组的8.407倍。随着患者年龄增加其衰弱发生的风险也增加,与既往研究[10-11]的结果相似,但在性别方面,国内外学者得出的结论略有差异,可能与老年人生活方式差异有关。脑卒中患者年龄越大机体不可避免地会出现退行性变化,加之体内激素失调、生理储备下降等,使身体不能及时发现外界不良刺激并进行有效抵抗,从而发生衰弱[12]。由此提示医护人员应根据衰弱评估结果,为不同年龄段的脑卒中患者制订针对性衰弱干预管理方案,从而最大程度地延缓年龄增加所致的衰弱。
3.2.2 睡眠障碍 本研究发现,存在睡眠障碍的患者衰弱发生风险较高(OR=5.244)。脑卒中患者睡眠质量较差,睡眠障碍发生率达到70%以上[13]。既往研究[14]表明,存在睡眠障碍的老年人认知衰弱的发病风险较高(OR=3.258)。Ensrud 等[15]研究也证明了睡眠问题与衰弱发生是密切相关的。良好的睡眠质量,有助于个体保持正常认知,开展日常活动,保持健康心态。因此,改善脑卒中患者睡眠质量最重要的措施是改善他们的健康状况,建议患者健康、规律地生活,医护人员还应考虑年龄、身体状况、生活状况等因素,制定一套适合脑卒中患者睡眠障碍的干预措施。
3.2.3 工具性日常生活能力 本研究显示,IADL也是老年脑卒中患者衰弱的影响因素(OR=5.166)。衰弱介于健康和失能之间的一种状态,并且失能也是衰弱患者临床不良后果之一。IADL关注人在特定环境中自力更生的能力,是老年人独立生活和进行社会交往活动,包括去超市购物、乘坐交通工具等所必需的高级技能。本研究与王湾湾等[16]研究结果相类似,该研究认为IADL评分是老年住院患者发生衰弱的影响因素,国外学者[17]也证明了这一观点。衰弱老年人有较高的失能风险,反过来,失能的老年人衰弱发生率极高,因此医护人员应鼓励老年人适当活动、维持身体机能,常规评估IADL对早期发现衰弱具有很大的帮助。
3.2.4 跌倒史 本研究发现,曾有跌倒史的老年脑卒中患者衰弱发生风险将增加5.067倍,说明跌倒与脑卒中患者衰弱的发生也密切相关,与既往研究[18]结果相一致(OR=18.32)。脑卒中患者身体各器官功能下降,抵抗外界压力的能力减弱,同时伴有身体平衡能力下降,促进了衰弱的发生和发展。相关指南[19]推荐65岁以上的老年人每周进行两个半小时的中等强度运动,运动不仅可以改善患者的中枢神经系统、运动系统等系统的功能,还可以改善身体机能和活动能力,有助于缓解肌肉减少症,降低跌倒的发生率,进而降低衰弱发生率。
3.2.5 独居 本研究显示,独居的老年脑卒中患者发生衰弱的风险是非独居者的4.928倍,说明独居也是老年脑卒中患者发生衰弱的影响因素,略高于Woo等[20]的研究结果(OR=1.53),这可能与国内外文化背景、家庭结构不同有关。作为老年人身心健康的主要影响因素,独居老人缺乏家人陪伴,容易产生孤独紧张等情绪且缺乏安全感,进而丧失了康复的信心,在一定程度上促使了衰弱的发生。因此,对于无家属陪伴的脑卒中患者,一方面应注重培养其自我护理能力,帮助其建立健康的生活模式;另一方面可提醒家属多关注陪伴患者,并根据实际情况请陪护照料等,以促进患者身心康复。
3.2.6 体育锻炼 本研究表明,体育锻炼是老年脑卒中患者发生衰弱的保护因素,即参加体育锻炼,会降低脑卒中患者衰弱发生率,与既往研究[21]结果相一致(OR=0.338)。究其原因,体育锻炼既能提升脑卒中患者健康状况,强化身体素质,改善睡眠质量,调节平衡系统,又能丰富患者的日常生活、促进身心的和谐发展。因此,医护人员应根据患者的年龄、身体情况、运动习惯等,制定循序渐进的运动计划,这样对老年脑卒中患者增强免疫力,改善健康,延缓衰弱具有重要意义。
3.3 老年脑卒中患者衰弱风险预测模型预测效果理想 本研究通过Logistic回归和人工神经网络两种统计学方法,构建的脑卒中患者衰弱的列线图模型和神经网络模型,建模组和验证组的灵敏度、特异度较高,ROC曲线下面积均大于0.90,表明模型预测效果理想,有利于护理人员早期筛查出衰弱高风险人群。
4 小结
本研究显示,老年脑卒中患者衰弱检出率较高,在纳入本研究衰弱风险预测模型的变量中,高龄、睡眠障碍、工具性日常生活能力受损、跌倒史、独居为老年脑卒中患者发生衰弱的独立风险因素,体育锻炼为老年脑卒中患者发生衰弱的保护因素。因此,医护人员应针对老年脑卒中患者衰弱的影响因素进行早期评估及筛查,并加强知识宣教以及指导患者运动锻炼,制定专业、安全、有效的干预方案,降低老年脑卒中患者衰弱的发生概率。目前,大家已经普遍认可神经网络的预测能力,但预测模型中各自变量对因变量影响的医学解释尚不明确。其次,本研究所纳入的脑卒中患者仅为本院患者,未来应该进行多中心、多区域的大样本量研究,不断调整使其更精确、更符合临床,以期在脑卒中患者中广泛使用。
