层叠烧结制备多孔钛合金及生物相容性研究
2023-02-11张云龙李若琳
张云龙 李若琳
(江苏理工学院 材料工程学院,江苏 常州 213001)
生物相容性是生物医用材料的重要指标,指的是材料在一段时间内充分发挥其功能而不对植入部位或附近组织和器官产生不利影响的能力[1]。钛及钛合金是生物惰性材料,耐所有体液和组织的腐蚀,钛植入物与宿主组织和骨骼的物理附着率很高,不易引起人体的排异反应。在氧化环境中,钛表面自发形成一层薄而粘接的TiO2层,具有诱导体液中钙、磷离子生成磷灰石的能力,表现出一定的生物活性,使其具有良好的生物相容性和耐腐蚀性[2]。凭借以上特性以及轻质且优良的力学性能,钛及钛合金在过去的几十年里成为人工关节、牙种植体、脊柱矫形内固定系统、髓内钉等人体硬组织替代物和修复物的首选材料[3]。
虽然医用钛合金已成为骨科、齿科和心血管等植介入物或器械用主要材料,但在应用中也暴露出了一些问题,其中最为关键的是钛合金与人骨的弹性模量不匹配,植入后产生应力屏蔽,导致植入体的松动、脱落等。合金化是降低应力屏蔽的有效方法之一,通过在钛合金中加入Ta、Nb、Zr、Sn等β相稳定元素,在组织中引入β相以降低弹性模量[4]。据报道,经过不同热处理获得的β钛合金的杨氏模量可从110 GPa降低至42 GPa[5]。另一种备受关注的方法是多孔化,多孔化不仅可以模仿天然骨的结构,还可以促进细胞增殖进入孔隙,为药物或蛋白质传递提供空间,实现结构功能一体化[6]。多孔钛的制备方法有很多,大体可分为粉末冶金法和化学合成法两类:粉末冶金法包括压制成型、无压成型、造孔剂法、浆料成型以及粉末床激光/电子束增材制造等;化学合成法包括反应烧结、燃烧合成、热还原以及去合金法等[7]。粉末烧结制备的多孔钛力学性能较差,钛纤维烧结法制备的多孔钛弹性模量较低,且孔隙形状和尺寸难以控制[8]。3D打印技术可以制造具有复杂内部结构的多孔钛零件,但在打印时金属粉末的氮氧含量显著增加,导致零件的疲劳性能降低[9- 10]。钛网层叠烧结是一种较为简便且可设计性高的方法,通过控制钛网孔径(目数)、层叠方式、压力可以调整烧结实体的孔隙率,实现对力学性能的调控[11]。
要实现植入体的长效安全性和功能性,钛合金的生物及力学相容性仍有待提高。多孔疏松结构是降低弹性模量的有效方法,但多孔化后可能对生物相容性有一定的影响。基于此,本文以常见的医用钛合金TC4(Ti- 6A1- 4V)网为原料,采用层叠烧结法制备多孔试样,对其显微结构进行表征,通过对比多孔和实体钛合金表面成骨细胞的黏附及铺展情况及后续的细胞毒性测试结果,研究了多孔钛合金表面的生物活性并探讨了其作用机制。
1 试验材料与方法
1.1 样品制备
试验材料选用纤维直径为150 μm的TC4钛合金网,化学成分为Ti- 6.2Al- 4.1V- 0.1Fe。首先将其用配比为1∶3∶7的酒精、硝酸、氢氟酸溶液进行酸洗,以去除纤维表面的油渍及缺陷,直至钛合金网表面呈现银白色金属光泽;随后,将TC4网裁剪成φ18 mm的圆片,放入丙酮中进行超声波清洗,空气中干燥后,将5个圆片放入台式电动压片机所配套的磨具内进行预压,压力为95 MPa,保压时间为80~120 s,所得样品高度约4 mm;最后,将装有试样的石英管置于真空固结设备,按图1(a)所示的升温曲线进行烧结,升温至1 100 ℃保温2 h,真空度保持在5×10- 3Pa。该升温曲线为经过多次试验所得的优选方案,能够获得表面质量和力学性能良好的多孔钛合金片状样品,如图1(b)所示。
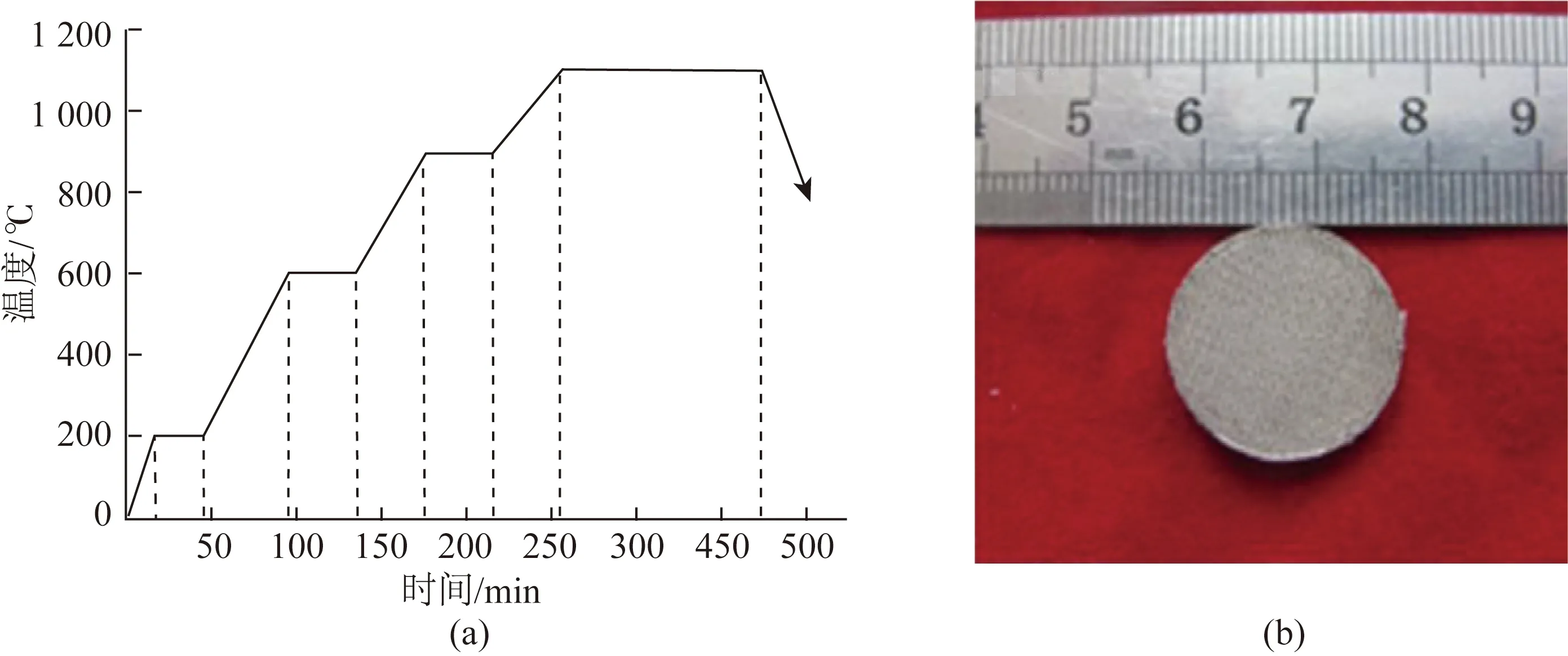
图1 多孔钛的烧结曲线(a)及其样品(b)Fig.1 Sintering curve of the porous titanium(a) and its sample(b)
1.2 体外细胞毒性试验
使用小鼠MC3T3- E1前成骨细胞进行体外细胞毒性试验,分别采用直接接触法和浸提液法检测细胞毒性。首先,将处理好的实体钛合金片和多孔钛合金试样用牛皮纸包裹,放在玻璃容器中,随后放入高压锅内(Sanyo Labo autoclave),120 ℃灭菌20 min,在医用干燥箱内烘干,取出后在超净台中冷却,静置过夜。为了降低试验误差,分别准备11个实体钛合金和多孔钛合金样品,其中3个进行浸提液试验,6个进行直接接触试验,2个用来观察细胞黏附行为。
次日,对超净台内所用物品进行紫外杀菌(30 min),将多孔和实体TC4支架试样分别放入24孔培养板内,其中实体和多孔钛合金两种浸提液分别种植3个孔,实体和多孔钛合金分别种植8个孔。浸提液法:浸提介质为含血清培养基,按照6 cm2/mL 的比例,在(37±1)℃条件下浸提(72±2)h;采用0.66 mL浸提液,将成骨细胞以2×104个/mL的密度种植于24孔板,连续培养5天。直接接触法:将实体和多孔钛试样置于24孔培养板内,每孔加入600 μL培养基,再将细胞以2×104个/mL的密度种植于试样表面,每孔200 μL细胞悬浮液,以空白组为对照,细胞贴壁长满后消化下来,未长满只需换液即可,连续培养5天后,对用于观察细胞黏附行为的样品进行固定处理,其余进行吸光度测试。细胞固定方法:将孔内未经消化的培养液吸出倒掉,加入95%乙醇(体积分数,下同)或10%甲醛固定10 min,用磷酸盐缓冲液冲洗两次,干燥后进行扫描电子显微镜(scanning electron microscope, SEM)观察。分别称取8 g NaCl、0.2 g KCl、1.42 g Na2HPO4和0.27 g KH2PO4配制1 000 mL磷酸盐缓冲液。
吸光度(optical density, OD)测试:细胞贴壁长满后将24孔板中培养液吸出倒掉,每孔加入200 μL胰酶,消化3 min后加入300 μL培养基/孔种植消化;吹匀均分到96孔板中(每孔125 μL),每孔加入100 μL培养基+20 μL MTT溶液(甲基噻唑基四唑5 g/L,溶于磷酸盐缓冲液,过滤后,-4 ℃避光保存,需提前配制);然后放入培养箱孵化4 h后,产生沉淀,吸去上清液,每孔加入150 μL的二甲基亚砜(DMSO)溶液,用Biorad 680型酶标仪(波长490 nm)测定各孔吸光度。根据测得的吸光度值计算细胞数量并作图。以细胞数量为横坐标,吸光度值为纵坐标绘制标准曲线。
2 结果与分析
2.1 多孔钛的显微组织
采用钛网层叠烧结制备的多孔钛的孔隙率约为50%,其微观结构如图2所示。钛合金网在压制过程中旋转一定角度后叠加,这种叠加方式可增大钛合金纤维之间的结合力。从图2可见,钛合金纤维之间基本以平行的方式排列,形成三维贯通规则孔隙,呈现规则的网孔结构,孔尺寸在一百到几百微米之间。多孔植入体植入人体后所发生的骨诱导是一个三维过程。目前普遍接受的是形成骨长入多孔钛孔隙尺寸大于100 μm即可。Parikh[12]研究指出,仅仅有孔隙对于形成骨内生长还远远不够,孔隙要相互贯通,且贯通孔尺寸大于100 μm。因此,本文所制备的多孔钛孔隙满足骨长入要求,且孔隙排列规则,有利于调控多孔钛的弹性模量和屈服强度,以适应不同环境的需要。
多孔钛合金支架在种植初期,由于表面有一层致密的TiO2钝化层,易与植入组织间形成一层纤维组织,植入人体后难以诱导磷酸盐沉积,因此在沉积磷酸盐涂层之前,需对多孔钛合金进行表面活化。钛合金纤维原料在拉拔过程中表面产生了大量裂纹,且在编织成钛网过程中表面黏附了大量油性润滑剂,因此需对钛合金网进行酸洗,并且酸洗可改善多孔钛合金的表面氧化层结构及表面粗糙度。图3为酸处理前后多孔钛合金表面SEM形貌。酸洗前多孔钛合金表面杂乱无规则,存在大量因纤维拉拔产生的裂纹、脱出颗粒等缺陷,不利于后续生物涂层的均匀附着,成为后续材料因涂层结合力差而失效及因纤维表面颗粒脱落而制毒等潜在危险因素。酸洗后多孔钛合金表面呈现规则的阶梯型层片结构,层片表面平整光滑,在无缺陷的前提下,层片结构可显著提高钛合金的表面粗糙度,增强了生物涂层的附着力和结合力,为后续表面改性提供良好的基础。酸洗还能够显著降低层叠烧结多孔钛的杨氏模量,而屈服强度变化不大[13]。

图3 酸洗前(a)、后(b、c) 多孔钛合金表面SEM形貌Fig.3 SEM morphologies of the surface of porous titanium alloy before(a) and after(b,c) pickling
2.2 多孔钛的生物相容性
图4(a)和图4(b)分别为装有实体和多孔TC4支架的24孔板底部细胞培养5天的形貌,图中黑色部分为实体和多孔钛合金支架。由图4(a)可以看出,细胞死亡较少,生长状态良好,已有部分细胞在孔板底部黏附和铺展。由图4(b)可知,细胞大量增殖,形态良好,在孔板底部黏附,铺展较充分。试验证明,多孔钛的浸出液无毒,且由于多孔钛特殊的多孔结构,培养液流动性更好,细胞增殖更多。但由于多孔钛不透光,细胞固定后才能观察到多孔钛表面黏附的细胞形态。图5为成骨细胞在多孔钛表面培养5天后的形貌。可见多孔钛表面有少量细胞黏附和铺展,并出现了跨纤维的孔内延伸生长,证明多孔钛合金无毒,且具有一定的生物相容性。
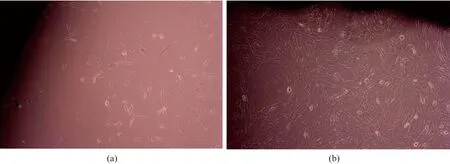
图4 装有实体(a)和多孔(b)TC4支架的24孔板底部细胞培养5天的形貌Fig.4 Micrographs of cells cultured for five days at the bottom of a 24- well plate containing solid(a) and porous TC4 scaffolds(b)

图5 成骨细胞在多孔钛合金表面培养5天后的黏附及铺展Fig.5 Adhesion and spreading of osteoblasts on the surface of porous titanium alloy after culturing for five days
显微镜观察发现,24孔板的对照孔内细胞培养5天后全部贴壁生长;多孔钛合金浸提液种植的3个孔中只有1个孔内细胞生长良好,细胞贴壁率可达85%以上,其余2个孔内细胞贴壁率只有35%~45%;而装有实体钛合金浸提液的3个孔内细胞贴壁情况均较差,细胞贴壁率只有15%~30%,说明钛合金支架的浸提液不利于小鼠前成骨细胞的生长和铺展。
图6为实体和多孔钛合金分别种植的6个孔的吸光度测试结果,每个孔内细胞数量均低于不放钛合金支架的6个孔板(空白对照组),且差异显著。以对照组细胞存活率为100%,计算得到实体钛合金浸提液孔、多孔钛合金浸提液孔、实体钛合金、多孔钛合金的细胞存活率分别为24.74%、43.05%、12.77%、28.60%。与实体钛合金相比,多孔钛合金的直接接触孔和浸提液孔内的细胞存活率即细胞数量相对较高,但差异不显著。实体和多孔钛合金种植的直接接触孔内细胞数量均低于浸提液孔内细胞数量,差异也不显著。4种样品的重复试验孔内细胞的生长和铺展情况均有差异,相应的吸光度差异也较大。试验证明,相较实体钛合金,多孔钛合金具有更好的生物相容性。

图6 吸光度- 细胞数量标准曲线(a)与各样品中细胞数量(b)Fig.6 OD standard curve against cell number (a) and cell number in each sample(b)
由于多孔钛合金特殊的三维贯通孔隙结构,培养基具有良好的流动性,并且钛合金纤维大大增加了细胞可生长和铺展的面积,更有利于细胞的黏附和增殖,钛合金纤维的直径越小,细胞越易出现跨纤维黏附生长[14]。而实体钛合金完全占据孔板底部,细胞的生长和铺展面积受限,培养液流动性差,因此细胞的铺展和增殖较少。
3 结论
通过层叠烧结法制备的多孔钛合金呈现规则的网孔结构,孔隙尺寸在一百到几百微米之间,满足骨长入要求。酸洗显著提高了钛合金表面粗糙度,增强了生物涂层的附着力和结合力。细胞毒性试验证明,多孔钛合金无毒,较实体钛合金具有更高的细胞存活率,即具有更好的生物相容性。
