万古霉素菌渣生物炭的制备及特性研究
2023-02-10马雅怡黄朝晖刘秋新陈黎
马雅怡 黄朝晖 刘秋新 陈黎
(1.海南热带海洋学院,海南三亚572000;2.武汉城市学院,湖北 武汉 430083)
0 引言
我国是抗生素生产大国且制药企业数量繁多,据统计我国每年约生产抗生素24.8万t,抗生素菌渣年产130万t,约占全球生产总量的70%,人均使用量也稳居世界第一[1]。2016年,利用生物技术生产生物化学药品、基因工程药物工程中的蒸馏及反应残渣(包含抗生素菌渣)危险废物属性进一步被确定为HW02医药废物类。由于多数制药企业规模较小,部分企业管理能力较差,产生的大量抗生素菌渣缺乏有效的科学处理。抗生素的不科学处理将导致严重后果[2]。因此,众多企业面临着如何实现抗生素菌渣合理安全处理与资源化这一难题。
国内外的研究主要集中于抗生素菌渣热解气化反应机理、各种因素对于热解气化过程的影响、污染物生成、转化、迁移与释放规律以及热解气化与其他技术的耦合等。本研究选用某制药厂发酵万古霉素湿菌渣(WG)为研究对象,对万古霉素菌渣(WG)制备生物炭进行研究,以了解其表面形貌特征,进一步拓宽抗生素菌渣生物炭在重金属废水处理中的应用;采用高效液相色谱仪、元素分析仪、扫描电子显微镜、傅里叶红外光谱仪、氮气吸脱附仪、同步热分析仪等多种现代分析技术对WG和由WG制备的生物炭的组成结构和结构特征进行分析,为抗生素菌渣的无害化处理和资源化利用提供技术支持和理论依据。
1 材料与方法
1.1 供试材料
本研究选用样品取自珠海市某制药厂万古霉素药物生产过程中产生的菌渣,首先将菌渣放入80℃烘箱内干燥24 h,将干燥后的菌渣研磨筛分,过60目尼龙筛,再将样品进行充分混合,以保证原料的均匀性,然后密封保存备用。
1.2 实验方法
1.2.1 菌渣生物炭的制备
取一定量备用的万古霉素菌渣放于100 mL瓷坩埚中,密封,于箱式马弗炉(KSL-1200X,中国合肥科晶材料技术有限公司)中热解,马弗炉设置10℃/min的升温速度,控制热解时间为1h。热解温度是一个很重要的参数,热化学变化比如从生物质中无组织相释放的挥发物和可冷凝的化合物都和温度有关,所以热解温度设置4个水平,分别为400、500、600、700℃。热解完成后关闭箱式马弗炉,降至室温后取出坩埚,密封保存备用。将菌渣在不同热解温度下热解时间为1 h时,所制备的生物炭标记为TB-400℃-1h,TB-500℃-1h,TB-600℃-1h和TB-700℃-1h。
1.2.2 材料的表征
采用元素分析仪(Vario EL CUBE型,德国Elementar公司)和傅里叶红外光谱分析仪(Fourier transform infrared spectrometer,FTIR)用于C、N、H、S、O元素和菌渣炭表面的官能团分析;采用场发射扫描电子显微镜(Sigma,Zeiss,Germany)对菌渣炭的表面形貌进行观察,氮气吸脱附仪(Micromeritics Tristar 3000 system,USA)用于表征材料的物理吸附性能及孔性质,在N2气氛中以40 mL/min的气流率和10℃/min的升温速度升至设定速度,同步热分析仪(STA449F3型,德国NETZSCH公司):测定各样品的TG-DTG谱图。
2 实验与分析
2.1 C、N、H、S、O元素分析
由菌渣制备的生物炭经烘箱干燥至恒重,C、N、H、S、O采用元素分析仪测定。万古霉素菌渣及菌渣在不同温度下制备生物炭的结果如表1所示。从表1可知,WG热解后的C含量比热解前大,且C含量都在60%以上,表明炭化程度加强,热解后菌渣生物炭中的C—H、C—O键断裂,H、O元素从生物炭中分离出来以气体或蒸汽的形式丧失,C元0素越来越富集,这与文献报道一致。菌渣热解前后H含量伴随温度的升高不断降低,是因为热解过程中它们以小分子有机物和H2O的形式析出。H/C可以表征生物的芳香性,菌渣热解后,H/C比值均下降,这说明热解后生物芳香性增强,生物炭越稳定,因为在热解过程中炭会发生环缩聚和再固化,脂肪族化合物会转化为芳香族化合物。O/C代表生物炭的亲水性和极性,O/C越高说明亲水性和极性越强,随着温度的升高,O/C下降,说明温度升高,亲水性和极性减弱,生物炭稳定性增强[3]。另外,WG制得的生物炭中N元素、S元素含量随着温度的升高先减小后增大,这说明生物炭中的N、S元素的含量的与不同热解温度没有明显变化关系。
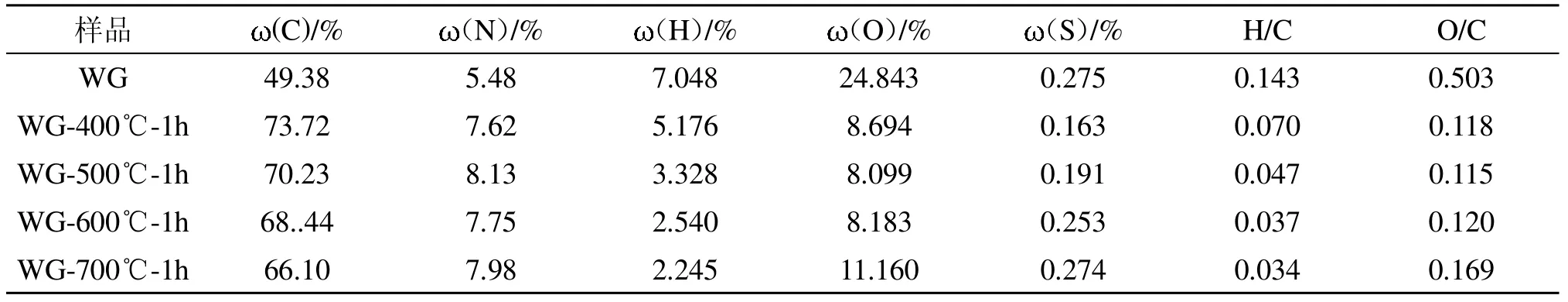
表1万古霉素菌渣以及菌渣在不同温度下制备生物炭元素分析结果
2.2 扫描电子显微镜分析(SEM分析)
利用扫描电子显微镜可以直观地分析活性炭成炭颗粒的大小、颗粒结合程度、孔分布情况和粗糙度等物理特征。取适量最佳条件下制得的万古霉素菌渣和菌渣在不同热解温度下所制备的生物炭固定在样品台先进行喷金处理,再做扫描电子显微镜分析。图1为菌渣和菌渣生物炭表面5 000倍的扫描电镜图,由图1(a)—(e)可以看出万古霉素菌渣表面凹凸不平,表面形状具有不均匀性,孔径大小不是很均匀,且随着温度的升高孔的数量增加,孔径增加,主要空隙从微孔和中孔变为大孔,且大孔中还分布和镶嵌着微孔和中孔,孔径分布也相对集中,孔的结构也更加规则,这说明随着热解温度的增加更有利于孔隙结构的增加,这种结构可有效提高活性炭的比表面积和吸附性能[4]。

图1 WG及WG在不同温度下制备的生物炭的SEM图(5 000倍)
2.3 红外光谱分析
众所周知,红外光谱可以作为鉴别氢键相互作用的方法,依据对红外光谱图吸收带的分析,可从中了解菌渣中有机质的化学结构及其变化。如图2所示为不同热解温度下万古霉素菌渣的红外光谱图,由图谱分析可知菌渣热解后官能团变少,万古霉素菌渣炭在3 700~3 300 cm-1之间出现较宽的吸收峰,可归属为糖类、脂类或碳水化合物中结合水的羟基O—H的伸缩振动产生的吸收峰,且热解后羟基数量在减少,说明随着温度的升高结合水的脱离和氢键结合的羟基逐渐断裂[5],羟基的存在不利于芳香化合物的吸附,因芳香化合物的吸附主要受活性炭基面和吸附质芳香环之间的-色散相互作用支配,与石墨边沿键合的氧能束缚电子并将电子从基面电子体系中移走,使-相互作用变弱;在波数为3 100~2 750 cm-1的波峰代表烷烃中C—H(甲基—CH3和亚甲基—CH2)伸缩振动峰,热解后随着温度的升高不断减弱,说明随着温度的上升,烷烃基团不断减少,脂肪类化合物彻底挥发或分解,生物炭芳香性增强[6],从而提高抗生素菌渣生物炭的吸附性能。蛋白质是菌渣的主要成分之一,1 802.7 cm-1处的谱峰来自仲酰胺Ⅰ带,是C=O的伸缩振动引起的,在1627.9cm-1出现较强吸收峰,主要是由于C=C的伸缩振动;1 495.6 cm-1处的峰来自对称伸缩离子羧基—COO—,热解后该峰减弱,并在500℃、600℃和700℃时逐渐消失,这与热解过程中挥发分的析出有关;1 070.6 cm-1处的吸收主要产生于O—H的弯曲振动和C—O—C(纤维素等中存在)的伸缩振动。这些官能团在一定程度上增强了生物炭的吸附性能。

图2 不同热解温度下万古霉素菌渣的红外光谱图
2.4 热重-差热分析
将菌渣原样和在500℃热解后的样品,在80℃下烘干8 h作为样品原料,通入40 mL/min的氮气,以保持动态气氛,升温速率为50℃/min,升温至800℃。万古霉素菌渣原样的热重分析结果如图3(a)所示,在500℃高温下热解后的样品热重分析结果如图(b)所示。一般生物质的热解可以分为3个阶段:第1阶段为失水阶段;第2阶段主要是热解析出大量的挥发分,导致大量的失重;第3阶段主要是残余物质继续发生缓慢的热解[7]。
由图3(a)可以看出万古霉素菌渣原样的热解符合一般生物质热解的3个阶段。第1阶段为失水阶段,由于实验用万古霉素菌渣已经烘干24 h,因此含水率较低,在图中仅有一个较小的失重峰出现。在230~320℃左右失重明显,这是由于万古霉素菌渣内部的粗蛋白以及其他有机物在此温度段大量分解造成,含碳化合物的C—C键断裂,产生了CO2和CO[8],整个过程中,失重率为84.28%。图3(b)405~430℃左右出现第3个失重高峰,原因主要是菌渣中有机物含量比较高,残余的物质继续分解。而图3(b)中经过500℃高温热解的菌渣在50~100℃出现明显失重,此时有机物大量分解,在200~400℃出现较小失重,500~650℃出现明显失重,失重率比原菌渣小19.099%,与原菌渣比较,WG-500℃-1h生物炭在200~400℃和500~650℃的吸热峰没有原菌渣明显,是因为生物炭在制备过程中有机物分解而含量下降。
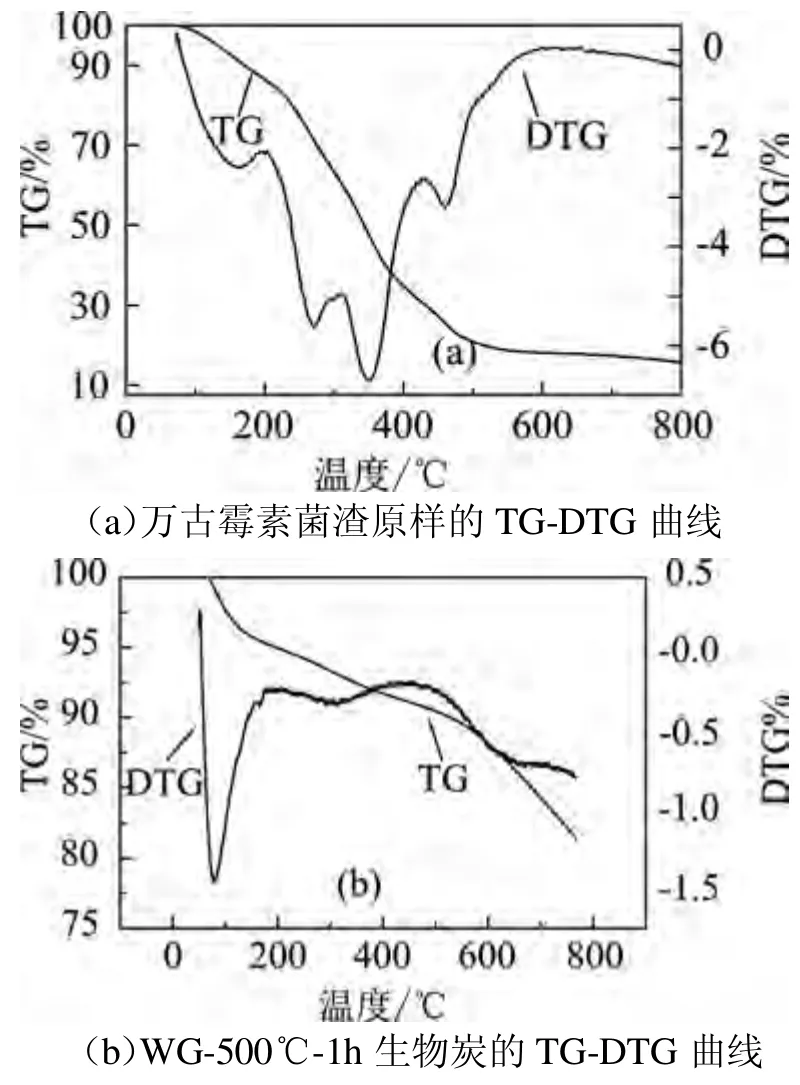
图3 万古霉素菌渣原样和500℃高温下热解后的样品的热重分析结果
2.5 菌渣的比表面积
从2.4节部分扫描电镜可以看出菌渣具有多孔结构。采用BET氮气吸附法测定菌渣的比表面积,不同热解温度下所制备生物炭的比表面积和孔径分析结果如表2。比较热解前后菌渣的比表面积,会发现热解后菌渣的比表面积增大,WG热解前的比表面积为0,而WG-700℃-1h的比表面积达到19.847 0 m2/g,菌渣的比表面积越大就越有利于吸附质的吸附。另外,热解前后万古霉素菌渣生物炭的孔径也在不断增大,据资料显示[9],它们的孔结构为中孔,中孔适合液体分子的吸附,因此由菌渣制备的生物炭孔结构和比表面积都有利于水中重金属离子和有机污染物的吸附。
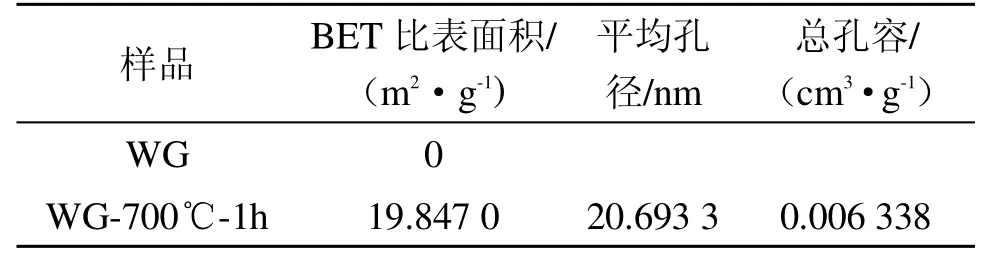
表2 万古霉素菌渣以及菌渣制备的生物炭的比表面积及孔径分析
3 菌渣生物炭吸附Pb(Ⅱ)的研究
3.1 实验方法
在250 mL锥形瓶中加入不同热解温度(WG-400℃-1h,WG-500℃-1h,WG-600℃-1h和WG-700℃-1h)下产生的生物炭0.2 g及Pb(Ⅱ)25 mg/L溶液50 mL,调节pH=4,盖紧盖子以防实验过程中体积变化。将其放入25℃的恒温水浴振荡器中,在转速为120 r/min下振荡3 h,过滤,取上清液,用原子分光光度计测定其中金属离子浓度。
3.2 不同吸附剂的影响
考察不同吸附剂对吸附Pb(Ⅱ)的影响,结果如表3所示,可以发现Pb(Ⅱ)的去除率随菌渣热解温度的的升高而增大,当热解温度为700℃时,对废水中重金属离子Pb(Ⅱ)去除率最大。WG-700℃-1h生物炭表面官能团丰富,比表面积和孔径相对较大,C元素相对较富集,有利于菌渣生物炭对重金属离子吸附的研究。

表3 不同热解温度下万古霉素菌渣对Pb(Ⅱ)的吸附
4 结论
本文借助多种鉴定物质组成和结构的分析检测方法如元素分析仪、红外光谱分析、扫描电镜、热重-差热分析氮气吸脱附等,确定了菌渣主要组成成分的含量和其结构特征,主要结论如下:
1)万古霉素菌渣生物炭热解前后C元素含量增大,H元素随温度的升高而减小,H/C下降,生物炭芳香性增强;O/C下降,温度升高,亲水性和极性减弱,生物炭稳定性增强。傅里叶红外光谱分析表明菌渣表面有丰富的官能团,有羟基、羧基、酯羰基等,这些官能团有利于生物炭对水中重金属离子的吸附。
2)热解后菌渣生物炭的表面有明显的多孔结构,而且菌渣热解后的比表面积和孔容也都比热解前高,有利于生物炭对水中重金属离子的吸附。
3)菌渣生物炭对重金属离子Pb(Ⅱ)的去除率随热解温度的升高而增大。
万古霉素菌渣表面特性受热解温度影响显著,菌渣生物炭表面含有丰富的官能团,比表面积和孔径相对较大,可用来用作生物吸附剂。本研究为菌渣生物炭吸附重金属和有机物污染物提供重要的理论依据。
