ACR TI-RADS联合微血流成像鉴别甲状腺结节良恶性的价值
2023-02-04苏泳安马海娇刘昕
苏泳安 马海娇 刘昕
随着超声仪器分辨率的增加,甲状腺结节的检出率显著提高[1]。2017年发布的ACR TI-RADS是基于二维超声图像的甲状腺结节风险分层系统,其根据结节的构成、回声、形状、边缘和局灶性强回声将每个结节赋予分值,为结节的管理提供了具体的建议[2],但该系统并未包含结节血流的相关信息,且诊断结节良恶性的效能相对较低[3-4]。由于特定的病理、生理基础,甲状腺良恶性结节在血流分布方面存在显著差异[5]。微血流成像(micro-flow imaging,MFI)技术采用新的多普勒算法,较传统的CDFI可更好地区分来自组织运动和血流的多普勒信号,从而检出低速血流[6]。本研究旨在探讨ACR TI-RADS联合MFI鉴别诊断甲状腺结节良恶性的应用价值。
资料与方法
一、临床资料
选取2021年10月至2022年10月于我院行超声检查并经病理证实的甲状腺实性结节患者97例(共97个结节),男21例,女76例;年龄20~77岁,平均(47.1±11.7)岁;结节最大径1.0~4.6 cm,平均(1.9±0.8)cm。纳入的97个甲状腺实性结节中,良性结节41个(良性组),包括结节性甲状腺肿35个,甲状腺滤泡性腺瘤4个,桥本甲状腺炎2个;恶性结节56个(恶性组),包括甲状腺乳头状癌51个(3个侵袭被膜),滤泡癌4个,髓样癌1个。纳入标准:①均完成二维超声和MFI检查,图像清晰并进行TI-RADS分类;②具有完整的病理结果。排除标准:缺乏病理结果或病理结果不明确者。本研究经我院医学伦理委员会批准,患者均知情同意。
二、仪器与方法
1.超声检查:使用Philips EPIQ 7彩色多普勒超声诊断仪,eL18-4探头,频率5~12 MHz;配备MFI软件。患者取仰卧位,充分暴露颈前区,首先行二维超声检查,观察并记录甲状腺结节的大小、部位、形状、边缘、构成、纵横比等;然后启动MFI软件对甲状腺结节进行检测,取样框大小应包含病灶,调整合适的标尺,以彩色增益增大至不出现彩色干扰为标准,记录结节的血流分布情况,全部图像均经录像记录存档供脱机分析。以上操作均由2名具有5年以上检查经验的主治超声医师采用盲法完成。
2.ACR TI-RADS分类标准:从结节的构成、回声、形状、边缘、局灶性强回声共5个方面对结节进行评分,分为5类:TIRADS 1类(0分)判为良性,2类(2分)判为不可疑,3类(3分)判为低度可疑恶性,4类(4~6分)判为中度可疑恶性,5类(≥7分)判为高度可疑恶性[2]。根据TI-RADS分类对结节进行穿刺或随访,其中1、2类结节无需进行穿刺和随访;3类结节中最大径≥2.5 cm者行穿刺,最大径1.5~2.5 cm者随访;4类结节中最大径≥1.5 cm者行穿刺,最大径1.0~1.5 cm者随访;5类结节中最大径≥1.0 cm者行穿刺,最大径0.5~1.0 cm者随访。
3.MFI血流分型及联合诊断标准:根据文献[7-8]标准将MFI模式分为4型:Ⅰ型,结节内无血流信号;Ⅱ型,结节周边见环形血流信号(连续或不连续),典型者动态图像呈“抱球征”;Ⅲ型,以内部血流为主;Ⅳ型,有穿支血管,从结节外穿入结节内,似“蟹爪征”;分布于结节外围,似“太阳征”;分布于结节中心部,似“轮辐征”。TI-RADS联合MFI诊断标准:若结节表现为Ⅳ型血流,则TI-RADS分类上升1级;若结节表现为Ⅱ型血流,则TI-RADS分类下降1级;若结节表现为Ⅰ、Ⅲ型血流,则TI-RADS分类保持不变。
三、统计学处理
应用SPSS 22.0和MedCalc统计软件,计量资料以±s表示,采用t检验;计数资料以频数表示,采用χ2检验或Fisher精确检验。绘制受试者工作特征(ROC)曲线分析单独TI-RADS、TI-RADS联合MFI鉴别诊断甲状腺结节良恶性的效能,曲线下面积(AUC)比较采用Z检验。P<0.05为差异有统计学意义。
结 果
一、两组临床资料、MFI血流分型及TI-RADS分类比较
两组性别、年龄、结节最大径、结节位置比较,差异均无统计学意义。见表1。良性组以Ⅱ型血流为主,恶性组以Ⅳ型血流为主,差异有统计学意义(P<0.01)。见表1和图1。

图1 甲状腺结节MFI图

表1 两组临床资料和MFI血流分型比较
97个 结 节TI-RADS分 类 为:2类16个,3类18个,4类14个,5类49个,恶性率分别为12.5%、27.7%、35.7%、89.8%。联合MFI后TI-RADS分类为:2类21个,3类16个,4类14个,5类46个,恶性率分别为9.5%、6.3%、71.4%、93.5%。见表2。

表2 单独TI-RADS、TI-RADS联合MFI诊断结果
二、诊断效能比较
单独TI-RADS、TI-RADS联合MFI鉴别诊断甲状腺结节良恶性的灵敏度分别为91.1%、94.6%,特异度分别为73.2%、82.9%,AUC及其95%可信区间分别为0.864(0.780~0.925)、0.930(0.860~0.972),二者AUC比较差异有统计学意义(Z=2.624,P=0.0087)。见图2。
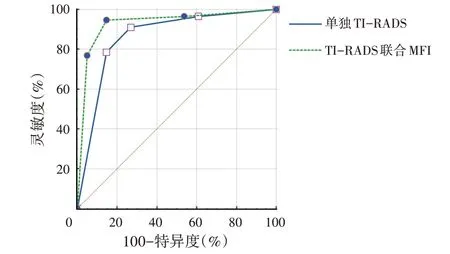
图2 单独TI-RADS、TI-RADS联合MFI鉴别诊断甲状腺结节良恶性的ROC曲线图
三、不必要穿刺率比较
根据TI-RADS分类,共78个结节需进行穿刺,其中恶性结节51个,良性结节27个,不必要穿刺率为27.8%(27/97)。TI-RADS联 合MFI后,共72个 结 节 需进行穿刺,其中良性结节8个,恶性结节64个,不必要穿刺率为8.2%(8/97),二者比较差异有统计学意义(χ2=8.966,P<0.05)。
讨 论
TI-RADS分类旨在提高超声对甲状腺结节进行评估和管理的一致性。但部分甲状腺良恶性结节的灰阶图像特征多有重叠,难以准确鉴别其性质。研究[9]表明观察病灶微血管结构特征有助于鉴别其性质。肿瘤的发展依赖新生血管的生成,由于大量周皮细胞和上皮细胞的参与,导致肿瘤血管内径增宽及血管分支扭曲、增多[10-11]。但传统彩色多普勒技术对结节微小血管的显示欠佳。大多指南[1,12-13]也并未提及甲状腺结节的血流信息,分析原因为传统的多普勒超声中壁滤波技术的应用,使得在消除受检者运动和背景组织运动产生杂波的同时,也抑制了低速血流信号的接收。而MFI技术采用更先进的算法,可以高效区分血流和组织运动产生的多普勒信号,准确检测到管径为0.1 mm、血流速度为1 cm/s的低速血流信号[14]。基于此,本研究旨在探讨ACR TI-RADS联合MFI在鉴别诊断甲状腺结节良恶性中的应用价值。
目前关于甲状腺良恶性结节的血流分布模式尚未统一,不同研究结果差异较大[15-16]。本研究采用MFI技术评估甲状腺结节的微血管分布,发现恶性组结节以Ⅳ型血流为主,良性组结节以Ⅱ型血流为主,二者比较差异有统计学意义(P<0.05)。且穿支血管对恶性结节的诊断具有较高的特异性,笔者根据血流特征对穿支血管进行了总结:分布于结节外围者呈“太阳征”;分布于结节中心者呈“轮辐征”;自结节外围穿入结节者呈“蟹爪征”。究其原因,恶性肿瘤周围组织的增殖较中心更活跃,微血管密度更高;而良性肿瘤呈膨胀性生长,瘤体将肿瘤内血管挤压至周边,在MFI图像上形成环状血流信号[17]。
近年来随医学影像技术的发展,甲状腺结节的检出率显著增加,从而导致更多的细针穿刺活检,过度诊断是近年来甲状腺癌增加的主要原因[18]。ACR TI-RADS是一种基于超声的甲状腺结节风险分层系统,较其他风险分层系统具有更高的特异性,且采用更高的临界值来推荐细针穿刺活检,减少了19.9%~46.5%良性结节的不必要穿刺活检次数;其对不符合活检标准的结节建议进行随访,降低了漏诊的风险[19-20]。本研究中TI-RADS联合MFI诊断时,16个结节因表现为Ⅱ型血流被下调分类(3个由5类降至4类,5个由3类降至2类,8个由4类降至3类),5个结节因表现为Ⅳ型血流而上调分类(由3类升为4类),5个结节从随访改为穿刺,11个结节从穿刺改为随访。在TI-RADS与MFI的血流特征联合应用过程中,将结节的血流特征作为最终分级的考量指标,同时相较于二维图像,血流特征又在整个考量指标中占据着较低的权重,体现了以二维图像为主、血流特征为辅的宗旨。本研究结果表明,与TI-RADS单独应用比较,二者联合应用诊断恶性结节的特异度从73.2%提高至82.9%,灵敏度从91.1%提升至94.6%,AUC从0.864提高至0.930,AUC比较差异有统计学意义(P<0.05),且在提高鉴别诊断效能的同时还降低了不必要穿刺率,减轻了患者额外的负担。
本研究的局限性:①作为回顾性研究,过多纳入了可疑实性甲状腺结节并进行穿刺的患者,导致一定的选择偏倚;②纳入结节的病理类型和数量较少,恶性结节多,良性结节较少,需进一步扩大样本量以提高准确性。
综上所述,ACR TI-RADS与MFI联合应用可有效提高鉴别诊断甲状腺结节良恶性的效能,并降低了不必要穿刺率,有一定的应用价值。
