脑小血管病认知障碍与外周血8-iso-PGF2α、P选择素水平的相关性分析
2023-02-02王道合施媛媛安得英高生云吴成斌
王道合,施媛媛,安得英,杨 勇,高生云,吴成斌,周 伟
(1. 甘肃省武威肿瘤医院神经内2科,甘肃 武威 733000;2. 甘肃省武威肿瘤医院肝病科,甘肃 武威 733000;3. 甘肃省武威肿瘤医院心血管专科,甘肃 武威 733000;4. 甘肃省武威肿瘤医院医技科室,甘肃 武威 733000)
脑 小 血 管 病(cerebral small vessel disease,CSVD)多发于老年人,是因颅内微小动静脉、毛细血管发生病变引起的神经系统疾病,疾病早期症状隐匿,病情进展慢,但长期发展可造成认知障碍、神经行为异常等慢性神经损伤[1-2]。脑小血管病是造成认知障碍的主要原因,约70%的血管性认知障碍由脑小血管病所致。采取早期诊断与干预有利于减轻脑小血管病造成的神经损伤程度,避免发展为血管性痴呆。目前,临床多采用蒙特利尔认知评估量表(Montreal Cognitive Assessment Scale,MoCA)作为认知障碍快速筛查评价工具,但应用该量表评估会受到患者情绪状态、文化背景、受教育程度等影响[4]。研究[5-7]发现,氧化应激、炎症反应、血小板活化可参与认知障碍病程过程。8-异前列腺素F2α(8-isoprostaglandin F2α,8-iso-PGF2α)为不饱和脂肪酸脂质过氧化末端产物,可反映机体氧化应激状况,可能与认知障碍发病有关[8-9]。P选择素(P-selectin,PS)为血小板活化特异标志物,与血栓形成、炎症反应等病理过程均有密切关系[10-11]。目前,关于8-iso-PGF2α、PS水平与脑小血管病并发认知障碍的关系临床尚不明确。本研究分析脑小血管病认知障碍与外周血8-iso-PGF2α、PS水平的相关性,以期为早期识别与预防脑小血管病发生认知障碍提供一定依据。报道如下。
1 资料与方法
1.1 一般资料
选取我院2019年6月-2022年6月82例脑小血管病患者。纳入标准:1)符合《中国脑小血管病诊治共识》[12]脑小血管病临床诊断标准,且经颅脑MRI、CT检查证实;2)年龄≥18岁;3)首发患者;4)可配合完成神经认知功能检查;5)无卒中、颅内动脉狭窄、精神疾病病史;6)患者与家属知情同意,签署知情同意书。排除标准:1)伴有视听力障碍、失语、阿尔茨海默病、帕金森病、额颞叶痴呆、路易体痴呆者;2)合并颅内感染、癫痫、颅脑创伤、脑积水、脑肿瘤;3)合并肢体功能障碍、呼吸衰竭、甲状腺功能低下、自身免疫性疾病、血液系统疾病者;4)合并肝、心、肾等脏器功能严重障碍者;5)滥用精神类药物或酗酒者。本研究经医院伦理委员会审核批准。
1.2 方法
资料收集:在患者入院后采集其性别、年龄、饮酒史、吸烟史、受教育年限、合并症(高血压、糖尿病、冠心病)等情况;应用全自动生化分析仪(西门子,Advia XPT)检测三酰甘油(triglycerides,TG)、总胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)、空腹血糖(fasting blood glucose,FBG)水平。
外周血8-iso-PGF2α、PS检测:入院第2天清晨采集患者5 mL空腹外周血,置入含乙二胺四乙酸抗凝管内,室温下离心(3 000 r·min-1,20 min),取上清液,-20 ℃冰箱内冻存待检;以酶联免疫吸附法测定8-iso-PGF2α、PS水平,试剂盒购于上海一研生物科技有限公司。
认知功能评定与分组:应用MoCA量表评定患者认知功能,量表内容包括定向力、计算、抽象思维、语言、记忆、执行功能、注意力与集中等维度,总分30分,评分<26分判定为认知障碍,受教育年限12年以内患者需在总得分基础上加1分,用于矫正由于教育因素造成的偏倚。据此将患者分为研究组(合并认知障碍)与对照组(未合并认知障碍)。
1.3 统计学方法
应用SPSS 23.0软件处理数据。计量资料均证实符合正态分布,以均数±标准差(±s)表示,采用t检验;计数资料以率(%)表示,采用χ2检验;外周血8-iso-PGF2α、PS水平与脑小血管病患者MoCA评分关系分析应用Pearson相关性分析;脑小血管病患者认知障碍影响因素分析应用Logistic回归分析;通过受试者工作特征(receiver operating characteristic curve,ROC)曲线观察外周血8-iso-PGF2α、PS水平对脑小血管病患者认知障碍的预测效能。以P<0.05为差异有统计学意义。
2 结果
2.2 2组基线资料与MoCA评分比较
2组性别、年龄、饮酒史、吸烟史、受教育年限、糖尿病、冠心病、TG、LDL-C、HDL-C、FBG水平比较,差异无统计学意义(P>0.05);研究组高血压比例、TC水平高于对照组,MoCA评分低于对照组(P<0.05)。见表1。

表1 2组基线资料与MoCA评分比较
2.2 2组外周血8-iso-PGF2α、PS 水平比较
见表2。
表2 2组外周血8-iso-PGF2α、PS水平比较(±s)

表2 2组外周血8-iso-PGF2α、PS水平比较(±s)
注:与对照组比较,#P<0.05
组别 例数 8-iso-PGF2α/(pg·mL-1) PS/(μg·L-1)研究组 44 326.92±70.23# 17.83±2.74#对照组 38 234.27±61.58 13.91±1.68
2.3 外周血8-iso-PGF2α、PS水平与脑小血管病患者MoCA评分关系
Pearson相关性分析显示,外周血8-iso-PGF2α、PS水平与脑小血管病患者MoCA评分均呈显著负相关(P<0.05)。见表3。
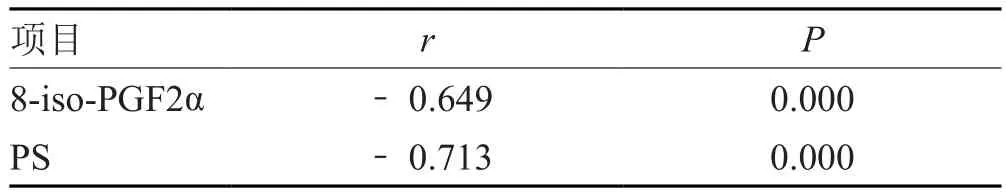
表3 外周血8-iso-PGF2α、PS水平与脑小血管病患者MoCA评分关系
2.4 脑小血管病患者认知障碍影响因素
将脑小血管病患者认知障碍为因变量,高血压、TC与外周血8-iso-PGF2α、PS为自变量,因量表赋值:认知障碍,合并=1,未合并=0;自变量赋值,高血压:有=1,无=0;TC与外周血8-iso-PGF2α、PS以平均值为界,>平均值=2,≤平均值=1。采取Logistic回归分析显示,高血压与外周血8-iso-PGF2α、PS均为脑小血管病患者认知障碍影响因素(P<0.05),TC并非脑小血管病患者认知障碍影响因素(P>0.05)。见表4。

表4 脑小血管病患者认知障碍影响因素
2.5 外周血8-iso-PGF2α、PS水平对脑小血管病患者认知障碍的预测效能
绘制ROC曲线显示,8-iso-PGF2α、PS预测脑小血管病患者认知障碍的曲线下面积(area under the curve,AUC)分别为0.836、0.894,通过Logistic回归得出8-iso-PGF2α、PS联合预测脑小血管病患者认知障碍的预测值P,引入ROC曲线,发现联合预测时AUC为0.934,高于单一指标。见表5,图1。

表5 外周血8-iso-PGF2α、PS水平对脑小血管病患者认知障碍的预测效能

图1 外周血8-iso-PGF2α、PS水平对脑小血管病患者认知障碍的预测ROC曲线
3 讨论
脑小血管病可引起脑供血不足与颅内渗透压变化,导致神经功能受损,引发认知障碍,主要特征为信息处理速度降低、语言功能障碍、注意力与执行力下降,虽病情进展慢,但会对患者生活质量造成明显影响,采取早期诊断与干预尤为必要[13-14]。
氧化应激是指机体遭受不良刺激时,产生氧化与抗氧化作用失衡,大量自由基未被清除,导致组织功能产生损伤。研究[15-17]发现,氧化应激在认知障碍、阿尔茨海默病发病中具有重要作用。脑小血管病可造成小血管结构产生改变,引起大脑低灌注、炎症反应、血管细胞线粒体功能异常及氧化应激等,且缺血缺氧可导致机体生物氧化功能产生异常,形成大量氧自由基,影响细胞膜通透性,加剧血脑屏障破坏,造成神经血管单元功能障碍,加速神经变性病变,促进认知障碍发生[18]。大脑作为代谢最活跃器官,需氧量较高,更易受到自由基的影响,自由基可促使神经细胞膜产生过氧化反应,并影响神经细胞膜稳定性,可引起认知障碍[19]。8-iso-PGF2α是细胞膜与线粒体膜等结构内自由基和花生四烯酸产生反应的脂质过氧化物,可准确反映机体氧化应激水平[20-21]。研究[22]报道,8-iso-PGF2α表达与痴呆患者认知障碍存在密切关系。研究[23]显示,神经功能异常患者8-iso-PGF2α表达可显著增高。脂质过氧化与神经功能损伤有着密切关系,正常生理状态下机体抗氧化能力较好,而当脑组织缺血缺氧时机体抗氧化体系会遭受破坏,造成自由基难以被充分清除,引起神经细胞损伤及凋亡,导致认知障碍发生。8-iso-PGF2α可促使下游因子表达提高,使脂质沉积在滋养层细胞和单核细胞黏附在血管内皮,并造成血管收缩与血管内皮细胞产生分化,导致血管损伤,影响脑局部血供,引起认知功能损伤[24]。研究[25]显示,8-iso-PGF2α表达与轻度认知障碍、阿尔茨海默病患者认知功能评分存在线性相关性。本研究结果显示,研究组外周血8-iso-PGF2α水平高于对照组,且经Pearson相关性分析显示,其水平与脑小血管病患者MoCA评分呈显著负相关,与上述研究相似,说明脑小血管病认知障碍与外周血8-iso-PGF2α密切相关,8-iso-PGF2α可能通过氧化应激途径参与脑小血管病认知障碍发生进展。本研究通过Logistic回归分析显示,外周血8-iso-PGF2α为脑小血管病患者认知障碍影响因素,且ROC曲线显示,其预测脑小血管病患者认知障碍的AUC为0.836,进一步提示8-iso-PGF2α与脑小血管病认知障碍的相关性,可将其作为预测脑小血管病患者出现认知障碍的候选指标。
血小板活化、炎症反应为认知障碍的重要发病机制,与认知功能下降、轻度认知障碍、痴呆具有密切关系[26-27]。PS为血小板活化可靠标志物,正常情况下处于低表达状态,当受到氧化应激或炎症刺激时,由于血小板被激活,产生血管内皮损伤,可导致PS水平增高[28]。PS可介导血管内皮细胞、血小板与中性粒细胞、单核细胞间产生黏附作用,致使机体炎症反应加剧,并可促进纤维蛋白合成,造成微循环障碍,最终引起脑局部血栓形成,影响脑供血、供氧,导致脑神经功能损伤,引发认知障碍[29]。本研究结果显示,研究组外周血PS水平较高,且其水平与脑小血管病患者MoCA评分呈负相关关系,与上述研究结果符合,表明外周血PS在脑小血管病认知障碍发生进展过程中具有重要作用,PS可能通过血小板活化、炎症反应途径参与了脑小血管病认知障碍发病。本研究结果显示,外周血PS为脑小血管病患者认知障碍影响因素,且其预测脑小血管病患者认知障碍的AUC为0.894,进一步证实PS与脑小血管病认知障碍密切相关,可为预测脑小血管病患者出现认知障碍提供参考。本研究结果发现,8-iso-PGF2α、PS联合预测脑小血管病患者认知障碍的AUC为0.934,预测效能更佳,提示8-iso-PGF2α、PS联合预测可为预测脑小血管病患者认知障碍提供更可靠依据,指导临床早期防治。
综上所述,脑小血管病认知障碍与外周血8-iso-PGF2α、PS水平密切相关,可作为预测脑小血管病患者出现认知障碍的候选指标。但关于8-iso-PGF2α、PS是否在脑小血管病认知障碍发病中有协同作用仍需将来实验研究进一步探究。
