质子导体固体氧化物燃料电池电化学性能计算研究
2023-01-30李会平
李会平,李 明
(1.华东理工大学无机材料系,上海 200237;2.武汉纺织大学化学与化工学院,湖北 武汉 430073)
1 引言
质子导体固体氧化物燃料电池(proton conducting solid oxide fuel cell,P-SOFC或H-SOFC),又称质子陶瓷燃料电池(proton ceramic fuel cell,PCFC)是在传统固体氧化物燃料电池(O-SOFC)基础上发展起来的一种新型全固态燃料电池,具有工作温度低、燃料灵活、燃料利用率高和实用范围广等特点,成为近年来能量转换装置的研究热点[1-3]。
燃料电池内电化学行为及其影响因素的研究对了解燃料电池的特性及电池堆的性能模拟有重要意义。Ni和Leung等人[4]分析了H-SOFC阴、阳极两侧气体的传质过程,利用多孔材料内的气体渗透理论和尘气模型(dusty gas model,DGM),得到了H-SOFC电池的浓差极化过电势,并通过与欧姆极化与活化极化过电势耦合,建立了H-SOFC的电化学综合模型。计算对比了H-SOFC与O-SOFC电池的电化学性能和电池支撑设计的作用,得出阳极支撑是最期望的电池结构。Patcharavorachot和Brandon等人[5]基于Fick扩散定律给出了H-SOFC阳极三相界面的H2浓度与燃料侧H2浓度和阴极三相界面的O2、H2O的浓度与空气侧O2、H2O浓度的显示表达式,简化了H-SOFC电化学性能的计算。Liu,Akhtar和Li等人[6]也分析了电池阴、阳极两侧的传质过程;不同于前二者,在Liu,Akhtar和Li等人的模型中考虑了阴、阳极两侧气体的对流传质;并将阴、阳极三相界面的组分浓度与传质系数和流过电池横截面的电流密度进行了关联。在验证模型的基础,文献6还研究了流道尺寸对电池性能的影响。最近,广东工业大学的邱瑞铭和刘建平提出了H-SOFC的漏电模型[7],并对H-SOFC的电池模拟工作做了综合评述,指出考虑电池内的气体输送,电化学和传热耦合的电池堆模拟将是H-SOFC模拟发展的方向[8]。
单电池的电化学模型是了解电池特性和电池堆性能模拟的基础。文献4的尘气模型成功关联了三相界面气体组分浓度与电池阴阳侧气体组分摩尔分数和局部压力之间的关系,但公式过于复杂,浓差极化过电势计算需进行反复迭代;文献5的显式表达式简化了浓差极化过电势的计算,但Fick扩散定律概念的应用不够严谨,且多孔电极层内多组分扩散系数的计算是基于Lennard-Jones电势的碰撞积分,需查表确定多个积分系数。为更好研究流道结构尺寸对电池性能的影响,文献6采用5层的等效电路模拟了电池的欧姆极化损失,但欧姆极化损失需迭代计算。本文在分析H-SOFC工作原理的基础上,修正了文献5中气体组分扩散传质的概念,调整了多孔电极中多组分扩散系数的计算式,吸纳了上述文献和其他文献中活化极化、欧姆极化和浓差极化过电势的显式表达式,给出了基于气体通道内柱塞流动的纯质子传导H-SOFC的电化学性能分析计算的一个简化模型,计算研究了单电池的基本特性,并探讨了电解质材料参数、电池工作温度和阴极侧气体组成等对电池性能的影响,以期提升国内对H-SOFC电池涉及的物理、化学现象的认识,并为下一步电池堆性能模拟奠定初步基础。
2 H-SOFC工作原理
质子导体固体氧化物燃料电池单电池由多孔的阳极层和多孔的阴极层以及用于分隔阴、阳极层的密实电解质层组成,阳极一侧(燃料通道)流着H2,阴极一侧(空气通道)流着空气,如图1所示[4]。

图1 H-SOFC单电池结构及工作原理示意图[4]Fig.1 Schematic of H-SOFC structure and working principle[4].
在阳极侧,由于浓度(或压力)差的作用,H2以对流扩散形成形式通过多孔阳极传输至阳极三相界面(three phase boundary,TPB),在那里在阳极催化作用失去电子,变成质子。释放的电子通过外电路流至阴极,实现对外发电;形成的质子,在电势差的作用下,通过固体电解质传输至阴极三相界面,并与从多孔阴极传输来的O2发生电化学反应生产H2O。气态H2O以扩散对流方式传输至阴极侧气流中,并被空气带走。
3 电化学模型
3.1 基本假设
为简化分析与计算,作如下假设:
(1)电池以纯氢气为燃料,以空气为氧化剂,各气体均为理想气体;
(2)在阳极侧流着H2,在阴极侧流着空气和H2O;各气体沿通道作柱塞流动;
(3)电解质层内的离子传导为纯质子传导。
3.2 多孔电极内的扩散系数
燃料电池的电极层通常为多孔材料。
多孔材料内的气体扩散主要有分子扩散和Knudsen扩散。当材料的孔径大于气体组分的分子平均自由程时,扩散以分子扩散为主;当材料的孔径远小于气体组分的分子平均自由程时,发生Knudsen扩散。对Knudsen扩散,组分i的Knudsen扩散系数Di,k可表示为[5,6,9]:
(1)
式(1)中:T为气体温度;Mi为组分i的分子量;r为孔半径。
对二元组分i,j系统,其分子扩散系数Di,j可表示为[6]:
(2)
式(2)中:Mi,Mj为组分i,j的分子量;P,T为压力,温度;Vi,Vj为组分i,j有关的常数,VH2=7.07,VN2=17.9,VO2=16.6,VH2O=12.7。
对多组分系统,组分i在混合物mix中的分子扩散系数Di,m可用下式表示[6]:
(3)
式(3)中:xi组分i的摩尔分数。
当材料的孔径与气体组分的分子平均自由程相近时,两种扩散同时存在,其有效扩散系数Di,eff除需考虑两种扩散外,还需考虑气孔率、气孔曲率等对扩散系数的影响,校正后的扩散系数可表达如下[9]:
(4)
式(4)中:εp为气孔率;τ为气孔曲率。
对文中考虑的H-SOFC电池,阳极侧主要为H2;阴极侧则同时存在O2,N2,和H2O。可应用上述公式计算有效扩散系数。
3.3 电化学模型
由电化学反应方程式,可得H-SOFC的可逆电势E为:
(5)
式(5)中:E0为标态开路电压,可表示为温度的函数[5];PH2,f为燃料通道(阳极侧)中的H2分压;PO2,a,PH2O,a分别为空气通道(阴极侧)中O2,H2O的分压。
电池实际电压V是电池可逆电势E减去各类极化的值,可用下式表示[10]。
V=E-(ηconc,anode+ηconc,cathode+ηact,anode+ηact,cathode+ηohm)
(6)
式(6)中:ηconc,anode,ηconc,cathode,ηact,anode,ηact,cathode分别阳极、阴极浓差极化过电势和活化极化过电势;ηohm为欧姆极化过电势。
3.3.1 欧姆极化
欧姆极化是由质子在电解质中的流动阻力和电子在电极和导电体内流动阻力及电池各组件的接触电阻引起的。欧姆定律描述了欧姆电压降ηohm与电流密度j和电阻Rohm之间的线性关系:
ηohm=jRohm
(7)
式(7)中:Rohm为各电池材料的总电阻,各材料电阻Ri可表示为:
(8)
式(8)中:δi为材料厚度,Ai为材料截面积,σi为各材料的电导率,可进一步表示为温度的函数,σi=aexp(-E/T)。
3.3.2 浓差极化
气体通道(阳极侧和阴极侧)中反应气体要通过多孔电极扩散到三相界面才能发生化学反应,由于扩散过程存在阻力,就使得化学反应界面处的反应物气体浓度低于其在气体通道中的浓度,这种由于反应区的反应物浓度偏离其主流通道浓度所造成的电动势损失称为浓差极化损失。
浓差极化过电势与气体在通道中的平均浓度和TPB的浓度有如下关系:
(9)
(10)
式(9)(10)中,Ci,f,Ci,a分别为组分i在燃料通道和空气通道的浓度;Ci,TPB为组分i在三相界面的浓度。
为求得三相界面的组分浓度,需分析组分在通道和电极层中的传质过程。假设气体在燃料通道和空气通道的流动为柱塞流动,且组分在电极材料层中的扩散为一维传质的情况下,经推导有[9]:
(11)
(12)
(13)
式(11)—(13)中,δanode,δcathode分别为阳极和阴极厚度;DH2,eff,DO2,eff,DH2O,eff分别为H2、O2、H2O在燃料通道(阳极侧)和空气通道(阴极侧)考虑了分子扩散和Knudsen扩散的有效扩散系数,见前述。
3.3.3 活化极化
活化极化是由于电极表面反应缓慢所致。活化极化可由Butler-Volmer方程导出。Butler-Volmer电流密度方程的一般形式为:
(14)
式(14)中,α为电荷转移系数,通常取0.5;n为转移的电子数;j0为交换电流密度。
整理有:
electrode∈{anode,cathode}
(15)
4 计算方法
上述方程构成了H-SOFC单电池的电化学模型。在给定阳极侧和阴极侧的组分浓度(压力)和电池温度后,根据事先确定的阴、阳极层和电解质层的材料和厚度,可计算研究电池的电流密度与实际电压之间的关系。改变材料参数(如电导率、气孔率等)、设计参数(如电池材料厚度、支撑方式)和操作条件(如电池温度、气体组成等)可探究材料、设计和操作参数等对电池性能的影响。
5 计算结果与分析讨论
电池材料是电池性能的基础。电池的支撑方式、各层材料厚度,操作参数(温度、压力)和过程参数(气体流道内的流速、流量,气体组成等)等均影响电池的性能。文献4和5的计算分析表明,H-SOFC电池以阳极支撑为佳;他们的研究还初步优化了电池各层材料的厚度。因此,本文主要研究阳极支撑时H-SOFC电池材料参数、温度和阴极层气体组成对电池性能的影响。
5.1 电池温度的影响
首先选定的电池材料取自文献4,分别是:电解质:涂Sm的BaCeO3(BCSO);阴极:Ba0.5Sr0.5Co0.8-Fe2O3-x-BCSO;阳极:Ni-BCSO。其厚度分别为500 μm,50 μm和50 μm。研究温度从773 K到973 K,电解质的电导率分别为[4]:773 K,0.416 Sm-1;873 K,0.662 Sm-1和973 K,0.938 Sm-1。阳极侧气体组成H2∶H2O=0.97∶0.03;阴极侧空气组成 O2∶N2∶H2O=0.18∶0.79∶0.03。电极材料孔半径0.5 μm,孔隙率0.4,孔曲率5。
根据前述模型,计算的电池温度为873 K,压力为1 atm时的电池实际电压及各种极化损失组成如图2所示。
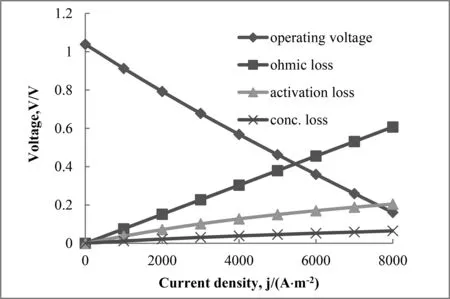
图2 电池的实际电压和各种极化损失与电流密度的关系Fig.2 The relationship between the operating voltage and various potential losses and the current density for a H-SOFC.
从图2可见,随电流密度增大,电池实际电压逐渐降低,各种极化电压损失逐渐增加。对阳极支撑的H-SOFC电池,其浓差极化损失很小。电池电压损失主要来自欧姆损失(873 K时)。
欧姆损失主要是电解质层中质子传导的结果。电解质传导质子的能力与材料的电导率有关,而电导率是温度的函数。为此,计算了不同温度下的电池欧姆极化,也一并给出了活化极化损失,如图3所示。
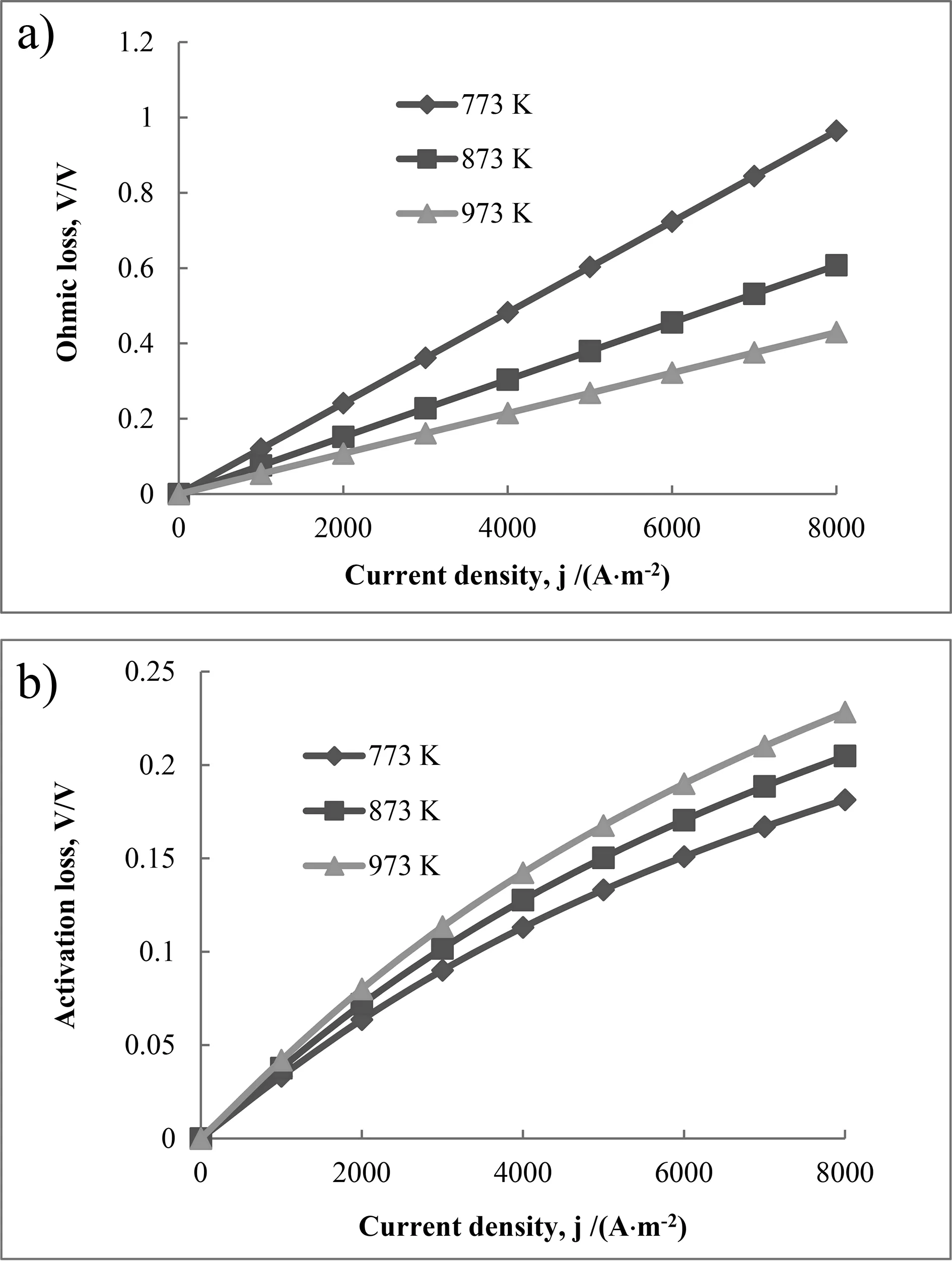
图3 电池温度对欧姆极化和活化极化损失的影响Fig.3 The effect of working temperature on the potential losses for a H-SOFC.a) ohmic loss;b) activation loss.
从图3a可见,随温度升高,欧姆极化损失逐渐降低,这主要是因为温度升高,材料电导率升高所致。这表明,低温时欧姆极化损失是H-SOFC的主要损失。
从图3b可见,在欧姆极化损失随温度升高而降低的同时,活化极化却明显增大。在973K时,活化极化损失与欧姆极化损失大体相当。因此,高温时H-SOFC电池的主要损失既有欧姆极化损失又有活化极化损失。
图4显示的是流过电池的电流密度与电池功率密度的关系。

图4 不同操作温度下的功率密度与电流密度之间的关系Fig.4 The relationship between the power density and current density for different working temperatures.
从图4可见,每一温度下有一个最大功率密度值(773 K,Pm为0.175 W·m-2;873 K,Pm:0.23 W·m-2;973 K,Pm:0.27 W·m-2;对应的电流密度分别约为3 500 A·m-2,5 000 A·m-2和6 000 A·m-2)。随温度升高,最低功率密度增大,对应的电流密度向大电流方向偏移。这与O-SOFC电池规律一样。
5.2 电池材料的影响
在前述研究的基础上,为进一步探讨电解质电导率的影响,计算了PtlSCYlPt电池的电化学特性。该电池的实际电压和各种极化损失构成和功率密度与电流密度的之间关系见图5。

图5 PtlSCYlPt电池性能Fig.5 Electro-chemical performance for PtlSCYlPt H-SOFC.a) operating voltage and various potential losses at 1 173 K;b) power density.
从图5a可见,在1 173 K时,该H-SOFC电池主要电压损失已变化为活化极化损失。这主要是因为温度较高(800~1 000 ℃),电解质的电导率较高,欧姆极化损失下降的缘故。从图5a可见,浓差极化损失仍很小。
从图5b可见,PtlSCYlPt电池的功率密度随温度的变化规律同前述:温度越高,最大功率密度越高,对应的电流密度向高电流密度方向移动。
5.3 阴极侧气体组成的影响
H-SOFC电池与O-SOFC电池的不同之处除了前者是质子在电解质中传输,后者是O-2在电解质中的传输外;另一个不同之处是,H-SOFC电化学反应发生在阴极,反应产生的H2O经扩散传至空气通道中并被空气带走。反应需要的O2则反向传输至阴极三相界面。H2O和O2在多孔材料中的传输比H2的传输慢许多;当电化学反应发生后,又因空气通道中H2O的浓度增加,O2浓度降低,其浓差极化损失会有很大不同。为此,计算了阴极侧H2O浓度的影响。
图6是阴极侧H2O浓度对电池特性的影响。

图6 阴极通道H2O含量对浓差极化和构成及功率密度的影响Fig.6 The effect of H2O content in air channel on the concentration loss and its components and the power density.a) concentration loss and its components;b) power density.
从图6a可见,对两种不同浓度的空气(3% H2O和12% H2O),其阳极浓差极化损失远小于阴极浓差极化损失,约小一个量级(图中的yc,yca,ycc分别代表总浓差极化、阳极和阴极浓差极化损失)。因此,H-SOFC电池的浓差极化损失主要是阴极浓差极化损失。
从图6a还可见,H2O浓度越大,阴极浓差极化和总浓差极化损失越大;图6b中,电池实际电压降低,功率密度也降低。这主要是因为,通道中H2O多,O2则少;O2向阴极三相界面的扩散动力就小,三相界面产生的H2O很难扩散至空气通道中。因此,应尽可能减少空气通道中H2O。
6 结论
结合质子导体固体氧化物燃料电池的特点,整理、综合了文献中欧姆极化、浓差极化和活化极化过电势的显式表达式,提出了基于柱塞流动的纯质子导电H-SOFC电池的电化学模型,并在计算机上进行了理论计算,得到以下结论。
(1)阳极支撑的H-SOFC的主要电压损失是欧姆极化损失和活化极化损失,阴极浓差极化损失远大于阳极极化损失。
(2)温度越高,欧姆极化损失越小,电池最高功率密度越大;随温度升高,最大功率密度对应的电流密度向大电流方向偏移。
(3)在相同温度下,高电导率的材料有高的电池效能。
(4)阴极侧H2O越多,O2向阴极三相界面扩散的推动力越小,在三相界面电化学反应生成的H2O向空气中扩散能力越差,最大电池功率密度降低。因此,应尽可能减少空气侧H2O的浓度。
